(25S)-26-OH-人参二醇的合成及抗宫颈癌活性研究
2021-09-07张馨妍韩诗淇吉林医药学院药学院吉林吉林132013
张馨妍,吴 迪,韩诗淇,韩 柳 (吉林医药学院药学院,吉林 吉林 132013)
宫颈癌是一种危害女性常见的恶性肿瘤,尤其是在发展中国家,其死亡率是在发达国家的18倍左右,占所有宫颈癌相关死亡人数的85%,严重危害女性健康[1]。(25S)-26-OH-人参二醇是近年来新发现的一种新型三萜皂苷类化合物,在治疗冠心病、再灌注损伤、心律不齐、心肌缺血方面有很好的药理作用[2],并且具有其他人参皂苷不具备的药理特性,这些优点使它具有很好的药物开发价值。因此,有效制备出(25S)-26-OH-人参二醇,对下一步药理作用的深入探讨与新药物的开发研制具有重要意义。
1 材料与方法
1.1 主要试剂与仪器
电热恒温水浴锅(天津市泰斯特仪器有限公司);电子天平(沈阳龙腾电子有限公司);旋转蒸发仪(上海亚荣生化仪器厂);硅胶G板(青岛海洋化工有限公司);核磁共振仪(美国Varian公司);(20S)-原人参二醇实验室自制,4-二甲基氨基吡啶(DMAP)、乙酸酐(Ac2O)、氢氧化钠、无水碳酸氢钠、二氯甲烷(DCM)、石油醚、正丁醇、乙酸乙酯、叔丁醇钾、过硫酸氢钾复合盐等试剂均为分析纯。
1.2 (25S)-26-OH-人参二醇的合成
称取23 g(20S)-原人参二醇(PPD)(50 mmol)和少量DMAP置于500 mL圆底烧瓶中,加入300 mL吡啶,室温下搅拌至样品溶解。然后缓慢滴加Ac2O 30 mL,室温反应过夜。薄层色谱实时监测反应进程,反应结束后,向体系中加入饱和NaHCO3溶液,然后用DCM分次萃取,合并有机相。浓缩除去有机溶剂后加入饱和NH4Cl溶液洗涤3次。再次加入DCM萃取,有机相浓缩至50 mL,至圆底烧瓶中,向反应物中加入20 mL 10%的浓硫酸,并加热回流7 h,同时薄层色谱实时监测反应进程。待反应结束后,取6 g叔丁醇钾分批加入到反应体系中参与反应,反应完全后加入饱和NaHCO3溶液,用DCM萃取,浓缩有机相至呈油状物,以50 mL甲醇溶解并加入等质量的NaOH,60 ℃回流4 h。用等体积水终止反应,稀硫酸调pH 3~5,用100 mL DCM萃取3次,合并有机相并浓缩,浓缩后产物经柱层析分离,二氯甲烷∶甲醇(25∶1)作为洗脱剂,乙酸乙酯重结晶,得25-烯-PPD 9.2 g。
将制得的25-烯-PPD加入到1,4-二氧六环中,直至全部溶解,经H2SO4调节pH值为3,在搅拌下逐滴加入氧化剂过氧间氯苯甲酸,于85 ℃加热回流40 min,冷却至室温,用0.1 mol/L氢氧化钠水溶液调节pH值为7.0,过滤并浓缩滤液,得(25S)-26-OH-人参二醇粗品,该过程如图1。将制得的(25S)-26-OH-人参二醇粗品装入硅胶柱,以石油醚∶乙酸乙酯(1.0∶1)为洗脱剂进行柱层析分离,将分离下来的溶液旋蒸蒸干,以乙酸乙酯重结晶进一步纯化,得(25S)-26-OH-人参二醇4.6 g。
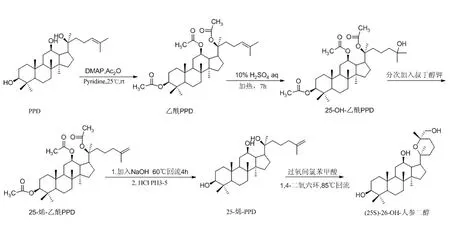
图 1 (25S)-26-OH-人参二醇的合成路线图
1.3 人参二醇抑制HeLa细胞增殖的活性
取对数期生长细胞以4.5×105个/孔接种于96孔板,培养24 h后更换为含不同浓度的(25S)-26-OH-人参二醇培养基继续培养24 h,小心弃去培养基,每孔中加入配好的CCK-8溶液100 μL,3副孔/组,并设置CCK-8检测试剂空白对照组[3]。37 ℃恒温培养箱孵育1~4 h后在450 nm吸收波长处进行OD值测量,以对照组OD值为1左右时的数值计算细胞增殖活性。
2 结 果
2.1 (25S)-26-OH-人参二醇的结构鉴定
白色粉末;MS m/z:477.4[M+H]+,确定分子式为C30H53O4;以氘代吡啶(pyridine-d5)为溶剂,在500 MHz下测定其核磁共振碳谱,得到1H NMR和13C NMR的谱图。
具体数据信息如下:1H NMR(500 MHz,Pyr)δ3.91(q,J=10.9 Hz,2H),3.76(td,J=10.0,4.8 Hz,1H),3.45(dd,J=11.0,5.2 Hz,1H),2.20(td,J=10.4,5.1 Hz,1H),2.13(ddd,J=12.4,4.9,2.3 Hz,1H),2.01-1.94(m,2H),1.89-1.75(m,5H),1.74-1.67(m,2H),1.65(s,3H),1.63-1.57(m,2H),1.55-1.42(m,8H),1.40(s,3H),1.36-1.26(m,3H),1.24(s,3H),1.07(s,3H),1.05(s,3H),1.03-0.96(m,2H),0.93(s,3H),0.91(s,3H),0.84(dd,J=10.9,2.3 Hz,2H);13C NMR(126 MHz,Pyr)δ78.68,78.49,77.71,70.98,67.72,56.91,52.72,52.67,51.02,49.75,40.57,39.96,39.91,37.84,35.62,32.82,32.54,32.48,29.06,28.67,28.00,27.93,27.89,27.49,19.24,18.49,16.99,16.74,16.64,16.21。由此确定合成的化合物为(25S)-26-OH-人参二醇。
2.2 (25S)-26-OH-人参二醇体外抗癌细胞活性结果
细胞实验结果表明,(25S)-26-OH-人参二醇对HeLa细胞的增殖有一定的抑制作用。随着药物浓度剂量的加大,其抑制率逐渐升高,尤其是在浓度为75 mg/L时,其抑制率可达到36.14%(图2)。
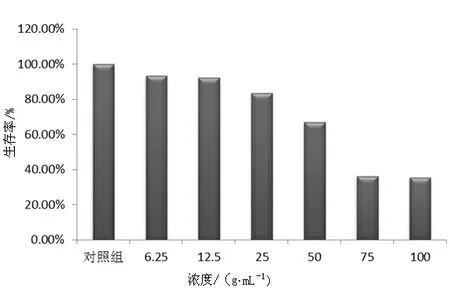
图 2 (25S)-26-OH-人参二醇对HeLa细胞存活率的影响
3 讨 论
本实验以(20S)-原人参二醇为原料,经过乙酰化、加成、消除、氧化环合等步骤可以成功合成(25S)-26-OH-人参二醇,经过纯化后其纯度可达98.0%以上。但因合成步骤多,因此,严格控制好每一步的反应进程是其提高合成产率的关键。尤其是在最后的一步氧化环合过程,除了应用过氧间氯苯甲酸作为氧化剂之外,还可以选择过氧化氢或过氧乙酸等强氧化性的物质来进行氧化环合[4],但是这些氧化剂都会存在生成差向异构体的缺点。因此,后续研究手性催化剂使其通过不对称的氧化环合作用,生成单一构型的产物,对于人参皂苷的合成具有重要意义。此外,(25S)-26-OH-人参二醇对HeLa细胞的增殖有一定的抑制作用,为其抗宫颈癌作用的研究奠定了基础。
