mpt64 mRNA作为结核化疗细菌学监控的分子标志物研究
2021-09-06雷杰王楠牛群谢贝吴玲邓丽刘志辉孟繁荣
雷杰 王楠 牛群 谢贝 吴玲 邓丽 刘志辉 孟繁荣
广州市胸科医院肺部疾病研究所呼吸疾病国家重点实验室 510095
结核病作为一类慢性传染性疾病,主要是由结核杆菌感染,在全球范围内流行,严重危害人类健康。化学疗法[1]是治愈结核病和限制结核杆菌传播的重要手段,找到一种能够快速反映结核病化疗疗效的生物标志物,实现对化疗疗效效果的监控与评价显得十分重要。近些年来,随着现代医学技术的快速发展,各种新型标志物不断被发现,它们的高敏感性、高特异性和快速性给结核病的化疗监控带来新的期望,然而这些标志物大都不能满足临床上对结核病化疗监控的全部要求。mpt64 是结核杆菌在生长早期大量分泌的特异性蛋白,可分泌至菌体外。mpt64 mRNA产生于结核杆菌合成mpt64分泌蛋白时,由结核杆菌内的mpt64基因编码并生成,属于活菌体中极为重要的一个组成部分,同时mpt64 mRNA 有较短的半衰期,一般仅为数分钟。由此可见,mpt64 mRNA作为一种监控结核病化疗疗效的细菌学分子标志物将大有可为。本研究探讨mpt64 mRNA 作为结核化疗细菌学监控的分子标志物可行性。
1 资料与方法
1.1 菌株 2021 年1 月至4 月,于广州市胸科医院分枝杆菌菌种库中,随机选取35 株对4 种一线抗结核药物敏感的临床分离株。
1.2 方法
1.2.1 主要试剂和仪器 Middlebrook 7H9、Middlebrook 7H10 培养基购自美国BD 公司,异烟肼购于瑞威尔生物科技有限公司,细菌总RNA 快速抽提试剂盒购自上海生工生物工程有限公司,反转录反应试剂盒(High-Capacity cDNA Reverse Transcription Kit)购自美国赛默飞世尔公司,实时荧光定量聚合酶链式反应(PCR)检测试剂盒(TB Green Fast qPCR Mix)购自北京宝日医生物技术有限公司。PCR 扩增仪(C1000TM Thermol cycle 系列)购自美国BIO RAD 公司,荧光定量PCR 扩增仪(Viia 7 DX)购自美国ABI公司。
1.2.2 实验方法
1.2.2.1 结核分枝杆菌培养及药物处理结核分枝杆菌经复苏培养后选取Middlebrook 7H10 培养基上处于对数期生长旺盛状态良好的菌株,制成浊度为1 麦氏的菌悬液,取100.0 μl 菌液接种至10 ml 新鲜Middlebrook 7H9 培养基,加入异烟肼药液使培养基中药物终浓度分别为0、0.2、0.5 μg/ml,37 ℃培养48 h后收集菌液3 ml,13 000 g离心10 min,菌体-70 ℃保存备用。
1.2.2.2 总RNA 提取纯化及反转录为保证RNA 提取效率一致,不同药物浓度处理的标本同时提取RNA。所用容器耗材均经0.1%DEPC 水浸泡24 h,121 ℃高压30 min处理,所有提取过程置于冰浴操作,提取过程遵照RNA 提取试剂盒说明书执行,获得的总RNA溶于20.0 μl DEPC水中。取10.0 μl 上述总RNA,加入2.0 μl 10×RT Buffer,0.8 μl 25×dNTP Mix(100 mM),2.0 μl 10X RT Random Primers,1.0 μl MultiScribe ™Reverse Transcriptase,1.0 μl RNase Inhibitor,3.2 μl DEPC 水配制成20.0 μl 反应体系,置于PCR 仪中,反应条件:25 ℃10min,37 ℃120 min,85 ℃5 min。
1.2.2.3 实时荧光定量PCRPCR 引物序列:正向5’GGTGATTGGCTTGCGATAGG3’,反向5’TGAATATCACCTCGGCCACA 3’,扩增片段长度152 bp,由北京六合华大基因科技有限公司生物合成。反应体系20.0 μl,包括TB Green Fast qPCR Mix 10.0 μl、正反向引物各0.8 μl、Rox Reference Dye 0.3 μl、cDNA模板1.0 μl以及灭菌水7.1 μl。反应条件:95 ℃30 s,95 ℃5 s,60 ℃15 s,40 个循环并设立溶解曲线阶段,每次反应设阴性、阳性对照。结果判读:扩增结束后,检查溶解曲线为单一峰,设定基线范围6.00~10.00,基线值0.01,判断扩增曲线呈S 形,读出cDNA的Ct值。
1.3 统计学分析 采用SPSS 26.0 软件进行统计学分析。数据经正态性检验,符合正态性分布,采用平均值、标准差等进行描述性统计。独立样本t检验比较不同处理组间的差异性。检验水准=0.05,P<0.05差异有统计学意义。
2 结 果
所有样本荧光定量PCR 检测均出现了典型的扩增曲线,无药处理组(C)mpt64 mRNA Ct 值为(25.34±2.56),0.2 μg/ml 异烟肼处理组(T1)mpt64 mRNA Ct 值为(29.09±3.25),0.5 μg/ml 异烟肼处理组(T2)mpt64 mRNA Ct 值为(30.14±3.23)。相较于无药对照组,0.2 μg/ml异烟肼处理组mpt64 mRNA 增加(3.75±2.68)个Ct 值,0.5 μg/ml 异烟肼处理组增加(4.80±2.33)个Ct 值,mpt64 mRNA 表达水平降低,与无药对照组比较差异均有统计学意义(t=-5.37、-6.89,均P<0.01)。0.2、0.5 μg/ml 两个处理组间差异无统计学意义(t=-1.36,P=0.18)。具体见表1、图1。
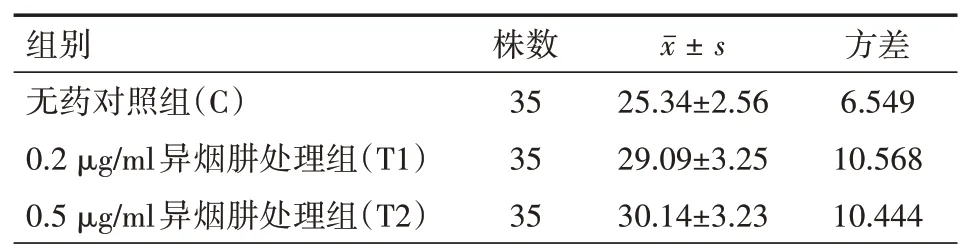
表1 35株对一线抗结核药物敏感的临床分离株不同处理组mpt64 mRNA实时荧光定量聚合酶链反应扩增Ct值

图1 35株对一线抗结核药物敏感的临床分离株不同处理组mpt64 mRNA实时荧光定量PCR扩增Ct平均值柱形图
3 讨 论
众所周知,临床上治疗结核病的方法是直接抗菌疗法[2],评价化疗疗效通常采用和诊断结核病相同的常规技术方法,包括细菌学、影像学、免疫学和分子生物学等方法[3-4],各自方法具有不同的实际价值。痰涂片抗酸杆菌镜检和结核分枝杆菌分离培养操作简便,设备费用要求低,是我国目前普及最广的方法,但痰涂片抗酸杆菌镜检并不能区分出死活菌,传统的改良罗氏培养法需要4~8 周时间,不能满足临床需要。胸部影像学检查(X 线胸片、CT 片)是发现和诊断肺结核的重要方法之一,能准确了解肺部病变部位的动态变化,尤其是对菌阴性肺结核[5-6]具有较高的敏感性,但肺部各种疾病的病变在胸部影像学检查上特异性较差,容易造成定性困难。
近些年来,随着免疫学技术与分子生物学的发展,各类分子标志物层出不穷,它们的高敏感度、高特异度和快速性给结核病的化疗监控带来新的期望。张雪等[7]、Tonby K等[8]的研究表明,血清干扰素诱导蛋白10(IP-10)可作为临床早期诊断活动性肺结核的检测指标,但Amanatidou V等[9]的研究表明,体内IP-10水平可能存在一定的年龄依赖性,儿童体液免疫功能跟成人不同,IP-10 在儿童结核诊断中仍存在很多问题。
目前临床上使用最广泛的荧光定量PCR 检测试剂盒大多数都是以IS6110 作为靶序列设计的,IS6110 作为结核杆菌DNA 基因组中一个多拷贝的保守片段,PCR 方法检测敏感度与特异度较好。但也有研究显示,PCR 方法检测易受如实验条件的设置、引物的设计、标本的类型不同和处理方法不同等多方面因素的影响,且有些菌株中缺乏IS6110,易造成假阴性结果。另外,结核分枝杆菌DNA 分子稳定,半衰期长,平台效应强,TB-DNA 不能区分活动性结核和潜伏性结核。
结核杆菌RNA 分子半衰期短,仅存在于活动性的菌体中,检测RNA 水平的变化用于结核病化疗疗效的监测[10-11]有着天然的优势。目前临床上使用最广泛的恒温扩增实时荧光检测技术(SAT)就是检测结核杆菌菌内核糖体RNA(rRNA),但研究表明,rRNA 分子稳定,具有平台效应且半衰期远大于mRNA。85B mRNA 编码结核杆菌85B 蛋白,特异性强[12],活菌细胞含量丰富,但相关研究显示,由于药物靶位效率不同,利福平对85B mRNA的表达量有着明显的抑制作用,产生出多药方案中利福平掩盖其他药物的预示作用。因此,上述标志物用于评价结核病化疗疗效监控均不理想。mpt64 mRNA 产生于结核杆菌合成mpt64 分泌蛋白时,由结核杆菌内的mpt64 基因编码并生成,属于活菌体中极为重要的一个组成部分,同时mpt64 mRNA 有较短的半衰期,其更新时间一般仅为数分钟。另外mpt64 蛋白只会存在于具有致病性的结核杆菌中,具有特异性。因此,有望通过监测mpt64 mRNA的变化,监测结核杆菌浓度的变化。
本研究结果显示,相对于无药处理组,异烟肼处理组结核杆菌mpt64 mRNA表达水平均低于无药处理组,0.2 μg/ml异烟肼处理组mpt64 mRNA 增加(3.75±2.68)个Ct 值,0.5 μg/ml 异烟肼处理组增加(4.80±2.33)个Ct 值,与无药处理组相比,差异均有统计学意义(均P<0.05),说明在短时间内,异烟肼可以抑制结核杆菌mpt64 mRNA的表达,mpt64 mRNA的分子表达水平与结核杆菌的活动情况有关;两个处理组间差异无统计学意义(P>0.05),说明结核杆菌mpt64 mRNA的表达水平与异烟肼药物浓度无关。
值得注意的是,有研究显示,mpt64 蛋白在部分结核杆菌中存在不表达的情况,导致假阴性的产生,其原因主要是mpt64 mRNA基因发生整体缺失和突变的情况,直接造成结核菌无法正常合成mpt64 mRNA[13]。本研究在引物的设计过程中,选择了比较保守的基因片段,对mpt64 mRNA的扩增均避开了易突变位点,不存在检测不到的情况,有效保障了检测结果的准确性与可靠性。
综上,mpt64 mRNA表达水平可在短时间内反映出药物对结核杆菌的作用效果,有望成为结核病化疗疗效监测的分子标志物,作为结核病化疗疗效评价的一个重要细菌学监控工具。本研究的不足之处是,未对结核杆菌药物敏感株进行更长时间的培养,缺少更长时间下mpt64 mRNA 变化情况的监测,在后续工作中会继续加强研究,如周期更长的临床标本验证以及与培养法检测结果的对比分析等,提供更为全面的数据支持。
利益冲突:作者已申明文章无相关利益冲突。
