光叶巴豆化学成分及其药理活性研究进展
2021-09-04韩正枝曹碧霞刘荣甘肃省精细化工重点实验室兰州730020甘肃省化工研究院有限责任公司兰州730020
韩正枝,曹碧霞,刘荣*(1.甘肃省精细化工重点实验室,兰州 730020;2.甘肃省化工研究院有限责任公司,兰州 730020)
大戟科巴豆属植物大约有1300 多种,主要分布于热带和亚热带地区[1]。巴豆属植物是结构多样性代谢产物的重要来源,具有重要的生物活性[2-3]。许多巴豆属植物被证明对癌症、糖尿病、便秘、发热、高血压等有一定的疗效[4-5]。光叶巴豆(大戟科)是中国特有的巴豆属植物[6],主要分布于云南、广东和海南三省,具有通经活血、散结消肿、退热止痛之功效,在中国傣族医学中被称为宝龙,长期以来被傣族人用来治疗骨折、疟疾和胃痛等疾病[6-7]。本文对光叶巴豆的化学成分、药理活性以及分离的色谱条件进行综述,以期为光叶巴豆的进一步开发研究奠定基础,也为相似类型化合物色谱分离条件的选择提供参考。
1 光叶巴豆中的化学成分[8-24]
研究表明二萜及其内酯、多酚类(鞣质)是巴豆属植物的主要化学成分,其他成分还包括三萜、黄酮及生物碱[5-7]。光叶巴豆的主要成分为半日花烷型二萜、松香烷型二萜、克罗烷型二萜、西松烷型二萜、其他类型的二萜类化合物、黄酮类化合物和单萜苷类化合物等。
1.1 半日花烷型二萜
半日花烷型二萜是目前从光叶巴豆中分离出数量较多的二萜类化合物,Huang 等[8]从云南光叶巴豆乙醇提取物中分离得到17 个半日花烷型二萜,其中16 个为新化合物;Liu 等[9]从海南光叶巴豆的乙醇提取物中分离得到7 个半日花烷型二萜,其中6 个为新化合物(化合物18 ~23)。化合物见表1和图1。
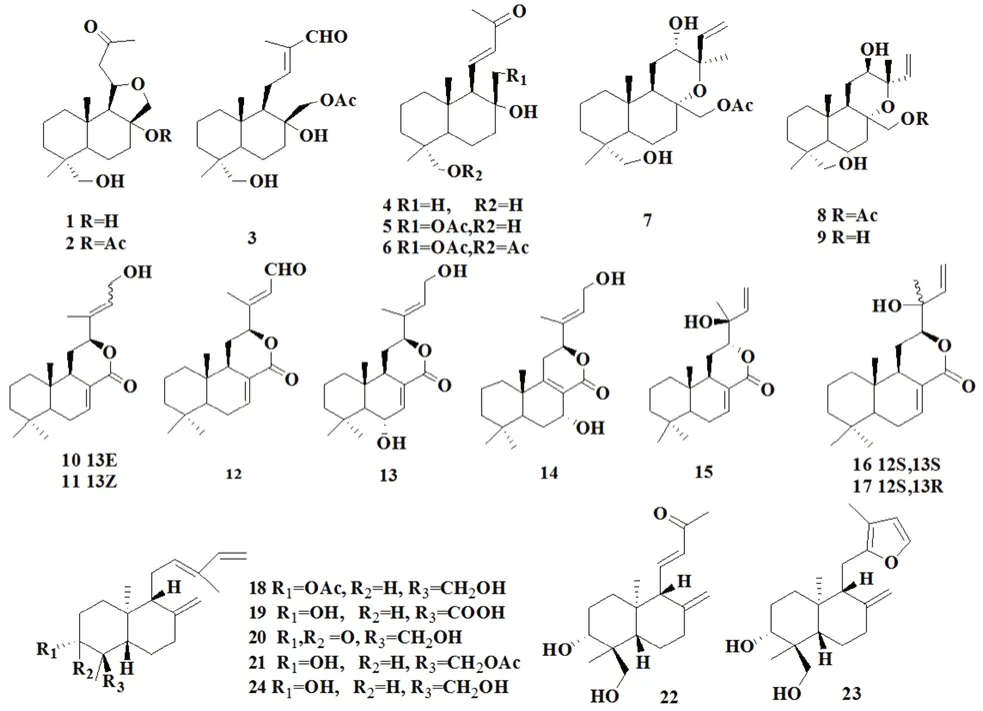
图1 光叶巴豆中的半日花烷型二萜类化合物Fig 1 Labdane-type diterpenoids in Croton laevigatus

表1 光叶巴豆中的半日花烷型二萜类化合物Tab 1 Labdane-type diterpenoids in Croton laevigatus
1.2 松香烷型二萜类化合物
Song 等[10]从云南光叶巴豆乙醇提取物中分离得到12 个单体化合物,其中7 个为松香烷型二萜,均为新化合物。化合物见表2和图2。
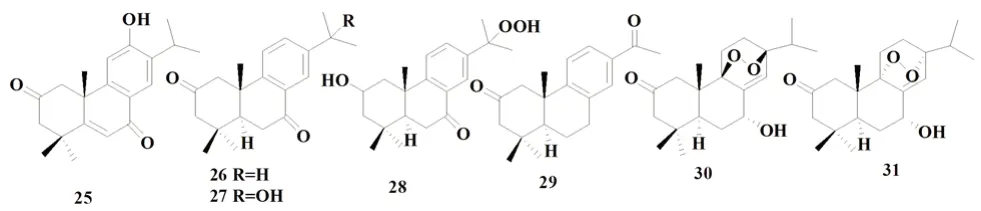
图2 光叶巴豆中的松香烷型二萜类化合物Fig 2 Abietane-type diterpenoids in Croton laevigatus

表2 光叶巴豆中的松香烷型二萜类化合物Tab 2 Abietane-type diterpenoids in Croton laevigatus
1.3 克罗烷型二萜类化合物
克罗烷型二萜也是从光叶巴豆中分离得到数量较多的化合物,Wang 等[11]从海南光叶巴豆的乙醇提取物中分离得到2 个新克罗烷型二萜;李昌松等[12]从云南光叶巴豆根的乙醇提取物中分离得到7 个单体化合物,其中4 个为克罗烷型二萜,均为首次从光叶巴豆中分离得到;Zhang 等[13]从广东省光叶巴豆的乙醇提取物中分离得到14 个单体化合物,其中8 个为克罗烷型二萜。化合物见表3和图3。
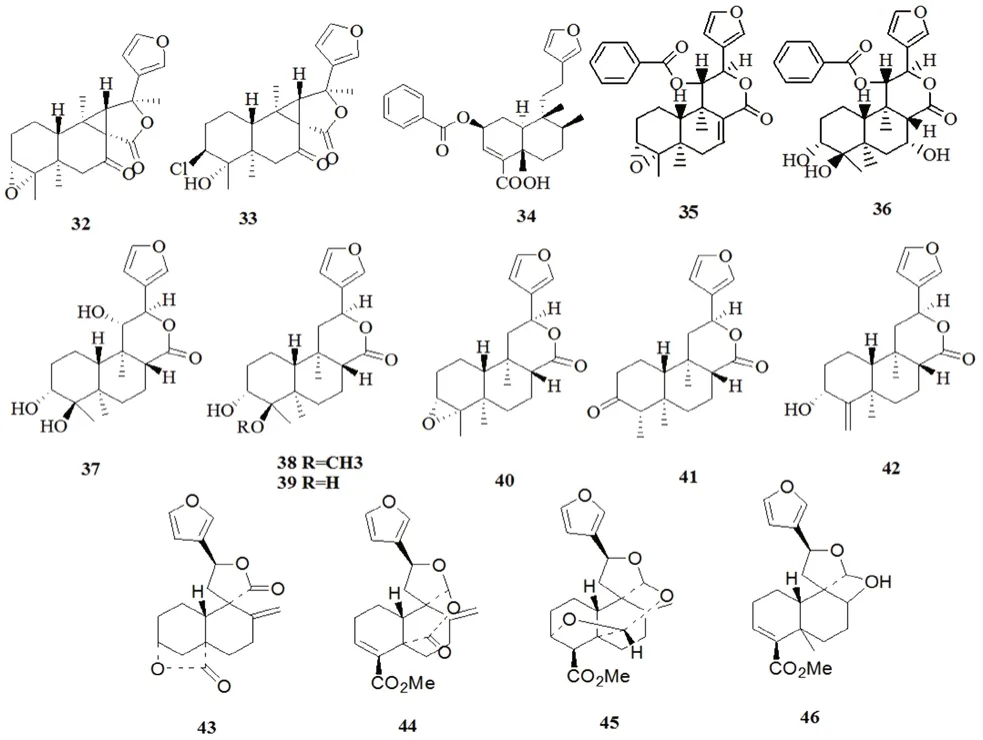
图3 光叶巴豆中的克罗烷型二萜类化合物Fig 3 Clerodane-type diterpenoids in Croton laevigatus

表3 光叶巴豆中的克罗烷型二萜类化合物Tab 3 Clerodane-type diterpenoids in Croton laevigatus
1.4 西松烷型二萜类化合物
Zou 等[17]从云南光叶巴豆的甲醇提取物中分离得到7 个化合物,其中6 个为新的西松烷型二萜类化合物(见表4和图4)。
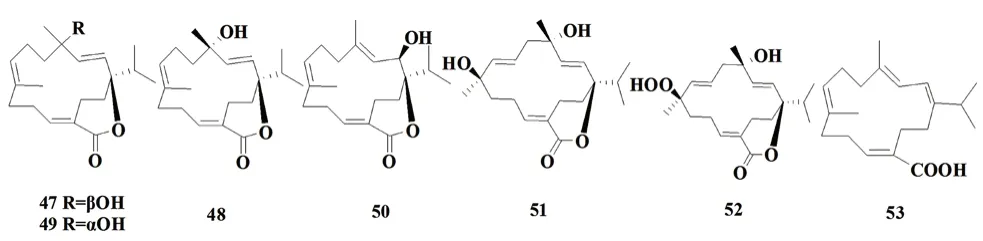
图4 光叶巴豆中的西松烷型二萜类化合物Fig 4 Cembrane-type diterpenoids in Croton laevigatus
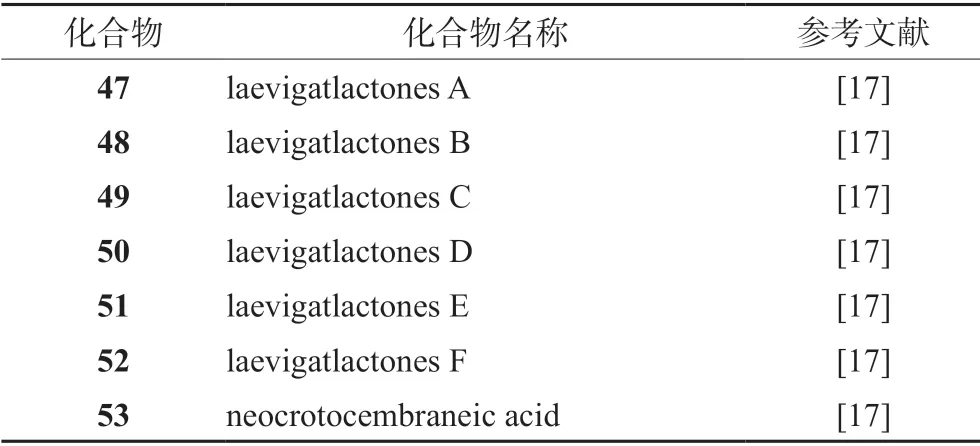
表4 光叶巴豆中的西松烷型二萜类化合物Tab 4 Cembrane-type diterpenoids in Croton laevigatus
1.5 其他类型的二萜类化合物
Li 等[18]从海南省的光叶巴豆乙醇提取物中分离得到5 种海松烷型二萜,其中1 个为新化合物,命名为Crolaevinoid A;Zhang 等[13]从广东光叶巴豆中分离得到14 个化合物,其中2 个为halimane 型二萜,2 个为laevinane 型二萜。化合物见表5和图5。
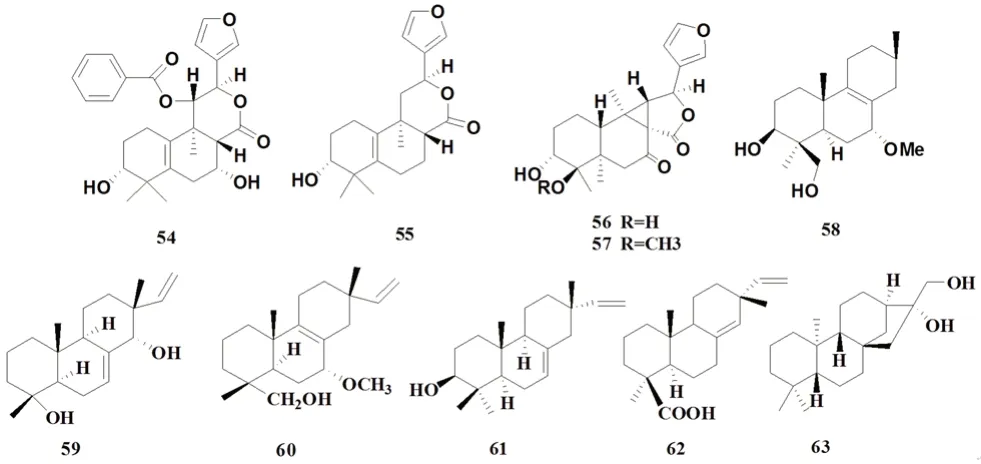
图5 光叶巴豆中其他类型的二萜类化合物Fig 5 Other diterpenoids in Croton laevigatus
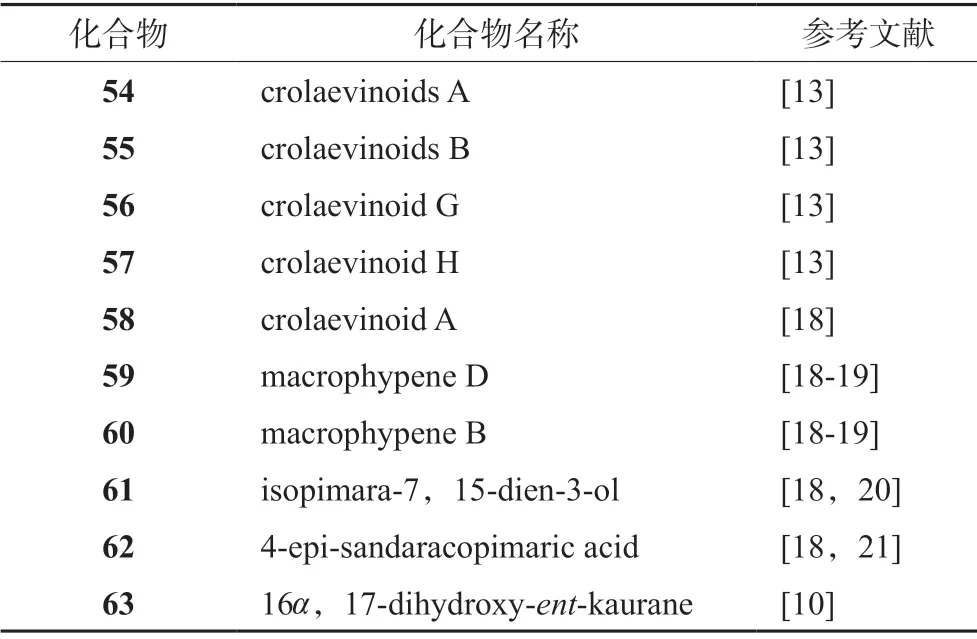
表5 光叶巴豆中的其他类型二萜类化合物Tab 5 Other diterpenoids in Croton laevigatus
1.6 其他类型的化合物
光叶巴豆中的成分除了二萜目前还分离得到其他类型的化合物,如黄酮类、单萜苷类、苯及其衍生物等(见表6)。

表6 光叶巴豆中的其他类型化合物Tab 6 Other compounds in Croton laevigatus
2 药理活性
Liu 等[9]从光叶巴豆中提取分离得到7 种化合物,并以齐墩果酸为阳性对照对蛋白酪氨酸磷酸酶1B(PTP1B)的抑制作用进行评价,发现化合物19 和化合物24 的抑制能力较强,其IC50值分别为4.11 μg·mL-1和8.33 μg·mL-1。
Song 等[10]从光叶巴豆中提取分离得到12 种化合物,并以阿霉素为对照对其抗癌细胞增殖作用进行评价,发现化合物26 和化合物31 有微弱的抗A549 和MDA-MB-231 细胞增殖作用,对A549 细胞的IC50值分别为21.2、25.6 μmol·L-1,对MDA-MB-231 细胞的IC50值分别为33.4、32.7 μmol·L-1,化合物63 对A549 细胞有明显的抑制活性,IC50值为9.8 μmol·L-1[10]。
Zhang 等[13]从光叶巴豆中提取分离得到14 种化合物,并以槲皮素为对照对所有化合物的NO 抑制作用进行评价,发现化合物39 和化合物40 能显著抑制NO 的产生,IC50值分别为(10.6±0.8)μmol·L-1和(6.0±1.0)μmol·L-1[13]。
邹国安等[22-25]从光叶巴豆中提取分离得到8种化合物,并对化合物的细胞毒活性进行评价,发现化合物34 和化合物48 对人宫颈癌细胞有弱的细胞毒活性,IC50值分别为45.4 μmol·L-1和38.4 μmol·L-1。
Fan 等[26]从巴豆属植物越南巴豆中分离得到了一种结构较新颖的高度重排的双桥螺旋形二萜Crokonoid A,其对HL-60 和A-549 具有显著的细胞毒性,IC50值分别为(1.24±0.56)μmol·L-1和(1.92±0.60)μmol·L-1。
Zhang 等[27]从巴豆属植物中分离得到两对大环二萜异构体mangelonoids A 和mangelonoids B,推测了其生源合成途径,其中(-)-mangelonoid A 对NF-κB 有抑制作用,其IC50值为(7.27±1.30)μmol·L-1。
3 化合物色谱分离条件和单晶培养条件
随着技术的发展,一些常规的天然产物提取方法如:硅胶柱层析、大孔树脂、葡聚糖凝胶色谱等不能满足学科发展需要,半制备型高效液相色谱越来越多被使用于单体化合物的分离。以下对分离光叶巴豆中化合物所应用的半制备型高效液相色谱条件进行分析总结[9-10,13],见表7。为了对类似化合物单晶培养条件的选择提供一定的指导,特将来自光叶巴豆并成功培养单晶的单体化合物及其培养条件进行整理,见表8。

表7 部分化合物高效液相色谱分离条件Tab 7 HPLC chromatographic conditions of some compounds
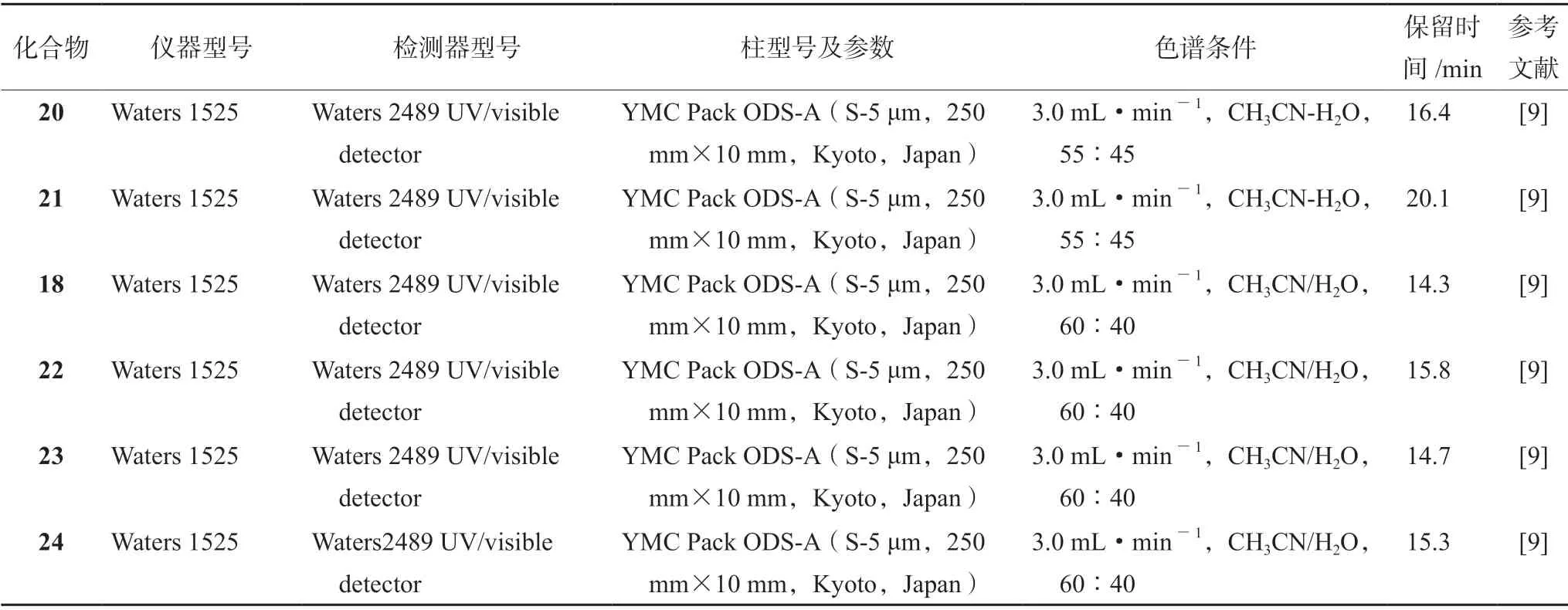
续表7
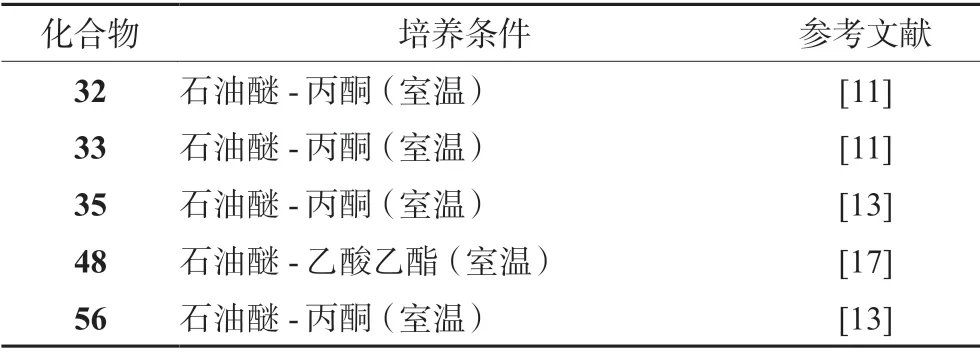
表8 部分化合物单晶培养条件Tab 8 Culture condition of some compounds in single crystal
单晶培养对于化合物结构和绝对构型的确定有重要意义,Zou 等[17]在石油醚-乙酸乙酯体系中成功培养出化合物48 的单晶。Wang 等[11]在石油醚-丙酮体系中成功培养出化合物32 和化合物33 的单晶。Zhang 等[13]在石油醚-丙酮体系中成功培养出化合物56 和35 的单晶。
4 结语和展望
光叶巴豆化学成分复杂多样,在抗癌、酶的抑制等方面活性较好,具有较大开发潜力。目前对光叶巴豆成分研究中单体化合物活性研究尚不成熟,应该向多方面拓展并进一步深入研究。对自光叶巴豆中分离得到的量大但活性表现不强的化合物进行衍生,研究其衍生物的应用,或将为药物分子及其先导化合物的发现提供更好的依据。
