奥卡西平导致的皮肤不良反应与HLA-B*1502、HLA-B*1301基因的关系
2021-09-03民福利王晓范翠霞郭静秦兵
民福利 王晓 范翠霞 郭静 秦兵
1广州市第一人民医院神经内科(广州510000);2暨南大学附属第一医院神经外科癫痫中心(广州510000);3广州医科大学附属第二医院神经科学研究所(广州510260);4广东三九脑科医院癫痫中心(广州510510)
奥卡西平(oxcarbazepine,OXC)是新型抗癫痫药物(antiepileptic drugs,AEDs),可用于治疗原发性全面性强直阵挛发作和部分性发作,伴或不伴继发性全面性发作,奥卡西平还可改善成人颞叶癫痫患者的认知障碍[1-2]。奥卡西平的分子结构、作用机制、临床疗效与卡马西平(carbamazepine,CBZ)相似,属于卡马西平的10-酮基衍生物,皮肤型药物不良反应(cutaneous adverse drug reactions,cADRs)是其常见不良反应之一,发生率为4% ~9%[3-4],易导致患者中断药物治疗[5]。尽管cADRs的具体机制尚不清楚,研究表明人类白细胞抗原(human leukocyte antigen,HLA)与cADRs 相关,中国汉族人群中HLA-B*1502 是卡马西平导致的Stevens-Johnson 综合症(SJS)/中毒性表皮坏死松解症(toxic epidermal necrolysis,TEN)遗传标志物[6],HLA-B*1301 可能与抗癫痫药物导致的皮肤型交叉反应相关[7]。鉴于奥卡西平与卡马西平在结构上相似,学者们陆续开展HLA 基因与奥卡西平导致cADRs 的关系研究,但因奥卡西平导致皮疹的发生率较低,目前相关的报道多为单中心的研究,本研究联合多中心采集样本探讨奥卡西平导致的cADRs 与HLA-B*1502、HLA-B*1301 基因的关系。
1 对象与方法
1.1 研究对象 本研究采用病例对照研究方法。本研究获得医院伦理委员会的批准。研究对象分为病例组、耐受对照组和正常对照组,所有入组对象均为汉族人群。
1.1.1 病例组 选取2017年1月至2020年12月服用奥卡西平后出现皮肤型不良反应患者为病例组,患者来源于广州市第一人民医院、广州医科大学附属第二医院、暨南大学附属第一医院和广东三九脑科医院。病例组纳入标准:患者首次服用奥卡西平,具有一定的潜伏期(1 ~60 d),经皮肤科医师诊断,符合药疹的诊断和分型标准,轻度斑丘疹(maculopapular exanthem,MPE)的临床特点为颗粒样斑丘疹,停服过敏药物后3 ~14 d 自行消失;重症皮疹的临床特点为水泡或大泡样皮疹,快速进展融合成片或表皮脱落,口腔或生殖器黏膜糜烂,表皮脱落或黏膜糜烂面积占体表面积<10%称为SJS;>30%称为TEN;介于10%~30%之间称为SJS 和TEN 重叠(SJS/TEN)[8]。排除标准:患者服用奥卡西平前2个月首次服用以下药物:卡马西平、拉莫三嗪、苯妥英钠、苯巴比妥。
1.1.2 耐受对照组 选取服用奥卡西平后至少3个月内未出现cADRs 的患者为耐受对照组。
1.1.3 正常对照组 随机选取2017年1月至2020年12月来广州医科大学附属第二医院体检的健康人群(既往未服用抗癫痫药物)作为正常对照组。
1.2 HLA 高分辨率基因分型 抽取每位受试者静脉血(约4 mL)置于EDTA 抗凝管,使用外周血基因组DNA 提取试剂盒(QIAamp DNA Blood Mini Kit,德国)抽提DNA。调整DNA 浓度后置于-80 ℃冰箱保存。PCR 扩增HLA-B 基因的DNA 片段所用的引物由上海生工生物工程有限公司合成,序列如下:BF(ACCCACCCGGACTCARARTCTCCT)和BR(CACTCTAGACCCCAAGAATCTCACCTTTT);使用ABI 3730 测序仪(美国)和vector NTI 6.0(美国)对HLA-B 基因进行测序和序列比对。
1.3 统计学方法 采用SPSS 25.0统计分析。计量资料用()表示,采用t检验;HLA-B*1502、B*1301基因的阳性率用直接记数法进行计算,计数资料比较用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 三组的一般资料比较 病例组、耐受对照组、正常对照组分别纳入15 例奥卡西平导致cADRs患者、64 例奥卡西平耐受的患者、100 例健康体检者。病例组中男8 例,女7 例,年龄为12 ~68 岁;耐受对照组中男34 例,女30 例,年龄11 ~69 岁;健康对照组中男58 例,女42 例,年龄18 ~65 岁。性别比、平均年龄在病例组和耐受对照组、病例组和正常对照组之间差异无统计学意义(P>0.05)。
2.2 治疗效果 病例组中14 例奥卡西平导致MPE 患者的皮疹主要分布于躯干和四肢,呈淡红色颗粒状,部分患者的皮疹突出表面,其中5例患者出现发热,但体温<38.5 ℃,8例患者出现皮肤瘙痒;奥卡西平导致MPE 组的过敏潜伏期最短为2 d,最长为26 d,平均潜伏期为(11.57±8.72)d,出现皮疹时奥卡西平平均剂量为(630.00 ± 235.13)mg/d;所有患者均在停用奥卡西平1周后皮疹自行消退。奥卡西平的起始剂量、最大剂量在病例组和耐受对照组之间差异无统计学意义(P>0.05),见表1。
表1 奥卡西平导致皮肤不良反应组与奥卡西平耐受对照组及正常对照组的临床资料比较Tab.1 Comparison of clinical character between OXC-induced cADRs group and OXC-tolerant group,as well as normal control group ±s
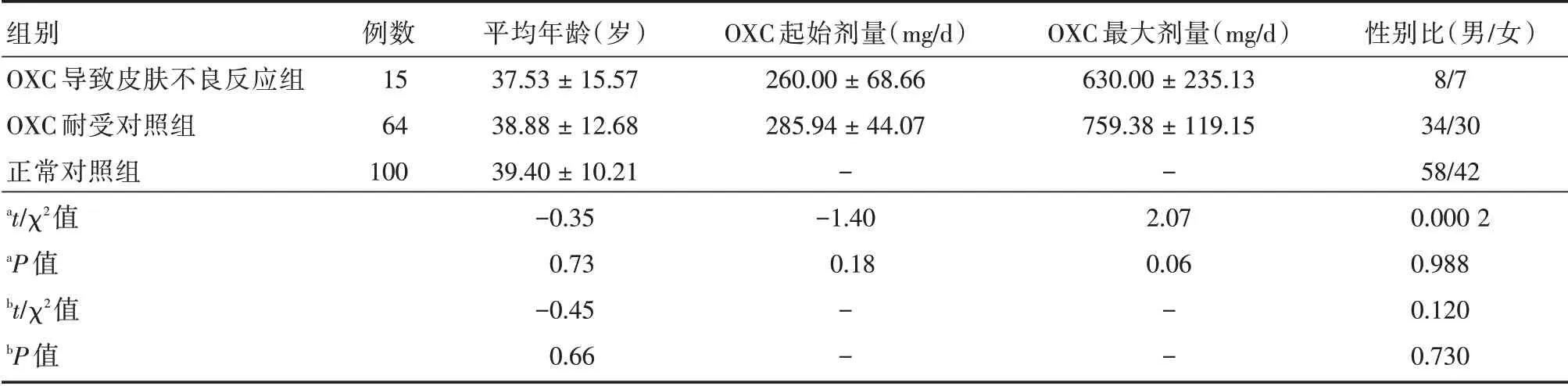
表1 奥卡西平导致皮肤不良反应组与奥卡西平耐受对照组及正常对照组的临床资料比较Tab.1 Comparison of clinical character between OXC-induced cADRs group and OXC-tolerant group,as well as normal control group ±s
注:OXC,奥卡西平;a,OXC 导致皮肤不良反应组与OXC 耐受对照组比较;b,OXC 导致皮肤不良反应组与正常对照组比较
组别OXC 导致皮肤不良反应组OXC 耐受对照组正常对照组at/χ2值aP 值bt/χ2值bP 值例数15 64 100平均年龄(岁)37.53±15.57 38.88±12.68 39.40±10.21-0.35 0.73-0.45 0.66 OXC 起始剂量(mg/d)260.00±68.66 285.94±44.07--1.40 0.18--OXC 最大剂量(mg/d)630.00±235.13 759.38±119.15-2.07 0.06--性别比(男/女)8/7 34/30 58/42 0.000 2 0.988 0.120 0.730
2.3 HLA-B*1502 基因与奥卡西平导致皮肤不良反应的关系 病例组中,仅有1 例患者的药疹表型为SJS/TEN,该患者携带HLA-B*1502 基因;HLAB*1502 在奥卡西平导致MPE 组、耐受对照组和正常对照组中的阳性率分别为14.29%(2/14)、10.94%(7/64)和13%(13/100),奥卡西平导致MPE组与耐受对照组、奥卡西平导致MPE 组与正常对照组之间HLA-B*1502 的阳性率差异均无统计学意义(P>0.05)。
2.4 HLA-B*1301 基因与奥卡西平导致MPE 的关系 奥卡西平导致MPE 患者中,6 例为HLA-B*1301 基因阳性(6/14);耐受对照组患者中,9 例为HLA-B*1301 基因阳性(9/64);正常对照组HLAB*1301 基因阳性率为12%(12/100),奥卡西平导致MPE 组的HLA-B*1301基因阳性率显著高于耐受对照组及正常对照组,差异有统计学意义(P<0.05),见表2。
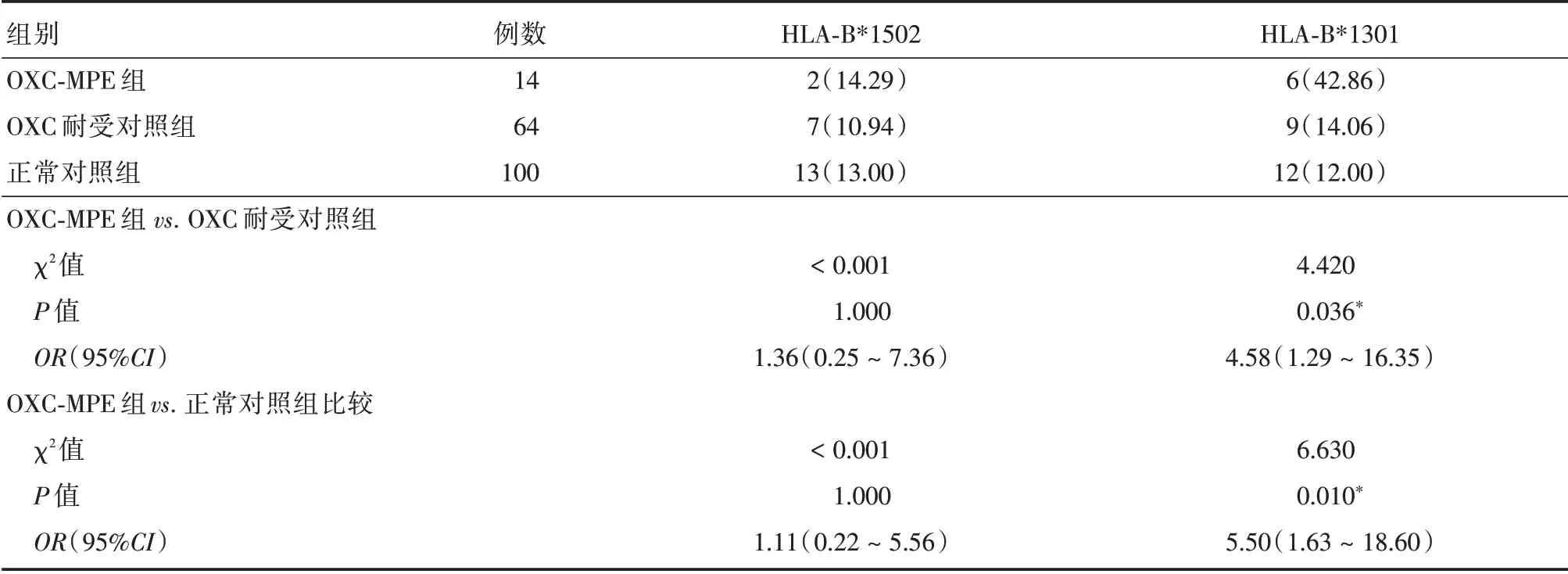
表2 HLA-B*1502、HLA-B*1301 与奥卡西平导致轻度斑丘疹的关系Tab.2 Association between HLA-B*1502,HLA-B*1301 allele and oxcarbazepine-induced MPE例(%)
2.5 典型病例 病例组中1 例为奥卡西平导致的SJS/TEN,该患者为男性,12 岁,被诊断为“额叶癫痫”,服用奥卡西平的起始剂量为300 mg/d,服药后第10 天面部及全身出现红色颗粒疹,伴发热,第12 天出现眼结膜充血、口腔黏膜破溃糜烂、面部及全身皮疹融合成暗红色片状,部分皮疹呈现为清亮水泡,体温高达38.9 ℃,给予口腔清洁、抗过敏和抗炎、皮肤护理等支持治疗,体温逐渐恢复正常,皮肤水泡吸收、结痂最后脱落,皮损部位残留色素沉着。
3 讨论
癫痫是神经科常见疾病之一,目前主要采用药物治疗。携带苯环结构的芳香族抗癫痫药物如卡马西平、拉莫三嗪、奥卡西平、苯妥英钠、苯巴比妥较为常用,但药物导致的皮肤不良反应常导致患者停药或撤药[9]。药物导致的皮肤不良反应是特异性、无法预测的过敏反应,与药物剂量无关,其包括轻度的斑丘疹、超敏反应以及重症皮肤不良反应如SJS、TEN。
目前药物导致皮肤不良反应的发病机制尚不明确,研究显示HLA与药疹相关。HLA基因是已知最复杂的基因复合体,位于第6 号染色体短臂6p21.3 区域,主要功能是将外来抗原或自身抗原呈递给T细胞,使T细胞活化,启动免疫应答。大量研究[6,10]表明亚洲人群中HLA-B*1502 是卡马西平导致SJS/TEN的强遗传标记物,据此美国FDA 建议亚洲人群服用卡马西平前筛查HLA-B*1502 基因,且携带该基因的患者禁止服用卡马西平[11-12]。奥卡西平是新一代的抗癫痫药物,是卡马西平的结构类似物,两者存在交叉过敏现象,25%~30%的卡马西平过敏患者再次暴露奥卡西平亦出现过敏[13]。研究表明,相比卡马西平,奥卡西平导致SJS/TEN临床严重程度较轻,且发生率较低[14-15]。
本研究中1 例奥卡西平导致的SJS/TEN 携带HLA-B*1502,这与既往的研究结果相似。CHEN等[14]对中国台湾地区汉族人群、泰国人群的研究结果显示HLA-B*1502 与奥卡西平导致的SJS/TEN相关。一项荟萃分析显示HLA-B*1502 与奥卡西平导致的重症皮疹相关[16]。这些研究结果提示HLA-B*1502 是奥卡西平导致的SJS/TEN 的遗传标志物,汉族人群中HLA-B*1502 的频率为1.5% ~12.8%,而日本人群和欧洲人群中的频率仅为0.3%和0 ~0.2%(http://www.allelefrequencies.net),这提示HLA 与奥卡西平导致SJS/TEN 的关系具有种族特异性。
本研究未发现HLA-B*1502 与奥卡西平导致的轻度皮疹相关。目前HLA-B*1502与奥卡西平导致MPE 关系的研究结果存在分歧,有研究[17-19]表明HLA-B*1502 与奥卡西平导致的MPE 不相关,但HU 等[20]报道显示HLA-B*1502 与奥卡西平导致的MPE 相关。结果的不一致可能与每个研究中纳入样本量有限有关,也可能是多基因共同参与药疹的发病机制,HLA 基因频率在人群中具有种族多样性,不同人群对药物易感性存在差异,如研究显示韩国人群中HLA-B*4002 和DRB1*0403 与奥卡西平导致的MPE 相关[21],汉族人群中HLA-B*3802、HLA-A*3201 和HLA-DRB1*0406 可能与奥卡西平导致的MPE 相关[17-19]。
本研究显示HLA-B*1301与奥卡西平导致MPE相关。近期研究表明汉族人群中HLA-B*1301 与抗癫痫药物导致的皮肤型交叉反应相关[7]。既往研究报道氨苯砜导致超敏反应[22]、三氯乙烯导致的皮炎[23]及柳氮磺胺吡啶导致伴有嗜酸性粒细胞增多症的药疹[24]均与HLA-B*1301 相关。这提示HLA-B*1301 可能参与多种药物导致皮肤不良反应的发病机制。目前HLA 基因如何参与药疹的发病机制尚不明确。研究表明,药物、HLA 基因、HLA 抗原结合肽及T 细胞受体等均参与药疹的发病机制,有学者认为药物与特异性HLA 分子结合后改变了抗原结合槽的结构,从而改变抗原性和诱发细胞毒性T 细胞免疫应答[9,25]。
综上所述,本研究结果提示汉族人群中HLAB*1502 可能与奥卡西平导致SJS/TEN 相关,HLAB*1301 可能与奥卡西平导致MPE 相关,因样本量有限,有待大样本研究和荟萃分析验证;此外,HLA 基因通过何种方式启动皮肤药物不良反应免疫应答还需后续实验研究探讨。
