越橘提取物中花色苷及游离花青素的测定
2021-09-03程益清
毛 丹,冯 睿,程益清,胡 青,季 申
(上海市食品药品检验所 国家药品监督管理局中药质量控制重点实验室,上海 201203)
越橘 (Vaccinium myrtillus),是一类生有浆果的多年生落叶或常绿灌木或小灌木树种[1],为杜鹃花科越橘属植物[2-4]。该属植物全世界约有300多种,我国约有60余种。越橘主要生长于欧洲、俄罗斯、北美和阿尔卑斯山海拔 1500~2000 m处,其中欧洲越橘(Vaccinium myrtillusL.)因富含花色苷,具有较强的抗氧化能力,作为保健食品原料已被消费者广泛认可[5]。越橘提取物是以欧洲越橘的新鲜果实为原料经加工而制成的提取物[6],其功效显著、应用范围广、副作用低,近年已广泛应用于保健食品与药品中[7]。
越橘提取物主要含花色苷活性成分,另外还含多糖、果胶、单宁等成分[8]。花色苷是由花青素与糖结合而成的一类物质的统称,因其基本骨架结构(图1)与2-苯色原酮结构十分相似,故花色苷类化合物也统称为黄酮类化合物。花青素是2-苯基苯并吡喃阳离子的多羟基和甲基衍生物,已有研究表明,越橘提取物中花青素主要为锦葵素、飞燕草素、矢车菊素、矮牵牛素、芍药素5种[9]。因花青素中存在共轭双键,能吸收可见光而呈现一定的颜色。其化学结构中黄烊盐阳离子缺乏电子,游离的花青素极不稳定,越橘提取物中花青素主要为糖苷形式,所结合的糖主要是葡萄糖、阿拉伯糖和半乳糖。本研究测定了越橘提取物中游离花青素及花色苷的含量,以期达到工艺及质量控制的目的。

图1 花色苷基本骨架结构
1 仪器与试药
1.1 仪器
Agilent 1100高效液相色谱仪(美国安捷伦),配有紫外-可见光检测器,ChemStation色谱工作站;Sartorius电子天平(梅特勒-托利多)。
1.2 试药
矢车菊素-3-O-葡萄糖苷对照品(上海诗丹德标准技术服务有限公司);矢车菊素(欧洲药典对照品);越橘提取物样品(批号:Q20200903-1,Q20200903-2,Q20200903-3,Q20200903-4,Q20200903-5,Q20200903-6,Q20200903-7,Q20200903-8,Q20200903-9,Q20200903-10,浙江天草生物科技股份有限公司);甲醇,乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 游离花青素的测定
2.1.1 色谱条件 安捷伦Zorbax Extend-C18色谱柱(4.6 mm×250 mm,5 μm);流动相A:甲酸-水(8.5:91.5,v/v),流动相B:乙腈-甲醇-甲酸-水(22.5:22.5:8.5:41.5,v/v/v/v),按表1进行梯度洗脱;流速1.0 ml/min,检测波长535 nm;柱温30 ℃;进样量10 μl。理论板数按矢车菊素计应不低于5000,见图2。
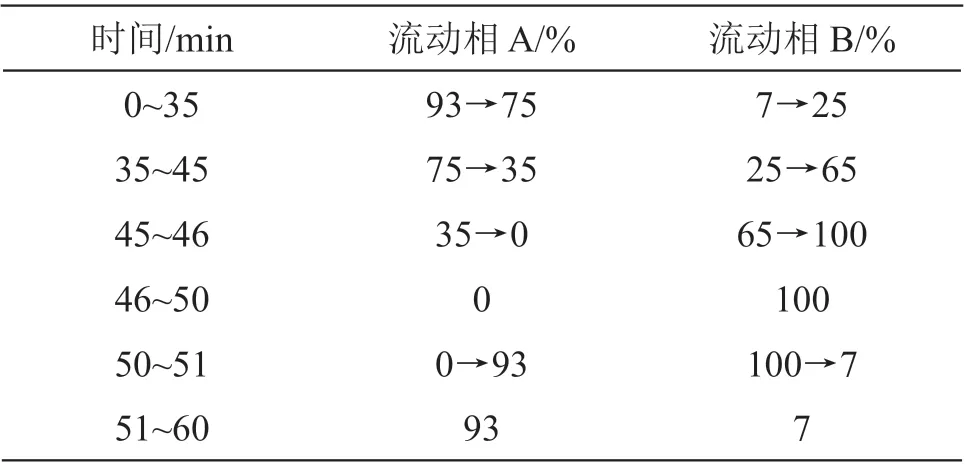
表1 梯度洗脱程序

图2 HPLC图谱
2.1.2 溶液的制备
2.1.2.1 对照品溶液的制备 精密称取矢车菊素对照品(精确至0.01 mg),加2 %盐酸甲醇溶液制成每1 ml含0.25 mg的溶液。精密量取2 ml上述溶液于100 ml量瓶中,加10 %磷酸水溶液稀释并定容至刻度,摇匀,即得。
2.1.2.2 供试品溶液的制备 称取试样125 mg(精确至0.1 mg),置100 ml量瓶中,加2 %盐酸甲醇溶液25 ml,超声使溶解,再用10 %磷酸水溶液稀释并定容至刻度,摇匀,即得。
2.1.3 线性关系考察 精密吸取矢车菊素对照品溶液(4.75 μg/ml)1,2,5,10 μl,矢车菊素对照品溶液(47.52 μg/ml)2,5,10 μl,注入液相色谱仪,记录峰面积。以进样量(ng)为横坐标,峰面积为纵坐标,绘制标准曲线。回归曲线方程为Y=5.2407X+4.0747,r=1.0000。结果表明,矢车菊素在4.75~475.24 ng范围内,进样量与峰面积线性关系均良好。
2.1.4 稳定性试验 精密吸取同一供试品溶液,4 ℃时分别于0,4,12,18,28 h进样分析,记录峰面积,计算RSD为0.7 %。表明供试品溶液保持其温度为4 ℃时在0~28 h内基本稳定。
2.1.5 精密度试验 精密吸取矢车菊素对照品溶液(4.75 μg/ml)10 μl,连续进样6次,记录峰面积,计算RSD为1.2 %。表明仪器精密度良好。
2.1.6 重复性试验 称取同一样品6份,按2.1.2.2项方法制备供试品溶液,进样分析,记录色谱图,测定矢车菊素的含量,计算RSD为0.7 %。表明方法的重复性良好。
2.1.7 加样回收率试验 取已知含量的样品,一式9份,以3份为一组,分别加入矢车菊素对照品溶液(浓度为475.24 μg/ml)适量,再按2.1.2.2项方法平行操作,进样分析,测定各自含量并计算加样回收率。结果见表1。
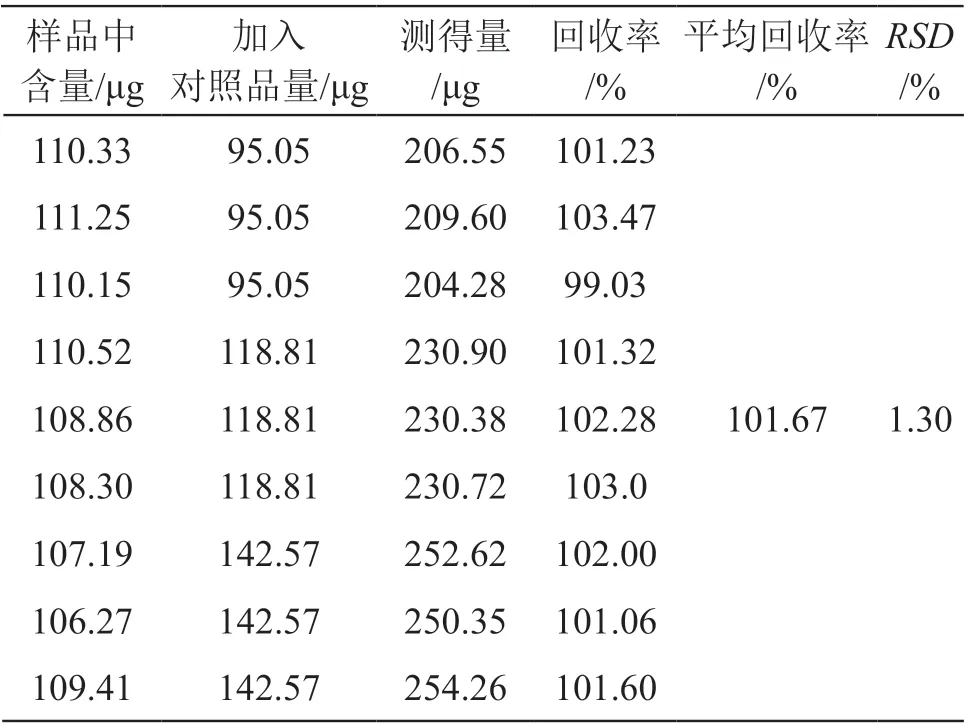
表1 加样回收率试验结果(n=9)
2.1.8 定量限与检出限 将矢车菊素对照品溶液(4.75 μg/ml)逐级稀释,按2.1.1项下色谱条件进样,记录色谱图,直至信噪比为10:1和3:1,对应浓度即分别为定量限和检出限。游离花青素的定量限(以矢车菊素计)为5.0 ng;检出限(以矢车菊素计)为1.5 ng。
2.1.9 样品测定 取样品,一式2份,按2.1.2.2项下供试品溶液的制备方法制备供试品溶液,另取2.1.2.1项下对照品溶液,分别精密吸取上述对照品溶液与供试品溶液各10 µl,采用外标法计算校正因子进行测定,平均测定结果见表2

表2 样品中矢车菊素含量测定结果
2.2 花色苷的含量测定
2.2.1 色谱条件 同2.1.1项下色谱条件。理论板数按矢车菊素-3-O-葡萄糖苷计应不低于5000,见图1。
2.2.2 溶液的制备
2.2.2.1 对照品溶液的制备 精密称取矢车菊素-3-O-葡萄糖苷标准品(精确至0.01 mg),加2 %盐酸甲醇溶液制成每1 ml含0.25 mg的溶液。精密量取2 ml上述溶液于10 ml量瓶中,加10 %磷酸水溶液稀释并定容至刻度,即得。
2.2.2.2 供试品溶液的制备 同2.1.2.2项下方法。
2.2.3 线性关系考察 精密吸取矢车菊素-3-O-葡萄糖苷对照品溶液(51.03 μg/ml)1,2,5,10 μl,矢车菊素-3-O-葡萄糖苷对照品溶液(510.32 μg/ml)2,5,10 μl,注入液相色谱仪,记录峰面积。以进样量(ng)为横坐标,峰面积为纵坐标,绘制标准曲线。回归曲线方程为Y=2.3399X+8.331,r=1.0000。结果表明,矢车菊素-3-O-葡萄糖苷在51.03~5103.24 ng范围内,进样量与峰面积线性关系均良好。
2.2.4 稳定性试验 精密吸取同一供试品溶液,4 ℃下分别于0,4,12,18,28 h进样分析,记录峰面积,计算RSD为0.3 %。表明供试品溶液保持其温度为4 ℃时在0~28 h内基本稳定。
2.2.5 精密度试验 精密吸取矢车菊素-3-O-葡萄糖苷对照品溶液(51.03 μg/ml)10 μl,连续进样6次,记录峰面积,计算RSD为0.2 %。表明仪器精密度良好。
2.2.6 重复性试验 称取同一样品6份,按2.1.2.2项方法制成供试品溶液,进样分析,记录色谱图,测定矢车菊素-3-O-葡萄糖苷的含量,计算RSD为0.3 %。表明方法的重复性良好。
2.2.7 加样回收率试验 取已知含量的样品,一式9份,以3份为一组,分别加入矢车菊素-3-O-葡萄糖苷对照品溶液(浓度为1.2758 mg/ml)适量,再按2.1.2.2项方法平行操作,进样分析,测定各自含量并计算加样回收率。结果见表3。

表3 加样回收率试验结果(n=9)
2.2.8 样品测定 取样品,一式2份,按2.1.2.2项下方法制备供试品溶液,另取2.2.2.1项下对照品溶液,分别精密吸取上述对照品溶液与供试品溶液各10 µl,采用外标法计算校正因子进行测定,平均测定结果见表4。

表4 样品中矢车菊素-3-O-葡萄糖苷含量测定结果
3 讨论
3.1 背景
越橘提取物是以欧洲越橘(Va c c i n i u m myrtillusL.)的新鲜冷冻果实为原料经提取加工而成的提取物,主要含花色苷活性成分。越橘提取物在欧美日等发达国家市场很大,是欧洲药典(EP)、美国药典(USP)及英国药典(BP)中收录品种。我国医药保健品进出口商会参考EP和USP,并结合国内越橘提取物的特殊情况,制订了越橘提取物国际商务标准,用于指导越橘提取物的出口质量控制。但越橘并不是传统的中药材,中国药典中未收录,也无相关的国家食品原料标准收录。因此,为保障国家外贸经济运行的安全和我国人民群众的食品卫生安全,加强标准建设,促进与国际标准对接,建立符合我国国情的越橘提取物国家质量标准具有重要的现实意义。
3.2 越橘提取物制备工艺
越橘提取物中主要活性成分花色苷为水溶性物质,易溶于甲醇、乙醇、水或它们所组成的混合溶液,不溶于石油醚、乙醚等非极性溶剂。提取花色苷的方法主要有热水提取法、醇提法、超临界流体萃取等。其纯化方法也有多种,如纸层析法、毛细管电泳法及较为经典的柱层析法等。
USP、EP和BP中越橘提取物提取采用醇提或水提,纯化可采用离子交换层析法。同时对我国越橘提取物的部分生产企业进行了调研,结果表明,目前国内在越橘提取物工业化生产中多采用醇提或水提法,而纯化方法则多采用大孔树脂精制方式。本实验收集的越橘提取物样品均采用水提取大孔树脂精制的制备工艺。
3.3 物质基础研究与分析
采用液相色谱-高分辨质谱对越橘原料和越橘提取物进行了物质基础研究,结果用于指导标志性成分项目的建立。分别采用正离子及负离子模式对越橘对照提取物溶液及两份供试品溶液扫描,结果其均在正离子模式下色谱峰信息量较多,故最终选择正离子模式扫描。
根据越橘对照提取物品质证书中所标示的各花色苷或花青素色谱峰的精确分子量、保留时间及二级碎片确证,对比分析越橘原料及越橘提取物供试品溶液,结果越橘提取物中检测到15种花色苷成分及5种游离花青素成分共20种化合物,而越橘原料中则仅检测到15种花色苷成分。
越橘中花青素少以游离态的形式出现,常与葡萄糖、阿拉伯糖、半乳糖等通过糖苷键形成花色苷。而越橘提取物主要保健功效为抗氧化、保护视力,起作用的活性成分为花色苷,故将15种花色苷设定为其标志性成分项。另由越橘提取加工制成的越橘提取物在工艺制备或贮存中会有降解现象,故设定游离花青素作为理化指标项进行控制。
3.4 色谱柱和柱温的选择
本研究对比了Zorbax Extend-C18(4.6 mm×250 mm,5 μm)、Zorbax SB-C18(4.6 mm×250 mm,5 μm)、Kromasil 100-5-C18(4.6 mm×250 mm,5 μm)作为目标物的预选分离柱,同时比较了3个不同柱温(30,25,20 ℃)。结果表明,采用色谱柱Zorbax Extend-C18(4.6 mm×250 mm,5 μm)和柱温30 ℃、色谱柱Zorbax SB-C18(4.6 mm×250 mm,5 μm)和柱温25 ℃、色谱柱Kromasil 100-5-C18(4.6 mm×250 mm,5 μm)和柱温30 ℃,花色苷及游离花青素各目标峰分离效果差别不大,均能满足检测要求。实验室可根据具体情况择优选取色谱柱及柱温。
3.5 流动相的选择及洗脱方式的确定
本研究参考欧洲药典(EP 10.0)中越橘提取物的含量测定项下流动相的选择及洗脱方式,对于洗脱方式也尝试了调整水相及有机相的不同比例,发现调整比例后花色苷及游离花青素各目标峰的分离效果均不及原洗脱方式,故最终确定流动相为A:甲酸+水(8.5:91.5,v/v),B:乙腈+甲醇+甲酸+水(22.5:22.5:8.5:41.5,v/v/v/v),洗脱方式同2.1.1项。
3.6 进样溶液温度的选择
本研究考察了供试品溶液的稳定性,发现常温放置1 h的供试品溶液就会出现花色苷成分含量降低,游离花青素含量增加的现象,故选择冷藏(4 ℃)供试品溶液,24 h时内各花色苷峰峰面积及游离花青素峰峰面积均基本稳定。
本研究建立了HPLC法同时测定越橘提取物中花色苷类成分及游离花青素的含量,该方法简便可行,精密度良好,准确度高,可有效控制越橘提取物的质量。
