以多流域脑梗死为特征的肺癌继发特鲁索综合征1例并文献复习
2021-09-03曹香琪霍康宋文峰罗国刚屈秋民
曹香琪,霍康,宋文峰,罗国刚,屈秋民
1 病例介绍
患者女性,63岁,以主诉“咳嗽、咳痰1月余,双下肢无力1天”于2020年10月30日入住胸外科,于2020年11月7日转入神经内科。患者1个月余前无明显诱因出现咳嗽、咳痰,为少量白色泡沫样痰,痰中无带血,行胸部CT见右肺上叶后段软组织团块影,边界不规则,可见毛刺及分叶,增强扫描见双期不均匀渐进性强化(图1),诊断为“右肺上叶癌”,于2020年11月5日行胸腔镜下肺癌根治术,术后病理报告为浸润性中-低分化腺癌(图2)。术后次日(2020-11-06)于活动中突然出现双下肢无力,伴大汗、面色苍白,随后出现嗜睡,行头颅CT检查示右侧额顶叶大面积脑梗死(图3),立即转入神经内科治疗。既往高血压病史。
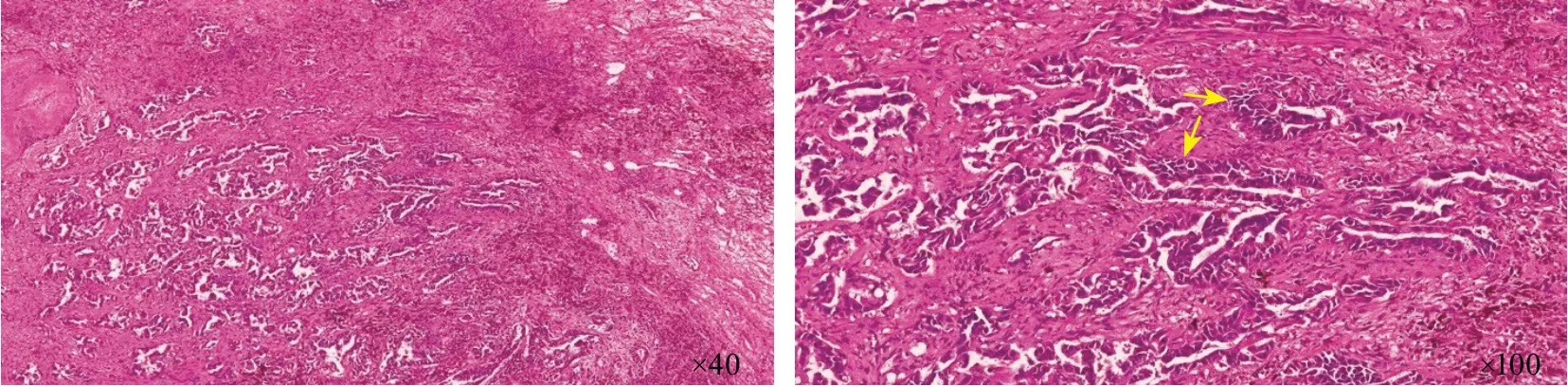
图2 肺癌病理报告结果
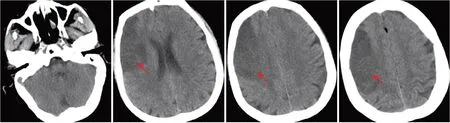
图3 卒中发病次日患者头颅CT检查结果
入神经科查体:血压160/85 mm Hg(1 mm Hg=0.133 kPa),GCS评分14分,NIHSS评分8分,嗜睡,呼之可应,简单问答配合,双眼向右侧凝视,左眼外展及右眼内收轻度受限,左侧额纹浅,左侧眼裂变小,左侧鼻唇沟浅,伸舌左偏;左上肢肌力4级,右上肢肌力5级,双下肢肌力3级;双侧Babinski征阳性。心、肺、腹部查体均未见明显异常。
诊疗经过:转入神经内科后完善头颅MRI示右侧额颞顶叶、右侧放射冠区、右侧小脑半球、双侧枕叶及左侧顶叶新发梗死灶,右侧额顶叶梗死灶内微出血转化;MRA示右侧大脑后动脉P2段局限性中度狭窄,余脑血管未见明显异常(图4)。颈部血管超声示右侧锁骨下动脉粥样斑块形成,双侧颈动脉及椎动脉未见明显异常。心动超声示左心房增大(左心房前后径为35 mm),左心室舒张功能减低,未见反常分流。动态心电图显示窦性心律,偶发室性期前收缩。肌酸激酶48 U/L,肌酸激酶同工酶18 U/L,肌钙蛋白0.045 ng/mL,乳酸脱氢酶、α-羟丁酸脱氢酶稍升高。四肢静脉超声示右上肢头静脉血栓,双下肢肌间静脉血栓。凝血常规示凝血酶原时间12 s,活化部分凝血酶原时间23.90 s(下降),纤维蛋白原3.75 g/L,D-二聚体7.43 mg/L(2周后升高至7.96 mg/L),纤维蛋白原降解产物24.96 μg/mL(升高)。血小板计数136×109/L。
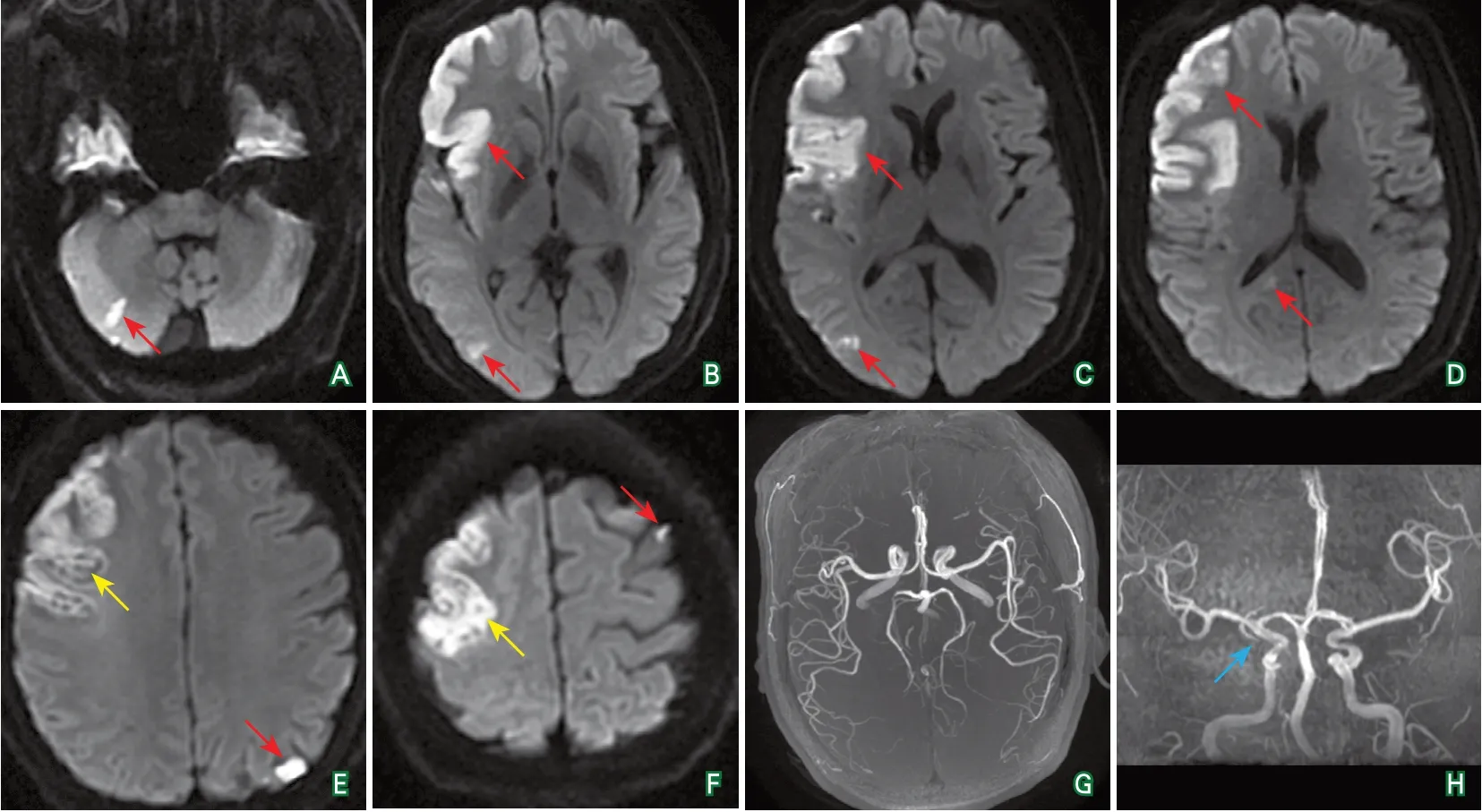
图4 头颅DWI及MRA结果
考虑患者起病急,短期内迅速达到高峰;脑部梗死灶累及额叶、顶叶、枕叶、小脑等前后循环多个区域,超过3个血管供血区(左、右大脑前动脉和左、右大脑后动脉),符合多流域分布的特点;血液呈现高凝状态倾向[1],静脉血栓发生风险评分(Caprini scale)2分;心房颤动鉴别评分(score for the targeting of atrial fibrillation,STAF)6分,反常栓塞风险量表(risk of paradoxical embolism,RoPE)评分5分,病史及辅助检查未找到心源性栓塞及大动脉粥样硬化证据。结合患者既往肿瘤病史、血液呈高凝状态倾向、脑梗死病灶呈多流域征,考虑此次脑梗死为特鲁索综合征所致。
诊断:
脑梗死(右侧额颞顶叶、右侧放射冠、
右侧小脑、左侧顶叶、双侧枕叶)
肺癌(中-低分化腺癌)伴特鲁索综合征
下肢深静脉血栓
高血压病3级(极高危)
给予患者抗血小板聚集、脱水降颅压、营养脑细胞、调脂稳定斑块等对症支持治疗。脑梗死1周后复查头颅CT示水肿较前减轻,未见明显出血灶(图5),考虑梗死为高凝状态引起,遂将抗血小板治疗更改为低分子肝素抗凝治疗,余治疗方案大致同前。治疗3个周后,患者症状好转(神志清、问答切题、双下肢肌力4~5级),自动出院。3个月后随访mRS评分1分,继续肺癌靶向药物治疗。
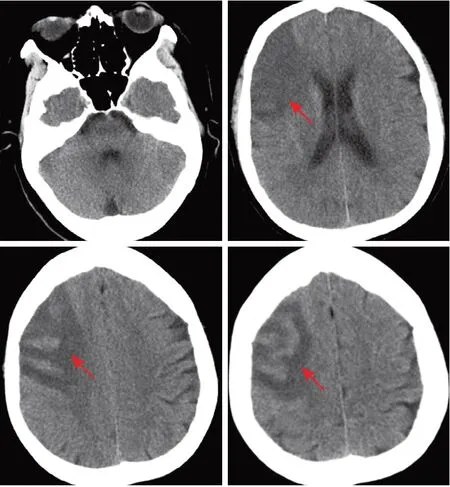
图5 卒中发病1周后患者头颅CT检查结果
2 讨论
1865年法国医生Trousseau[2]首次报道了一例由多发性静脉血栓引起脑栓塞和肺栓塞的胃癌患者,后将癌症患者并发游走性静脉血栓统称为特鲁索综合征(Trousseau’s syndrome)。戏剧性的是,Trousseau本人于2年后被发现患有左上肢静脉血栓,此后不久被诊断为恶性肿瘤,且于当年死于胃癌[3-4]。1977年Sack等[5]将特鲁索综合征定义扩大为与恶性肿瘤相关的高凝状态所致的慢性弥漫性血管内凝血、多发性静脉血栓、动脉血栓及非细菌性血栓性心内膜炎等一系列血栓栓塞综合征。恶性肿瘤可通过多种机制导致血液高凝状态,诊断特鲁索综合征时,高凝状态需满足下列条件:凝血酶原时间缩短>3 s;活化部分凝血酶原时间缩短>3 s;纤维蛋白原>4.0 g/L;D-二聚体≥0.5 μg/L;血小板计数>350×109/L,有两项或两项以上异常者[1]。由于部分恶性肿瘤早期常以高凝状态为首发表现,因此加强合并高凝状态脑栓塞的病因学识别尤为重要。
该患者于活动中突然发病,影像学符合多流域脑梗死特征(脑大动脉及分支的供血区形成该动脉的“流域”,累及两个或两个以上动脉系统的脑梗死灶),从发病年龄、起病状态、速度和临床症状分析,此患者符合脑栓塞表现。患者既往无心房颤动病史,经超声心动图检查未见静息状态下右向左分流,未见室壁运动异常和附壁血栓存在,动态心电图未见心律失常,STAF评分为6分,基本排除心源性脑栓塞诊断;RoPE评分5分,考虑反常性栓塞的可能性也不大。虽然此患者有高血压病史,但颈部血管超声和MRA均未发现与梗死相关的脑动脉粥样硬化证据。结合此患者脑梗死特点、血液高凝倾向、四肢多发静脉血栓,故考虑其病因可能为感染、免疫、血液及遗传性血管病等疾病,最终经肺部CT和肿瘤病理类型证实此患者为肺中-低分化腺癌继发的特鲁索综合征引起的脑栓塞。根据既往文献[6-10]绘制的特鲁索综合征诊断流程见图6。
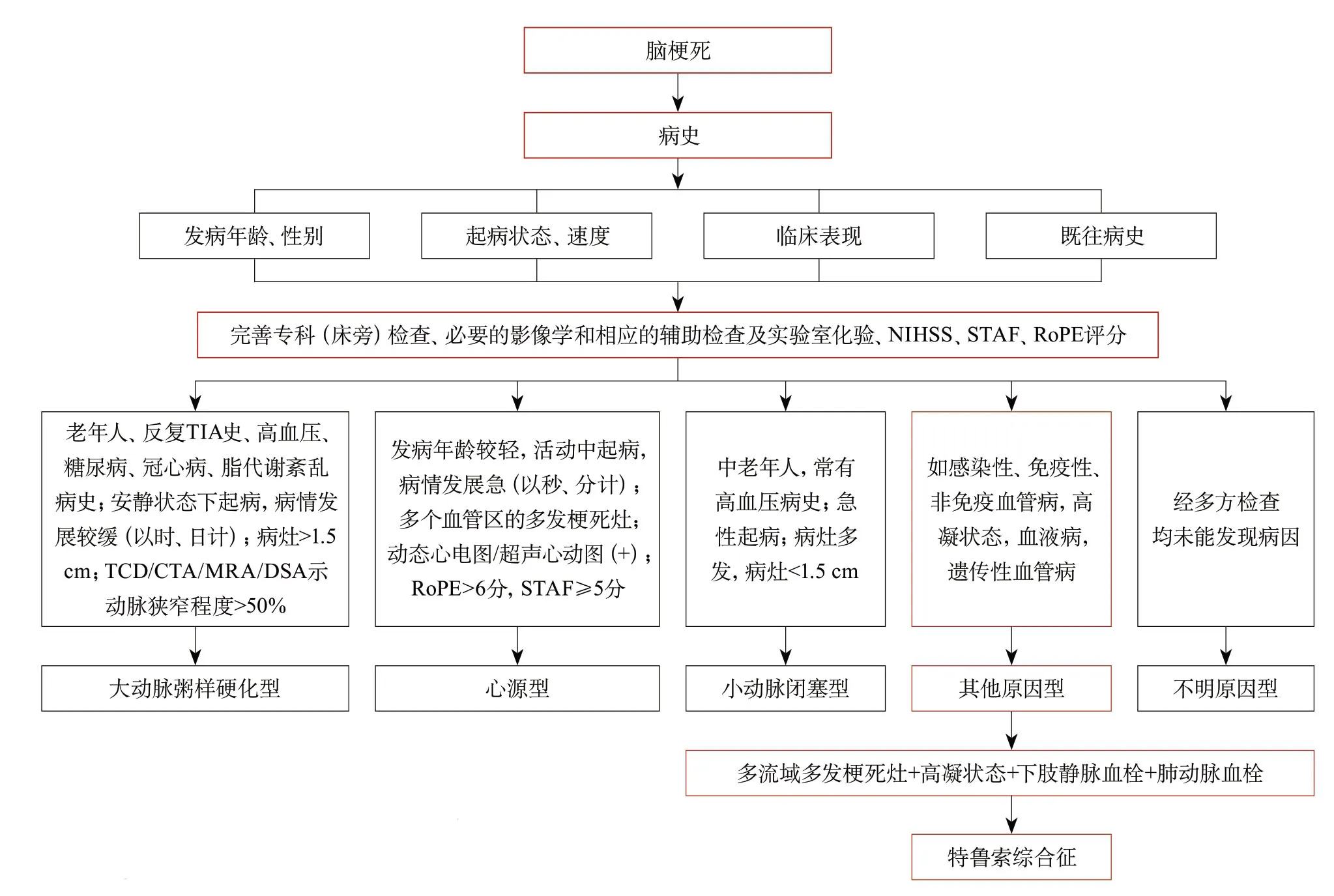
图6 特鲁索综合征合并脑梗死的诊断流程
肺癌明显增加患者的卒中风险[11-14](图7),当合并高血压、冠心病、糖尿病等危险因素时,肺癌患者的卒中风险将进一步增加。肺腺癌患者的卒中风险最高,为非腺癌患者的3倍,小细胞肺癌患者与非小细胞肺癌患者卒中风险无明显差异(图8)[15-18]。肺癌引起卒中的机制包括[8,19-20]:①恶性肿瘤继发高凝状态:肿瘤细胞分泌促凝因子、黏蛋白等高凝物质[21];②静脉系统血栓形成后通过反常栓塞途径进入体循环系统,如卵圆孔未闭、肺动静脉瘘等;③非细菌性血栓性心内膜炎:心脏瓣膜及升主动脉内膜的纤维蛋白与血小板黏附形成赘生物,脱落后随血液循环栓塞体循环动脉血管;④肿瘤的侵袭与转移:肺癌由于生长位置的特殊性及肿瘤细胞的侵袭性,易侵犯心脏、主动脉等器官组织,癌栓通过体循环系统导致动脉栓塞事件。该患者为胸腔镜术后出现脑梗死,未找到大动脉粥样硬化、心源性栓塞证据,故推测术中可能形成了异常的动-静脉通道,来自下肢的静脉血栓经肺循环异常分流进入体循环,导致了脑栓塞。
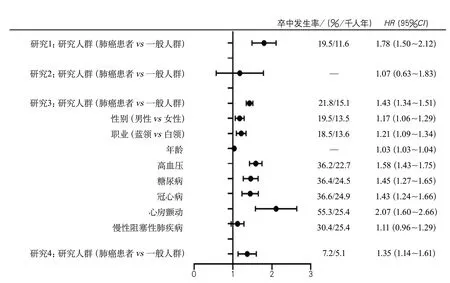
图7 不同研究中肺癌患者发生卒中的风险[11-14]
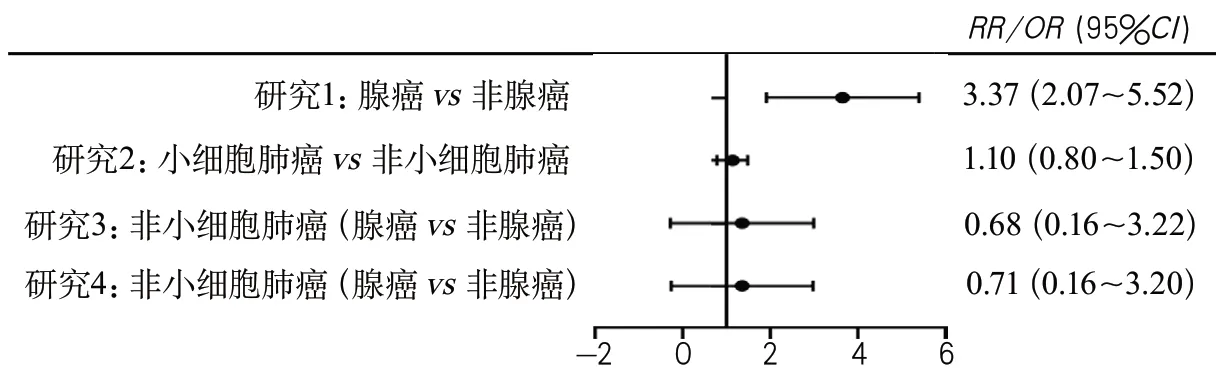
图8 不同病理类型肺癌患者发生卒中的风险[15-18]
抗凝治疗是预防特鲁索综合征卒中复发的关键[5,22]。肝素能有效控制卒中症状及预防再发[13,19,22]。肝素除具有抗凝血酶、缓解高凝状态作用外,还可抑制癌细胞分泌黏蛋白[23]。与普通肝素相比,低分子肝素出血风险低[24],能降低患者死亡率。有研究显示在预防特鲁索综合征患者卒中复发方面,华法林的有效性优于低分子肝素,但出血风险较高[25]。此外,新型口服抗凝剂如达比加群,对合并特鲁索综合征的卒中患者有一定疗效[26]。《肿瘤相关静脉血栓栓塞症预防与治疗指南(2019版)》建议对于癌性静脉血栓的抗凝治疗,口服凝血Xa因子直接抑制剂可作为首选单药治疗方案之一,急性期口服利伐沙班15 mg,2次/日,3周后改为20 mg/d[27]。
特鲁索综合征合并脑梗死患者通常预后较差。Mai等[9]进行的一项回顾性研究发现,超过一半的患者(58%)一个月内卒中复发。复发的卒中患者中,有68%(13/19)的患者存在恶性肿瘤引发的高凝状态,这可能是卒中复发的主要原因,大部分患者(84%,16/19)在6个月内死亡[28]。合并特鲁索综合征的卒中患者死亡率可高达50%~79%,高于不伴肿瘤的卒中患者[29]。
综上,对于短时间内出现复发性卒中,影像学表现为多流域梗死灶,并伴有纤维蛋白原、D-二聚体、纤维蛋白原降解产物持续升高的患者,临床上应考虑特鲁索综合征可能,应及时对患者进行相关肿瘤的实验室及影像学检查,以排查肿瘤。合并特鲁索综合征的卒中患者通常预后较差,卒中复发风险及死亡率较高,针对病因的抗癌治疗及抗凝治疗,可减少卒中复发风险,改善患者预后。
