栝楼桂枝汤对氧糖剥夺诱导的HT22细胞损伤保护作用机制研究
2021-09-01杨劲博朱晓勤胡海霞
杨劲博,朱晓勤,胡海霞*
(1.福建中医药大学中西医结合研究院,福建 福州350122;2.福建省中西医结合老年性疾病重点实验室,福建 福州350122)
脑卒中是全球第二大死亡原因[1],据其发病机制可分为缺血性脑卒中和出血性脑卒中,缺血性脑卒中占所有脑卒中病例的87%[2]。目前脑卒中发生的机制较为复杂,兴奋毒性、氧化应激和炎症在内的多种机制都可以引起脑损伤,诱导神经细胞凋亡。针对脑卒中的治疗,溶栓治疗是缺血性脑卒中急性期最为有效的治疗手段之一,静脉溶栓组织型纤溶酶原激活剂(recombinant tissue plasminogen activator,rt-PA)是唯一获得美国食品和药物管理局(FDA)批准的药物[3]。然而,rt-PA的治疗时间窗口狭窄,仅为脑卒中发生后4.5 h,仅有3%~5%的患者能够时得到救治,显著降低了其对缺血性脑卒中的疗效[4]。其他药物如谷氨酸受体抑制剂阿替加奈、钙通道抑制剂尼莫地平、氧自由基清除剂及抗氧化剂依达拉奉等[5],在临床前实验中都已证实能够抑制神经细胞凋亡,改善神经细胞状态,但在临床使用中疗效欠佳。其中主要原因在于这些药物治疗作用靶点较为单一,仅针对整个脑卒中病程中的单一病理过程和发病机制,而脑卒中是多种病理过程共同作用的结果。近年来,中药复方因其具有多组分协同,可在多系统、多层次、多靶点上发挥整体治疗作用,且毒副作用小、成本低,已成为治疗脑卒中的研究热点。栝楼桂枝汤(Gualou Guizhi decoction,GLGZD)出自东汉末年张仲景《金匮要略》,已有研究表明栝楼桂枝汤可以减轻脑缺血再灌注损伤[6-8],课题组前期实验也已证明GLGZD可通过多途径、多机制缓解神经细胞损伤[9],发挥神经保护作用,但其作用机制尚未深入探讨。基于此,本研究以小鼠海马HT22神经细胞为切入点,从减轻神经元凋亡角度探讨栝楼桂枝汤对脑卒中神经保护作用机制,为临床用药提供理论依据。
1 实验材料与仪器
1.1 实验材料 小鼠海马神经元细胞HT22(上海泽叶生物科技有限公司,批号:C8339);DMEM高糖培养基(美国Hyclone公司,批号:SH30022);EBSS无糖培养基(美国S igma公司,批号:M5017);PBS缓冲液(美国Hyclone公司,批号:SH30256);胎牛血清(批号:10099141)、胰酶消化液(批号:15050057)均购自美国ThermoFisher公司;栝楼桂枝汤药材购自福建中医药大学国医堂;CCK-8试剂盒(大连美仑生物技术有限公司,批号:MA0218-50);ELISA试剂盒(上海酶联生物科技有限公司,批号:ml003167);细胞凋亡DAPI染色试剂盒(批号:KGA215-50)、Caspase-3荧光检测试剂盒(批号:KGA202F)均购自江苏凯基生物技术股份有限公司;BCA蛋白定量试剂盒(北京博奥森生物技术有限公司,批号:C05-02001)。
1.2 实验仪器 超净工作台(苏州安泰仪器设备有限公司);酶标仪(美国Bio-Tek公司);CO2培养箱(香港力康仪器设备有限公司);倒置显微镜(日本Nikon公司);低速离心机(湖南湘仪实验仪器开发有限公司);细胞低氧培养工作站(英国Don Whitley公司);恒温水浴箱(江苏太仓医用仪器厂);细胞相差荧光显微镜(日本OLYMPUS公司)。
2 实验方法
2.1 栝楼桂枝汤水提液制备 取天花粉30 g,白芍15 g,生姜9 g,甘草6 g,桂枝9 g,大枣12枚混合,5倍量水加热回流2次,每次1 h,过滤,滤液合并,旋转蒸发仪减压浓缩,真空干燥成干浸膏,-20℃冰箱冻存备用。使用前用培养基将干浸膏稀释成50 mg/mL液体,过滤后4℃冰箱保存备用。
2.2 HT22细胞培养 将小鼠海马神经元HT22细胞用完全培养基[含10%胎牛血清(FBS)、1%双抗(青链霉素)的DMEM培养基]于37℃、5%CO2恒温培养箱中培养备用。细胞贴壁生长至80%,用0.25%胰酶消化并传代培养,用于后续实验。
2.3 实验分组和处理 HT22细胞分为正常组、模型组、低剂量组、中剂量组、高剂量组。正常组:HT22细胞在完全培养基,37℃、5%CO2恒温培养箱中培养。模型组:氧糖剥夺/再灌注(OGD/R)诱导损伤,完全培养基培养24 h后,将完全培养基更换无糖EBSS培养基后,置于1%O2、5%CO2、94%N2低氧培养工作站培养90 min,此即为氧糖剥夺过程;再将无糖EBSS培养基更换为完全培养基,放置于37℃、5%CO2恒温培养箱复氧培养24 h,复氧复糖,此过程即为再灌注过程。HT22细胞经OGD/R模型损伤后,细胞生长活力明显下降,活力在50%~60%左右。正常HT22细胞轮廓清晰,贴壁牢固,立体感强,而OGD/R损伤后,细胞突起皱缩、变圆,贴壁状态较差,部分细胞漂浮在培养基中,甚至死亡。低、中、高剂量组:在OGD/R模型复氧复糖过程中分别于完全培养基中加入50、100、200μg/mL GLGZD药液。
2.4 CCK-8法筛选GLGZD药物最佳干预浓度 取上述5组HT22细胞,按照1×105个/mL密度,接种在96孔板,每孔100μL,各组细胞处理结束后,每孔加入10μL CCK-8毒性检测液,置于培养箱中继续培养4 h后,使用酶标仪于波长450 nm处检测OD值,根据公式计算各组细胞生长活力,实验重复3次。CCK-8实验显示:氧糖剥夺再灌注后,HT22细胞生长活力降至57.36%(见模型组),说明模型建立成功;而使用低、中、高不同剂量(50、100、200μg/mL)GLGZD干预,则可显著恢复细胞的生长活力,并随着剂量的加大,细胞活力增加,呈现剂量性依赖,高剂量组细胞活力达到85.43%,最佳药物浓度为200μg/mL,见图1。故后续实验以高剂量组浓度200μg/mL作为药物干预浓度。
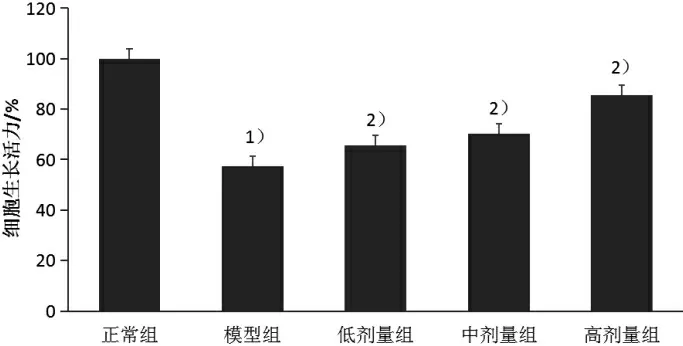
图1 各组细胞生长活力结果图
2.5 DAPI染色检测HT22细胞凋亡 DAPI(4,6-Diamidino-2-phenylindole,4,6-二氨基-2-苯基吲哚)是一种DNA染料,对细胞膜有半通透性,可以透过细胞与DNA产生非嵌入式结合,发出蓝色荧光。HT22细胞分为正常组、模型组、GLGZD组。正常组与模型组细胞处理同“2.4”,GLGZD组在复氧复糖过程于完全培养基中加入200μg/mL GLGZD药液。按照1×105个/mL密度接种于6孔板,每孔2 mL。制备1.5μg/mL DAPI工作液,各组细胞处理结束后吸弃6孔板中的培养基,PBS清洗,加入500μL DAPI工作液,37℃避光15 min,50μL甲醇漂洗,加入50μL Buffer A,荧光显微镜下以340/380 nm紫外光激发,×200、×400显微镜观察细胞凋亡情况。
2.6 荧光定量法检测Caspase-3活性 HT22细胞分组和处理同“2.4”,干预完成后裂解细胞,收集细胞后加入100μL冰冷Lysis Buffer,冰上裂解30 min,其间涡旋振荡3~4次,每次10 s,4℃,10 000 r/min离心1 min。小心吸取上清液(含裂解的蛋白质)转移至新的管中,进行BCA蛋白定量,于波长562 nm处测定OD值,根据标准曲线计算出蛋白浓度。根据Caspase-3活性检测试剂盒说明书,用荧光酶标仪测定荧光强度(激发波长=485 nm,发射波长=535 nm),通过公式计算Caspase-3活性荧光强度比值。
2.7 统计学方法 采用SPSS 22.0软件进行统计学处理。计量资料属正态分布的以(±s)表示,组间数据比较采用单因素方差分析,非正态分布采用非参数检验;计数资料采用χ2检验。
3 结 果
3.1 栝楼桂枝汤对HT22细胞凋亡的影响 正常细胞的核形态呈圆形,边缘清晰,染色均匀;凋亡细胞的膜通透性增加,细胞核边缘不规则,染色体浓集,荧光着色较重,且细胞核固缩,核小体碎片增加。DAPI染色结果显示:正常组细胞形态正常,无损伤,模型组呈现明显的凋亡形态,GLGZD组细胞凋亡形态有所恢复,见图2,说明GLGZD可以抑制神经元凋亡。

图2 3组细胞凋亡形态DAPI染色结果图
3.2 栝楼桂枝汤对Caspase-3活性的影响 Caspase-3是凋亡的执行因子,通过多种途径介导细胞的凋亡[10-11]。图3所示:模型组Caspase-3活性荧光强度比值明显增强,GLGZD组Caspase-3活性荧光强度比值虽未达到正常水平,但是较模型组明显下降,说明GLGZD可通过降低Caspase-3活性水平,抑制凋亡,减轻神经细胞损伤。
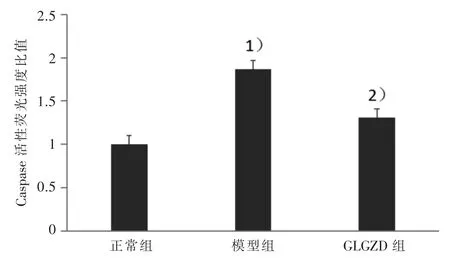
图3 3组细胞Caspase-3活性检测结果图
4 讨 论
本研究通过CCK-8实验证明:氧糖剥夺再灌注后,在各种损伤机制作用下,HT22神经生长活力迅速下降,细胞受到明显损伤;在GLGZD作用下,HT22细胞的生长活力明显上升,其中以200μg/mL药物浓度最佳,初步证实GLGZD对损伤HT22细胞的保护作用。而DAPI染色实验显示:模型组细胞出现明显的凋亡形态,染色体浓集,细胞核边缘不规则,荧光着色较重;经过GLGZD干预后,细胞凋亡形态虽未恢复至完全正常的细胞形态,但较模型组细胞形态有了明显改善,细胞形态较为完整,染色质均一。细胞凋亡[12]是指存在于大多数生物体内由基因调控的细胞自主、有序的死亡过程,凋亡具有独特的形态学和生物化学特征,如细胞质膜泡状化、胞质浓缩、染色质凝集、DNA片段化等,GLGZD可以通过改善细胞的凋亡形态,进而起到神经细胞保护的作用。Caspase-3是凋亡的最终执行者[13],在凋亡级联反应中居于核心地位,Caspase-3正常情况下以无活性的酶原形式存在,在凋亡级联反应下活化为Cleaved Caspase-3,抑制Caspase-3活化可抑制细胞凋亡。当细胞遭受OGD/R损伤后,Caspase-3活性明显升高并活化,启动凋亡级联反应。经GLGZD干预后,Caspase-3活性虽未降至正常水平,但是较模型组有了明显下降,故GLGZD是通过抑制细胞凋亡关键蛋白Caspase-3的活性水平,减轻凋亡,从而达到神经保护作用。综上所述,GLGZD对卒中后神经细胞损伤起到保护作用,机制主要是抑制凋亡关键蛋白Caspase-3活化,减轻凋亡损伤。
本研究主要探讨GLGZD对卒中后HT22细胞生长活力和凋亡方面的影响,为其临床治疗提供科学依据。但是卒中后神经细胞损伤受到众多机制的调控,凋亡是其中一种,GLGZD对卒中后神经细胞保护作用是否涉及其他机制,有待进一步研究。
