提高POCT血气分析检验质量的管理实践*
2021-08-30潘婕倪军丁海薛缪群陈雨欣沈瀚南京医科大学鼓楼临床医学院检验科南京20008南京大学医学院附属鼓楼医院a检验科质量管理办公室南京20008
潘婕,倪军,丁海,薛缪群,陈雨欣,,沈瀚(.南京医科大学鼓楼临床医学院检验科,南京 20008;2.南京大学医学院附属鼓楼医院a.检验科,b.质量管理办公室,南京 20008)
床旁检测(point of care testing,POCT)在我国的应用时间相对于国外较短。通过国家“863”计划、“十二五”科技计划对POCT产业发展的大力支持,我国POCT产业迅速崛起。2012年中华医学会联合原卫生部临床检验中心发表了POCT 的应用指南及共识《POCT临床应用建议》[1],2013年公布的《GB/T29790—2013 即时检测质量和能力的要求》[2]对POCT 产品的质量保证提出了明确要求。目前POCT领域只有便携式血糖检测仪相关的法律法规比较成熟,自2010 至2016 年我国相继出台了《医疗机构便携式血糖检测仪管理和临床操作规范》[3]、《中国血糖监测临床应用指南(2015 年版)》[4]、《便携式血糖仪临床操作和质量管理规范中国专家共识》[5],增强了便携式血糖仪操作及质量管理的科学性及规范性。但同样在各级医院的检验科及临床科室被广泛使用的POCT 血气分析仪,却缺乏相应的规范、共识及指南。在实际应用过程中,临床科室的血气分析仪操作者主要为非检验科人员,在使用及管理中不能像检验科那样具备完善的质量保证体系,因此还存在诸多问题[6-7]。诸如检测地点分散、仪器品牌繁杂、质量标准和操作标准不统一、操作人员缺乏有效培训及考核、仪器缺少定期校准、维护程序、缺少室内质控、很少参加室间质评等,影响了结果的准确性和一致性,给临床诊疗带来了一系列隐患[8]。据报道,国外临床POCT血气分析比对一致率约为70%~73.9%,我国大约为73%[9]。因此,建立针对各临床科室血气分析仪质量管理体系和程序,对其进行有效的质量监管是保证临床POCT 检测结果准确性的重要前提[10]。
2019年,我院成立POCT 质量管理委员会,由质量管理办公室牵头成立POCT 血气分析质量管理小组,对临床科室的POCT 血气分析进行统一质量管理,检验科参与对临床科室进行人员培训、协助建立室内质控程序等,并通过定期组织院内室间比对活动等措施来达到提高临床科室POCT 血气分析检测质量的目的。通过对本单位使用雅培i-STAT1手持式血气分析仪的3 个病区,在实施POCT质量管理前后的室间比对结果及管理后的室内质控变异系数进行分析,旨在为三甲医院的检验科建立规范化、可执行、可推广的POCT 血气分析质量评价方案,帮助临床科室建立POCT 质量管理体系并提高血气分析检测的准确率。
1 材料与方法
1.1 研究对象 纳入南京大学医学院附属鼓楼医院呼吸科1病区(以A表示)、呼吸科2 病区(以B表示)和妇产科病区(以C 表示)所使用的雅培i-STAT 1手持式血气分析仪作为研究对象。将A、B、C病区按质量管理时间点分为管理前(2019年4月)、管理后6 个月(2019 年10 月)、管理后12 个月(2020年4月)3个组进行室间比对,分别在3个时间点选取每个病区5 位患者采集动脉全血血气标本。评价项目:pH、氧分压(PO2)、二氧化碳分压(PCO2)、钾离子(K+)、钠离子(Na+)、钙离子(Ca2+)。
1.2 主要仪器与试剂 i-STAT 1 手持式血气分析仪及其配套试剂、i-STAT TriControls Control 商品化质控物(美国雅培公司);GEM Premier3000 血气分析仪及其配套试剂(美国沃芬公司)。
1.3 构建POCT质量管理组织架构 由分管院长主管,成立POCT 质量管理委员会,由质量管理办公室负责构建POCT质量管理体系并组建POCT血气分析质量管理小组,小组成员由质量管理办公室、检验科、设备科及各临床科室相关人员构成,对全院POCT 血气分析进行统一规范的管理。检验科将临床POCT项目纳入质量管理体系,参与对临床科室POCT 血气分析仪操作人员的培训、考核,指导临床POCT血气分析仪的室内质控,并负责室间比对的实施及结果汇总。
1.4 室间比对方法 将A、B、C病区的室间比对分为管理前(2019 年4 月)、管理后6 个月(2019 年10月)、管理后12 个月(2020 年4 月)3 组。每组从A、B、C 3个病区各选取5名需行血气分析患者,每名患者抽取双份动脉全血标本,分别由相应病区血气分析仪和检验科血气分析靶机(靶机近三年参加国家卫生健康委临床检验中心血气和酸碱分析室间质评成绩均为100%,且近2 年血气分析各项目室内质控变异系数在3%以内)进行同时检测;以靶机结果作为比对靶值,分别计算3个病区每组检测值与靶值的误差。室间比对参考国家标准GB/T20470—2006[11]规定的允许误差范围进行判读:若某项目某组比对中某份样本结果偏倚≤规定允许误差范围,则判定该项目此份样本比对得分为20分,若大于规定允许误差范围则不得分。依次累加该项目每组5份样本比对得分,各项目每组满分100分;若某组某项目得分≥80 分,则判定该组此项目比对通过。分别计算每个病区每组各项目得分、每组各项目的平均偏倚(%)(平均偏倚=各项目每份样本偏倚绝对值之和/5)、每组POCT 血气检测合格率(%)(POCT 血气检测合格率=POCT血气分析室间比对通过的项目数/POCT 血气分析的总项目数×100%),并分别进行组间比较。
1.5 室内质控 3 个病区在施行POCT 统一质量管理前均缺少室内质控,施行POCT 质量管理后日常进行低值和高值2个水平的室内质控检测,统计分析3个病区5个月(2019年7月至11月)内血气分析各项目2 个水平室内质控结果的变异系数并进行评估,室内质控评估标准:各项目允许不精密度根据生物学变异数据库[12]导出适当、最低、最佳评价标准(PO2由于没有生物学变异数据,则参考1/3室间质量评价允许误差作为不精密度评价标准),将管理后POCT 血气分析室内质控的各项目变异系数与之比较,评价标准见表1。
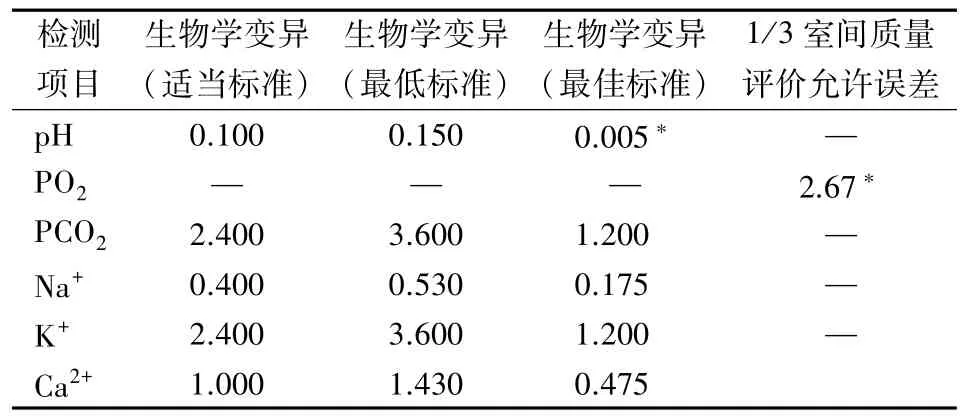
表1 血气分析不同项目允许不精密度的规范(%)
1.6 统计学分析 采用SPSS 20.0 统计软件及GraphPad Prism 6 软件进行。室间比对各项目得分、血气检测合格率的组间比较采用Fisher精确概率法;室间比对各项目平均偏倚组间比较采用单因素方差分析;以P<0.05为差异有统计学意义;室内质控变异系数用中位数(范围)表示。
2 结果
2.1 室间比对各项目的得分比较 A 病区pH 和K+3次室间比对得分均为100,PO2管理后6 个月(得分80)、管理后12 个月(得分100)均比管理前(得分60)提高,PCO2管理后6 个月、管理后12 个月(得分均为80)均比管理前(得分60)提高,Na+管理后6个月、管理后12 个月(得分均为100)均比管理前(得分80)提高,Ca2+管理后6 个月、管理后12个月(得分均为100)均比管理前(得分60)提高。
B病区K+3次室间比对得分均为100,pH、Na+和Ca2+管理后6 个月、管理后12 个月(得分均为100)均比管理前(得分均为80)提高,PO2管理后6个月(得分60)、管理后12个月(得分80)均比管理前(得分20)提高,PCO2管理后6 个月(得分80)、管理后12个月(得分100)均比管理前(得分40)提高,Ca2+管理后6 个月、管理后12 个月(得分均为100)均比管理前(得分80)提高。
C病区Ca2+3次室间比对得分均为100,pH、K+管理后6个月、管理后12 个月(得分均为100)均比管理前(得分均为60)提高,PO2管理后6 个月(得分100)、管理后12 个月(得分80)均比管理前(得分0)提高,PCO2管理后6个月(得分80)、管理后12个月(得分100)均比管理前(得分60)提高,Na+管理后6个月与管理前得分相同(得分80),管理后12个月(得分100)比管理前提高。
2.2 室间比对各项目的平均偏倚比较 见图1。A病区pH、PCO2、Na+、Ca2+管理后6个月较管理前的平均偏倚均下降(F分别为15.77、17.83、17.15、21.31,P均<0.05);管理后12个月与管理后6个月比较平均偏倚亦减小,差异均有统计学意义(F分别为17.10、20.45、18.83、18.67,P均<0.05)。虽然PO2管理后6 个月较管理前平均偏倚增大(F=20.63,P<0.05),其管理后12 个月较管理前、管理后6个月平均偏倚均减小,差异均有统计学意义(F分别为21.77、24.45,P均<0.05)。K+管理后12 个月较管理后6个月平均偏倚下降,差异有统计学意义(F=15.63,P<0.05)。
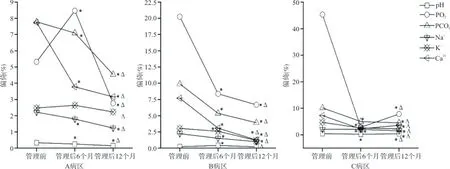
图1 3个病区室间比对各项目的平均偏倚(%)
B病区PO2、PCO2、Na+、K+和Ca2+管理后6 个月较管理前平均偏倚均减小,差异均有统计学意义(F分别为23.32、20.03、15.45、15.01、17.06,P均<0.05);管理后12个月较管理后6 个月平均偏倚均较小,差异均有统计学意义(F分别为17.67、17.55、15.30、16.12、17.87,P均<0.05)。pH管理后6个月较管理前平均偏倚增大,差异有统计学意义(F=15.37,P<0.05),其管理后12个月较管理后6 个月平均偏倚有所改进,差异有统计学意义(F=15.12,P<0.05)。
C病区pH、PO2、PCO2、K+和Ca2+管理后6 个月较管理前平均偏倚均下降,差异均有统计学意义(F分别为15.02、26.53、17.25、16.33、17.85,P均<0.05)。PCO2、Na+和K+管理后12 个月较管理后6个月平均偏倚均减小,差异均有统计学意义(F分别为17.45、14.84、16.08,P均<0.05),而pH、PO2和Ca2+管理后12个月较管理后6个月平均偏倚均增大,差异均有统计学意义(F分别为15.02、17.25、15.68;P均<0.05)。Na+管理后6 个月较管理前的平均偏倚无显著变化(P>0.05)。
2.3 室间比对的合格率比较 A、B、C 病区管理前、管理后6个月、管理后12个月室间比对血气检测合格率经Fisher精确概率法统计分析,差异无统计学意义。见表2。

表2 3个病区室间比对血气检测合格率(%)比较
2.4 POCT血气分析室内质控变异系数 3个病区质量管理后血气分析室内质控各项目的变异系数见表3。除PO2未达表1中提到的1/3室间质量评价允许误差外,其余项目的室内质控变异系数均达到生物学变异最低标准,且pH和K+的变异系数均达到了生物学变异适当标准。
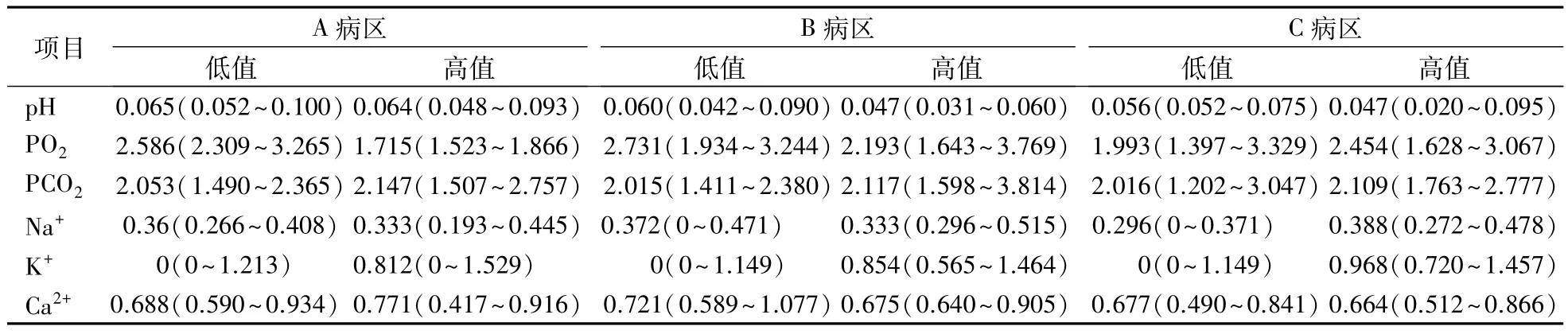
表3 3个病区管理后血气分析室内质控各检测项目的变异系数(%)
3 讨论
目前本院有3 个病区选用雅培i-STAT 1 手持式血气分析仪。在进行统一POCT 质量管理前,3个病区的POCT 血气分析室间比对项目得分从0到100不等,各项目检测平均偏倚结果也参差不齐,比对合格率较低。经过调研发现临床科室的仪器操作人员不固定,流动性大;操作人员接受培训次数少,培训效果差;对仪器性能状态不了解,缺少定期维护校准;在仪器使用过程中没有标准化操作程序;没有开展室内质控,没有参加室间质评,缺乏质量风险意识,缺乏统一规范的管理,这些都是造成临床科室血气分析不准确性的原因。针对临床POCT 血气分析存在的问题和质量风险,我院POCT质量管理小组制定了一系列质量改进方案,包括完善临床POCT 血气分析检测的标准操作程序、做好仪器定期维护保养,落实人员培训上岗-考核-授权制度,提高操作人员的熟练度和对检测结果的综合判断能力,每日执行POCT 血气分析的室内质控,以及定期组织临床科室和检验科的室间比对,通过质量控制数据和室间比对结果分析对临床科室POCT血气分析进行质量的监管和评价,并制定针对性的整改方案,以达到检测质量的持续改进。本研究中,3个病区在统一管理后的2 次室间比对中,项目的平均偏倚较管理前改进显著,血气分析合格率较管理前均有提高,且管理后12 个月与管理后6个月相比,得分为100 的血气项目均有增加,说明本研究中的质量管理措施和质量评价方案有效提高了临床POCT 血气分析的检验质量。本研究中直接将患者动脉全血标本作为室间比对的样本,而并未使用商品化的质控物,这是因为通过前期研究发现商品化的质控物存在较大的基质效应,在检验科靶机和临床科室的血气分析仪上检测存在结果不稳定、比对结果存在较大差异的问题,而使用动脉全血标本作为比对样本则更稳定、更经济,更具有可操作性。
本研究中,相对其他项目,各组PO2偏倚最明显(图2),是影响POCT血气分析室间比对合格率的主要因素。同时,对质量管理后的POCT 血气分析室内质控变异系数发现,仅PO2不精密度未达评价标准。通过对分析前、分析中和分析后各个环节的实地调研,我们分析可能与标本采集不当有关[13],采集时混入气泡、采血不畅导致标本溶血、采集后未及时与针管内肝素快速混匀,以及未及时将采样针加塞隔绝空气等均可导致PO2的假性增高。针对这一问题,我们将对血气标本采集人员加强培训考核,对标本采集过程和相应质量指标进行持续监督和改进,后续我们将持续跟进对改进效果进行评价。
C病区管理后12个月与管理后6 个月比,PO2得分从100 降到80,且管理后12 个月pH、PO2、Ca2+的平均偏倚与管理后6 个月比较有不同程度增加,分析原因,可能与C 病区负责仪器操作与维护保养人员不固定,更换操作人员后操作流程不熟练有关。针对这一问题后续我们将适当增加对C病区的培训、考核及室间比对频次,针对人员操作、检测质量等安排不定期抽查,并将对C病区利用全面质量管理工具对出现此问题从人、机、物、料、法、要、环等方面对具体原因进行进一步分析,形成PDCA循环。
本研究的数据量有限,对i-STAT 1 血气分析仪在施行POCT质量管理中的应用分析仍有很多不足,笔者将在后续的研究中加以完善。后续本院临床科室POCT血气分析仪也将定期参加国家或省卫生健康委临床检验中心组织的能力验证,结合院内组织的室间比对以得到更全面的质量评价,以便更好地为临床病患提供高质量服务。本研究希望通过对POCT血气分析质量管理的实践,推广至院内其他POCT检测,建立规范的POCT 实验室间质量评价方案和标准化管理指南,为POCT 质量管理和改进提供新思路。
