凝血酶原时间衍生法与冯·克劳斯法测定纤维蛋白原结果的一致性及临床应用*
2021-08-30张艳杨怡金心国药葛洲坝中心医院三峡大学第三临床医学院检验科湖北宜昌443002
张艳,杨怡,金心(国药葛洲坝中心医院&三峡大学第三临床医学院检验科,湖北宜昌 443002)
纤维蛋白原(fibrinogen,Fib)是一种由肝细胞合成[1]的具有凝血功能的蛋白质,是纤维蛋白的前体。Fib具有双重生物活性,既是凝血酶作用的底物,又是高浓度纤溶酶的靶物质,其主要生理功能是进入血液循环后参与凝血和调节纤溶[2],与应激反应、动脉血栓形成、弥漫性血管内凝血等密切相关[3]。目前,Fib 的检测方法主要有冯·克劳斯(Von Clauss)法及凝血酶原时间衍生法(prothrombin time-derived,PT-der法)2 种[4]。Von Clauss法是WHO推荐的参考方法[5],也是美国国家临床检验标准委员会推荐的Fib 常规测定方法[6]。Fib 因基因多态性[7]而具有高度异质性,其检测受较多因素影响。文献报道[8]在没有异常Fib 存在的情况下,PT-der法检测结果在2.00~4.00 g/L 时可替代Von Clauss 法。但在验证过程中发现,几乎所有PT-der 法检测Fib 的结果均比Von Clauss 法高10%~20%。在查阅资料后推测,2 种方法检测结果误差的原因可能是使用了同一校准品但赋值不同。本研究拟用量值传递的方法校准PT-der法,即以可溯源的Von Clauss 法赋值混合血浆对PT-der法进行重新定标,再用大量临床样本确立其与Von Clauss法检测结果的一致性区间和适用范围。
1 材料和方法
1.1 仪器和试剂 沃芬TOP 700和TOP 300 全自动凝血分析仪及其配套试剂(Von Clauss法试剂批号N0688281,PT-der法试剂批号N0386789)、校准品(批号E0177755)和双水平质控品(批号N0386250和H0864436)。校准品中Fib 可溯源至英国国家生物制品检定所(National Institute for Biological Standards and Control,NIBSC)。
1.2 样本
1.2.1 标本来源 国药葛洲坝中心医院2018年11月至2019年4月住院及门诊检测凝血项目的患者5 142例,年龄2~95 岁(中位年龄52 岁),其中男2 619例,女2 523例。采集清晨空腹静脉血1.8 mL于真空凝血采血管(含0.2 mL 0.109 mmol/L 枸橼酸钠抗凝剂)中,以离心力2 000×g离心15 min,剔除黄疸、溶血、脂血标本及重度贫血患者标本。
1.2.2 混合血浆制备 用30 份新鲜血浆按低值、正常和高值以4 ∶23 ∶3 的比例等量混合(基于本院近2年约50 000份临床样本结果分布所得)。
1.3 PT-der法校准
1.3.1 混合血浆赋值 用Von Clauss 法连续检测混合血浆Fib 20次,计算其剔除离群值(超3 倍标准差)后的均值,以此均值作为该混合血浆的赋值。
1.3.2 校准 用已赋值的混合血浆作为校准品依照原厂校准方法(六点拟合直线)校准PT-der法。
1.4 性能验证
1.4.1 精密度验证 参照美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)EP15-A文件[9]推荐方法进行。选择正常和异常2个浓度水平的质控品,用PT-der法测定Fib。先将各浓度水平取1支复溶,再分装成5 份,冷藏,每天取出各1份复温后在1批中检测,每批每个水平重复测定3次,每个项目连续测定5 d,将所测定结果进行统计学分析,计算批内精密度、批间精密度、实验室内标准差(s1)、自由度(T)和验证值(V)。当s1<V时认为厂家声明的精密度通过验证。
1.4.2 线性范围验证 参照CLSI EP6-A文件[10],选择低值(L)和高值(H)样品各1 份,将低值和高值样本按4 ∶0、3 ∶1、2 ∶2、1 ∶3、0 ∶4 的比例混合,得到5份线性试验样本。对上述样本重复测定3 次,取平均值。各样本浓度的预期值按公式(CL×VL+CH×VL)/(VL+VH)计算(式中C 为样本浓度,V 为样本体积)。将实测平均值与预期值先进行数据检查,剔除离群值,再用多元线性回归分析,并绘制散点图进行评价。
1.4.3 重新制定本区域人群的参考区间 参照WS/T 402—2012《临床实验室检验项目参考区间的制定》[11],选取不低于120 例表观健康体检者(排除妊娠、糖尿病、血栓类疾病、肾病、免疫系统疾病、血液病、肝脏疾病),采集空腹抗凝血用Von Clauss法和PT-der法检测Fib,分别取总体结果的95%置信区间(P2.5~P97.5)为本区域人群参考区间。
1.5 样本检测 在室内质控检测结果在控的情况下,在TOP700 和TOP300 上同时用Von Clauss 法及PT-der法检测血浆样本Fib,采集样本2 h 内完成检测。各项操作严格按照仪器、试剂说明书及操作规程进行。将PT-der 法检测结果设为观察组,Von Clauss法检测结果设为参照组。
1.6 确立一致性区间及适用范围 用2018 年11月至2019年4月本院凝血样本分别用PT-der法与Von Clauss法检测Fib。以Von Clauss法检测为参照,确立PT-der法与Von Clauss法99%的结果符合WS/T 406—2012《临床血液学检验常规项目分析质量要求》[12]中Fib 准确度要求(偏倚≤20%)范围内的数值区间和适用范围。偏倚以Von Clauss法检测结果为比对标准;符合率为同一样本用以Von Clauss法结果为靶值,PT-der 法检测结果达到准确度要求(偏倚≤20%)的比例。
1.7 统计学分析 采用Excel 2010 软件进行。计算ˉx、s、偏倚等,计量资料以表示,进行线性回归分析,拟合线性方程并计算相关系数(r)。
2 结果
2.1 校准前PT-der法与Von Clauss法Fib 检测结果一致性分析 在用原厂校准模式时,对PT-der法线性范围(0.70~7.00 g/L)内的855 例样本结果进行了比对,总计70.18%(600/855)的PT-der 法检测结果符合WS/T 406—2012的准确度要求,见表1。

表1 重新校准前两种Fib检测结果的比较
2.2 校准后PT-der法的性能验证
2.2.1 精密度验证结果s1(分别为0.081 和0.068)在正常和异常商业质量控制参考水平下均小于V(分别为0.101和0.085),表明厂家声明的精密度通过验证。
2.2.2 线性范围验证结果 PT-der 法检测Fib 的预期值(y)与实测值(x)无明显离群值,最佳拟合方程为二次多项式,回归方程为y=-0.006 2x2+0.949 4x+0.036 7,r2=0.999 9,5个浓度梯度标本的偏差为-0.58%~0.62%,平均偏差为-0.07%。以WS/T 406—2012 的偏倚(≤10%)为评判标准,PT-der法检测Fib在0.70~7.01 g/L 范围内呈临床可接受的三阶线性,厂家声明的0.70~7.00 g/L 线性范围通过验证。
2.2.3 本区域人群的参考区间 127 例符合入选标准的体检者,年龄23~73 岁(中位数为42 岁),其中男72 例,女55 例。用PT-der 法检测Fib 结果为2.18~5.11 g/L(95%置信区间为2.29~5.02 g/L),用Von Clauss法检测结果为2.25~5.07 g/L(95%置信区间为2.33~4.95 g/L),均无离群值。本实验室PT-der法、Von Clauss法检测Fib 的参考区间分别为2.29~5.02 g/L、2.33~4.95 g/L。
2.3 校准后的PT-der法与Von Clauss法Fib 检测结果的一致性分析
2.3.1 样本分布 2018 年11 月至2019 年4 月用2 种方法检测Fib总计5 142例,其中Von Clauss法检测结果异常1 199例,低于参考区间723例,高于参考区间476例。
2.3.2 适用条件 结果比对时发现,一些特殊情况(总计44份,占总样本的0.86%)的检测结果偏差较大,包括:(1)大量使用抗凝药物后(如透析后);(2)明确诊断肝硬化失代偿期等影响凝血的疾病;(3)纤维蛋白降解产物(FDP)≥30 mg/L;(4)凝血酶时间(TT)≥25 s时;(5)活化部分凝血活酶时间(APTT)≥80 s。
2.3.3 PT-der法适用范围的确定 排除上述异常样本后,总计有5 098 份,年龄区间为2~93 岁,其中男2 596例,女2 502 例,PT-der法结果在1.51~7.00 g/L区间内时4 995份样品中4 981 份符合一致性要求(相对偏差≤20%),符合率为99.72%,见表2。
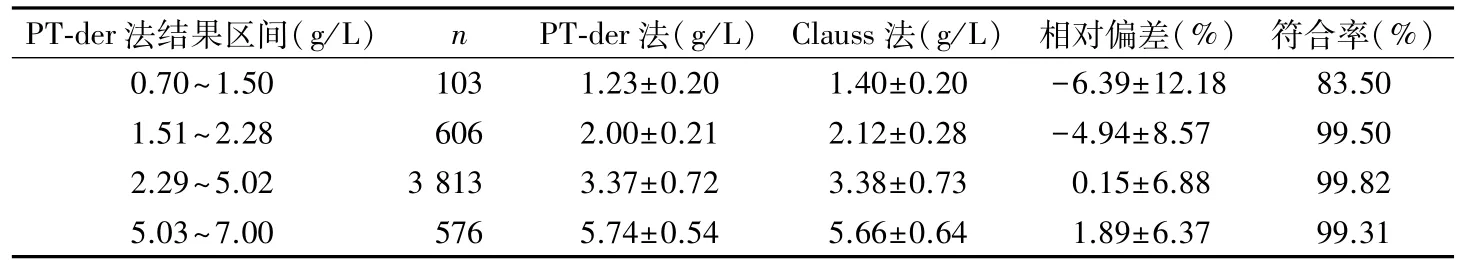
表2 重新校准后2种Fib检测结果的比较
2.4 实际应用 结合以上研究和验证结果设立本实验室Fib 的检测方案:2 台TOP Family 系列凝血仪先分别用本研究方法进行PT-der法校准,再用2种方法同时检测20 例以上样品,如PT-der 法95%及以上样品结果与Von Clauss 法结果的偏倚≤20%,则认为校准成功,反之重新校准。校准成功后日常所有Fib 的样本均使用PT-der 法进行初次检测,(1)如结果在1.51~7.00 g/L 范围内且未出现2.3.2中不适用条件时,直接报告结果;(2)如出现2.3.2中不适用条件,手动使用Von Clauss 法复测Fib;(3)如结果不在1.51~7.00 g/L范围内则会自动使用(已设置好的复检程序)Von Clauss 法复测Fib;(4)使用自建PT-der 法参考区间进行临床报告。在确立本方案后,本实验室半年中Fib 复测率仅为3.89%(418/10 975),如使用相关文献[8]报道方案估算复测率为35.65%(3 913/10 975),大幅度的提高了检测速度(PT、APTT、TT 和Fib 在TOP700联合检测可由原先的每小时60 例提升至每小时78例)和效率并减少了试剂开支。
3 讨论
Fib是凝血状态的重要标志物[13],近年来研究发现其水平过高易引起缺血性心脏病、心源性猝死等心血管疾病[14],其水平过低也会导致凝血过程中血凝块形成质量下降[15],从而易引起出血性疾病。Von Clauss法目前是Fib 检测的参考方法[5];而PT-der法可在仪器测定凝血酶原时间(prothrombin time)时,通过Fib形成的纤维蛋白,根据纤维蛋白浊度推算出Fib的含量[16],更为经济实用。有文献报道[4,17]PT-der 法和Von Clauss 法在正常范围内的检测结果较为接近,而在异常范围内则相差较大,也有学者认为PT-der 法不是一种可靠的方法[5,17-18]。
本实验室验证2种方法检测2.00~4.00 g/L浓度Fib的一致性时发现,PT-der 法检测Fib 的结果几乎均高于Von Clauss法10%~20%。查阅说明书后发现,上述2种方法使用同一校准品但赋值却不相同,所以推测赋值不同引起检测结果不同。一项多中心研究指出PT-der 和Von Clauss方法之间的偏差取决于校准曲线,且差异程度与校准曲线和血浆样品浊度有关[19]。而制造商提供的校准品浊度较高,考虑到这两方面因素,我们采用量值传递方式给新鲜清澈的混合血浆赋值,并以此重新校准PT-der法[16]。所谓量值传递就是将国际(国家)计量基准所复现的量值,通过检定或校准方式传递给下一级计量标准,并依次传递到工作计量器具,以保证量值准确一致[20]。本研究正是使用参考方法校准常规(下一级)方法,完全依照量值传递方式进行。因为Von Clauss法具有完整溯源链,所以重新校准的PT-der 法也可以沿着Von Clauss法溯源链一级一级追溯到NIBSC(原厂的溯源计量标准)。
关于2种方法结果相关性的研究较多,但大多数只停留于结果比对阶段,分析PT-der 法的结果是否准确,但不同品牌、不同型号的血凝仪2 种方法的差异程度也不尽相同[4]。而本研究却通过量值传递的方法重新校准并验证了PT-der 法,并使用大量样本的结果比对建立了PT-der 法的适用条件和范围,使2种方法检测结果在一定范围内可以互换。与此同时Rizzo等[21]也发现,不同方法检测到的Fib水平的偏差与肝硬化的严重程度有关,与本研究结果一致,即在肝硬化失代偿期,2 种方法的检测值偏差可能超过20%。
值得注意的一点是,2 种方法原厂给出的参考区间并不完全相同,但所查阅到的文献均未提及。因此,本研究对PT-der 法进行了重新校准,重新建立了本实验室的参考区间。在研究中,我们发现2种方法的一致性区间涵盖了2种方法的参考区间,而PT-der法参考区间又涵盖了Von Clauss法参考区间,加之实际应用中几乎所有一致性区间内的结果均使用PT-der 法检测,故可用PT-der 法参考区间进行临床报告。
需要指出,本研究仅使用本区域人群的检测数据,基于本实验室的设备和试剂并制定检测方案,不具有普遍适用性。不同实验室可借鉴此方法制定出适宜自己实验室的检测方案,在保证检验质量前提下以最小的成本和最快的速度为临床和广大患者服务。
