小儿宣肺止咳颗粒对大鼠的长期毒性反应*
2021-08-25郏自明任平远葛朝郑艳华樊军黎炎梅
郏自明,任平远,葛朝,郑艳华,樊军,黎炎梅
[1.湖北省疾病预防控制中心、应用毒理湖北省重点实验室,武汉 430075;2.健民集团叶开泰国药(随州)有限公司,随州 441300]
小儿宣肺止咳颗粒由麻黄、防风、西南黄芩、桔梗、芥子、苦杏仁、葶苈子、马兰、黄芪、山药、山楂、甘草等12味中药组成,临床功效为宣肺解表、清热化痰,主要用于治疗小儿外感咳嗽、痰热壅肺所致的咳嗽痰多、痰黄 黏稠、咳嗽不爽等症[1]。现代药理学表明麻黄、防风、西南黄芩、桔梗有解热镇痛的作用;麻黄、甘草、防风、西南黄芩、桔梗、马兰能有效抗菌、抗病毒;苦杏仁、山楂有明显的抑菌作用;麻黄、苦杏仁、甘草、桔梗、白芥子、葶苈子、山楂有镇咳祛痰的功效;甘草、防风、黄芪、西南黄芩、山楂能调节免疫功能[2],在体外培养细胞及小鼠体内对流感病毒株和柯萨奇B6病毒株均有抗病毒作用[3]。根据临床观察结果该药具有宣肺止咳、清热化痰的功效,可以用于治疗小儿支气管肺炎,可为临床用药提供新的选择[4]。本产品已在临床应用,批准文号为(97)卫药准字Z-029号,按照国家食品药品监督管理总局对该产品中药保护品种审批意见需完善药理、毒理等基础研究,因临床用药周期以3 d为1个疗程,所以本实验按照《药物非临床研究质量管理规范》(国家食品药品监督管理总局2017年9月1日颁布)和《药物重复给药毒性试验技术指导原则》(国家食品药品监督管理总局2014年5月颁布)设计大鼠重复经口给予小儿宣肺止咳颗粒1个月毒性实验,观察大鼠出现的毒性反应,并通过4周的恢复期观察,评估其所产生不良反应的性质和程度,寻找毒性靶器官和长期用药后可能出现的延迟性毒副反应,以期确定无毒性反应剂量,为拟定人用安全剂量提供参考。
1 材料与方法
1.1药物、溶媒与实验动物 小儿宣肺止咳颗粒由健民集团叶开泰国药(随州)有限公司提供,批号:160354,溶媒为纯化水。选取5~6周龄SPF级SD大鼠,雌雄各60只,雌性体质量80.8 ~110.5 g,雄性体质量87.1~112.0 g,大鼠体质量均未超出平均体质量的20%,购于湖北省实验动物研究中心,实验动物生产许可证号:SCXK(鄂)2015-0018,实验动物质量合格证号:42000600017879,实验大鼠饲养于屏障系统,实验动物使用许可证号:SYXK(鄂)2012-0065。实验动物设施使用证明号:00185628。
1.2主要仪器 SYSMEX2000全自动血球计数仪、CA-510全自动血凝分析仪(均为日本SYSMEX公司);AU680型全自动生化分析仪(贝克曼库尔特有限公司);迪瑞H-800全自动尿液分析仪(长春迪瑞医疗科技有限公司);Practum612-1CN动物天平[赛多利斯科学仪器(北京)有限公司,感量:10 mg];PL1501-S组织天平[梅特勒-托利多仪器(上海)有限公司,感量:0.01 mg];Excelsior ES全自动脱水仪、HistoStar全自动包埋仪、HM340E轮转切片机、Varistain Gemini全自动染色机、ClearVue全自动盖片机(均为美国Thermo公司);DM2500光学显微镜(德国LEICA公司)。
1.3实验方法 小儿宣肺止咳颗粒儿童每天最大临床用量为36.0 g,1 kg小儿宣肺止咳颗粒浸膏相当于2.595 kg成品颗粒,换算成浸膏每日用量为13.87 g。根据由体表面积公式lgS=0.876 2+0.698 lgW计算大鼠等效剂量(浸膏)为1.47 g·kg-1。根据厂家提供的资料及本中心前期做的大鼠急性毒性实验结果显示该供试品毒性较低,按照《药物重复给药毒性试验技术指导原则》要求大剂量应出现明显毒性反应或达到最大给药量,本实验大剂量采用最大给药量法,小剂量采用高于大鼠等效剂量的原则进行剂量设计。小儿宣肺止咳颗粒浸膏的最大密度为1.35 g·mL-1,大鼠按15 mL·kg-1灌胃计算得大剂量为20.25 g·kg-1·d-1(相当于临床剂量的72倍),小剂量大于大鼠等效剂量为3.00 g ·kg-1·d-1(相当于临床剂量的11倍),再设一中剂量为7.80 g ·kg-1·d-1(相当于临床剂量的28倍)。
大鼠按体质量分层随机分组设计[5]分为4组,即正常对照组和小儿宣肺止咳颗粒小、中、大剂量组(简称小、中、大剂量组)。每组大鼠30只,雌雄各15只。每天按15 mL·kg-1灌胃给药1次,连续给药1个月,正常对照组给予等体积的纯化水,每周按体质量调整一次给药量。给药1个月后各组取20只大鼠(雌雄各半)进行末期检查,停药后各组余10只大鼠(雌雄各半)进行4周的恢复期观察。每日观察1次大鼠的一般症状,包括外观体征、毛色、行为活动、尿液、粪便性状;每周检测1次大鼠体质量、进食量;血液学、血液生化学、尿液学、脏器系数和病理组织学检查分别在给药末期和恢复期观察结束后进行。
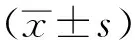
2 结果
2.1对大鼠一般状况的影响 本实验中未发生非计划大鼠死亡,给药期和恢复期各组大鼠的外观体征、行为活动、毛色、呼吸及对外界反应均未见明显异常。
2.2对大鼠体质量的影响 雌鼠:大剂量组大鼠体质量在给药第8天低于对照组(P<0.01),给药第15,22,29天和恢复期与正常对照组比较差异无统计学意义;小、中剂量组在给药期和恢复期大鼠体质量与正常对照组比较均差异无统计学意义。结果见表1。

表1 4组雌性大鼠在不同时间的体质量变化
雄鼠:大剂量组大鼠体质量在给药第8,15,22,29天均低于正常对照组(P<0.01),恢复期第36天大鼠体质量低于正常对照组(P<0.05),恢复期第43,50,57天大鼠体质量与正常对照组比较差异无统计学意义;中剂量组大鼠体质量在给药第8,15天均低于正常对照组(P<0.01),给药第22,29天和恢复期与正常对照组差异无统计学意义;小剂量组大鼠体质量在给药第8,15,22天均低于正常对照组(P<0.01,P<0.05),给药第29天和恢复期正常对照组比较差异无统计学意义。结果见表2。

表2 4组雄性大鼠在不同时间的体质量变化
2.3对大鼠摄食量的影响 雌鼠:大剂量组摄食量给药第1天低于正常对照组(P<0.01),给药第29摄食量低于正常对照组(P<0.05),给药第8,15,22天和恢复期摄食量与正常对照组比较差异无统计学意义;小剂量组在给药期和恢复期摄食量与正常对照组比较均差异无统计学意义。见表3。

表3 4组雌性大鼠在不同时间的摄食量变化
雄鼠:大剂量组摄食量在给药第1,8,22,29天均低于正常对照组(P<0.01,P<0.05),给药第15天和恢复期摄食量与正常对照组比较差异无统计学意义;中剂量组在给药期和恢复期摄食量与正常对照组比较均差异无统计学意义;小剂量组摄食量在给药第8天低于正常对照组(P<0.05),给药第1,15,22,29天和恢复期摄食量与正常对照组比较差异无统计学意义。见表4。

表4 4组雄性大鼠在不同时间的摄食量变化
2.4对眼科检查的影响 4组大鼠眼科检查双眼瞳孔反射均正常、眼底检查均无可见损伤。
2.5对血液学指标的影响 给药末期雌鼠中、大剂量组白细胞(WBC)均高于正常对照组,嗜酸性粒细胞比率(EOS%)低于正常对照组(P<0.01),红细胞平均血红蛋白浓度(MCHC)高于正常对照组(P<0.05);中剂量组大鼠淋巴细胞百分率(LYMP%)高于正常对照组(P<0.05);小、中、大剂量组大鼠EOS%低于正常对照组(P<0.01);恢复期中、大剂量组大鼠凝血酶原时间(prothrombin time,PT)低于正常对照组(P<0.05);其他指标与正常对照组比较均差异无统计学意义。给药末期雄鼠大剂量组EOS%低于正常对照组(P<0.05);恢复期中剂量组大鼠WBC、MCHC、血红蛋白(Hb)低于正常对照组(P<0.05)。其他指标[红细胞(RBC)、红细胞比容(HCT)、血小板(PLT)、红细胞平均体积(MCV)、红细胞平均血红蛋白含量(MCH)、中性粒细胞(NEUT)、单核细胞(MONO)、嗜碱性粒细胞(BASO)、网织红细胞(RET)、活化部分凝血活酶时间(APTT)]与正常对照组比较均差异无统计学意义。见表5,6。
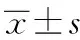
表5 4组雌性大鼠血液学指标的变化
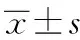
表6 4组雄性大鼠血液学指标的变化
2.6对血液生化学指标的影响 给药末期雌鼠大剂量组丙氨酸氨基转移酶(ALT)、总胆红素(T-BiL)、尿素氮(BUN)均高于正常对照组(P<0.05或P<0.01),血糖(GLU)、钠离子(Na+)、氯离子(Cl-)均低于正常对照组(P<0.05,P<0.01);中剂量组白蛋白(ALB)高于正常对照组(P<0.05)。其他指标与正常对照组比较均差异无统计学意义。给药末期雄鼠大剂量组ALT、BUN、T-BiL、碱性磷酸酶(ALP)高于正常对照组(P<0.01),GLU、Na+、Cl-低于正常对照组(P<0.01);中剂量组大鼠ALP、BUN高于正常对照组(P<0.01),Cl-低于正常对照组(P<0.05)。其他指标[天冬氨酸氨基转移酶(AST)、肌酐(CREA)、总胆固酮(CHOL)、三酰甘油(TG)、肌酸激酶(CK)、谷氨酰转移酶(γ-GT)、钾离子(K+)]与正常对照组比较均差异无统计学意义。见表7,8。
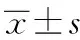
表7 4组雌性大鼠血液生化指标的变化
表8 4组雄性大鼠血液生化指标的变化
2.7对脏器系数的影响 给药末期和恢复期小、中、大剂量组大鼠脏器系数与正常对照组比较均差异无统计学意义。结果见表9,10。

表9 4组雌性大鼠脏器系数的变化

表10 4组雄性大鼠脏器系数的变化
2.8对脏器病理组织学的影响 给药末期大剂量组6只大鼠肝脏内少量炎症细胞浸润;大剂量组2只大鼠肝脏内少量肝细胞灶性坏死,炎症细胞浸润。中、小剂量组及恢复期正常对照组各仅1只大鼠肝脏内少量炎症细胞浸润,应属于大鼠自发病理改变,但大剂量组肝脏的病理改变发生数较正常对照组有所增加,表明该病理改变可能与供试品有关。停药4周,该病理改变消失。见图1。

图1 4组大鼠的肝脏病理组织学变化(HE,×200)
2.9尿液分析 给药末期大剂量组大鼠潜血、尿蛋白阳性率均低于正常对照组(P<0.01);中剂量组潜血阳性率低于正常对照组(P<0.01);小、中、大剂量组pH值均低于正常对照组(P<0.01);小、中、大剂量组大鼠尿胆原、尿胆红素、酮体、白细胞、尿糖、密度等指标与正常对照组比较均差异无统计学意义。结果见表11。

表11 4组大鼠尿液学指标的变化
3 讨论
小儿宣肺止咳颗粒由12味中药组成,按照工艺提取浓缩至浸膏后加入适量的蔗糖粉和糊精混匀制成颗粒。糊精和蔗糖粉均收录在药用辅料手册(原著第4版)[6],糊精在颗粒制剂中起到黏合剂的作用,蔗糖粉可以增加甜味和黏度,作为辅料应用的剂量下用于口服制剂处方中,基本无毒、无刺激性。小儿宣肺止咳颗粒中浸膏的含量占38.5%,而辅料占61.5%,为了充分观察受试物在大鼠体内最大暴露量的毒性反应情况,所以本实验采用去除糊精和蔗糖粉等辅料的浸膏作为受试物。
大鼠连续灌胃给予小儿宣肺止咳颗粒1个月,大剂量组雄性大鼠体质量在给药期至恢复期1周均低于正常对照组,大剂量组大鼠至恢复期结束体质量逐步恢复正常;中剂量给药后2周和小剂量给药后3周大鼠体质量低于正常对照组,之后中、小剂量大鼠体质量逐步恢复正常;雌性大鼠仅大剂量组给药后1周体质量低于正常对照组;由此表明本品对大鼠体质量有一定的抑制作用,尤以大剂量对体质量的影响较大,并且对雄性大鼠的影响较雌性大鼠明显,恢复4周后大鼠体质量可以恢复。大剂量组雄性大鼠摄食量在给药期低于正常对照组,恢复期恢复正常;小剂量组大鼠仅在给药后第2周摄食量低于正常对照组,雌性大鼠中、大剂量组仅给药后第1周和第29天大鼠摄食量低于正常对照组,未呈现规律性的剂量关系;由此表明本品大剂量对雄性大鼠摄食量有一定的抑制作用,停药后恢复。通过对本品大剂量对雄性大鼠体质量和摄食量的抑制作用分析,其原因可能与雄性大鼠因供试品灌胃浓度和体积较大有关。
大鼠血清生化指标的结果显示,大剂量组大鼠的ALT、T-BiL、ALP高于正常对照组,GLU低于正常对照组,以上血清生化指标均为反映肝功能的指标,同时病理组织学观察发现大剂量会引起部分大鼠肝脏炎症细胞浸润和个别大鼠少量肝细胞坏死,恢复期结束时以上指标均恢复正常;中剂量组仅雄性大鼠ALP、雌性大鼠ALB高于正常对照组,但其他反映肝功能的指标未见异常,病理组织学观察未发现中剂量组大鼠肝脏出现病理改变,并且这些数据处于文献数据[7-9]正常参考值的范围内,所以该两项指标数据在统计学上虽有一定的统计学意义,但无生物学意义;本研究表明小儿宣肺止咳颗粒大剂量可引起肝脏轻度损伤,停药4周后可恢复正常。中、大剂量组大鼠的BUN高于正常对照组,Na+、Cl-低于正常对照组,但这些数据处于本中心大鼠历史背景数据正常血液学参考值和文献数据[7-9]正常血液学参考值的范围内,结合病理组织学观察未发现大鼠肾脏出现病理改变,在本实验中可判定以上数据虽有一定的统计学意义,应无生物学意义。
从实验结果可知大鼠血清γ-GT测定值水平较低,陈威等[10]报道γ-GT是一种胚胎蛋白,在成年大鼠活性很低,只有在化学致癌剂诱发肝癌的早期阶段其活性才会异常升高,说明在本实验中大鼠血清的γ-GT活性水平很低,和文献报道基本一致。
给药末期中、大剂量组大鼠WBC高于正常对照组,EOS(%)低于正常对照组;恢复期中剂量组大鼠WBC低于正常对照组,中、大剂量组大鼠PT低于正常对照组,以上数据未呈现一定的规律性,也无一定剂量反应关系,并且这些数据均处于文献数据[6-8]正常参考值的范围内,提示在本实验中可判定以上数据虽有一定的统计学意义,但无生物学意义。
给药末期潜血、尿蛋白阳性率与正常对照组比较有显著差异,由于该两项指标阳性率低于低于正常对照组,虽然有一定的统计学意义,但无生物学意义。给药末期小、中、大剂量组大鼠尿液pH值低于正常对照组,停药4周后恢复正常,文献资料[11]显示大鼠尿液pH正常值参考范围7.38~8.50,杨趁霞[12]报道影响尿液pH值的因素多是食物酸碱性和所服药物酸碱性所造成,委托方提供的小儿宣肺止咳颗粒检测报告显示样品pH值为4.44,由此分析小、中、大剂量组大鼠尿液pH值下降的原因可能为供试品呈酸性所致,结合尿液其他指标可判定无生物学意义。
综上所述,大鼠连续灌胃给予小儿宣肺止咳颗粒1个月, 7.80 g·kg-1·d-1为安全剂量,根据体表面积等效剂量换算为临床剂量的28倍;对大鼠体质量有一定的抑制作用,尤以大剂量对体质量的影响较大,并且对雄性大鼠的影响较雌性大鼠明显;大剂量对雄性大鼠摄食量有一定的抑制作用,大剂量可引起肝脏轻度损伤,停药4周后药物的毒性反应可逆,亦未见药物引起的其他延迟性毒性反应。
