精制冠心片质控方法再评价研究
2021-08-23鄢必新田淋淋
李 双,鄢必新,张 颖,田淋淋,张 斌,李 敏,徐 建*
(1.吉林修正药业新药开发有限公司,吉林省中药标准化关键工程技术重点实验室,长春130103;2.修正药业集团股份有限公司,通化134000)
精制冠心片处方由丹参、川芎、赤芍、红花、降香5味中药组成,具有活血化瘀的功效,用于淤血内停所致的胸痹,症见胸闷、心前区刺痛;冠心病心绞痛见上述候症者。质量标准收载于《中国药典》2020年版一部,标准中采用薄层色谱法对丹参、赤芍、川芎、红花进行定性鉴别;采用高效液相色谱法对丹参中丹酚酸B、丹参酮ⅡA和赤芍中芍药苷进行定量分析;为有效控制产品质量,保证产品疗效,对《中国药典》中检测方法进行再评价研究,并对其未收载的降香进行薄层鉴别研究,以有效控制其产品内在质量。
1 仪器与试药
1.1 仪器
戴安U3000高效液相色谱仪(赛默飞世尔科技(中国)有限公司);MS205DU型电子天平(梅特勒-托利多公司);SB25-12DT型超声波清洗器(宁波新芝生物科技股份有限公司);薄层色谱摄影仪SLD-1(天津思利达色谱技术开发公司)。
1.2 试剂与试药
1.2.1试药
精制冠心片(批号:01-03糖衣片、04-06薄膜衣片),均由修正药业集团股份有限公司提供;对照品来源:丹参对照药材(批号:120923-201615)、川芎对照药材(批号:120918-201411)、红花对照药材(批号:120907-200609)、降香对照药材(批号:120952-200506)、芍药苷对照品(批号:110736-201438)、丹参酮ⅡA对照品(批号:110766-201721)、丹酚酸B对照品(批号:111562-201716)以上均购于中国食品药品检定研究院。
1.2.2 试剂
乙醚、乙酸乙酯、石油醚(60~90℃)、甲醇、正己烷、甲苯、正丁醇、丙酮、甲酸、硫酸、乙醇、磷酸、三氯甲烷、三氯化铝、香草醛等均为分析纯,乙腈为色谱纯,水为纯化水。
2 方法与结果
2.1 丹参的薄层鉴别
取本品5片,糖衣片除去糖衣,研细,加乙醚20ml,超声处理15分钟,滤过,滤液挥干,残渣加乙酸乙酯lml使溶解,作为供试品溶液。另取丹参对照药材0.2g,加甲醇2ml,超声处理10分钟,静置,取上清液作为对照药材溶液。再取缺丹参阴性样品,同供试品方法制成阴性样品溶液。照薄层色谱法(中国药典2020年版四部通则0502)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(8∶3)为展开剂,展开,取出,晾干。在日光下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点。阴性无干扰。结果见图1。
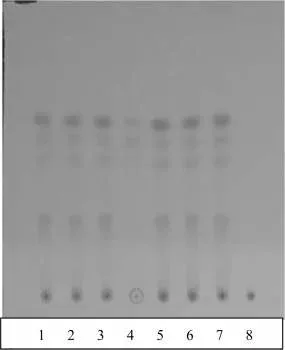
图1 丹参薄层色谱图
2.2 川芎的薄层鉴别
取川芎对照药材0.2g,加甲醇2ml,超声处理10分钟,静置,取上清液作为对照药材溶液。另取缺川芎阴性样品,同(2.1)供试品制备方法制成阴性样品溶液。照薄层色谱法(中国药典2020年版四部通则0502)试验,吸取[鉴别]2.1项下的供试品溶液及上述对照药材溶液各2μl,分别点于同一硅胶G薄层板上,以正己烷-甲苯-乙酸乙酯(9∶2∶1)为展开剂,展开,取出,晾干,在紫外光(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光主斑点。阴性无干扰。结果见图2。
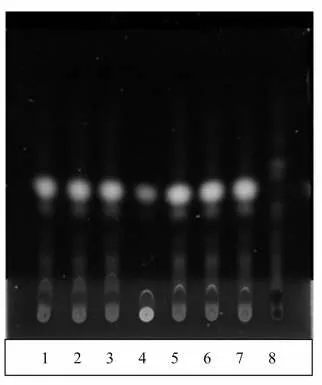
图2 川芎薄层色谱图
2.3 红花的薄层鉴别
取本品15片,糖衣片除去糖衣,研细,加甲醇30ml,摇散,超声处理30分钟,滤过,滤液回收溶剂至干,残渣加水20ml,加热搅拌使溶解,放冷,以脱脂棉滤过,滤液用水饱和的正丁醇振摇提取2次,每次20ml,合并正丁醇液,加水15ml洗涤,取正丁醇液回收溶剂至干,残渣加水10ml,加热约3分钟,充分搅拌使溶解,放冷,以少量脱脂棉滤过,滤液加于聚酰胺柱(2g,80~100目,柱内径为1.5~2cm,干法装柱)上,依次以水25ml、20%甲醇15ml洗脱,合并上述两种洗脱液,备用,继以75%甲醇30ml洗脱,收集洗脱液,回收溶剂至干,残渣加甲醇1ml使溶解,作为供试品溶液。另取红花对照药材0.2g,加甲醇10ml,超声处理15分钟,滤过,滤液回收溶剂至干,残渣加水10ml使溶解,以脱脂棉滤过,滤液自“加于聚酰胺柱........”起同法制成对照药材溶液。再取缺红花阴性样品,同供试品方法制成阴性样品溶液。照薄层色谱法(中国药典2020年版四部通则0502)试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-甲酸-水(6∶3∶0.3∶1)为展开剂,展开,取出,晾干,喷以含2%三氯化铝的10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,在紫外光(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光主斑点,阴性样品无干扰。结果见图3。
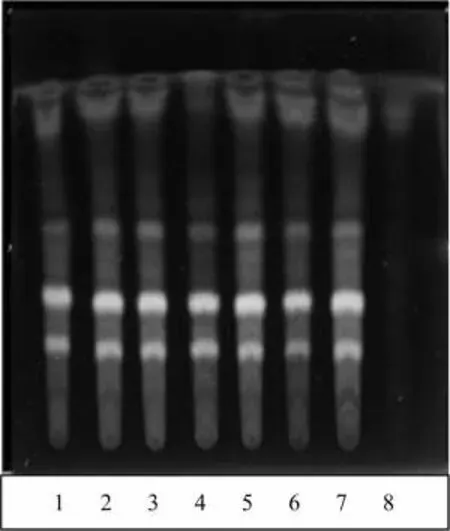
图3 红花薄层色谱图
2.4 赤芍的薄层鉴别
取(2.3)项下的备用洗脱液,用水饱和正丁醇20ml振摇提取,分取正丁醇液,回收溶剂至干,残渣加甲醇1ml使溶解,作为供试品溶液。另取芍药苷对照品,加甲醇制成每1ml含2mg的溶液,作为对照品溶液。再取缺赤芍阴性样品,同供试品制备方法制成阴性样品溶液。照薄层色谱法(中国药典2020年版四部通则0502)试验,吸取上述三种溶液各2μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以2%香草醛硫酸溶液,在105℃加热至斑点显色清晰,置日光下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,阴性样品无干扰。结果见图4。
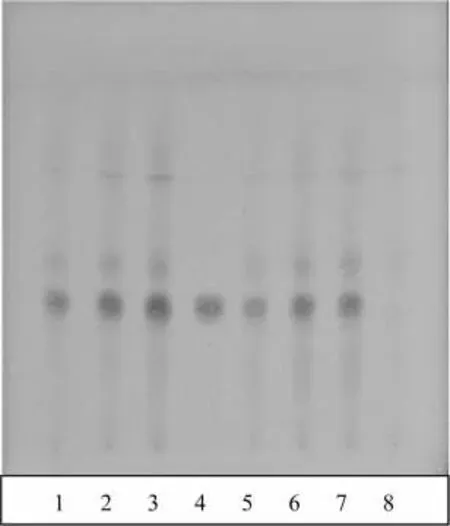
图4 赤芍薄层色谱图
2.5 降香鉴别方法摸索
2.5.1 色谱条件选择
参照中国药典2020年版有关降香及其他文献对降香的薄层鉴别方法进行摸索,具体试验及结果如下。
2.5.2 条件筛选
2.5.2.1 供试品制备方法筛选
方法一:取本品5片,糖衣片除去糖衣,研细,加甲醇30ml,超声30分钟,滤过,滤液蒸干,残渣加甲醇2ml使溶解作为供试品溶液(1)。另取降香对照药材0.5g,同法制成对照药材溶液。再取缺降香阴性样品,同供试品制备方法制成阴性样品溶液。
方法二:取本品5片,糖衣片除去糖衣,研细,加70%乙醇,超声处理30分钟,滤过,滤液蒸干,残渣加乙醇2ml使溶解作为供试品溶液(2)。另取降香对照药材0.5g,同法制成对照药材溶液。再取缺降香阴性样品,同供试品制备方法制成阴性样品溶液。
2.5.2.2 色谱条件筛选
照薄层色谱法(中国药典2020年版四部通则0502)试验,分别吸取上述供试品溶液(1)及相应的对照药材、阴性样品溶液及供试品溶液(2)及相应的对照药材、阴性样品溶液各2μl,分别点于同一硅胶G薄层板上,再分别以甲苯-乙醚-三氯甲烷(7∶2∶1)、石油醚(60~90℃)-乙酸乙酯(16∶3)、甲苯-乙酸乙酯-甲酸(8∶10∶2)、甲苯-乙酸乙酯(2∶1)为展开剂,展开,取出,晾干,置紫外光(365nm)下检视。
2.5.2.3 结果
上述供试品色谱中在与对照药材色谱相应的位置上显相同颜色的斑点,但阴性样品均有干扰,专属性不强,故降香的薄层鉴别未收载于精制冠心片质量标准项下。
2.6 丹参、赤芍的含量测定
2.6.1 色谱条件
以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以0.1%磷酸溶液为流动相B,按下表中的规定进行梯度洗脱;芍药苷、丹酚酸B检测波长为230nm,丹参酮ⅡA检测波长为270nm。理论板数按芍药苷峰计算应不低于8000。
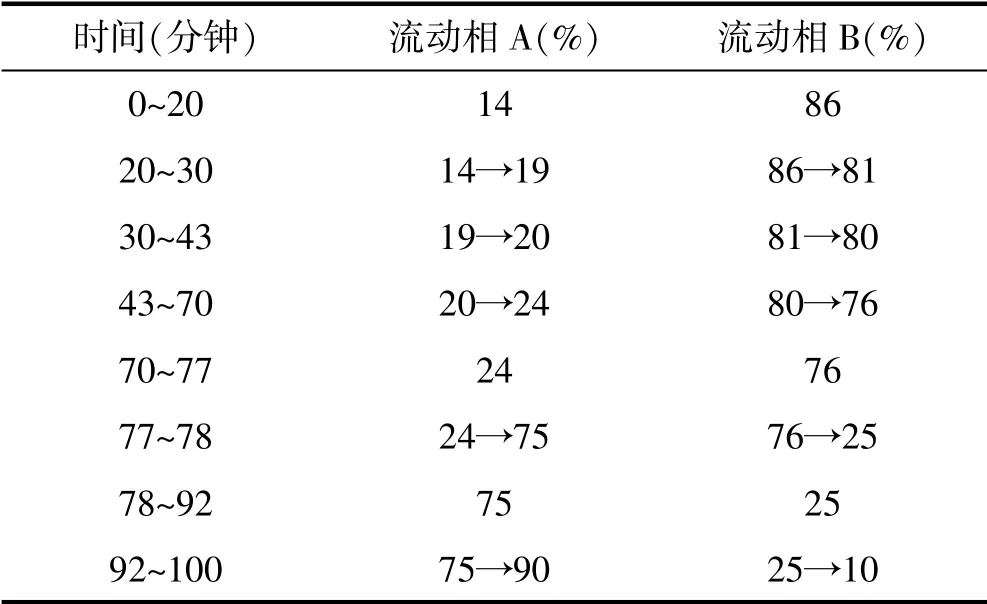
时间(分钟) 流动相A(%) 流动相B(%)0~20 14 86 20~30 14→19 86→81 30~43 19→20 81→80 43~70 20→24 80→76 70~77 24 76 77~78 24→75 76→25 78~92 75 25 92~100 75→90 25→10
2.6.1.1 对照品溶液的制备
取芍药苷对照品、丹酚酸B对照品、丹参酮ⅡA对照品适量,精密称定,加甲醇制成每lml各含芍药苷80μg、丹酚酸B 0.16mg、丹参酮ⅡA10μg的混合溶液,即得。
2.6.1.2供试品溶液的制备
取装量差异项下本品10片,除去包衣,精密称定,研细,取约0.5g,精密称定,精密加入75%甲醇25ml,密塞,称定重量,超声处理(功率400W,频率40kHZ)40分钟,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.6.1.3 阴性样品溶液的制备
取按处方比例缺丹参的阴性对照样品和按处方比例缺赤芍的阴性对照样品,按“2.6.1.2”项下方法分别制备丹参、赤芍阴性样品溶液。
2.6.1.4 测定法
分别精密吸取对照品溶液与供试品溶液各5μl,注入液相色谱仪,测定。
2.6.2 线性关系考察
取芍药苷对照品溶液,浓度分别为0.0163、0.0490、0.0817、0.1144、0.1470mg/ml。精密吸取上述对照品溶液各5μl,分别注入液相色谱仪,测定峰面积,以峰面积为纵坐标(Y),以进样量为横坐标(X),绘制标准曲线,回归方程为Y=24.906x-0.9882,r=0.9998。表明芍药苷在0.1785~3.57μg范围内呈良好线性关系。
取丹参酮ⅡA对照品溶液,浓度分别为0.0024、0.0071、0.0119、0.0190、0.0238mg/ml。精密吸取上述对照品溶液各5μl,分别注入液相色谱仪,测定峰面积,以峰面积为纵坐标(Y),以进样量为横坐标(X),绘制标准曲线,回归方程为Y=106.96x-0.5349,r=0.9997。表明丹参酮ⅡA在0.0297~0.5944μg范围内呈良好线性关系。
取丹酚酸B对照品溶液,浓度分别为0.0059、0.0177、0.0294、0.0412、0.0530mg/ml。精密吸取上述对照品溶液各5μl,分别注入液相色谱仪,测定峰面积,以峰面积为纵坐标(Y),以进样量为横坐标(X),绘制标准曲线,回归方程为Y=32.757x-0.368,r=0.9998。表明丹酚酸B在0.1462~2.9234μg范围内呈良好线性关系。
2.6.3 专属性试验
分别精密吸取“2.6.1”项下对照品溶液、供试品溶液及阴性样品溶液各5μl,注入液相色谱仪,依法测定。结果阴性对照样品的色谱图中,在与芍药苷、丹参酮ⅡA、丹酚酸B对照品吸收峰保留时间的相应位置上,无吸收峰出现,表明阴性对照无干扰,此方法专属性强。详见图5~11。
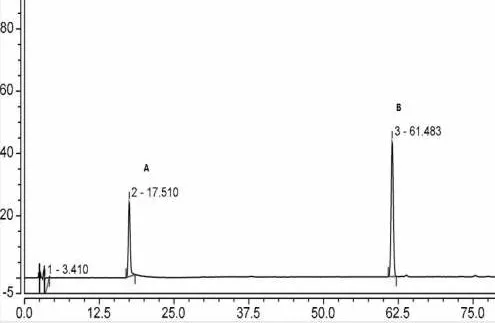
图5 230nm-混合对照品
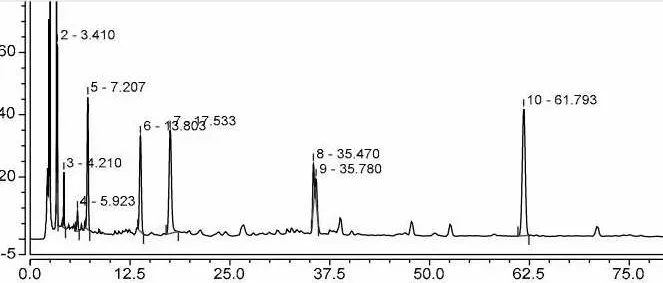
图6 230nm-供试品
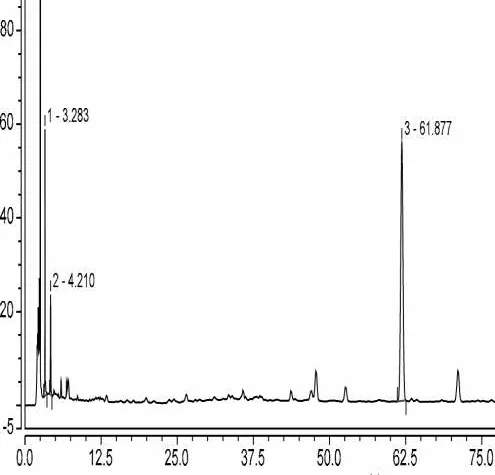
图7 230nm-赤芍阴性(芍药苷)
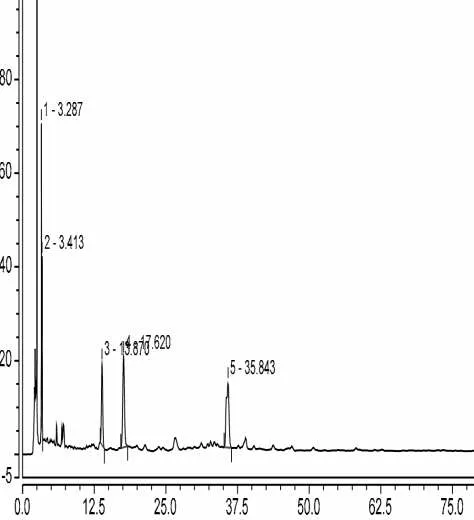
图8 230nm-丹参阴性(丹酚酸B)

图9 270nm-混合对照品(C丹参酮ⅡA对照品)
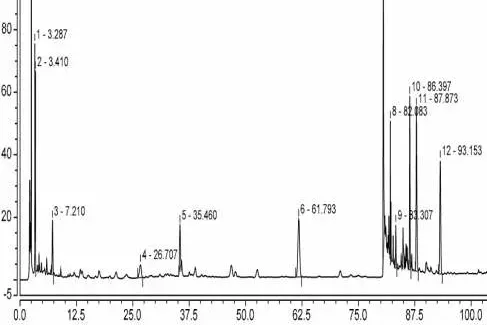
图10 270nm-供试品
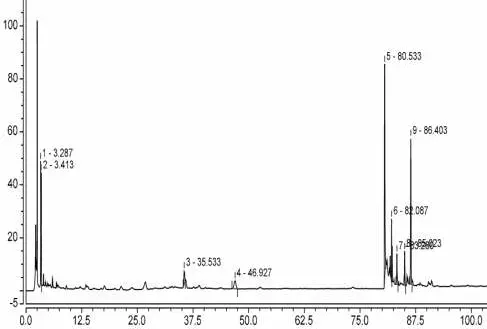
图11 270nm-丹参阴性(丹参酮ⅡA)
2.6.4 精密度试验
取芍药苷、丹酚酸B、丹参酮ⅡA混合对照品溶液重复进样6次,每次5μl,结果芍药苷峰面积RSD=0.91%(n=6),丹酚酸B峰面积RSD=0.24%(n=6),丹参酮ⅡA峰面积RSD=0.36%(n=6),表明仪器精密度良好。
2.6.5 稳定性试验
取同一供试品溶液,分别于0、2、4、8、12、18、24h按“2.6.1”项下色谱条件测定,记录峰面积,结果芍药苷RSD=1.14%、丹酚酸B RSD=0.90%、丹参酮ⅡA RSD=0.12%,表明供试品溶液在24小时内稳定。
2.6.6 重复性试验
取同一批样品(01批)适量,除去包衣,精密称定,研细,取约0.5g,精密称定,共6份,按“2.6.1”项下方法制备供试品溶液,按“2.6.1”项下色谱条件测定芍药苷、丹酚酸B、丹参酮ⅡA含量。结果芍药苷的平均含量为7.85mg/g,RSD=0.37%,丹酚酸B平均含量为11.44mg/g,RSD=0.38%(n=6),丹参酮ⅡA平均含量为1.20mg/g,RSD=0.31%,表明此方法重复性良好。
2.6.7 加样回收率试验
精密称取已知含量(芍药苷含量7.85mg/g、丹酚酸B含量11.44mg/g、丹参酮ⅡA含量1.20mg/g)的同一批供试品(01批)粉末共6份,每份约0.25g,分别精密加入适量混合对照品溶液,按“2.6.1”项下方法制备供试品溶液并测定,计算回收率,结果芍药苷、丹酚酸B、丹参酮ⅡA平均回收率分别为99.08%、98.76%、99.12%,RSD值分别为0.62%、0.48%、0.65%。结果见表1。
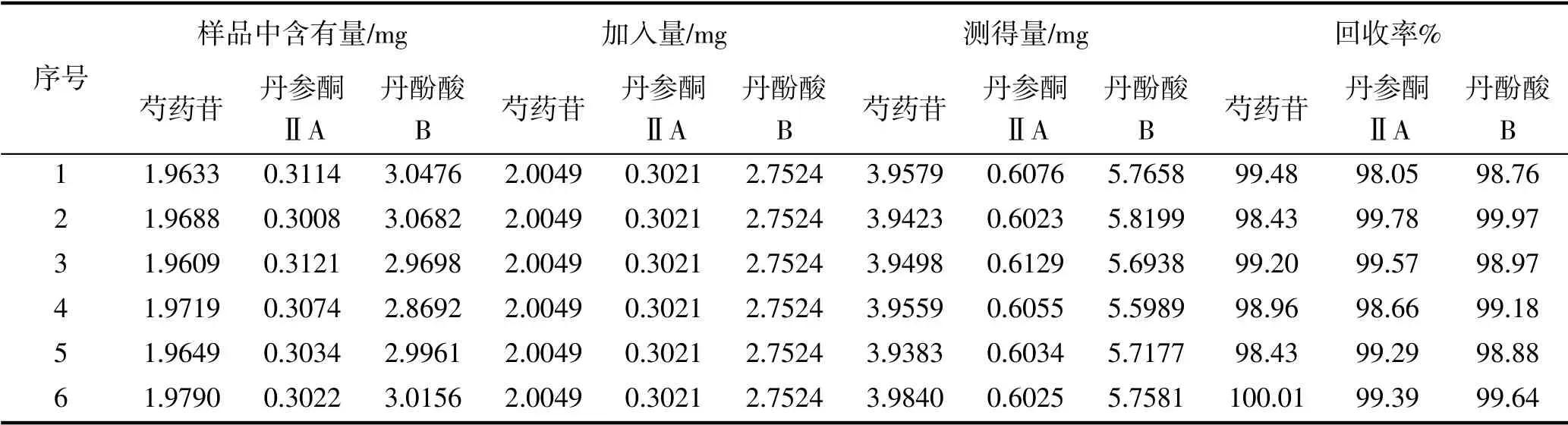
表1 加样回收率试验结果
2.6.8 样品含量测定
依“2.6.1”项下方法对上述6批精制冠心片(批号:01-06)进行含量测定,结果见表2。
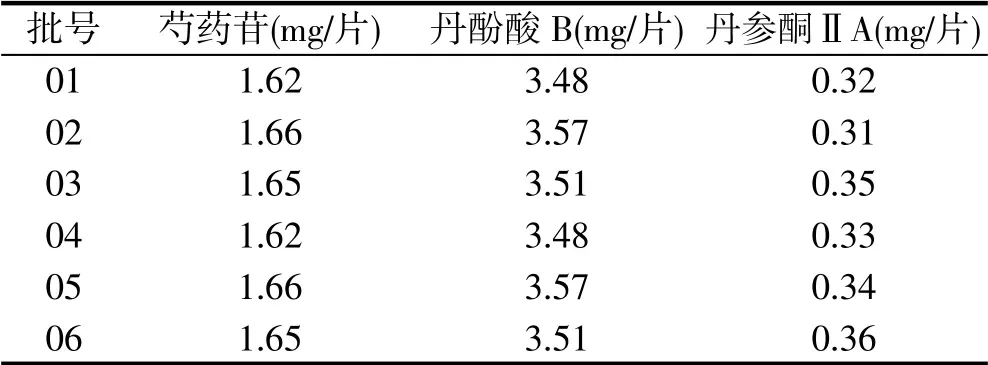
表2 6批样品含量测定结果
3 讨论
本次研究对方中各药味进行了较系统的质量标准研究,采用薄层色谱法对制剂中的丹参、赤芍、川芎、红花、降香进行定性鉴别研究,结果表明丹参、川芎、红花、赤芍薄层色谱鉴别方法重现性好,专属性强,可以列入质量标准,降香薄层色谱鉴别阴性有干扰,专属性较差,故未列入质量标准。同时本实验采用高效液相色谱法,对丹参中有效成分丹酚酸B、丹参酮ⅡA和赤芍中有效成分芍药苷进行定量分析研究。经方法学验证,方法可行、精密度高、重现性好,可准确有效控制产品质量。本次质控方法再评价研究,为精制冠心片质量控制方法提供了一定数据支持,具有重要研究和应用价值,并能更加全面地把控精制冠心片的质量。
