不同产地丹参药材中四种丹参酮类成分的定性鉴别和含量测定
2021-05-24胡国辉
胡国辉
(广州中医药大学第一附属医院 药学部,广东 广州 510405)
丹参为唇形科植物丹参(SalviamiltiorrhizaBge.)的干燥根和根茎,具有活血祛瘀、通经止痛、清心除烦、凉血消痈的功效[1-3]。临床上主要用于治疗心血管疾病、肝脏及神经系统疾病,丹参药材的活性成分主要分为两大类,脂溶性成分[4-7]和水溶性成分[8-10],脂溶性成分主要是丹参酮型的二萜醌类化合物,是丹参活血化瘀、抗炎和抑制血管平滑肌细胞增殖的主要成分,包括丹参酮IIA、丹参酮IIB、隐丹参酮、二氢丹参酮I等,其中丹参酮IIA含量是最高的,也是丹参治疗冠心病的主要有效成分之一[11-12],此外就是丹参的水溶性化学成分,主要是酚酸类化合物,包括原儿茶醛、原儿茶酸、丹参素钠、丹酚酸A、迷迭香酸、咖啡酸等,丹参的水溶性成分与药理活性基本相似,均具有抗心肌缺血与缺氧的作用[13-15],2015版药典[2]丹参药材项下脂溶性成分主要是通过一测多评法测定丹参酮IIA、隐丹参酮和丹参酮I的含量及薄层鉴别法鉴别丹参酮IIA,本实验在前期的预实验中发现丹参药材中脂溶性成分二氢丹参酮也可以同时测出,且二氢丹参酮也具有抗菌、抗氧化和扩张冠状血管等活性,与丹参的药理作用一致,因此有必要对其进行测定,故本实验增加丹参酮类成分的定性鉴别及含量测定,从而更加全面控制丹参药材的质量。
1 仪器与试药
Agilent 1260高效液相色谱仪(美国安捷伦仪器公司),Agilent chemstation色谱工作站,Agilent XDB C18(4.6 mm×250 mm,5 μm)色谱柱,硅胶GF254薄层板(10 cm×20 cm)(Merck公司),乙腈为色谱纯(美国Fisher公司),磷酸为GR级(上海国药化学试剂公司);ML204T、XPE205电子分析天平(METTLER TOLEDO公司)。对照品:二氢丹参酮,批号:D101537,含量以98.0%计;丹参酮I,批号:T118876,含量以97.0%计,购自上海阿拉丁生化科技股份有限公司;隐丹参酮,批号:110852-200806,含量以98.7%计;丹参酮IIA,批号:110766-201520,含量以98.9%计,购自中国食品药品检定研究院。石油醚(60~90 ℃)、乙酸乙酯、环己烷等试剂均购自上海国药化学试剂公司,不同产地丹参药材来源见附表1。

表1 丹参药材样品来源
2 方法与结果
2.1 四种脂溶性成分的TLC鉴别
取不同产地的丹参药材粉碎,过二号筛,取粉末1 g,加乙醚10 mL,静置1 h,然后滤过,滤液挥发溶剂至干,残渣加甲醇1 mL使溶解,作为供试品溶液,另取二氢丹参酮、丹参酮I隐丹参酮和丹参酮IIA对照品,加甲醇制成每1 mL分别含1 mg的溶液,作为对照品溶液。按照薄层色谱法(通则0502)试验,吸取上述供试品溶液和对照品溶液各2 μL,分别点于同一高效硅胶GF254薄层板上,用石油醚(60~90℃)-乙酸乙酯-环己烷(5∶3∶2)为展开剂,展开,取出,晾干,分别在日光及紫外灯(254 nm)下检视,供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上显相同颜色的斑点和荧光斑点。见图1。
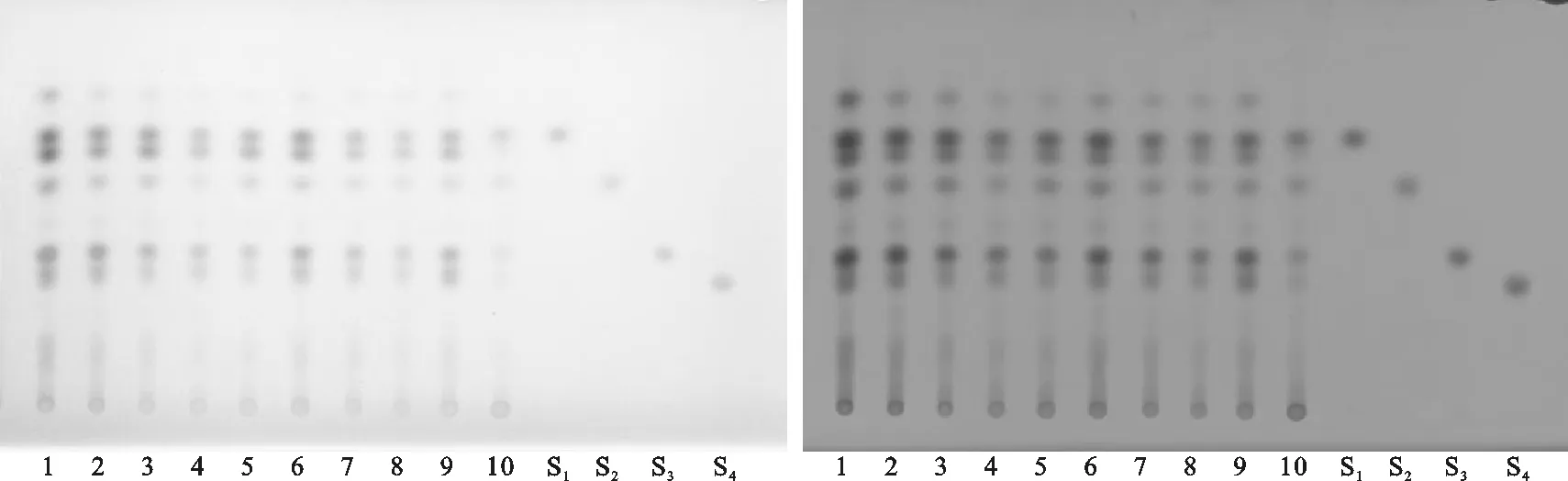
注:1.山东泰安薛家庄;2.山东临沂麦坡村;3.山东临沂常岭村;4.山东潍坊临朐县;5.四川中江县金钱村;6.四川广元苍溪县;7.四川广元青川县;8.陕西商洛镇安县;9.陕西汉中西乡县;10.陕西商洛商南县;S1 丹参酮IIA;S2丹参酮I; S3.隐丹参酮;S4.二氢丹参酮。
2.2 色谱条件
Agilent XDB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相:以乙腈为流动相A,0.03%磷酸为流动相B,按下表2梯度洗脱;柱温20 ℃,流速1.0 mL·min-1,检测波长:270 nm;理论塔板数按丹参酮IIA峰计算应不低于10 000。
2.3 对照品溶液制备
精密称取二氢丹参酮对照品10.58 mg、隐丹参酮对照品12.39 mg、丹参酮I对照品6.52 mg,丹参酮IIA对照品17.26 mg置同一25 mL量瓶中,加二氯甲烷2 mL,振摇使溶解,加甲醇稀释至刻度,摇匀,作为6号对照品溶液;精密吸取6号对照品溶液3 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为5号对照品溶液;精密吸取5号对照品溶液3 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为4号对照品溶液;精密吸取4号对照品溶液3 mL,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为3号对照品溶液;精密吸取3号对照品溶液,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为2号对照品溶液;精密吸取2号对照品溶液,置10 mL量瓶中,加甲醇稀释至刻度,摇匀,作为1号对照品溶液。

表1 流动相洗脱程序
2.4 供试品的制备
取山东泰安薛家庄丹参药材粉末样品(过三号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入75%甲醇溶液50 mL,称定重量,超声处理(功率500 W,频率53 kHz)30 min,取出放凉,再称定重量,用75%甲醇补足减失重量,摇匀,滤过,取续滤液用0.45 μm滤膜滤过,即得。
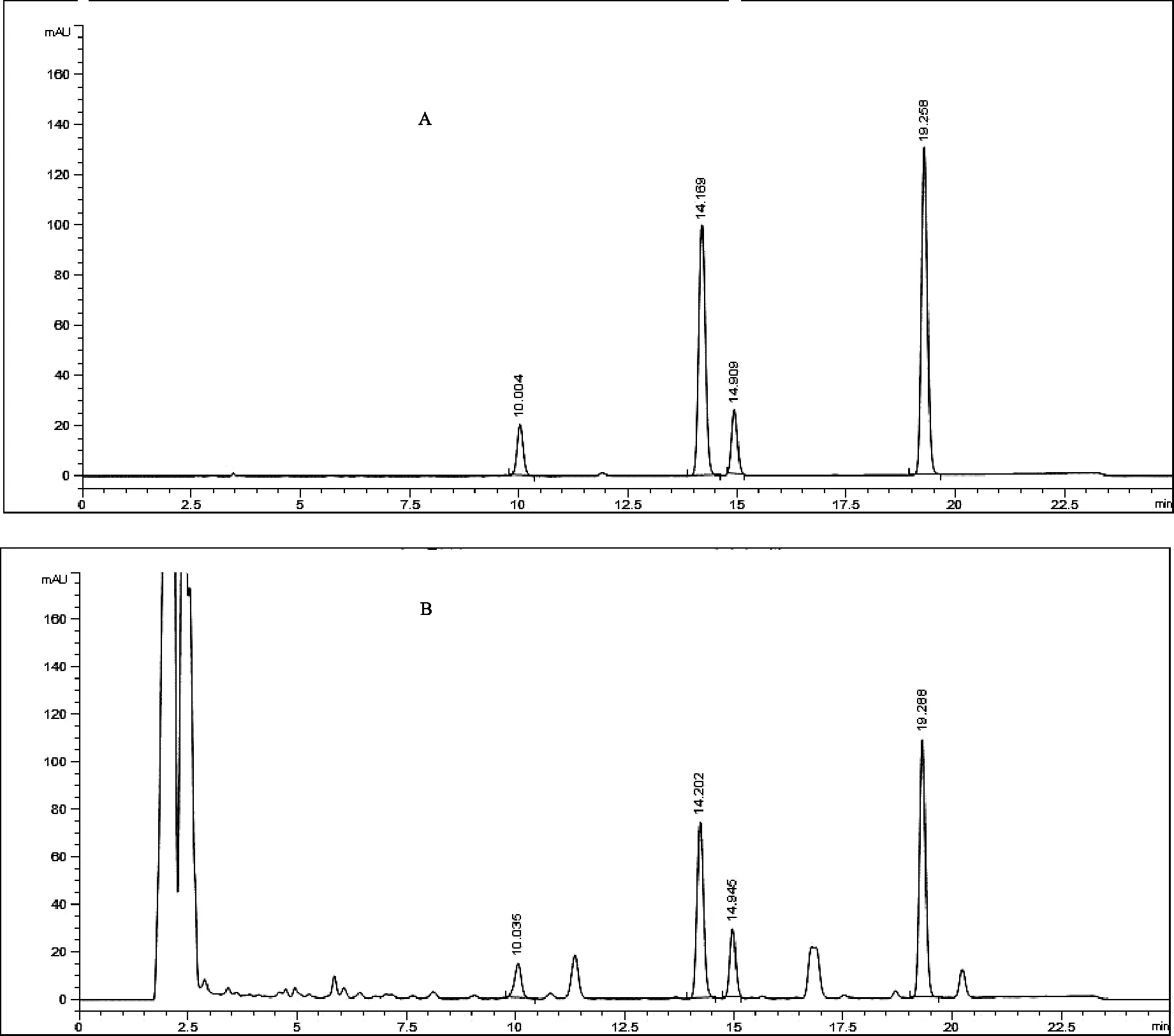
注:A为混合对照品;B为供试品(从左到右四个峰依次为二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA)
2.5 方法学考察
2.5.1 线性关系考察 精密吸取1~6号对照品溶液各10 μL,注入液相色谱仪,各进样2次,按照预实验确定的色谱条件(C18色谱柱,4.6 mm×250 mm,5 μm,流动相,A为乙腈,B为0.03%磷酸,梯度洗脱,柱温20 ℃,流速1.0 mL/min,检测波长:270 nm)测定峰面积,以峰面积的平均值为纵坐标,进样量的质量(ng)为横坐标,计算回归方程,结果见表2。

表2 4种丹参酮类成分的线性方程、线性范围及相关系
2.5.2 精密度 分别精密吸取上述“2.3”项下的1、3、6号混合对照品溶液各10 μL,注入液相色谱仪,按照“2.2”项下的色谱条件各进样6次,结果1号对照品中二氢丹参酮、丹参酮I、隐丹参酮和丹参酮IIA峰面积的RSD分别为0.55%、0.38%、1.22%和0.76%;3号对照品中二氢丹参酮、丹参酮I、隐丹参酮和丹参酮IIA峰面积的RSD分别为1.58%、2.02%、1.77%和1.62%;6号对照品中二氢丹参酮、丹参酮I、隐丹参酮和丹参酮IIA峰面积的RSD分别为0.47%、0.51%、0.56%和0.32%,结果表明仪器的进样精密度良好。
2.5.3 重复性 取山东泰安薛家庄丹参药材粉末(过三号筛)约0.5 g,精密称定,共6份,置具塞锥形瓶中,分别精密加入75%甲醇溶液50 mL,称定重量,超声处理20 min,取出放凉,再称定重量,用75%甲醇补足减失重量,摇匀,滤过,取续滤液用0.45 μm滤膜滤过,即得。按照“2.2”项下的色谱条件测定,结果二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA含量值的RSD分别为0.27%、0.58%、0.42%和1.03%,表明该方法重复性良好。
2.5.4 稳定性 取上述重复性项下的一份样品,分别于0 h、1 h、2 h、4 h、8 h、12 h、16 h、20 h和24 h各进样1次,按照“2.2”项下的色谱条件测定,结果二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA峰面积值的RSD分别为1.05%、0.92%、0.35%和1.66%,结果表明该供试品溶液在24 h内稳定性良好。
2.5.5 加样回收试验 精密称取二氢丹参酮对照品6.82 mg,丹参酮I对照品8.56 mg,置同一10 mL量瓶中,加二氯甲烷1 mL使溶解,然后加甲醇稀释至刻度,摇匀,作为储备溶液;另精密称取隐丹参酮对照品5.88 mg、丹参酮IIA对照品7.36 mg,置同一10 mL量瓶中,精密加入上述储备溶液2 mL,加入甲醇溶解至刻度,摇匀,作为加样用对照品溶液。另精密称取山东泰安薛家庄丹参药材(过3号筛)样品0.25 g,共6份,分别置具塞锥形瓶中,每组分别精密加入上述加样用对照品溶液各1 mL,再精密加入75%甲醇50 mL,称定重量,超声处理30 min,取出放凉,再称定重量,用75%甲醇补足减失重量,摇匀,滤过,取续滤液用0.22 μm滤膜滤过,取续滤液即得。按照重复性项下的色谱条件和对照品溶液进行测定,结果见表3。

表3 丹参药材中4种丹参酮类成分的加样回收试验结果 (n=6)
2.5.6 检出限和定量限 按照空白溶剂实验分别计算3倍噪音和10倍噪音作为方法的检出限和定量限,结果二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA的检出限分别为0.612 μg·g-1、0.307 μg·g-1、0.528 μg·g-1和1.34 μg·g-1,定量限为2.04 μg·g-1、1.02 μg·g-1、1.76 μg·g-1和4.47 μg·g-1。
2.6 含量测定
取不同产地的10批次丹参药材按照上述“2.4”方法制备,“2.2”项下色谱条件进行测定,测定结果见表4。
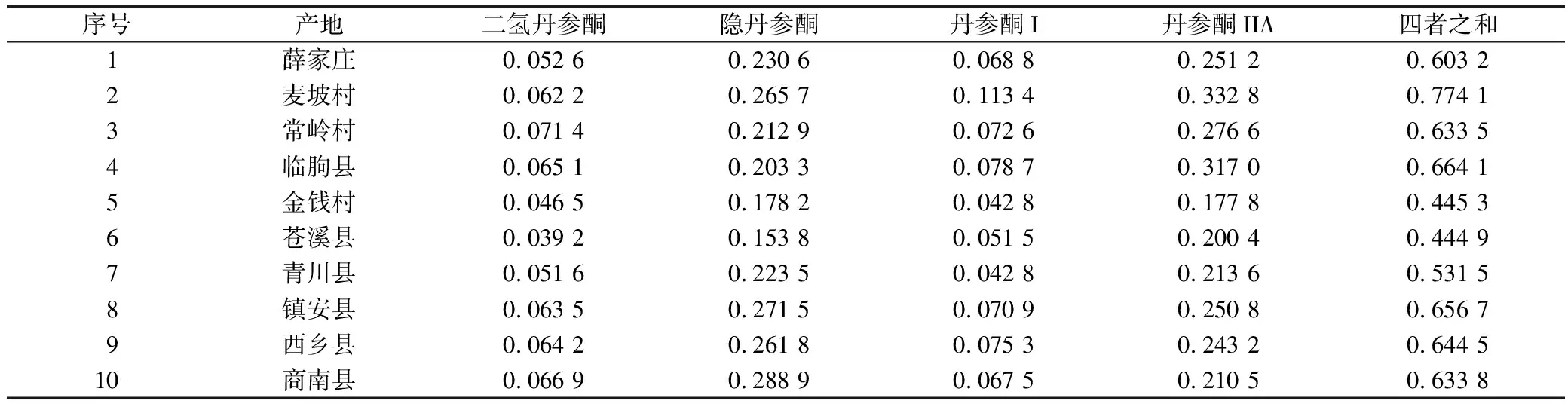
表4 丹参药材中二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA含量测定结果 (%)
3 结果与讨论
3.1 标准曲线绘制
由于不同产地药材中含量差异较大,因此在标准的制备中应充分考虑,本实验采用逐级稀释法,等比数列稀释,最大浓度与最小浓度相差411倍,这样才能更好地适用于中药材的含量测定,保证药材的含量在标曲线性范围之内。如果采用等差数列进行标准制备,则线性范围较窄,不能很好地保证适用于所测药材,如果中成药含量测定中,由于药材的产地来源固定,含量相差不大,可以采用等差比例稀释作标准曲线。
3.2 供试品制备的考察
本实验在供试品溶液制备过程中分别考察了不同溶剂(甲醇,75%甲醇、50%甲醇、甲醇),不同提取方法(冷浸、超声、回流)、不同超声时间(20 min、30 min、40 min),超声功率(150 W、350 W、500 W),发现丹参酮类化合物不稳定,容易相互转换,最终考察采用75%甲醇作为提取溶剂、超声提取方法、提取30 min中功率500 W为最佳供试品制备方法,该条件下4种丹参酮脂溶性成分含量最高,因此选择上述条件作为供试品溶液的制备方法。同时由于丹参酮类成分对热和光不稳定,相互之间易于转换,因此在测定过程中需采用棕色瓶子避光操作,同时超声时注意温度控制。
3.3 限度的确定
本实验通过对10个不同产地的丹参药材中二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA的含量测定,按照2015年版《中国药典》规定,按干燥品计算,含隐丹参酮、丹参酮I和丹参酮IIA三者之和不少于0.25%,上述药材的含量均符合规定,本实验所测其他批次药材中的二氢丹参酮中的含量在0.039 2%~0.071 4%之间,四者之和在0.444 9%~0.774 1%之间,平均值为0.603 2%,因此建议规定中增加二氢丹参酮的含量,以平均值的80%计算作为限度较为合理,因此为了提高优质丹参药材标准,丹参药材按照干燥品计算,含二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA四者之和不少于0.48%。
本研究建立的不同产地丹参药材中脂溶性成分二氢丹参酮、隐丹参酮、丹参酮I和丹参酮IIA的TLC鉴别方法,具有斑点清晰、分离良好、含量测定方法分析速度快、灵敏度高的优点,可以用于丹参药材中4种脂溶性成分的含量测定。
