ICP-MS检测脂肪乳注射液及包材中的18种元素
2021-08-19张乃斌陈真李春焕张迅杰由鹏飞
张乃斌,陈真,李春焕,张迅杰,由鹏飞
(山东省食品药品检验研究院,仿制药研究与评价重点实验室,山东 济南 250101)
脂肪乳注射液是由大豆油(供注射用)、甘油三酸酯、油酸、精制蛋黄卵磷脂(E80)、氢氧化钠、甘油(供注射用)以及注射用水等主要成分制成的白色乳状液体,临床作为胃肠外营养和能量补充药剂使用。脂肪乳注射液作为肠外营养剂可用于补充能量和必需氨基酸,临床注射用量较大,最大日剂量为4 g·kg-1,其元素含量需要严格控制[1]。但由于其成分较为复杂,同时含有大量的油脂,元素检测较为困难,如若采用原子吸收法测定元素,又存在灵敏度差,操作复杂,结果不稳定,无法同时测定多种元素等诸多缺点[2]。如若采用直接进样的方式进行电感耦合等离子体质谱(ICP-MS)测定,高温燃烧后的样品会导致采样锥的锥孔堵塞,对样品的前处理要求较高[3-6]。
脂肪乳注射液的包装材料多为中硼硅玻璃输液瓶和注射液用溴化丁基橡胶塞6720GC,在样品长期存储过程中,容易发生包材与注射液相互侵蚀或者包材表面碎片脱落等问题,通过阳性破坏试验和电镜扫描可清楚地观察到上述现象,所以两者相容性问题就尤为突出[7-9]。
脂肪乳注射液作为肠外营养剂,长期的存储过程中,其包材中元素会向药物产生迁移,这对药物质量安全有着重要影响[10],但由于脂肪乳注射液含有大量油脂,分析困难,导致现有的可参考文献中并未有对脂肪乳注射液以及其包材中元素迁移的研究[11-12]。本研究基于对药液质量和用药安全性的考虑,对脂肪乳注射液及其包材中的元素进行检测。参考《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则》《化学药品与弹性体密封件相容性研究技术指导原则》《2015-药包材标准》及《ICH Q3D元素杂质指导原则》相关要求,结合包材的生产、加工、使用过程等工艺及包装药品的特性,经过严格的方法学验证,确立了脂肪乳注射液包材(中硼硅玻璃输液瓶、溴化丁基橡胶塞)的前处理方法,确立了能够同时检测脂肪乳注射液及其包材中铅、砷、镉、汞、钴、钒、镍、铝、铁、锌、钡、锑、锂、铜、铈、钛、硼、硅共18种元素的含量测定的有效方法,为研究脂肪乳注射液包材相容性实验奠定基础。
1 仪器与试药
1.1 试验仪器 电感耦合等离子体发射质谱仪(珀金埃尔默);超纯水机 (Q-POD ElementMilli-Q);扫描电子显微镜(TM4000Plus,HTACHI)。
1.2 试验试剂 超纯水(自制);硝酸(江苏晶瑞化学股份有限公司);亚甲基蓝(国药集团);无水乙醇(莱阳市康德化工有限公司);氢氧化钠(国药集团)。
1.3 试验对照品 标准元素镉(M2-CD659870)、汞(M2-HG659921)、钴(K2-CO02072)、铅(M2-PB655591)、钒(K2-V02108)、砷(K2-AS654224)、镍(M2-NI660480)、锑(K2-SB650297)、铝(M2-Al658405)、钡(K2-BA02100)、铁(K2-FE04060)、锌(K2-FE04060)、铈(K2-ZN650949)、钛(K2-TI02120)、硼(M2-B660377)、硅(K2-SI03065)、铟(K2-IN01118)、铋(K2-BI02014)、锗(K2-GE01122AA)购于美国Inorganic Ventures公司,规格均为1 000 μg·mL-1。元素锂(156949-34)、铜(140652-124)、金(166660-73)购于美国O2Si公司,规格均为1 000 μg·mL-1。钪(GSB04-1750-2004)购于国家有色金属及电子材料分析测试中心,规格均为1 000 μg·mL-1。
1.4 试验样品 脂肪乳注射液,批号:2007111,规格:100 mL∶30 g(大豆油)∶1.2 g(卵磷脂)生产企业:西安力邦制药有限公司。
2 试验方法
2.1 试验条件
2.1.1 包材迁移元素种类确定 依据ICH Q3D指导原则“元素分类”、“元素杂质的风险评估和控制的要求”及胶塞和中硼硅玻璃配方表中添加的元素等确定最终需要测定的迁移元素种类。
2.1.2 胶塞引入的元素 具体见表1。

表1 胶塞配方
由表1可知,根据胶塞配方表中添加的物质,其可能迁移至药液中的元素有:硫、钛。其中硫元素一般采用高效液相色谱法测定,不再做ICP-MS方法研究。
2.1.3 中硼硅玻璃引入的元素 具体见表2。

表2 中硼硅玻璃配方
其中,钾、钠元素,因有其相关的大剂量注射液(如:氯化钠注射液、氯化钾注射液),且未见毒性报道,不作为本报告中需要研究的元素。
2.1.4 ICH Q3D指导原则规定测定元素 根据“元素杂质的风险评估和控制”项下“风险评估建议”考虑的元素的要求,非有意加入的元素注射用药液必须测定的元素有:镉、汞、铅、砷、钴、钒、镍、锂、锑、铜。
2.5.4 ICH Q3D指导原则规定不测元素 根据“元素分类-分类”项下的规定,对于注射和吸入给药产品,在风险评估过程中应对含有此类元素杂质的可能性进行评估,除非给药途径的特定PDE值高于 500 μg·d-1。此类元素包括:钡、铬、铜、锂、钼、锑和锡。其中元素钼、锡、铬、钡的PDE值均高于500 μg·d-1;又因钡元素为玻璃包材添加元素,必须做,其他3个元素不做测定。
2.2 测定方法的确定
2.2.1 中硼硅玻璃输液瓶阳性破坏试验 在比较剧烈的条件下,对中硼硅玻璃输液瓶进行破坏性侵蚀试验研究。筛选出一种能使中硼硅玻璃输液瓶产生微量脱片的破坏条件,并观察此条件下中硼硅玻璃输液瓶亚甲基蓝染色情况、中硼硅玻璃输液瓶内表面的侵蚀样貌和产生脱片后元素(硅、硼、铝)迁移情况。
2.2.2 供试品制备 取未接触过药物的中硼硅玻璃输液瓶,清洗干净,晾干后灌装0.07 mol·L-1氢氧化钠121 ℃高压蒸汽灭菌0.5 h,同时做空白对照。选择此条件作为中硼硅玻璃输液瓶破坏侵蚀条件,并观察此条件下亚甲基蓝染色情况、中硼硅玻璃输液瓶内表面的侵蚀样貌和产生脱片后元素(硅、铝、硼)浸出情况。
2.2.3 电镜扫描 将染色过后的中硼硅玻璃输液瓶,于瓶身、瓶底、瓶颈各切割制取约5 mm边长的矩形样品,加水超声5 min,无水乙醇超声5 min,重复一遍,取出,晾干,粘于导电胶上,氮气吹扫,离子溅射仪镀金,氮气吹扫,放入电镜观察;同时以未接触侵蚀液的中硼硅玻璃输液瓶同法操作,作为空白对照。
2.2.4 亚甲基蓝染色 取灌装0.07 mol·L-1氢氧化钠121 ℃高压蒸汽灭菌30 min的中硼硅玻璃输液瓶,将0.07 mol·L-1氢氧化钠侵蚀液倒出,把中硼硅玻璃输液瓶清洗干净,灌装0.5%亚甲基蓝溶液,静置20 min后倒出,用低流速水灌入瓶内并倒出,反复10次,观察是否有亚甲基蓝挂壁现象;同时以未接触侵蚀液的中硼硅玻璃输液瓶同法操作,作为空白对照。
2.3 元素测定
2.3.1 仪器参数 仪器参数见表3~4。
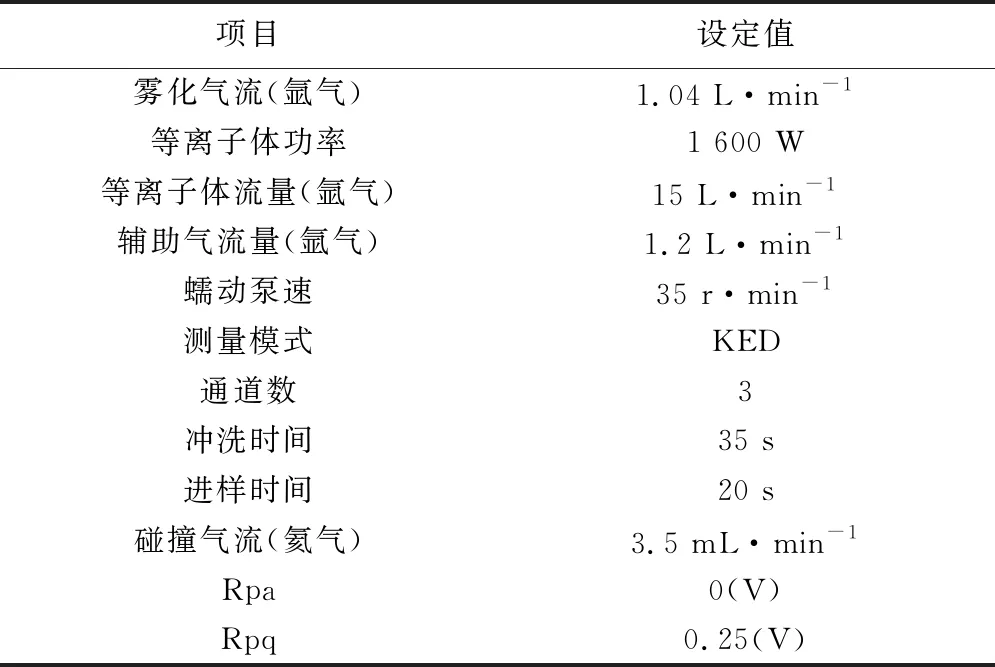
表3 ICP-MS仪器参数信息表
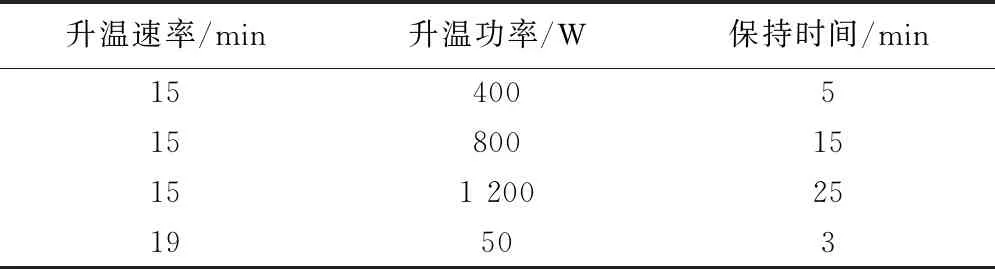
表4 微波消解程序
2.3.2 溶液的制备 (1)溶液的制备
溶剂:取硝酸200 mL,加入水中使成1 000 mL,摇匀,即得。
金溶液(40 μg·mL-1):精密量取金单元素标准溶液2 mL,置50 mL量瓶中,加溶剂稀释至刻度,摇匀,即得。
内标溶液(50 ng·mL-1):依次精密量取锗、铟、铋单元素标准溶液1 mL,加溶剂制备成50 ng·mL-1溶液。
(2)混合贮备溶液:分别依次精密量取单元素标液锂元素0.25 mL、铝元素0.25 mL、铜元素0.3 mL、钡元素0.7 mL、铁元素1.25 mL、锌元素1.25 mL、铈元素0.15 mL、钛元素0.5 mL、硼元素1.75 mL、硅元素2.5 mL,镉元素0.2 mL、汞元素0.3 mL、钴元素0.5 mL、铅元素0.5 mL、钒元素1 mL,砷元素0.3 mL、镍元素0.4 mL,锑元素1 mL,置同一50 mL量瓶中,精密量取混合贮备1溶液0.5 mL、混合贮备2溶液0.5 mL、贮备3溶液1 mL、加溶剂稀释至刻度,摇匀;
(3)线性溶液:依次精密量取混合贮备线性溶液125 μL、250 μL、500 μL、750 μL、1 mL,分别置不同50 mL量瓶中,精密加入金溶液250 μL,加溶剂稀释至刻度,摇匀。
取上述各线性溶液,注入电感耦合等离子体发射质谱仪,记录检测结果。
各元素的具体浓度见表5。
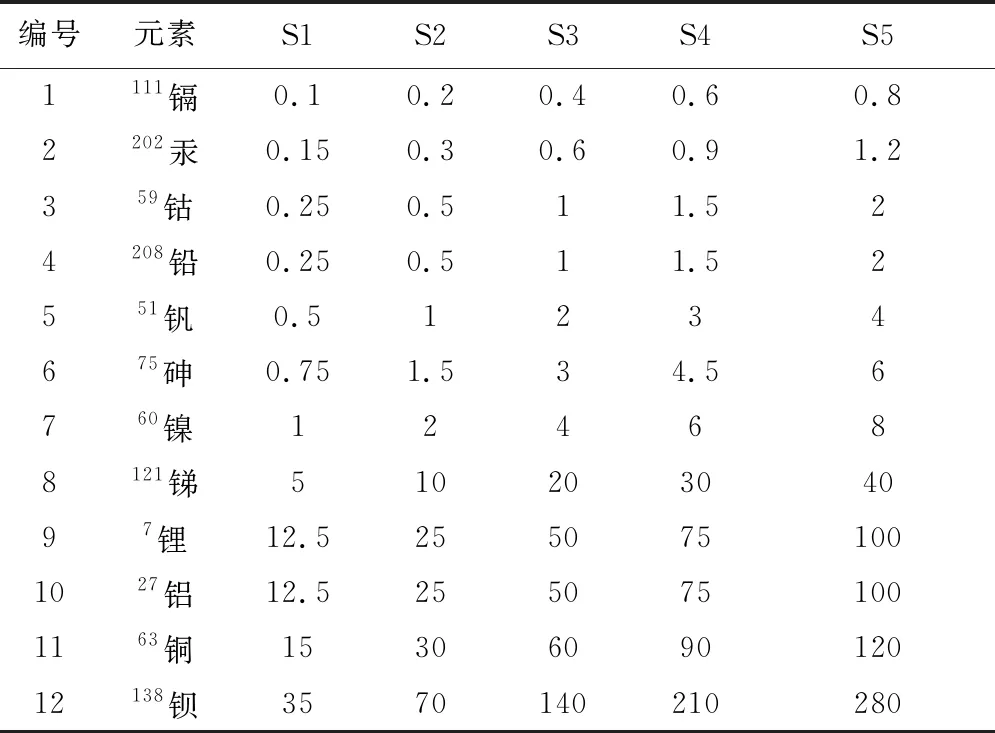
表5 各元素线性浓度表(ng·mL-1)
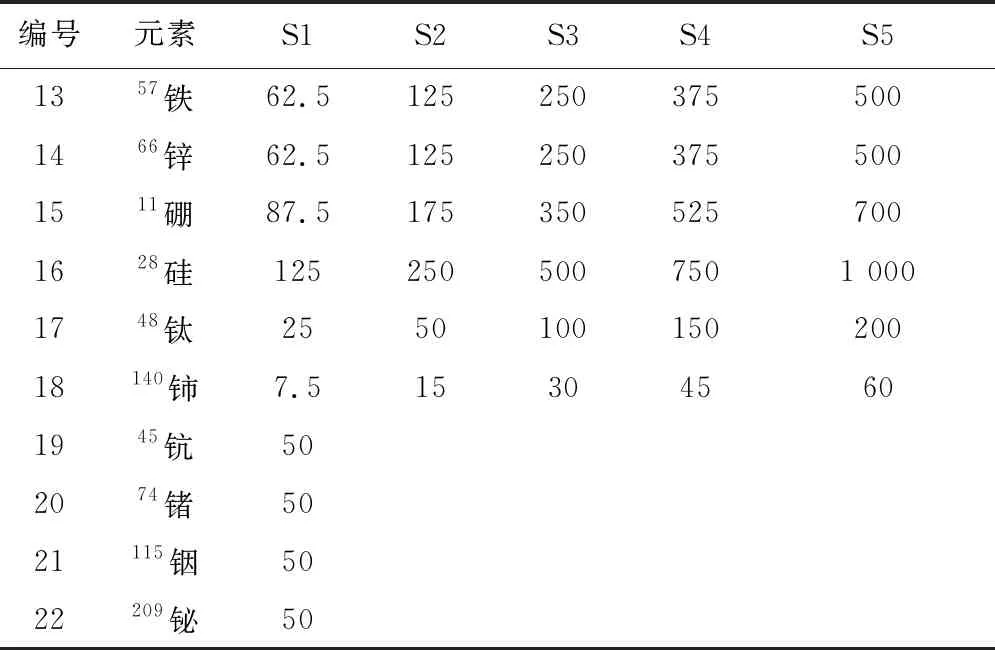
表5(续)
其中,元素锂、铝、钒、硼、硅和钛以元素钪为内标元素;元素铁、钴、镍、铜和砷以元素锗为内标元素;元素镉、铈、锑、钡以元素铟为内标元素;元素汞、铅以元素铋为内标元素;金元素起稳定汞元素的作用,不做测定。
2.3.3 样品检测 玻璃瓶侵蚀溶液制备:取灌装0.07 mol·L-1氢氧化钠121 ℃高压蒸汽灭菌30 min的中硼硅玻璃输液瓶,将0.07 mol·L-1氢氧化钠侵蚀液倒出,精密量取0.25 mL,置50 mL量瓶中,用溶剂稀释至刻度,摇匀,即得。
胶塞提取溶液制备:称取剪碎的胶塞5 g,置微波消解管中,加硝酸12 mL,置微波消解炉中消解,放冷,过滤,取滤液加水容至50 mL。同法处理空白样品。
专属性空白溶液:取微波消解罐,加入硝酸5 mL,金储备溶液(40 μg·mL-1)0.15 mL,用水转移并定容置25 mL量瓶中,摇匀,滤过,取续滤液。
供试品溶液制备:取同一批次放置0 h与置于37 ℃培养箱中放置3个月的脂肪乳注射液样品,分别精密量取5 mL,置微波消解罐中,精密加入金溶液(40 μg·mL-1)250 μL,硝酸5 mL,放置48 h后,置微波消解仪中消解,放冷,用水转移并定容置至25 mL;剩余供试品置于37 ℃培养箱中继续放置,定期取样检测元素迁移情况。
以分析元素的响应值与内标元素响应值的比值为纵坐标,其对应浓度为横坐标,绘制标准曲线,计算回归方程。根据相应的标准曲线回归方程计算得到目标元素的浓度,计算目标元素的含量。参考USP41“元素杂质-程序”进行方法学验证。
3 结果与讨论
3.1 待测元素种类统计结果 依据ICH Q3D指导原则的要求及对中硼硅玻璃瓶和溴化丁基胶塞添加引入元素的统计,综合多方面信息,最终确定需验证性控制的元素有:镉、汞、钴、铅、钒、砷、镍、锑、铝、钡、铁、锌、铈、钛、硼、硅、锂、铜共18种元素,此18中元素对研究脂肪乳注射液及包材相容性具有较高代表性。
3.2 电镜扫描 由图1~4可知,中硼硅玻璃输液瓶灌装0.007 mol·L-1氢氧化钠侵蚀液121 ℃高压蒸汽灭菌30 min后,从所切割的部位观察,瓶身、瓶底、瓶颈均观察到不同程度的侵蚀样貌,说明该条件下,中硼硅玻璃可被破坏,可在该条件下研究侵蚀样貌和产生脱片后元素(硅、硼、铝)迁移情况。

图1 未接触侵蚀液的中硼硅玻璃输液瓶电镜扫描图

图2 侵蚀后的中硼硅玻璃输液瓶瓶身电镜扫描图

图3 侵蚀后的中硼硅玻璃输液瓶瓶底电镜扫描图

图4 侵蚀后的中硼硅玻璃输液瓶瓶颈电镜扫描图
3.3 亚甲基蓝染色 由图5可知,中硼硅玻璃瓶经侵蚀后,出现亚甲基蓝挂壁现象,未经侵蚀的中硼硅玻璃瓶并未出现亚甲基蓝挂壁现象,进一步验证中硼硅玻璃输液瓶灌装0.007 mol·L-1氢氧化钠侵蚀液121 ℃高压蒸汽灭菌30 min的试验破坏条件对表面侵蚀破坏程度。

图5 亚甲基蓝染色结果
3.4 方法学验证 校正强度与浓度呈良好的线性关系,相关系数r均大于0.999;RSD均小于相关要求,该方法的精密度及稳定性良好;空白溶液对待测元素的测试不产生干扰,专属性较好;各元素的测定回收率结果均规定范围内,说明该方法的准确度良好。以该方法测得18种元素的定量限、检测限结果均能够满足限度要求(见表6)。
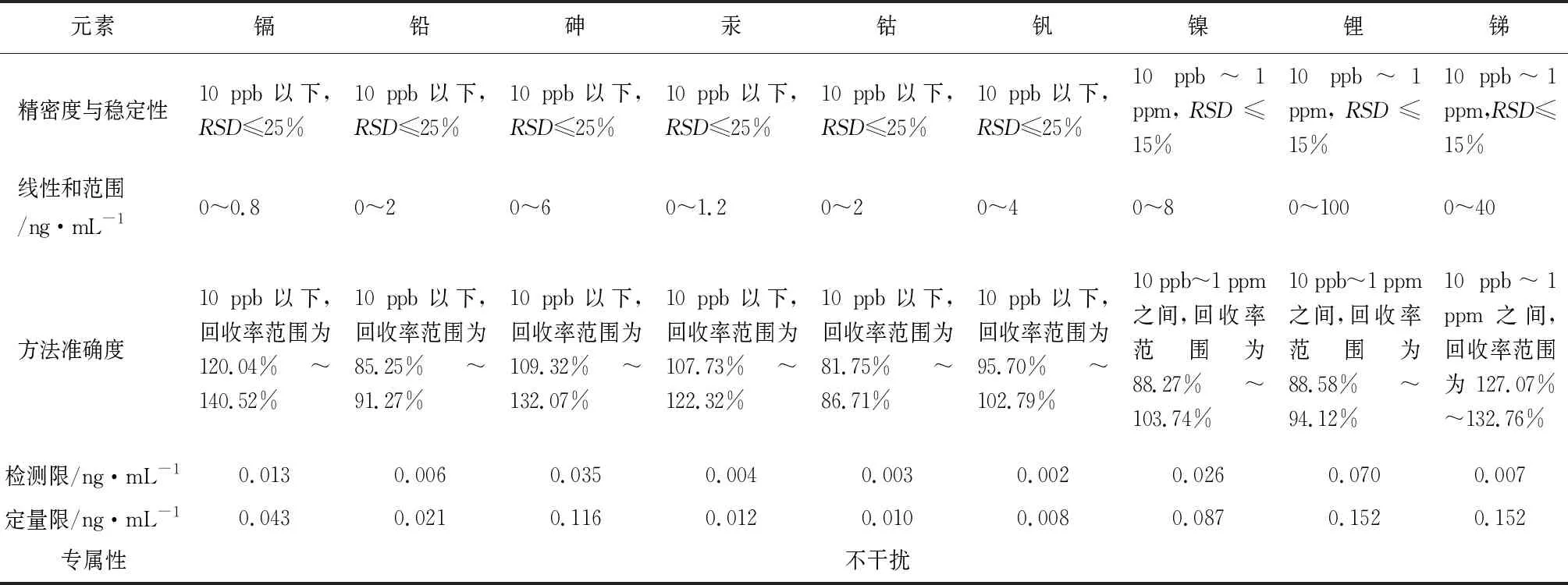
表6 方法学验证结果
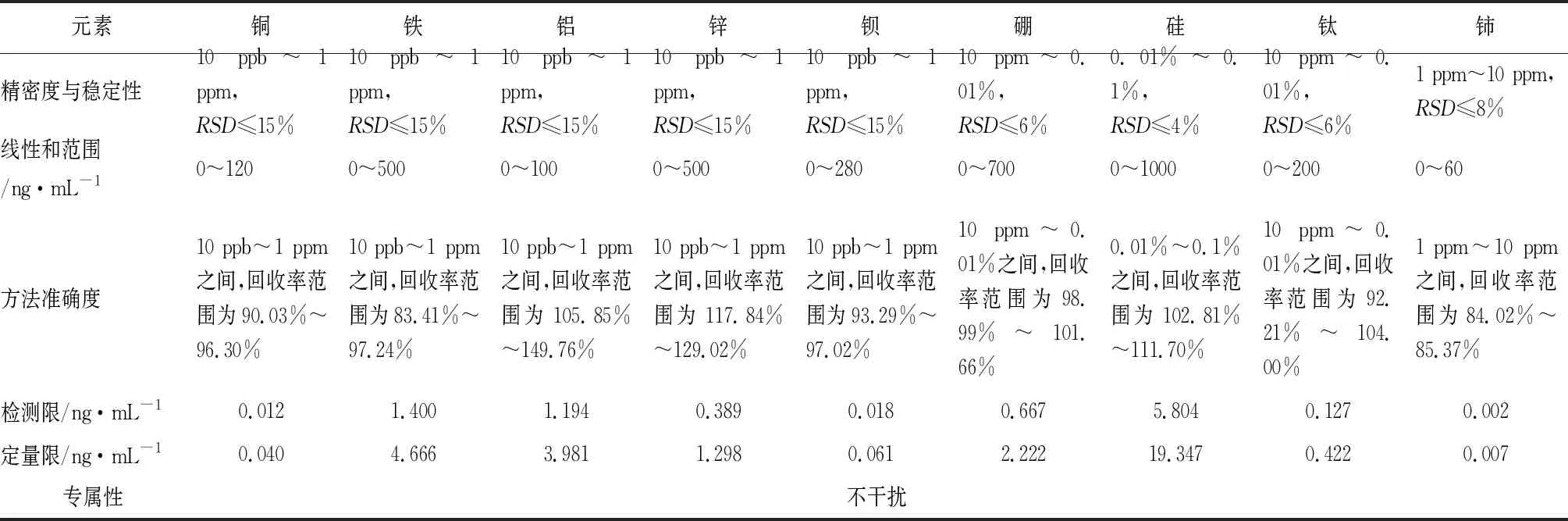
表6(续)
3.5 样品迁移试验结果 各待测元素的含量若小于定量限,均报告为未检出。
对放置0 h和3个月的样品元素检测结果显示,各批次样品中待测元素的含量变化不大,各元素在样品存放过程中均存在一定量的迁移情况,但由于放置时间较短,各元素的迁移量相对较小(见表7)。

表7 放置3个月后样品元素变化结果
4 结论
本文研究确定了包材相容性中迁移元素的种类,明确了脂肪乳注射液及其包材中硼硅玻璃输液瓶和溴化丁基橡胶塞样品的前处理方法,对该条件下处理后的样品进行硅、铝、硼元素迁移量检测,为脂肪乳注射液药物与包材相容性研究奠定基础。采用标准曲线法,优化ICP-MS技术参数,检测脂肪乳注射液及包材中镉、汞、钴、铅、钒、砷、镍、锑、铝、钡、铁、锌、铈、钛、硼、硅、锂、铜共18种元素含量,并进行方法学验证。该方法操作简便、准确,精密度、准确性、稳定性、专属性好。
本项研究仅仅确定了脂肪乳注射液及包材中元素含量的测定方法,未能够对脂肪乳注射液及包材相容性进行进一步的研究,未能就药物储存6个月、12个月、18个月、24个月、36个月时的元素迁移情况做进一步研究,这在未来的工作中需要做进一步探索。
