高效液相色谱法测定射麻口服液中黄芩苷含量
2021-08-16杨巧虹邓开英申丽莎
杨巧虹 ,邓开英 ,申丽莎
(1. 重庆医疗器械质量检验中心,重庆 401147; 2. 重庆市食品药品检验检测研究院·重庆市药物过程与质量控制工程技术研究中心,重庆 401121; 3. 重庆市中药研究院,重庆 400061)
射麻口服液由黄芩、麻黄、胆南星、射干、醋五味子等10 味药材提取制成,具有清肺化痰、止咳平喘功效,临床主要用于外邪犯肺、入里化热所致咳嗽、痰多稠黏、胸闷憋气、气促作喘、喉中痰鸣、发热或不发热、舌苔黄或黄白、或舌质红、脉弦滑或滑数等证,效果良好[1]314。方中黄芩清热燥湿、泻火解毒,用于胸闷呕恶、湿热痞满、肺热咳嗽等[1]1469,但现行质量标准未对其进行含量控制。本研究中参考文献[2 -14],建立了测定射麻口服液中黄芩所含有效成分黄芩苷含量的高效液相色谱(HPLC)法,为其质量控制提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1260 型高效液相色谱仪(美国安捷伦仪器公司);BP211S 型电子天平(北京赛多利斯仪器有限公司,精度为十万分之一);Simplicity-185 型超纯水机(美国密理博公司)。
1.2 试药
黄芩苷对照品(中国食品药品检定研究院,批号为171241 -201508,含量为 93.3% );射麻口服液(海南中盛合美生物制药有限公司,批号分别为20190102,20190301,20190401,规格为每支 10 mL);甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Waters SunFire C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇 -0.2% 磷酸溶液(47 ∶53,V / V);流速:1.0 mL / min;柱温:30 ℃ ;检测波长:280 nm;进样量:10 μL。在此色谱条件下,供试品溶液的黄芩苷色谱峰达到基线分离,峰形对称,分离度良好,且阴性对照无干扰,分离度大于1.5,理论板数按黄芩苷峰计不低于5 000。色谱图见图1。
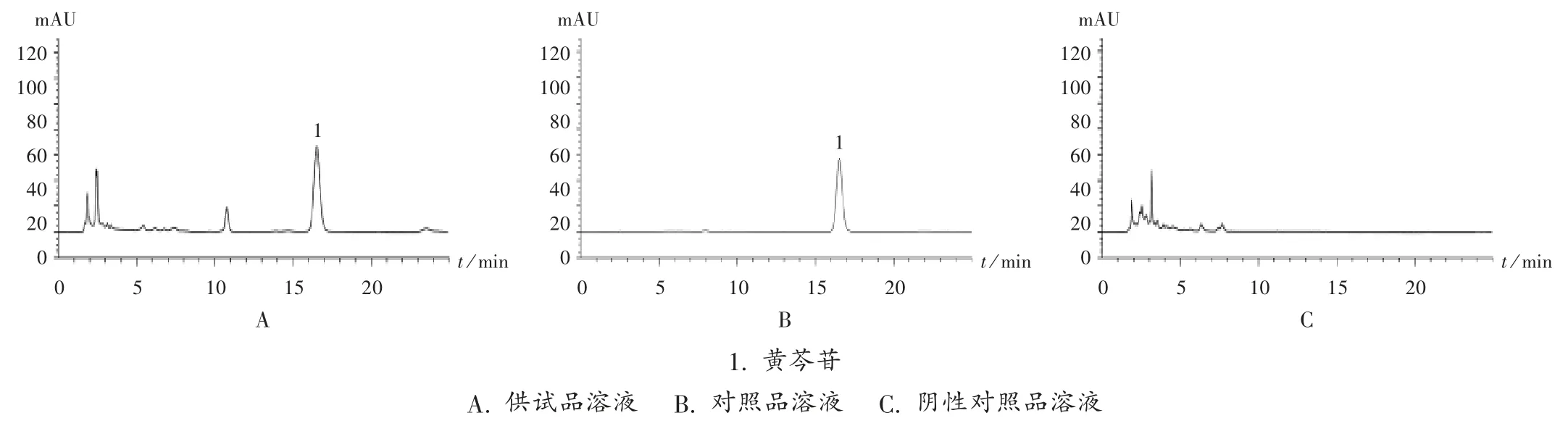
图1 高效液相色谱图1. baicalinA. Reference solution B.Test solution C.Negative reference solutionFig.1 HPLC chromatograms
2.2 溶液制备
对照品溶液:取黄芩苷对照品0.011 23 g,精密称定,置50 mL 容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品贮备液。精密量取对照品贮备液2 mL,置10 mL 容量瓶中,加甲醇稀释至刻度,摇匀,即得。
供试品溶液:取射麻口服液适量,混匀,精密量取1 mL,置25 mL 容量瓶中,加甲醇稀释至刻度,摇匀,滤过,精密量取续滤液1 mL,置10 mL 容量瓶中,加甲醇稀释至刻度,摇匀,即得。
阴性对照品溶液:按处方比例和制备工艺制备不含黄芩的阴性样品,照供试品溶液制备方法制备阴性对照品溶液。
2.3 方法学考察
线性关系考察:分别精密吸取2.2 项下对照品溶液 1,5,10,15,20 μL,按 2.1 项下色谱条件进样测定,记录峰面积。以进样量(X,μg)为横坐标、峰面积积分值(Y)为纵坐标进行线性回归,得回归方程 Y =3 693.4 X - 5.843 3,r = 0.999 9( n = 5)。结果表明,黄芩苷进样量在0.041 91 ~ 0.838 20 μg 范围内与峰面积线性关系良好。
精密度试验:精密吸取2.2 项下对照品溶液10 μL,按2.1 项下色谱条件连续进样测定5 次,记录峰面积。结果黄芩苷峰面积的 RSD 为 0.63% (n = 5),表明仪器精密度良好。
稳定性试验:按2.2 项下方法制备供试品溶液,分别于室温下放置 0,2,4,8,12 h 时各进样 10 μL,测定并记录峰面积。结果黄芩苷峰面积的 RSD 为0.58%(n =5),表明供试品溶液室温下放置12 h 内稳定性良好。
重复性试验:取同一批(批号为20190102)样品适量,精密称定,混匀,分别按2.2 项下方法制备供试品溶液,平行5 份,按2.1 项下色谱条件进样测定。结果黄芩苷含量的 RSD 为 0.84%(n = 5),表明方法重复性良好。
加样回收试验:分别精密量取已知含量的样品(批号为 20190102)各 0.5 mL,共 6 份,分别置 25 mL 容量瓶中,分别加入一定量的黄芩苷对照品溶液,按2.2 项下方法制备供试品溶液,按2.1 项下色谱条件进样测定,并计算加样回收率。结果见表1。

表1 黄芩苷加样回收试验结果(n =6)Tab.1 Results of the recovery test of baicalin(n = 6)
2.4 样品含量测定
取样品 3 批(批号分别为 20190102,20190301,20190401),按 2.2 项下方法制备供试品溶液,按 2.1 项下色谱条件进样测定。结果样品中黄芩苷的含量分别为12.46 g /L,11.08 g /L,12.41 g /L。
3 讨论
参考文献[2-14],考察了不同流动相甲醇-水-磷酸溶液(47 ∶53 ∶0.2,V / V / V)、甲醇 - 0.2% 磷酸溶液、乙腈-0.1%磷酸溶液、乙腈-0.2%磷酸溶液、甲醇-0.1%甲酸溶液、乙腈-0.1%甲酸溶液对黄芩苷含量测定结果的影响。甲醇比乙腈的毒性小,价格便宜,为检测实验室常用试剂,故参照2020 年版《中国药典(一部)》黄芩药材含量测定项下色谱条件,即色谱柱为C18柱,流动相为甲醇 - 水 - 磷酸溶液(47 ∶53 ∶0.2,V / V / V),检测波长为280 nm。本研究中将流动相简化为甲醇-0.2%磷酸溶液(47 ∶53,V / V),检测波长为 280 nm。经试验考察,于280 nm 波长下检测,以甲醇-0.2%磷酸(47 ∶53,V / V)为流动相,射麻口服液中黄芩苷分离效果良好,且阴性对照无干扰。经二极管阵列检测器检测,供试品溶液中黄芩苷色谱峰与黄芩苷对照品溶液色谱峰紫外光谱图一致。
考察供试品溶液制备方法时,取样品,分别加入70%乙醇、甲醇稀释,结果加入70%乙醇时样品中未见沉淀产生,加入甲醇则产生了大量沉淀,沉淀后的溶液颜色明显变浅,故制备供试品溶液时采用甲醇,以沉淀的方式除去杂质。
本研究中采用了2 个不同品牌的色谱柱和2 个不同厂家的液相色谱仪对供试品溶液进行了检测,结果黄芩苷色谱峰均达到基线分离,色谱效果和含量测定结果一致,表明方法耐用性良好。
