溪黄草药材质量标准研究∗
2021-08-16马鹏文师庆媛朱昱澜任一杰
马鹏文,师庆媛,朱昱澜,任一杰,2△
1 甘肃省中药固体分散制剂重点实验室/甘肃陇神戎发药业股份有限公司,甘肃 兰州730102;2 甘肃省中药质量与标准研究重点实验室
溪黄草在南方各地应用普遍,具有清热利湿、退黄、凉血散瘀的功效,可用于治疗湿热黄疽、湿热泻痢、瘾闭、跌打疲肿等疾病[1]。随着中药发展及中成药生产规模的不断扩大,溪黄草的应用也越来越广泛。消炎利胆片、胆石通胶囊中均以溪黄草作为主要原料,但《中华人民共和国药典》2015年版一部药材项下未收载溪黄草药材品种[2],现行质量检验标准均为地方标准[3-4]。各地方标准中溪黄草的质量控制标准均未制定定性指标和含量测定指标。为此,本研究采用薄层色谱法检测溪黄草中迷迭香酸成分,采用HPLC法测定齐墩果酸、熊果酸含量,以期为溪黄草药材质量控制提供参考。
1 材料
1.1 仪器AX204 万分之一电子天平(上海梅特勒公司);MS205DU 十万分之一电子天平(上海梅特勒公司);HH-6 数显恒温水浴锅(常州国华电器有限公司);SB25-12DTD 数控超声波清洗器(宁波新芝生物科技股份有限公司);TU1901 紫外分光光度计(北京普析通用仪器有限公司);Waters 152高效液相色谱仪(美国Waters公司)。
1.2 试剂迷迭香酸对照品(批号:111871-201706)、齐墩果酸对照品(批号:110709-201607)、熊果酸对照品(批号:110742-201622)均购于中国食品药品检定研究院。银龙牌硅胶G 薄层板(烟台市化学工业研究所);甲醇、乙腈、乙酸铵为色谱纯,水为哇哈哈纯净水,其他试剂均为分析纯。本实验中10 批溪黄草药材为单位药材供应商提供,产地分别为安徽、广东、广西、河南,依次编号1~10。
2 方法与结果
2.1 迷迭香酸薄层鉴别取溪黄草药材粉末2.0 g,加甲醇50 mL,超声处理30 min(功率500 W,频率40 kHz),滤过,滤液蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取迷迭香酸对照品,加甲醇制成每1 mL含1 mg的溶液,作为对照品溶液。按照薄层色谱法试验,吸取对照品溶液与供试品溶液各2µL,甲醇作为空白溶液,分别点于同一硅胶G 薄层板上,以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2∶3∶4∶0.5∶2)为展开剂,展开,取出,晾干,置紫外光(365 nm)下检视,供试品色谱中在与对照品色谱相应的位置上显相同颜色的荧光斑点,空白无干扰。因该方法操作简便、快速,斑点显色清晰,确认该方法可用于溪黄草药材中迷迭香酸的定性鉴别。薄层色谱图见图1。

图1 溪黄草药材中迷迭香酸薄层鉴别
2.2 齐墩果酸、熊果酸含量测定
2.2.1 色谱条件 色谱柱:CAPCELL PAK C18MGⅡ,以十八烷基硅烷键和硅胶为填充剂;流动相:乙腈-甲醇-0.5%乙酸铵(67∶12∶21),等度洗脱;流速:1 mL/min;检测波长:210 nm;柱温:30℃;进样量:20µL。
2.2.2 对照品溶液 取齐墩果酸及熊果酸对照品适量,精密称定,加甲醇制成每1 mL含齐墩果酸80µg,熊果酸0.2 mg的混合溶液,摇匀,即得。
2.2.3 供试品溶液 取溪黄草药材粉末2.0 g,精密称定,置具塞三角瓶中,精密加入甲醇50 mL,称定重量,超声处理(功率500 W,频率40 kHz)30 min,放冷,用甲醇补足减失的重量,微孔滤膜(0.45µm)滤过,取续滤液,即得。
2.2.4 空白对照溶液 取提取溶剂甲醇作为阴性样品,按供试品溶液制备方法制备,即得。
2.2.5 系统适用性试验 取“2.2”项下对照品溶液、供试品溶液、空白对照溶液各20µL,按“2.1”项下色谱条件进样测定,记录色谱。在该色谱条件下,各成分均能达到基线分离,齐墩果酸与熊果酸的分离度为1.59,理论板数以熊果酸计为7355,齐墩果酸与熊果酸保留时间分别为21.670 min和22.720 min。结果表明该方法专属性好,其他成分对测定无干扰。见图2—4。
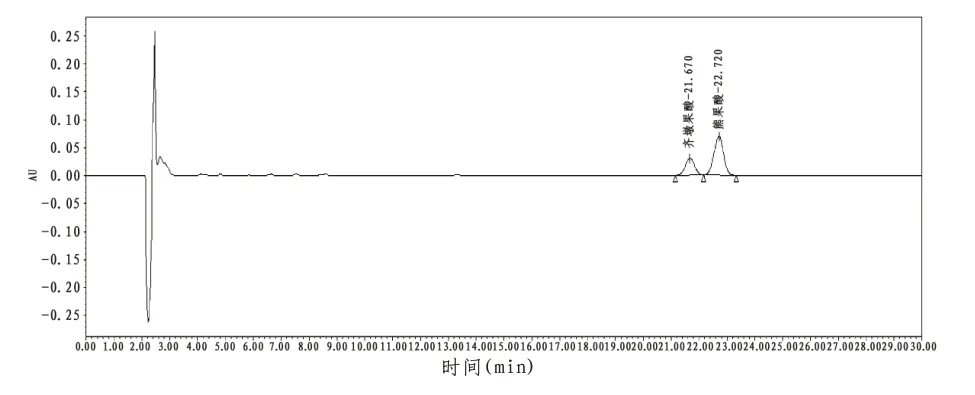
图2 齐墩果酸、熊果酸混合对照品
2.2.6 线性关系考察 精密移取“2.2.1”项下齐墩果酸、熊果酸混合对照品溶液0.5、1.0、2.0、3.0、4.0、5.0 mL 于10 mL 容量瓶中,定容,分别进样20µL,以峰面积值(Y)对进样量(X)进行线性回归,得标准曲线方程:齐墩果酸回归方程为:Y=1.09×104X-11 300,r=0.9998,线性范围:5.066-50.664 2µg/mL;熊果酸回归方程为:Y=6.9×103X-8660,r=0.9998,线性范围:9.735-97.352µg/mL。结果表明线性关系良好。
2.2.7 精密度试验 精密吸取“2.2.1”项下对照品溶液20 µL,按“2.1”项下色谱条件连续进样6次,记录峰面积。结果齐墩果酸峰面积RSD=0.7%,熊果酸峰面积RSD=0.6%。仪器精密度良好。
图3 空白溶剂色谱图

图4 溪黄草样品HPLC色谱图
2.2.8 稳定性试验 取“2.2.2”项下供试品溶液20µL,分别于室温下放置0、3、6、9、12、24 h 时测定,记录峰面积。结果齐墩果酸峰面积的RSD=0.9%,熊果酸峰面积的RSD=0.5%,表明供试品溶液在室温下24 h内稳定性良好。
2.2.9 重复性试验 取1号样品适量,按“2.2.2”项下供试品溶液制备方法平行制备6 份供试品溶液,计算齐墩果酸含量为0.749 mg/g,RSD=1.2%,熊果酸含量为1.503 mg/g,RSD=0.9%,表明本方法重复性良好。
2.2.10 加样回收率试验 取已知齐墩果酸含量(齐墩果酸含量为777.197µg/g)的溪黄草样品9份,每份约0.5g,精密称定,分别精密加入对照品溶液(齐墩果酸对照品382.389 µL/mL)0.8、1.0、1.2 mL 至50 mL 容量瓶中,加甲醇定容至刻度,按“2.2.2”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积并计算齐墩果酸的加样回收率。取已知熊果酸含量(熊果酸含量为1.754 mg/g)的溪黄草样品9 份,每份约0.5 g,精密称定,分别精密加入对照品溶液(熊果酸对照品0.786 mg/mL)0.8、1.0、1.2 至50 mL 容量瓶中,加甲醇定容至刻度,按“2.2.2”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积并计算熊果酸的加样回收率。见表1—2。
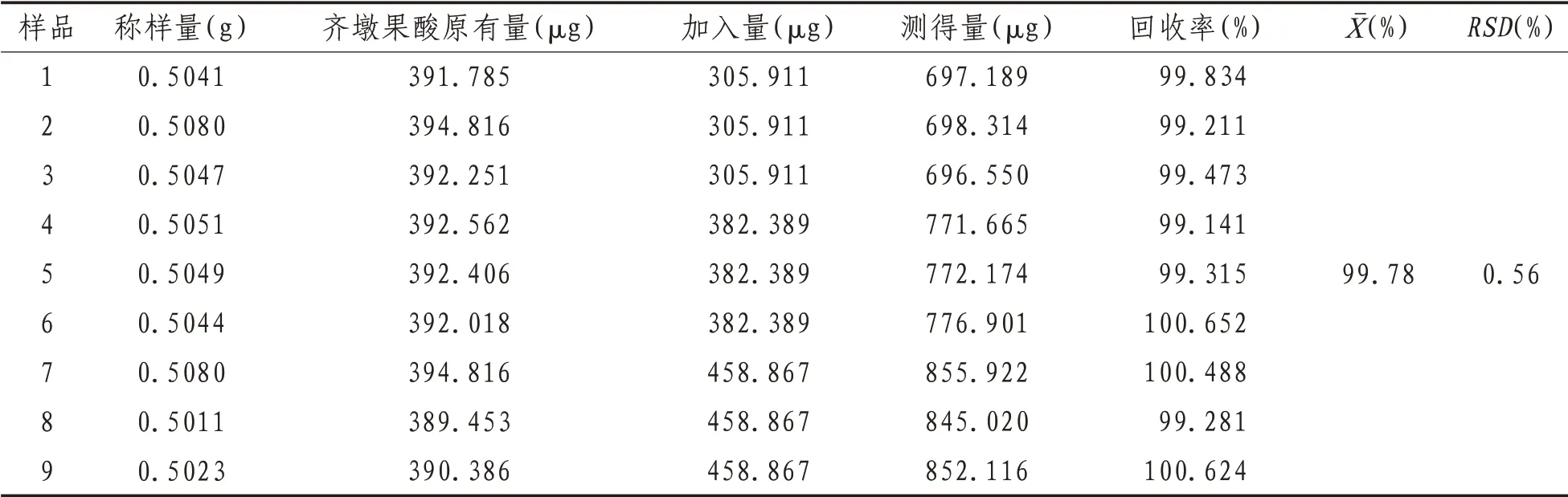
表1 齐墩果酸的加样回收率(n=9)

表2 熊果酸的加样回收率(n=9)
2.2.11 样品含量测定 选取10 个批次的溪黄草样品,按“2.2.2”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积并计算齐墩果酸和熊果酸的含量(按干燥品计),结果见表3。

表3 齐墩果酸与熊果酸含量测定结果 mg/g
3 讨论
溪黄草中含有齐墩果酸和熊果酸,其中熊果酸具有体外抗乙肝病毒的作用[5-6]。近年来对溪黄草药材中化学成分和质量标准的研究文献[7-9]众多,相关文献[10-11]中分别检测溪黄草中迷迭香酸、齐墩果酸及熊果酸含量,但不同品种间迷迭香酸含量差异较大,无法统一标准[12-13];溪黄草药材不同品种间齐墩果酸和熊果酸含量差异小于迷迭香酸,故选择迷迭香酸为定性鉴别的检查指标,齐墩果酸和熊果酸为含量控制指标。
TLC 实验中分别选择环乙烷-乙酸乙酯-异丙醇-甲酸(15∶3∶3.5∶1)、正己烷-乙酸乙酯-甲酸(3∶3∶0.2)、甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2∶3∶4∶0.5∶2)为展开剂,对迷迭香酸的展开条件进行优化,结果以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2∶3∶4∶0.5∶2)为展开剂时展开效果最好;另选用乙醇、70%乙醇、甲醇作为提取溶剂,结果以甲醇作为提取溶剂时展开效果最好。
根据资料[14-15]探索齐墩果酸、熊果酸含量的检测条件。对样品的提取条件进行优化,包括提取方法、提取时间、溶剂选择等,分别对比了甲醇超声提取、回流提取、索氏提取45 min 的提取效果,结果超声45 min提取的齐墩果酸、熊果酸含量最高;同时对比超声15、30、45 min时的提取效果,结果超声30 min 和超声45 min 时齐墩果酸、熊果酸含量差异不大,故选择超声30 min;溶剂选择考察了70%甲醇、甲醇、70%乙醇、乙醇的提取效果,结果用甲醇提取时效率最高。
