冠心七味片提取工艺优化研究
2021-08-16张彭鹏
张 寅,康 跃,薛 妍,张彭鹏
(包头中药有限责任公司,内蒙古 包头 014040)
冠心七味片是一种安全可靠[1]、疗效确切[2]的冠心病、心绞痛用药,蒙药名称为乌兰温度顺-7,处方由丹参、檀香、降香、山柰、肉豆蔻、广枣、沙棘七味药材组成,功能主治:理气,宽胸,止痛。用于寒凝气滞、心脉不通所致的胸痹,症见胸闷、心前区疼痛;冠心病心绞痛见上述证候者[3]。该品种质量标准含量测定项指标性成分为丹参酮ⅡA[3],丹参酮ⅡA具菲醌结构,对湿和热均不稳定[4-6]。该品种生产过程中涉及提取工艺,提取过程涉及的湿热因素会导致丹参酮ⅡA降解,竟而影响产品质量,需要进行具体的分析和研究,以确定提取过程中的湿热因素对丹参酮ⅡA含量的影响程度,从而优化提取生产工艺、保障产品质量。本研究对冠心七味片提取工艺中的湿热因素进行了分析识别,通过单因素试验法优化提取生产工艺,为生产工艺关键控制点的制定提供了依据。
1 仪器与试剂
高效液相色谱仪,LC-2030 (日本岛津),FA2204B电子天平(上海精密科学仪器有限公司)。丹参酮ⅡA对照品(中国药品生物制品检定所提供,批号:110766-202022,含量:98.9%),冠心七味片(由包头中药有限责任公司提供),乙腈、甲醇(色谱纯),水为重蒸馏水。
2 方法与结果
2.1 色谱条件
色谱柱:以十八烷基硅烷键合硅胶为填充剂,流动相:乙腈-水(70:30),检测波长:270nm。理论塔板数按丹参酮ⅡA峰计算应不低于2000。
2.2 线性关系考察
精密称取丹参酮ⅡA对照品8.40mg,置100mL棕色量瓶中,用甲醇溶解并稀释至刻度,摇匀,制得丹参酮ⅡA的对照品溶液。精密量取上述对照品溶液2mL、4mL、6mL、8mL、10mL,分别置10mL棕色量瓶中,用甲醇稀释至刻度,摇匀,分别取10μL注入液相色谱仪,以丹参酮ⅡA的浓度为横坐标,峰面积为纵坐标进行线性回归分析,测定结果见表1,丹参酮ⅡA标准曲线见图1。回归方程:Y=58435X-16876,相关系数r=0.9999,说明丹参酮ⅡA的浓度与峰面积在16.6~83.1μg/mL范围内呈良好的线性关系。

表1 线性关系表
2.3 重复性与中间精密度试验
2.3.1 供试品溶液的制备
取冠心七味片20片,精密称定,研细,取约1g,精密称定,置50mL量瓶中,加甲醇40mL,超声处理20分钟,放冷,加甲醇稀释至刻度,摇匀,滤过,取续滤液即得。
2.3.2 对照品溶液的制备
取丹参酮ⅡA对照品适量,精密称定,加甲醇制成每1mL含40μg的溶液,即得。

图1 丹参酮ⅡA标准曲线
2.3.3 测定法
分别精密吸取对照品溶液与供试品溶液各10μL注入液相色谱仪,测定。
2.3.4 重复性及中间精密度试验
按照2.3.1至2.3.3实验内容,重复进行6份样品的检验,更换仪器及检验人员,再进行6份样品的检验。结果(见表2)表明,丹参酮ⅡA重复性、精密度良好。

表2 重复性与中间精密度试验结果
2.4 稳定性试验
取冠心七味片30片,研细,称取三份,按“2.3.1”项下的配制方法处理,制得三份供试品溶液。分别取上述三份供试品溶液各10μL,在0、4、8小时测定峰面积,结果(见表3)表明,供试品溶液在8小时内测定结果稳定性良好。

表3 稳定性试验结果
2.5 加样回收率测定
精密称取丹参酮ⅡA对照品12.43mg,用甲醇定容至250mL的容量瓶中,作为加样回收对照品溶液。取已知含量的冠心七味片粉末,每份精密称取0.5g,取6份,分别置50mL量瓶中,精密加入上述加样回收对照品溶液25mL,加甲醇15mL,超声处理20分钟,放冷,加甲醇稀释至刻度,摇匀,滤过,取续滤液,作为加样回收供试品溶液。分别精密吸取加样回收对照品溶液与加样回收供试品溶液10μL注入液相色谱仪测定。计算加样回收率,结果见表4。
2.6 提取工艺单因素试验
2.6.1 冠心七味片提取生产工艺
冠心七味片质量标准制法项下内容为[3]粉碎(取檀香、降香、山柰、肉豆蔻四味,混合粉碎成细粉)以及提取(丹参、广枣和沙棘用乙醇提取2小时,滤过;药渣加70%乙醇提取2小时,滤过;合并滤液,回收乙醇得稠膏状物;药渣加水煎煮2小时,滤过,滤液浓缩成稠膏;两膏合并,将檀香、降香、山柰和肉豆蔻四味药材细粉与稠膏拌匀,低温干燥,粉碎成细粉)。

表4 加样回收试验结果
2.6.2 湿热因素分析及研究内容的确定
分析提取工艺中与湿热有关的因素并确定研究内容,见表5。

表5 提取工艺中与湿热有关的因素分析及研究内容的确定
2.6.3 考察因素水平的确定
根据以上分析结果,确定将要考察的因素水平如表6所示。

表6 单因素试验考察因素和水平
下面根对确定的考察因素和水平进行单因素试验法进行试验。
2.6.4 一遍煎液与二遍煎液合并浓缩、分开浓缩对丹参酮ⅡA含量的影响
试验方法:分别进行两组冠心七味片工艺试验,A组按“粉碎”和“提取”步骤进行试验(即一遍煎液与二遍煎液合并浓缩),B组按“粉碎”和“提取”步骤进行试验,并在进行“提取”步骤试验时,将一遍煎液和二遍煎液分开浓缩,再混合,继续后续工艺步骤。根据丹参酮ⅡA对湿热不稳定的特性,另外两个因素固定为醇提膏与水提膏出膏后24h内开始混合烘干、混合膏低温干燥(烘干温度控制在55~60℃之间)。每组分别进行两个重复试验,并使用2.1项下色谱条件、2.3.1项下供试品溶液制备方法(将膏粉作为冠心七味片研细后的粉末进行处理)、2.3.2项下对照品溶液制备方法以及2.3.3项下测定法对所得膏粉进行丹参酮ⅡA含量测定,计算转移率。
试验结果:试验结果(见表7)表明,A组试验结果的丹参酮ⅡA含量和转移率均显著高于B组,说明一遍煎液与二遍煎液合并浓缩较分开浓缩更有利于减少丹参酮ⅡA的降解,后续试验选用一遍煎液与二遍煎液合并浓缩的方法进行。
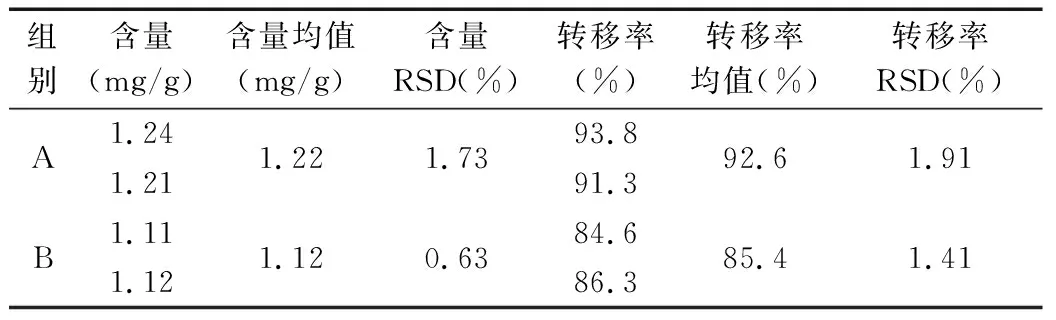
表7 A组与B组试验结果对比
2.6.5 醇提膏与水提膏合并放置时间对丹参酮ⅡA含量的影响
试验方法:按照“粉碎”和“提取”步骤进行C组试验(即一遍煎液与二遍煎液合并浓缩),将“提取”中两膏合并得到的稠膏在常温、避光、密闭条件下放置至第5天(稠膏放置时间113h)进行混合、烘干,根据丹参酮ⅡA对湿热不稳定的特性,另一因素固定为低温干燥(烘干温度控制在55~60℃之间),继续后续工艺步骤。每组分别进行两个重复试验。对所得膏粉进行丹参酮ⅡA含量测定,计算转移率。
试验结果:试验结果与A组(A组为两膏出膏后当天进行混合烘干,两膏合并后的稠膏放置时间为4h,另外两个因素均与D组试验相同)进行对比,见表8,可以看出,A组试验结果的丹参酮ⅡA含量和转移率均显著高于C组,说明醇提膏与水提膏混合所得稠膏在常温、避光、密闭条件下的放置过程中,丹参酮ⅡA发生明显降解,其丹参酮ⅡA含量已降低至质量标准以下(根据成品标准推算膏粉含量标准为不低于1.0mg/g),后续试验选用两膏出膏后当天进行混合烘干。

表8 A组与C组试验结果对比
2.6.6 药材细粉与稠膏拌匀后的烘干温度
试验方法:按照“粉碎”和“提取”步骤进行D组试验(即一遍煎液与二遍煎液合并浓缩),将“提取”中药材细粉与稠膏拌匀后的混合膏烘干温度控制在80~85℃之间,另一因素固定为两膏出膏后当天进行混合烘干,继续后续工艺步骤。每组分别进行两个重复试验。所得膏粉进行丹参酮ⅡA含量测定,计算转移率。
试验结果:试验结果与A组(A组烘干温度为55~60℃,另外两个因素与D组相同)进行对比(见表10),A组试验结果的丹参酮ⅡA含量和转移率均显著高于D组,说明烘干温度由55~60℃改变为80~85℃导致丹参酮ⅡA的含量和转移率显著下降,见表9。

表9 A组与D组试验结果对比
2.7 单因素试验工艺优化结果
根据以上试验结果,确定优化的工艺为:一遍煎液与二遍煎液合并浓缩;烘干温度控制在55~60℃之间;结合生产实际,确定醇提膏与水提膏的放置时间不超过24h,且为避免受到水分影响,进一步要求两膏出膏后分开放置,至烘干前再进行合并。
2.8 验证试验
根据以上试验结果,按照“粉碎”和“提取”步骤进行三组平行试验(及一遍煎液与二遍煎液合并浓缩),设置两膏出膏后当天开始混合烘干,烘干温度控制在55~60℃之间,试验规模放大至中试规模,对所得膏粉进行丹参酮ⅡA含量测定,结果见表11,其中丹参酮ⅡA含量能够满足质量标准要求(膏粉含量标准为不低于1.0mg/g),且转移率较高,转移率RSD为1.64%,表明丹参酮ⅡA含量稳定,方法可行,见表10。
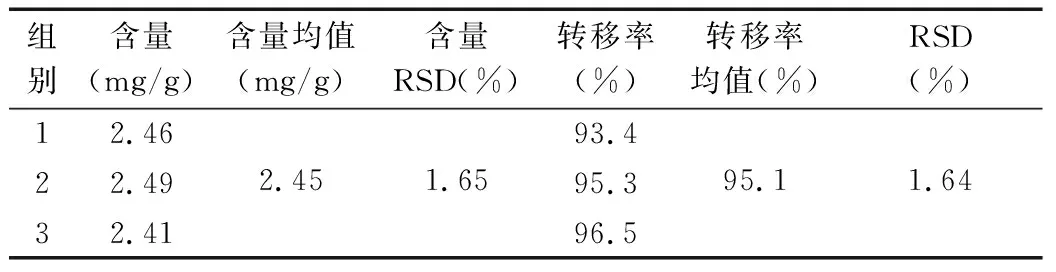
表10 验证试验结果
进一步的,将烘干后的膏粉在常温、避光、密闭条件下放置至第五天进行第二次丹参酮ⅡA含量测定,与初次检测结果对比(见表11),只有第三组试验的丹参酮ⅡA含量是下降的,且下降幅度较小,为3.32%,说明混合膏烘干后,丹参酮ⅡA含量较为稳定,短时间内未发生明显降解反应;作为对比,C组试验稠膏状态放置五天再烘干后的含量与A组试验的未放置情况相比,含量下降明显,含量均值下降了27.9%,进一步证明了丹参酮ⅡA对“湿”的不稳定性,也说明在没有加热和光照的条件下,“湿”的因素可单独影响丹参酮ⅡA的含量。

表11 膏粉在常温、避光、密闭储存条件下的含量变化情况
3 讨论
冠心七味片提取过程中存在较多湿热因素,是造成指标性成分丹参酮ⅡA降解的主要因素,其降解机理可能与丹参酮ⅡA在水中转化成酮类,发挥递氢作用,促进氧化还原反应有关[6]。本研究对提取工艺中的湿热因素进行了分析和识别,通过单因素试验法确定了优化的提取工艺,为回答有关的湿热因素能否优化、如何优化的问题以及生产工艺关键控制点的制定提供了依据。
试验过程中发现,一遍煎液与二遍煎液先混合后浓缩的情况,较先浓缩后混合的情况丹参酮ⅡA含量高,推测先混合后浓缩时,提高了二遍煎液的含醇量,使二遍煎液中的丹参酮ⅡA受湿热的影响导致降解的情况更少发生,同时虽然一遍煎液的含醇量有所降低,但对一遍煎液中丹参酮ⅡA的含量影响较小;也有可能由于浓缩过程中药液中的含醇量不断下降,导致浓缩成稠膏时,部分丹参酮ⅡA成分析出,粘附容器壁,造成含量损失,而两遍煎液先浓缩后混合的情况可能会加剧这种情况的发生,从而导致含量和转移率更低。
以往对丹参酮ⅡA降解规律的研究,或单独研究受热因素对丹参酮ⅡA的降解影响[4],或将湿热因素对丹参酮ⅡA的降解影响放在一起进行研究[5-6],本研究试验过程中发现,在没有加热和光照的条件下,“湿”的因素也会对丹参酮ⅡA产生显著的降解影响,其意义在于提示水分对丹参酮ⅡA含量的影响,如:含丹参酮ⅡA成分的中间品在贮存环节需要注意水分对丹参酮ⅡA含量的影响;丹参药材贮存过程中常发生丹参酮ⅡA的含量随贮存时间的延长含量下降[7],结合本研究结果,提示要注意贮存环节丹参药材本身的水分和环境湿度对丹参酮ⅡA含量的影响;《中国药典》规定丹参饮片的炮制方法为除去杂质和残茎,洗净、润透、切厚片,干燥[8],实际生产过程中应评估和控制其中水分对丹参酮ⅡA的降解影响。
