前路手术治疗颈椎后纵韧带骨化症45例
2021-08-05唐步顺颜程何丽蔚张小克
唐步顺 颜程 何丽蔚 张小克
后纵韧带骨化症(OPLL)易发于颈椎,东亚人群多见,欧美人发病率明显低于亚洲人[1]。诊断明确、符合手术指征的颈椎OPLL患者应选择手术治疗。手术方式一般有前路手术、后路手术和前后路联合减压手术3种。颈椎OPLL手术的具体方式仍存在争议[2]。本院从2015年1月至2019年6月采用前路手术治疗45例颈椎OPLL,取得了较好的疗效,现报告如下。
1 临床资料
1.1 一般资料
2015年1月至2019年6月对符合上述标准的45例颈椎OPLL采用前路手术治疗。其中男34例,女11例;平均年龄(59.40±4.52)岁;平均病程1.8 a(3个月~4.5 a);合并内科基础疾病10例;明确头颈部外伤史5例;局灶型14例,节段型23例,混合型8例;窄基型42例,宽基型3例。手术方式:椎间隙减压融合术(ACDF)5例,椎体次全切除减压融合术(ACCF)28例,ACDF+ACCF 12例。骨化的后纵韧带切除41例,漂浮4例。
1.2 纳入标准
1)病变范围为C3~C7;2)局灶型、节段型及部分混合型(局灶型与节段型混合);3)节段型范围≤2节;4)病灶厚度<5 mm;5)椎管狭窄率≤50%;6)窄基型及部分宽基型(骨化灶双侧边界不超过钩椎关节的内侧缘)。
1.3 排除标准
1)<30岁或>80岁者;2)连续型OPLL;3)感染性疾病活动期;4)发育性椎管狭窄;5)强直性脊柱炎已累及颈椎;6)颈椎类风湿性关节炎;7)心、肺等重要脏器功能失代偿期。
2 方法
2.1 手术方式选择
对于局灶型OPLL邻近椎间隙者选择ACDF,对于远离椎间隙的局灶型或节段型OPLL通常选择ACCF,对混合型OPLL通常选择ACDF+ACCF。
2.2 手术方法
全身麻醉、仰卧位且颈椎轻度后伸,颈前横切口,透视定位后咬骨钳咬除椎体前缘骨赘,依次用尖刀、刮匙和髓核钳清除椎间盘,交替应用刮匙和超薄枪钳去除椎体后缘骨赘,显露后纵韧带。如为邻近椎间隙的局灶型OPLL拟行ACDF,可适当潜行切除部分椎体后缘,利用神经钩、高速磨钻及枪钳去除骨化的后纵韧带。如拟行ACCF,则用咬骨钳或超声骨刀开槽并去除椎体前部约4/5骨质,磨钻或超声骨刀去除剩余的椎体后壁并修薄骨化的后纵韧带,用神经剥离钩潜行分离、超薄椎板钳咬除骨化物,若发现骨化灶与硬膜囊粘连严重且分离困难则采用“漂浮法”将其游离、使硬膜囊向前漂浮。止血、冲洗后植入填充有自体骨或人工骨的Cage或钛网及锁定钛板,留置引流管、缝合切口、颈托固定。
2.3 术后处理
一般术后第2天拔除引流管,佩戴颈托、家属陪护下地活动,1个月去除颈托,进行适量的功能锻炼。
2.4 评估指标
2.4.1神经功能评定 术前、术后1周、术后3个月及末次随访时的神经功能以日本整形外科学会(JOA)评分法进行评价(17分)。神经功能恢复率=[(术后评分-术前评分)/(17-术前评分)]×100%。疗效根据恢复率分为4级:恢复率≥75%为优,恢复率≥50%且<75%为良,恢复率<50%且≥25%为可,恢复率<25%为差。
2.4.2影像学评价 术前、术后1周及1、3、6、12个月摄颈椎正侧位及动力位X线片,术后3个月、6个月行颈椎CT重建检查,评价植骨融合情况及内植物有无移位。测量C2~C7Cobb角评估颈椎生理曲度的恢复情况。
2.5 统计学方法
3 结果
本组共45例患者,手术时间(105±21)min(90~134 min);出血量(220±65)mL(150~550 mL),术中均未输血。随访12~22个月,平均(15.5±3.6)个月。45例患者术后1周、3个月及末次随访的JOA评分均较术前明显改善,JOA总分从术前(10.28±1.39)分增加到(14.58±1.27)分,差异有统计学意义(P<0.01);其中优24例,良17例,有效4例,优良率为91.11%。术后不同时期的C2~C7Cobb角度均较术前明显改善,差异有统计学意义(P<0.01)(见表1)。术后声音嘶哑3例,饮水呛咳2例,吞咽疼痛和困难7例,通过调节饮食、雾化吸入、营养神经等保守治疗,均在1周~2.5个月内得到明显缓解或痊愈,切口均一期愈合。术后6~9个月植骨全部融合,2例发生钛网塌陷。典型病例见图1-图2。
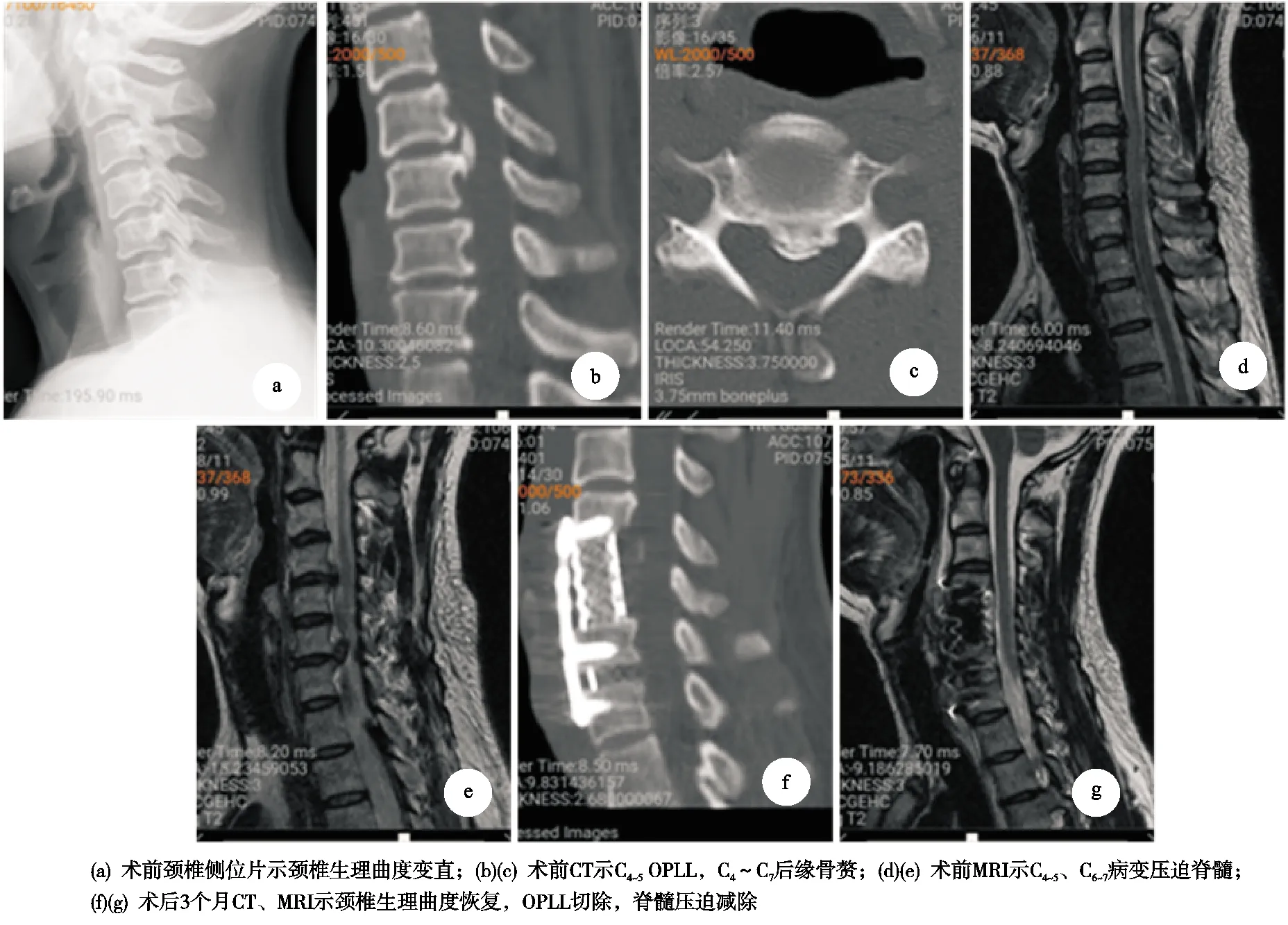
图1 病例1,男,66岁,C4~5 OPLL,脊髓型颈椎病,手术方式为ACDF +ACCF
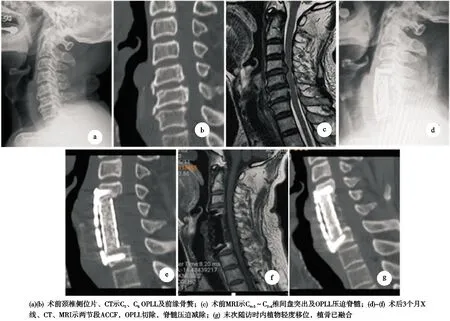
图2 病例2,男,73岁,C5、C6 OPLL,手术方式为ACCF
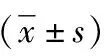
表1 手术前后神经功能JOA评分及C2~C7 Cobb角比较
4 讨论
后纵韧带骨化症最常见于颈椎,发病机制仍不十分明确,研究显示其与年龄、激素、环境、遗传、机械性刺激、糖尿病、肥胖、高钠饮食及生物力学改变等局部或全身因素密切相关[3]。颈椎OPLL基本的影像学检查是颈椎正侧位和动力位X线片,但常因拍摄质量、角度、病变程度、阅片水平等原因导致漏诊、误诊[4]。MRI可良好显示脊髓受压迫的部位和程度,但骨化的后纵韧带在T1和T2加权像上均呈低信号,易与突出的椎间盘组织混淆。而CT二维重建诊断OPLL的准确率可达99%,在颈椎OPLL的诊断中必不可少[5]。CT矢状位片上OPLL分为孤立型、节段型、混合型和连续型,轴位片上分为窄基型和宽基型。但仅有影像学资料显示后纵韧带骨化而无相应临床症状和体征者不能诊断为OPLL;只有当影像学特征性表现、症状和体征同时存在且一致时才可诊断为颈椎OPLL。
对于症状较轻或暂不宜手术的患者可先行非手术治疗。保守治疗无效且有加重趋势或症状较重的OPLL患者需要行手术治疗。手术入路和方式的选择应根据骨化灶的形状、椎管狭窄率、影像学特征、颈椎曲度、患者身体和经济条件、医生技术擅长等因素综合考量,而并非最新的术式就是最好的选择[6]。手术入路包括前路、后路或前后联合入路。其中前入路手术方式主要有椎体次全切除减压融合术、经椎间隙减压融合术及Hybrid技术等。目前对颈椎OPLL前路手术的适应证仍存在争议,但基本原则是一致的[7]。前入路手术适用于:1)局灶型OPLL;2)≤2个椎节的节段型窄基OPLL;3)部分混合型OPLL;4)少部分宽基型OPLL;5)骨化灶位于C3~C7节段。颈椎OPLL前路减压的关键之一是OPLL的边界:1)矢状面的边界(俗称长度)。仅少部分局灶型的OPLL可通过单纯的椎间隙减压切除,大部分患者需要做椎体次全切除,如果需切除椎体≤2个可以选择前路手术。当切除椎体≥3个时术后并发症明显增加,原因如下:(1)手术时间长,过度牵拉气管和食道,入路相关并发症增多;(2)长节段脊柱重建易出现内固定松动,如钛网下沉、移位等;(3)过多节段的融合,颈椎的活动范围明显降低。所以对于3个或3个以上的椎体次全切除减压融合术应慎重选择。本组病例选择累及C3~C7且节段型OPLL范围均≤2个椎节。2)横断面的边界(俗称宽度)。对窄基型OPLL,一般可以在Luschka关节内侧找到骨化灶的边界,前路手术易于切除骨化灶,可先从骨化韧带的蒂部周围开始,因为蒂部周缘往往存在潜在间隙,分离相对容易;而对宽基型OPLL,标准的椎体切除宽度不能达到骨化物的边界,常常需要减压到Luschka关节外侧,容易损伤椎动脉。少部分宽基型、其外侧边界未超过双侧Luschka关节的内侧缘者可行前路手术[8],本组3例宽基型OPLL均符合上述标准;根据CT成像结果,从骨化灶薄弱处逐渐进行。但因减压范围宽,术中操作相对复杂,需谨慎选择和操作。本组45例患者的手术方式:ACDF 5例,ACCF 28例,ACDF+ACCF 12例,均减压满意。前路手术有很多优点[9]:1)体位简单,便于操作;2)可以直接切除骨化韧带、骨赘、突出椎间盘等病变处,解除脊髓和神经根压迫;3)易于矫正颈椎曲度。陈德玉等[10]运用前路技术治疗61例颈椎OPLL均获得了满意的减压和神经功能恢复,5例脑脊液漏经保守治疗后痊愈。
术前可根据影像学资料初步评估骨化物切除的可能性,CT成像对判断骨化灶与硬脊膜等周围组织的关系非常重要。若CT轴位片示骨化灶呈“单影征”者为中央成骨,即骨化从后纵韧带中央向周围呈膨胀式发展,则硬脊膜发生粘连及骨化的可能性相对较小、易于切除。假如骨化灶呈“双影征”者为周围成骨、即骨化始于韧带周围,矢状位CT显示为分层结构——高密度骨化物包裹中间低密度的未完全骨化的后纵韧带,则硬脊膜存在粘连、骨化的可能性较大,完全切除难度大,盲目切除易引起硬膜撕裂、脑脊液漏及脊髓损伤[11-12]。由此产生了“漂浮法”技术——先应用高速磨钻将骨化灶磨薄至3~5 mm,形成贝壳样弧度,再游离骨化灶头尾两侧缘并咬除骨化灶外围未与硬膜发生粘连的部分,最后解除整个骨化物与椎体的连接,骨化灶旷置并在脑脊液的压力下缓慢向前漂移,同样可以达到直接减压的目的[13]。本组病例中单影征41例,双影征4例,术中发现单影征者与硬脊膜均无明显粘连,4例双影征者骨化灶与硬脊膜有不同程度粘连,未强求切除全部骨化灶,采用“漂浮法”减压术后疗效满意,未发生脑脊液漏。王瑞等[14]采用“漂浮法”减压治疗36例孤立型颈椎OPLL,获得了良好的神经功能改善。
虽然前路手术有诸多独特的优势,但也有发生各种并发症的可能,需谨慎操作。主要是咽喉部刺激症状、喉返神经损伤、气管和食管损伤、脑脊液漏等。本组45例患者,术后声音嘶哑3例、饮水呛咳2例、吞咽疼痛和困难7例。无切口感染、脑脊液漏、植骨不融合等并发症发生;2例发生钛网塌陷,随访无特殊不适,未做处理。对于颈椎OPLL,同样范围的前路手术较脊髓型颈椎病更为困难,风险更高,须谨慎操作。
因此,对于OPLL只要严格掌握适应证、仔细操作,可以获得脊髓的直接减压和满意的疗效。但前路切除OPLL是一项技术性非常强的操作,稍有不慎后果严重,建议由经验丰富的术者完成,有条件者可以配合脊髓电生理监测,有助于降低脊髓损伤的风险。
