关节突关节内植骨在下颈椎后路减压融合术中的应用
2021-08-033
3
(1.北部战区总医院/全军重症战伤救治中心骨科,辽宁 沈阳 110016;2.大连医科大学研究生院,辽宁 大连 116044;3.天津医院骨科,天津 300211)
后纵韧带骨化是根据主要致病因素而命名的颈椎疾病,颈椎后纵韧带骨化的病因至今尚不明确,多数学者认为应归因于颈椎的退行性改变,也可能与糖、钙代谢障碍及遗传因素有关[1-2]。后纵韧带骨化后会在长轴方向和水平方向进展,长轴方向上后纵韧带骨化会减少颈椎活动度,加重颈椎的退行性变;水平方向上的后纵韧带骨化会占据椎管前部空间,导致颈椎管狭窄,而脊髓被来自前方骨化的后纵韧带挤压,加之椎管后壁的阻挡,会出现感觉和运动功能障碍,且随着脊髓压迫的加重最终会造成不可逆的损害[3-4]。目前颈椎后纵韧带骨化症的手术治疗方式大体分为颈椎前路、后路及前后路联合手术,对于多节段颈椎后纵韧带骨化症患者,临床常倾向于选择后路手术。下颈椎后路减压融合术后,侧块螺钉只是起到临时固定颈椎的作用,坚强的植骨融合才是下颈椎后路融合术成功的关键。植骨方式主要有椎板间植骨、侧块表面植骨、关节突关节内植骨。对于植骨骨质选择来说,自体松质骨因含有骨诱导和骨引导因子、可提升植骨融合率而被视为最佳选择[5-6]。椎板间及侧块表面植骨往往需要大量的松质骨粒,而自体松质骨粒有限,植骨量不足会形成假关节,导致下颈椎后路融合术失败,且会随着颈椎活动应力不均而加重颈椎退行性变[7]。为了达到坚强内固定,必须要有足够的植骨面积,即需要大量松质骨粒,这时候就需要使用人工骨代替完成植骨,然而使用人工骨植骨会增加手术费用,且植骨融合率低,临床应用受到一定限制。关节突关节内植骨只需要少量松质骨粒就可以达到坚强的骨性融合,且不需要人工骨代替,假关节发生率低,但仅见用于治疗寰枢椎不稳[8],对于下颈椎后路融合术尚未见相关报道。本研究将关节突关节内植骨应用于下颈椎后路减压融合术,取得了良好疗效,现报告如下。
1 资料与方法
1.1 临床资料
选取2016年1月至2019年12月就诊于北部战区总医院骨科的多节段颈椎后纵韧带骨化症患者60例,均行颈椎后路单开门椎管扩大成形、侧块螺钉内固定术,利用随机数字表法将其分为观察组和对照组,每组30例。观察组患者行术中门轴侧植骨、开门侧关节突关节内植骨;对照组患者行术中门轴侧植骨、开门侧侧块表面植骨。2组患者术前均行颈椎正侧位X射线、颈椎三维CT、颈椎MR平扫以明确诊断,部分患者加做过伸过屈位X射线检查。纳入标准:①具有感觉和运动障碍,影像学表现为多节段椎管变窄,明确诊断为多节段颈椎后纵韧带骨化症;②随访时间≥12个月;③均有脊髓受压症状,且呈进行性加重;④伴外伤、不稳,需行颈椎后路单开门椎管扩大成形、侧块螺钉内固定术。排除标准:①强直性脊柱炎;②肿瘤或感染导致下颈椎不稳;③保守治疗有效或存在手术禁忌。2组患者年龄、性别、手术时间、失血量比较差异均无统计学意义(P>0.05),见表1。

表1 2组患者临床资料比较
1.2 手术过程
患者全身麻醉后取俯卧位,腹部悬空,头部固定于头架上并保持中立位,调整患者体位至头高足低位,术野常规消毒、铺巾,于颈部后方C3~C7作正中切口,依次切开皮肤、皮下及深筋膜。纵切项韧带及颈肌附着点,分别向两侧剥离,显露C3~C7椎板。一般选择触摸C2棘突及C7棘突定位,难以触摸分辨时可以进行透视定位,避免因切口延长导致过多的组织损伤。使用软组织撑开器将肌肉及软组织撑开保护,充分暴露术区。应用Anderson置钉技术,依次于C3~C7双侧侧块以适当角度用开口器开口、手钻钻孔、攻丝,然后涂抹骨蜡止血,制备钉道备用。
常规后路单开门椎管扩大成形术:咬骨钳咬除C2/C3和C6/C7棘上、棘间韧带,修剪C3~C7棘突,避免棘突过长影响椎板掀开,并于棘突根部打孔备用。用椎板咬骨钳于双侧椎板开骨槽,选取压迫较轻一侧作为门轴侧,保留内层骨板,压迫较重一侧作为开门侧,切开椎板全层骨质。将咬下的椎板骨中的松质骨粒留用。切开C2~C3、C6~C7间黄韧带及开门侧黄韧带,剥离并切断粘连带后,将C3~C6椎板向门轴侧掀起。术中可见减压后脊髓较饱满,搏动好。门轴侧拧入合适长度侧块螺钉,适度折弯并安放连接棒,锁紧螺帽。10号丝线穿过棘突根部孔道后悬吊并收紧、打结,将C3~C6椎板固定于连接棒上并维持开大状态。
开门侧处理:观察组拧入合适长度侧块螺钉,用丝锥反复旋入、旋出,破坏关节突关节软骨,适度折弯连接棒,安放连接棒并适度加压,锁紧螺帽;对照组拧入合适长度侧块螺钉,将侧块表面皮质骨打磨毛糙,安放适度折弯的连接棒,锁紧螺帽。2组患者均采用C型臂X射线机透视确认侧块螺钉位置良好,连接棒长度及弯曲度合适。随后用3 000 mL生理盐水彻底冲洗术区,仔细止血,保证硬脊膜局部无致压物。门轴侧松质骨粒植骨:观察组开门侧于丝锥破坏的关节突关节间隙内植入松质骨粒,表面覆盖明胶海绵;对照组开门侧于侧块表面植入松质骨粒,表面覆盖明胶海绵。2组患者切口内均放置负压引流管2根。由浅层到深层仔细止血,术区无肉眼可见出血,清点纱布及棉片数量无误后逐层缝合切口,术毕。患者术中生命体征平稳,麻醉满意,术后安返病房。
1.3 术后处理
术后患者均常规使用抗菌药物预防感染,严格遵守抗菌药物使用原则。术后第3天拔除双侧引流管,行颈椎正侧位X射线检查,影像结果示内固定位置良好后嘱患者佩戴颈托下地活动,常规颈托固定3个月,之后去颈托行颈部康复锻炼。术后3个月复查颈椎正侧位X射线,术后6、12个月复查颈椎三维CT,之后每年复查颈椎正侧位X射线。
1.4 观察指标
比较2组患者手术前后日本骨科协会评估治疗(Japanese Orthopaedic Association,JOA)评分、疼痛视觉模拟量表(visual analogue scale,VAS)评分及骨性融合情况[9]。
1.5 统计学分析

2 结果
2.1 术后恢复及并发症情况
术后患者症状均显著改善,均未发生脑脊液漏。3例患者术后出现C5神经根麻痹:观察组1例患者于术后3 d出现C5神经根麻痹,于术后6周恢复;对照组1例患者于术后6 d出现C5神经根麻痹,于术后8周恢复,1例患者于术后1周出现C5神经根麻痹,于术后4周恢复。3例患者术后出现切口愈合不良:观察组1例患者术后切口感染,经过清创缝合处理后切口愈合良好;对照组1例患者术后切口延迟愈合,经红外线灯理疗后切口愈合良好,另1例患者术后切口感染,经过清创缝合处理后切口愈合良好。观察组11例、对照组10例患者术后出现不同程度颈肩部轴性痛。于术后6、12个月进行随访,患者内固定位置良好。2组患者术后6、12个月JOA评分及疼痛VAS评分均较术前明显改善,差异有统计学意义(P<0.05),见表2。患者术后6个月三维CT均可见关节突关节内、侧块表面明显骨桥形成,骨性融合率为100%。

表2 2组手术前后JOA评分、VAS评分比较分)
2.2 典型病例
患者,男,47岁,因“外伤致四肢麻木无力1 d”入院。专科查体:双上肢、左下肢皮肤浅感觉迟钝,三角肌左/右=4级/4级、肱二头肌左/右=4级/4级、肱三头肌左/右=2级/2级、屈腕肌左/右=2级/2级、屈指肌左/右=0级/0级、伸腕肌左/右=2级/2级、伸指肌左/右=0级/0级、手内在肌左/右=0级/0级、下肢肌力左/右=5级/3级,四肢肌张力增高,肱二头肌腱反射左/右=正常/正常、肱三头肌腱反射左/右=活跃/活跃、桡骨膜倒错反射左/右=(+)/(+)、膝腱反射左/右=正常/活跃、跟腱反射左/右=正常/活跃,Hoffmann征左/右=(+)/(+)、Babinski征左/右=(-)/(+),见图1。入院后完善相关检查,无手术禁忌,于全身麻醉下行颈椎后路减压融合术,手术顺利完成,术后安返病房,术后2周拆线出院,见图2。
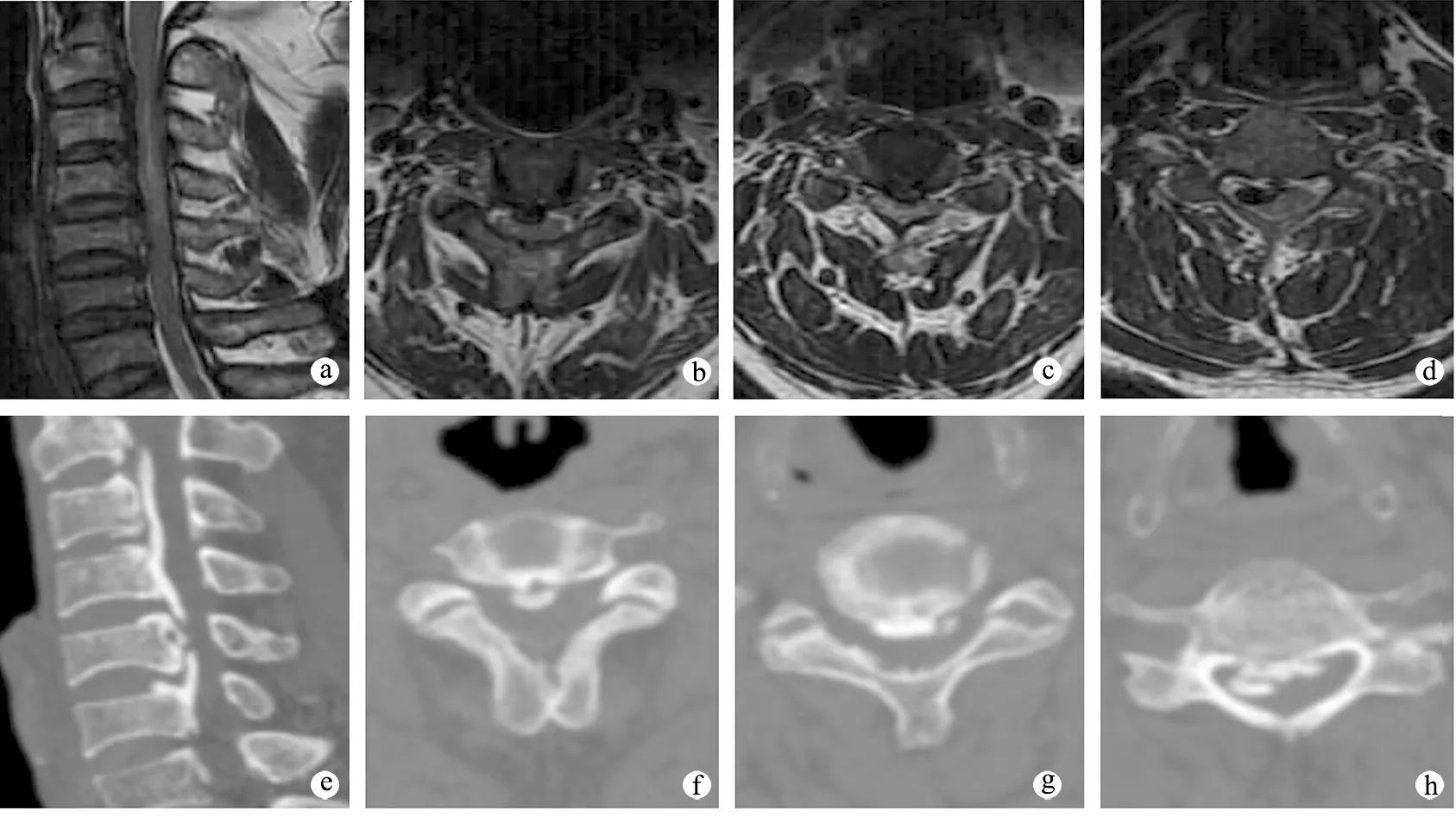
a~d:术前MRI示多节段颈椎管狭窄,颈脊髓明显受压;e~h:术前三维CT示颈椎后纵韧带骨化,多节段颈椎管狭窄图1 术前影像学资料

a~b:术后X射线示内固定位置良好;c~h:术后6个月三维CT示关节突关节间形成牢固骨性融合图2 术后影像学资料
3 讨论
一直以来,无明显症状的颈椎后纵韧带骨化症患者是否采取手术治疗都存在争论。当脊髓严重受压时,T2加权的MRI会出现高信号,反映脊髓水肿或脊髓软化,异常体感诱发电位反应显示延迟,再结合患者的临床表现,这些都是考虑预防性手术的适应证[10]。目前颈椎后路手术大多采用单开门椎管扩大成形术,即非融合手术,可以达到脊髓减压和保留颈椎部分活动度的目的。对于多节段颈椎后纵韧带骨化伴外伤、不稳的患者,临床大多采用全椎板切除联合侧块螺钉内固定术,充分减压脊髓的同时可起到稳定颈椎的作用,但全椎板切除术手术时间长,创伤大,出血量多,术后颈脊髓后移程度较大,加之缺少椎板保护,术后形成的肌肉瘢痕会再次对颈脊髓造成压迫,因此,C5神经根易受牵拉而引起麻痹。本研究采用颈椎后路单开门椎管扩大成形、侧块螺钉内固定术,与全椎板切除术相比,该术式在脊髓减压的同时保留了后方椎板,保留下来的椎板可以防止肌肉瘢痕压迫脊髓,从而起到保护脊髓的作用,并可将后移的颈脊髓约束在一个适当的范围内,降低过度牵拉引起C5神经根麻痹的概率;而内固定系统的预弯棒、旋棒等技术可以帮助颈椎恢复生理前凸,并对术后颈椎的稳定性重建起到关键作用,使得颈脊髓再损伤的发生率降低,为脊髓功能的恢复创造了有利条件,这也说明了侧块螺钉内固定的必要性[11]。虽然后路手术避免了许多前路手术存在的并发症,但仍会出现明显的术后颈肩部肌肉痉挛和疼痛、术后C5神经根麻痹,其中C5神经根麻痹最为常见,发生率为4.4%~7.2%[12-13],其原因目前仍不清楚,但本研究尽量通过保护颈椎旁肌肉来减弱这种轴性疼痛[14]。
本研究对于多节段颈椎后纵韧带骨化伴外伤、不稳的患者采用单开门椎管扩大成形、侧块螺钉内固定术,术中钉棒系统只起到临时固定颈椎的作用[15-16]。而坚强的植骨融合才是下颈椎后路融合术成功的关键。自体松质骨因具有成骨性、骨传导性和骨诱导性,故作为最佳选择,但自体骨移植物的数量有限,而椎板间及侧块表面植骨往往需要大量的松质骨粒,椎管扩大成形术椎板开槽时椎板咬骨钳咬下来的剔除软组织的松质骨粒通常无法满足其植骨需要[9,15,17]。为了达到坚强的内固定,需要大量松质骨粒保障足够的植骨面积,植骨量不足易导致融合率低而形成假关节,引起术后疼痛,且随着长期颈椎活动应力不均会加重颈椎退行性改变[8]。关节突关节内植骨所需植骨量少,且可以获得较高的植骨融合率,因此不会受到该因素的限制。关节突关节在整个脊柱的稳定性中起着重要的作用,不仅承担着脊柱30%的负荷,还参与脊柱各个方向的活动。有研究显示关节突损伤是术后脊柱后凸的主要原因,若关节突关节面部被切除范围超过50%,则会导致脊椎明显后凸和不稳定[18]。通过关节突关节内的植骨融合,限制关节突关节各个方向的活动,所以关节突关节内才是较为可靠的植骨部位。传统下颈椎后路融合术中后外侧植骨,也就是侧块表面植骨,因为植骨粒位于侧块表面,术中固定及术后患者体位变化均会导致植骨粒进入椎管,从而压迫颈脊髓,而关节突关节内植骨因植骨粒位于上下关节突之间,位置较牢固,不存在上述风险,相对安全。本研究采用的关节突关节内植骨较侧块表面植骨具有明显优势,术中操作简便,创面小,不存在植骨粒进入椎管压迫颈脊髓的风险,只需要少量松质骨粒即可达到坚强的骨性融合,不需要人工骨代替,植骨融合率高,假关节发生率低,可以达到下颈椎各个方向运动的生物力学稳定。
对术后植骨融合情况的准确评估一直是困扰术者的问题。改良的脊柱内固定使融合评估更具挑战性,因其具有放射性不透明的内固定器械,会模糊融合骨块的外观,并且提供坚强的固定,即使植骨融合失败,也可以限制颈椎的屈曲和旋转运动。这样会误导仅依靠颈椎X射线来判断植骨融合情况的术者,得到与实际不相符的植骨融合率。因此,带重建的颈椎三维CT已成为评价植骨融合是否成功的标准[9,19]。所以本研究要求患者术后必须复查颈椎三维CT,以作为观察关节突关节内骨性融合情况的关键证据。
本研究结果显示,关节突关节内植骨可达到缓解脊髓压迫症状的目的,不会造成其他不良影响;采用JOA评分对患者身体状况进行评估,即采用17分制对颈脊髓病的严重程度进行量化分级,可以帮助临床医生准确评估患者病情以便制订合适的治疗方案[20-22]。术后颈椎三维CT也可以从不同层面上观察到植骨区骨桥形成,说明关节突关节内植骨具有可行性,而重建的颈椎三维CT已成为评价植骨融合是否成功的标准,这种评判方法也被证实是真实可靠的[9]。
对于多节段颈椎后纵韧带骨化伴外伤、不稳的患者,本研究采用颈椎后路单开门椎管扩大成形、侧块螺钉内固定术,相较于全椎板切除联合内固定术,其在减压脊髓、稳定颈椎的同时,还具有手术时间短、创伤小、能保护颈椎后方附件、降低C5神经根麻痹风险、防止术后肌肉瘢痕形成造成脊髓二次压迫的优势,在临床中应用前景良好。多节段颈椎后纵韧带骨化症患者采用关节突关节内植骨,可以获得较高的骨性融合率,所需植骨量少,且假关节发生率低,可以达到下颈椎各个方向运动的生物力学稳定。因而关节突关节内植骨融合可以代替传统侧块表面植骨融合,为进一步研究关节突关节间融合器奠定了理论基础,提供了实践参考[23]。但本研究也有局限性:病例数较少,均是多节段颈椎后纵韧带骨化伴外伤、不稳患者,未包含全部颈脊髓病需行下颈椎后路融合术的患者,且本研究的手术方式结合了颈椎后路单开门椎管扩大成形术和颈椎多个侧块螺钉内固定术,对于术者操作技术以及手术设备要求较高。
