炼钢用钙铁包芯线主次元素测定方法的试验研究
2021-08-02关漫漫李存根
关漫漫 李存根
(安阳钢铁股份有限公司)
0 前言
随着现代工业科学技术的发展,对钢的性能要求越来越高。而钢中非金属夹杂物是影响钢材性能的主要因素之一,有的甚至是决定性的因素。提高钢水的纯净度,降低钢中氧含量和氧化物夹杂,一直是钢铁冶炼的一大难点。目前,对纯度要求较高的钢种,大都采用金属铝进行预脱氧或终脱氧。但采用金属铝进行预脱氧或终脱氧,钢水的浇铸性不稳定,容易发生水口结瘤,结瘤物的主要成分为Al2O3。通过喂入钙铁包芯线,可以把脱氧生产的大颗粒高熔点脆性的Al2O3夹杂物变成低熔点的钙铝酸性盐夹杂(如12CaO·7Al2O3),有效促进夹杂物上浮,提高钢水洁净度[1]。使用钙铁包芯线进行钙处理是一种高效的脱氧技术,能起到脱氧、脱硫、去夹杂的作用,净化钢水,控制钢中AlS含量。钙铁包芯线可提高钢的可浇性,使钢水不增硅,稳定钢的力学性能,改善钢的横向冲击韧性,热加工性,塑性,提高产品质量,降低生产成本。
安阳钢铁集团公司尚未开展钙铁线的化学分析工作,对钙铁线中钙、铁的成分检测虽有报道[2-5],但都是个别元素,且方法不尽相同,对其中主次元素的分析未见报道。结合安钢生产情况,研究开发钙铁线中主元素和杂质元素联合测定方法。本文采用盐酸、双氧水低温溶样,分别用EDTA标准溶液滴定法测定钙;氯化亚锡-三氯化钛还原,重铬酸钾标准溶液滴定法测定铁;ICP-AES法测定铝铬磷钛硅锰磷等杂质成分。炼钢用钙铁包芯线主元素及杂质元素测定方法的分析研究应用,彻底结束该品种外检的历史,按公司使用量及外委检验频次,年节省外检资金近九万元。这项技术的开发应用,可开展进厂钙铁包芯线原料抽查检验,及时反馈钙铁包芯线的成分指标,准确把控产品质量,指导精准配料及采购结算。随着环保意识的逐步增强,开始使用无汞测铁,消除使用有毒物质汞对环境及人身的毒害,符合健康、环保的发展理念,炼钢用钙铁包芯线主元素及杂质元素测定方法的应用具有可观的经济效益和现实的社会效益。
1 实验部分
1.1.1 试剂
乙二胺四乙酸二钠标准溶液(EDTA):CEDTA=0.0100 0 moL/L;重铬酸钾标准溶液: C1/6K2Cr2O7=0.050 00 moL/L; Al、Cr、P、Ti单元素标准溶液(北京纳克公司):1 000 µm/mL;Si元素标准溶液(北京纳克公司):500 µm/mL;Mn元素标准溶液(北京纳克公司):100 µm/mL;Fe、 Ca元素标准溶液:10 mg/mL;三乙醇胺溶液(1+3):一份三乙醇胺加三份水,同时含3%盐酸羟胺;氢氧化钾溶液:250 g/L;三氯化钛溶液(1+9):取三氯化钛溶液(15%~20%)用盐酸(1+19)稀释20倍,用时现配;钨酸钠溶液:250 g/L;氯化亚锡溶液:60 g/L;硫磷混酸(1.5+1.5+7);二苯胺磺酸钠指示剂:2 g/L;盐酸(1+4);双氧水(30%);钙黄绿素指示剂:固体,0.2 g钙黄绿素+0.2 g百里香酚酞+50 g氯化钾研细混匀。试验用水均为去离子水。
1.1.2 仪器及工作条件
试验所用仪器为美国Thermo Fisher 公司iCAP7400型电感耦合等离子体原子发射光谱仪,优化仪器参数见表1。

表1 仪器参数
1.2 方法原理
试样经盐酸处理,分次滴加双氧水,使试样氧化分解,定容制成母液。分取一定量母液,利用络合反应原理,加入掩蔽剂,调整酸度,加入适量指示剂,以EDTA标准溶液滴定钙离子,根据消耗EDTA标准溶液的量,计算钙的含量。分取一定量母液,利用氧化还原反应原理,先把Fe3+还原成Fe2+,加入硫磷混酸络合剂,以二苯胺磺酸钠作指示剂,以重铬酸钾标准溶液滴定Fe2+,根据消耗重铬酸钾标准溶液的量,计算铁的含量。母液在电感耦合等离子体原子发射光谱仪上,按照选定的仪器最佳工作条件,和选定的分析谱线测定Al、Cr、P、Ti、Si、Mn各元素的谱线强度,根据标准系列换算试样待测元素含量。
1.3 试验方法
1.3.1 试样的处理
称取0.250 0 g试样于250 mL烧杯中,加入50 mL盐酸(1+4)待剧烈反应结束后,低温加热溶解,分次滴加2 mL双氧水,至试样溶解完全,煮沸驱除过量的双氧水。流水冷却至室温,定容至250 mL容量瓶,摇匀,制成母液,待用。
1.3.2 钙的测定
移取25.00 mL母液于500 mL烧杯中,加三乙醇胺(1+2)10 mL,搅拌均匀,加水至250 mL,加入氢氧化钾(250 g/L)20 mL,加少许钙黄绿素指示剂,以EDTA标准溶液滴定至溶液荧光黄消失为终点,记录消耗EDTA标准溶液的体积V1。随同试样做空白试验,记录消耗EDTA标准溶液体积为V0。试样中钙含量的计算方法见式(1)。

式中:C——EDTA标准溶液的浓度,moL/L;V1——滴定所消耗EDTA标准溶液的体积,mL;V0——空白试验所消耗EDTA标准溶液的体积,mL;m——试样质量,g;25/250——从250 mL母液中分取25 mL的换算关系;0.040 08为钙的换算关系。
1.3.3 铁的测定
移取100.00 mL母液于500 mL锥形瓶中,加热以氯化亚锡(60 g/L)还原至浅黄色,冷却,加水稀释至150 mL,加钨酸钠溶液10滴,用三氯化钛溶液还原至深蓝色,用重铬酸钾标准溶液滴定至蓝色消失(不计读数)。加硫磷混酸20 mL,二苯胺磺酸钠指示剂5滴,用重铬酸钾标准溶液滴定至稳定的紫色为终点,记录消耗重铬酸钾标准溶液体积V2。随同试样做空白试验,记录消耗重铬酸钾标准溶液的体积V0。试样中铁含量的计算方法:

式中:C——重铬酸钾标准溶液的浓度,moL/L;V2——滴定所消耗重铬酸钾标准溶液的体积,mL;V0——空白试验所消耗重铬酸钾标准溶液的体积,mL;m——试样质量,g;100/250表示从250 mL母液中分取100 mL的换算关系;0.055 85为铁的换算关系。
1.3.4 铝铬磷钛硅锰的测定
1.3.4.1 标准系列溶液的配制
用可调微量移液器分别移取(1.1.1)中0 µL、25.0 µL、50.0 µL、75.0 µL、100.0 µL、125.0 µL Al标液;0 µL、1.0 µL、2.0 µL、3.0 µL、4.0 µL、5.0 µL Cr标液;0 µL、10.0 µL、15.0 µL、20.0 µL、25.0 µL、30.0 µL P标液;0 µL、1.0 µL、2.0 µL、3.0 µL、4.0 µL、5.0 µL Ti标液;0 µL、20.0 µL、40.0 µL、60.0 µL、80.0 µL、100.0 µL Si标液;0 µL、100.0 µL、200.0 µL、300.0 µL、400.0 µL、500.0 µL Mn标液,于6个50 mL容量瓶中,加入(1.1.1)中1.5 mLCa标液、3.5 mLFe标液,使Ca、Fe基体分别为30%、70%,加10 mL盐酸(1+4)定容至刻度,摇匀。此标准溶液系列中Al的质量浓度为0%、0.050%、0.10%、0.15%、0.20%、0.25%;Cr、Ti、的质量浓度分别为0%、0.002 0%、0.004 0%、0.006 0%、0.008 0%、0.010%;P的质量浓度为0%、0.020%、0.030%、0.040%、0.050%、0.060%;Si、Mn的质量浓度分别为0%、0.020%、0.040%、0.060%、0.080%、0.10%。
1.3.4.2 测定
在iCAP7400型电感耦合等离子体原子发射光谱仪上,按照选定的仪器工作条件,测定标准系列中各元素的谱线强度,校准工作曲线,测定待测各元素的含量。
2 结果与讨论
2.1 溶样酸的选择
钙铁包芯线主要是由金属铁粉和金属钙组成。首先须将试样完全分解,制成溶液,才能进行化学方法及ICP-AES方法的测定。在金属活动顺序中,铁位于氢之前,是一种中等活性的金属,能与酸发生反应。铁和浓硫酸无明显变化,因为在常温下,浓硫酸能使铁表面形成一层致密的保护层,产生钝化,阻止内部金属继续和硫酸发生反应。而硫酸钙是一种微溶物质,溶解度较小,易形成沉淀,不利于钙的测定。在常温下金属铁与浓硝酸发生钝化,与稀硝酸作用主要生成N2O、NO。由于硝酸的化学性质,在测定Fe3+时硝酸根影响还原和滴定。使用稀盐酸处理样品,样品溶解迅速,反应彻底,双氧水是一种有效氧化剂,分解试样时与盐酸联用,加速试样的分解,加热煮沸双氧水即分解。盐酸粘度小,有利于电感耦合等离子体原子发射光谱仪激发。使用盐酸溶解样品有效解决上述酸处理样品带来的问题,对各元素的测定不会造成影响。选用盐酸(1+4)加H2O2分解样品。
2.2 钙测定条件的优化
2.2.1 掩蔽剂
钙铁线是由Ca、Fe主元素及Al、Cr、P、Ti、Si、Mn等杂质元素组成。在用EDTA标准溶液滴定Ca时,基体中的Fe及Al、Mn、Ti会对指示剂产生封闭作用,因此,必须加以掩蔽消除这些金属离子的干扰。常采用的掩蔽剂有柠檬酸胺、三乙醇胺、酒石酸钾钠、氰化钾等,氰化钾有剧毒,一般不采用。通过对几种掩蔽剂的掩蔽效果进行比较,三乙醇胺加盐酸羟胺复合掩蔽能力强,效果好,使用安全方便。采用三乙醇胺加盐酸羟胺作复合掩蔽剂。
2.2.2 铁离子干扰的考察
溶液中含有大量的Fe3+,Fe3+可与EDTA发生络合反应,使测定结果偏高,Fe3+也能对指示剂产生封闭作用,使滴定终点拖后。消除Fe3+的干扰可采用氨水分离法和三乙醇胺、盐酸羟联合胺掩蔽法,这两种方法分别对附企公司送检的编号为10-1、11-2两个样品进行了6次测定,结果见表2。
从表2可以看出,两种方法测定结果一致。由于氨水分离Fe3+法的步骤繁琐,故选用三乙醇胺、盐酸羟联合胺掩蔽Fe3+法进行滴定。
2.2.3 指示剂的选择
在络合滴定中,通常利用一种能与金属离子生产有色络合物的显色剂,它可以指示等当点时金属离子浓度的突变。为减少滴定误差,所选指示剂应尽量使其变色点与滴定等当点一致。EDTA滴定Ca2+时,Al、Fe、Ni、Cu等与铬黑T指示剂形成十分稳定的有色络合物,使铬黑T指示剂失去指示Ca2+滴定终点的作用。二甲酚橙只适用于PH<6的酸性溶液,且 Al、Fe、Ni、Ti离子有封闭作用。PAN与Ca2+不显色,PAN不能直接作滴定Ca2+的指示剂。钙试剂,在溶液酸度PH=12~13时与Ca2+形成红色络合物,滴定终点呈指示剂本身的蓝色,由于干扰离子的存在,使指示剂突变不明显。钙黄绿素指示剂在碱性溶液中能与痕量 Ca2+显色,呈绿色荧光,可指示0.08 µg钙,灵敏度高,其指示剂所不及,溶液中的Fe、Al、Mn、Ni的干扰可用三乙醇胺加盐酸羟胺掩蔽,钙黄绿素中加入适量百里香酚酞使滴定终点变化更明显。选用钙黄绿素百里香酚酞联合指示剂。

表2 两种方法测定结果 %
2.3 铁测定的优化条件
2.3.1 钨酸钠的选择
在以盐酸为介质的溶液中用钨酸钠作指示剂,是因为钨酸钠比其他有机指示剂都优越,变色灵敏,氧化态为无色,对重铬酸钾滴定全铁时观察终点的颜色变化没有影响,当溶液中使用的介质不同时,指示剂所受影响不大。随着环保意识的逐步增强,开始使用无汞测铁,试样溶解后,以氯化亚锡将大部分Fe3+还原,再以钨酸钠为指示剂,用三氯化钛还原W(Ⅱ)至W(Ⅴ),钨的蓝色出现,表示Fe3+已被还原完全。消除使用有毒物质汞对环境及人身的毒害。
2.3.2 K2Cr2O7滴定介质
在进行K2Cr2O7标准溶液滴定Fe2+时,选用在硫酸-磷酸介质中进行。主要作用:保证反应的酸度、 Fe3+与H3PO4生成稳定的Fe(HPO4)-2络合物,降低Fe3+/Fe2+电对的电位,使等当点附近电位突跃范围增大、生成无色Fe(HPO4)-2络合物,消除了FeCl63-络合物的黄色,有利于终点的观察。
2.3.3 干扰元素
由于氯化亚锡能将Cu2+还原为Cu+,Cu+能被重铬酸钾氧化,同时铜离子又能促使Fe2+被空气中氧氧化,所以铜含量高时进行干扰测定,试验表明铜含量小于0.2%,无干扰。钒大于0.5 mg时影响铁的测定,钼大于0.2%会使铁的测定结果偏高,铬有色离子含量高时影响铁的还原和滴定终点的辨别[7]。上述干扰离子可以通过分离或加掩蔽剂的办法加以消除。在本样品中,上述元素含量极低均小于0.005%,不干扰铁的测定。
2.4 杂质元素测定条件的选择
2.4.1 酸介质对各组分测定的影响
由于不同酸介质会使发射强度发生改变,在处理样品时,一般采用黏度、密度及表面张力小,雾化效率高的盐酸、硝酸。考察盐酸对杂质元素测定的影响,按1.3.4.1配制标准系列溶液,并控制HCl介质浓度为4%(V/V),与未加HCl介质的标准溶液系列的各组分比较。按照试验条件测定标准中各组分质量浓度,6次测定结果均值见表3。

表3 盐酸介质的影响 %
从表3可以看出,4%(V/V)的HCl介质测定结果与理论值一致,且处理样品效果好,故选择4%(V/V)的HCl介质。
2.4.2 分析谱线
元素分析线是根据元素谱线特征、元素间的干扰情况及该仪器对元素的检测灵敏度来确定的[6]。选择无光谱干扰,能够合理扣除光谱背景,待测元素含量低时,选择分析线背景比较大的灵敏线。在选定仪器工作条件下,对混合标准溶液中各元素的常用谱线进行扫描,根据仪器显示的各元素的谱线、背景轮廓、峰的强度值,对应的校准曲线的线性拟合值,选择各元素的分析谱线表4 。2.4.3 基体干扰的考察

表4 元素分析线及背景校正
钙铁线的主要成分为钙和铁,占比分别为30%、70%。它们的存在可能会对杂质元素的测定产生一定的干扰,需要进一步考察。
首先,配制不同浓度Ca、Fe标准溶液,分别加入Al、Cr、P、Ti、Si、Mn元素标准溶液,使Al、Cr、P、Ti、Si、Mn浓度分别为0.20%、0.008 0%、0.050%、0.008 0%、0.080%、0.080%,按试验方法测定各元素含量,平行操作6次,结果见表5 。
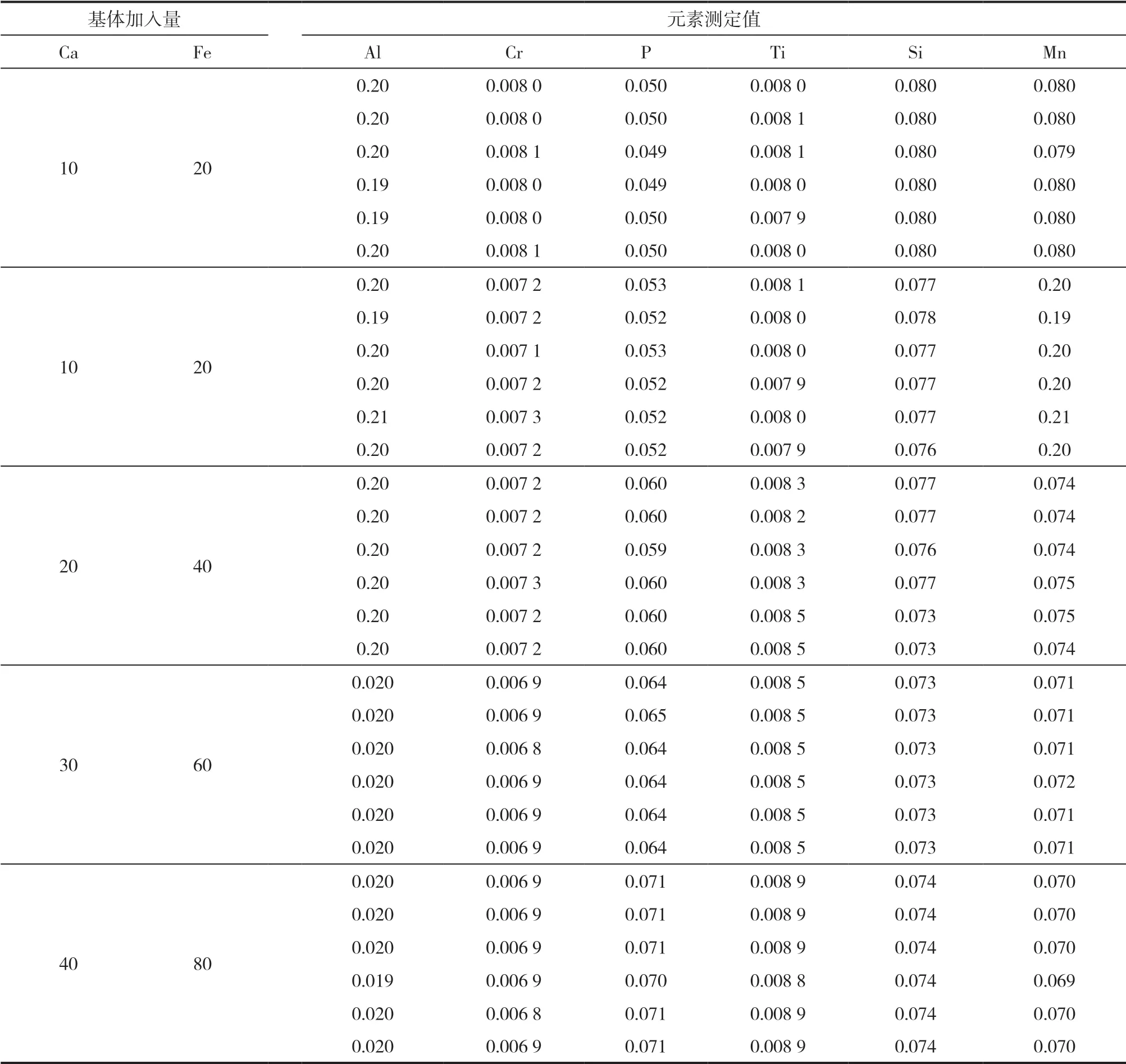
表5 基体元素的影响 %
从表5可以看出,基体对Al测定结果基本没有影响,随着基体含量的增加,P、Ti测得值逐渐升高, Cr、Si、Mn测定结果偏低。
2.4.4 校准曲线及检出限
在选择的仪器条件下,测定标准系列溶液各元素的谱线强度,以待测元素的质量浓度(γ)为横坐标,发射谱线强度(Ⅰ)为纵坐标,绘制校准曲线。对空白溶液连续测定10次,以测定结果标准偏差(SD)的3倍计算各元素的检出限(LOD),以测定结果标准偏差(SD)的10倍计算各元素的定量限。校准曲线的线性回归方程、相关系数、检出限及定量限见表6。
2.5 样品分析
按照试验方法,对附属公司送检的编号为190601、200302两个钙铁包芯线样品平行测定10次,同时对杂质元素进行加标回收试验,结果见表7 。
从表7可以看出,测定结果的相对标准偏差(RSD)为0.6%~3.7%,加标回收率为92%~109%。

表6 标准曲线的线性方程、相关系数、检出限和测定下限
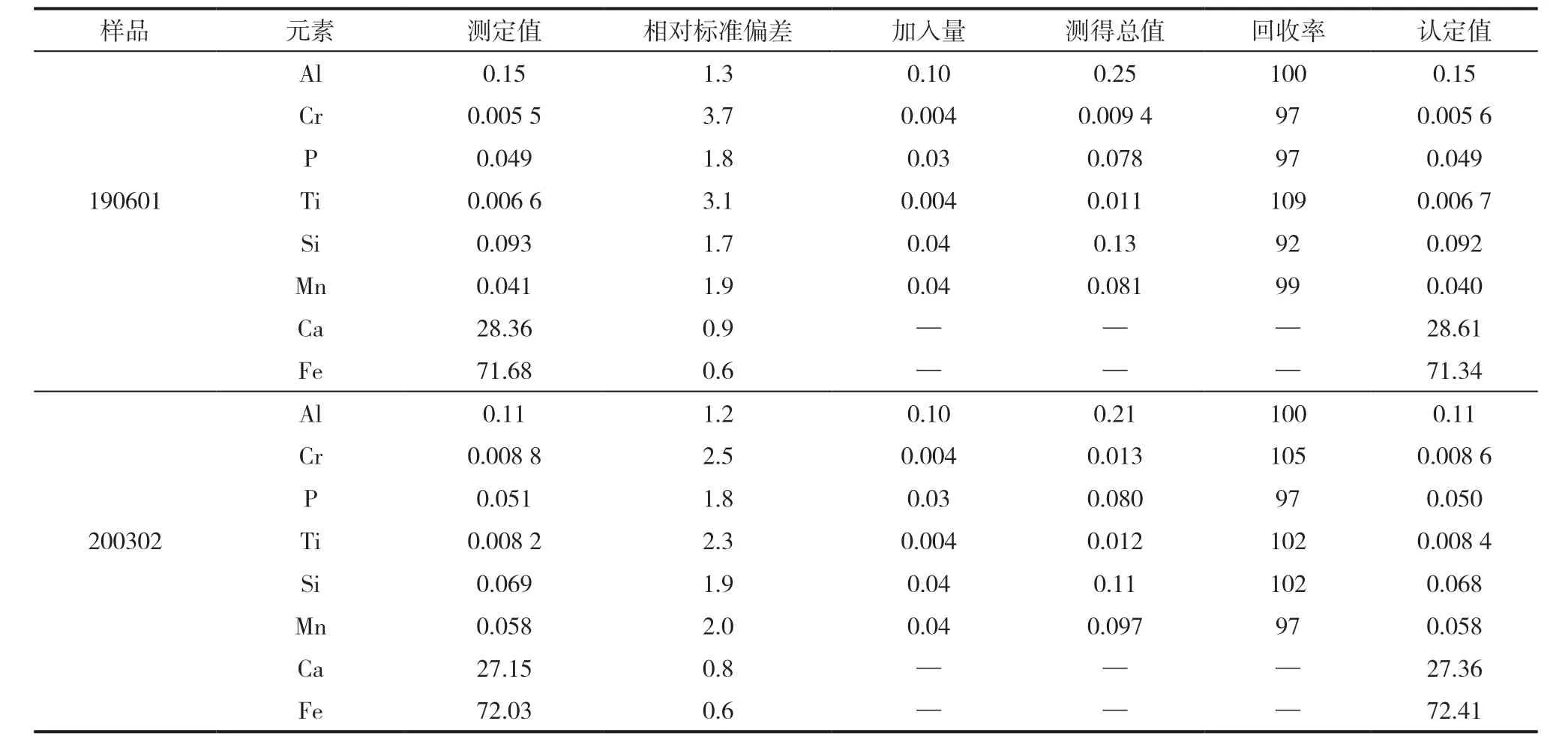
表7 钙铁包芯线样品测定结果 %
3 结论
通过对炼钢用钙铁包芯线主元素及杂质元素测定方法的分析研究,制定了炼钢用钙铁包芯线主元素及杂质元素测定方法,方法准确稳定、分析精度高。填补了公司钙铁包芯线主元素及杂质元素指标检测的空白,拓展了检测领域,提升了质量检测水平。
