重铬酸钾及相关化学性质的实验探究
2017-09-06张金恒黄都莫宇妃
张金恒+黄都+莫宇妃

关键词:重铬酸钾;平衡移动;酸碱性;化学性质;实验探究
文章编号:1005–6629(2017)7–0067–04 中图分类号:G633.8 文献标识码:B
重铬酸钾作为一类常见的化学物质,中学教材并无对其性质做过多表述(表1)。近几年作为特定情境呈现的重铬酸盐已成为各类教辅、模拟考试、高考试题的载体(表2),情境类型参考赵雪老师分类[1]。不少中学教师对重铬酸盐的性质了解不深,此外也并无更多文献对其性质做系统的讲述。现以重铬酸钾为例,对其相关的化学性质做一系统探究,以期中学教师能对这一在高考中频繁出现的物质有较好的理解。以能力测验为主的高考,不断呈现出陌生物质为情境的趋势,学生在掌握基础知识的同时,需要陌生情境刺激以掌握学习方法。
实验仪器:量筒、试管、胶头滴管、电子天平
实验试剂:0.1mol/L重铬酸钾溶液、稀硫酸溶液、氢氧化钠溶液
1.1 实验步骤、现象
用电子天平称取7.20g重铬酸钾,用容量瓶配制成0.1mol/L的溶液250mL。于一支試管中加入4mL 0.1mol/L重铬酸钾溶液,先后加入氢氧化钠溶液、稀硫酸,观察实验现象,记录如表3所示。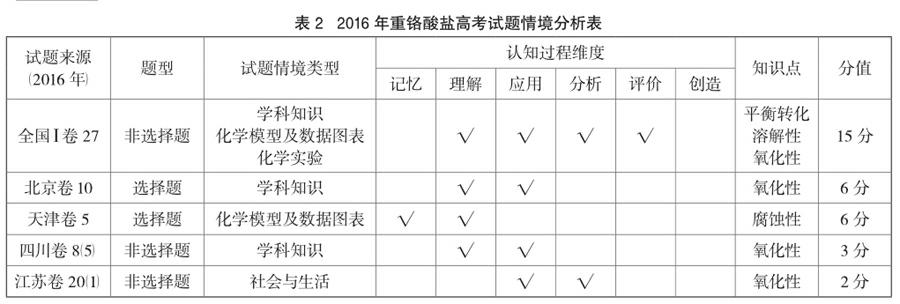

与人教版选修4《化学反应原理》第26页教材实验相比,本实验采用一支试管,通过两次改变条件,溶液颜色恢复,说明平衡发生移动。
2 稳定性
南照东等通过对重铬酸钾晶体低温热容的直接精密量热测定,表明在100~390K温区内,该化合物结构稳定,无相变或其他热异常现象发生,在白热温度下分解放出氧气[2]。重铬酸钾溶液非常稳定,可以长期保存和使用,0.017mol/L的重铬酸钾溶液保存24年后浓度无显著变化[3]。因此,重铬酸钾性质稳定,实验室常用于配制标准溶液。
3 氧化性
人教版教材在选修5《有机化学基础》第52页简单提到重铬酸钾在酸性条件是一种氧化剂,在碱性条件下是否具有氧化性?在不同条件下其氧化能力是否有差异?我们设计如下实验进行探究。
实验仪器:剪刀、电子天平、镊子、量筒、药匙、烧杯、试管、胶头滴管
实验试剂:0.1mol/L重铬酸钾溶液、硫酸、氢氧化钠溶液、乙醇溶液、乙醛溶液、橡胶、聚乙烯、蔗糖、麦芽糖、苯酚、甲苯、硫酸亚铁、碘化钾溶液、过氧化氢溶液、硫化钠溶液、氯化钠溶液、盐酸、硫、活性炭、铜粉、铁粉、锌粉
3.1 实验步骤、现象
取100mL 0.1mol/L重铬酸钾溶液于2个不同烧杯中,分别滴加硫酸、氢氧化钠溶液,取酸化、碱化的重铬酸钾溶液4mL于不同试管中,滴加表4、表5中液体;再称取0.40g物质(橡胶、聚乙烯为块状,蔗糖、麦芽糖、苯酚为颗粒状,硫、活性炭、铜粉、铁粉、锌粉为粉末状)放入不同试管中,再分别滴加酸化、碱化的重铬酸钾溶液4mL,观察实验现象,记录如表4、表5所示。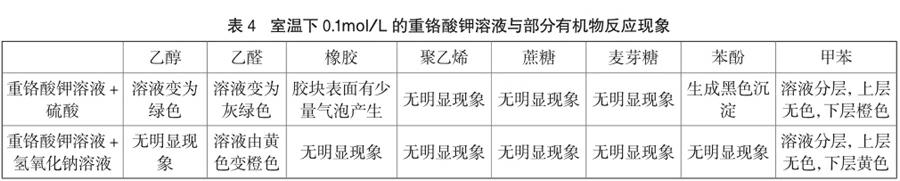

3.2 实验结论
4 腐蚀性
重铬酸钾和高锰酸钾性质相似,高锰酸钾具有腐蚀性,重铬酸钾是否具有腐蚀性呢?我们设计如下实验进行探究。
实验仪器:剪刀、电子天平、镊子、量筒、药匙、试管、胶头滴管
实验试剂:0.1mol/L重铬酸钾溶液、铝粉、锌粉、铁粉、铜粉、活性炭、硫、棉花、橡胶、聚乙烯、猪皮
4.1 实验步骤、现象
用剪刀把棉花、橡胶、聚乙烯塑料袋、猪皮剪成细小块,然后称取表6中样品0.40g放入不同试管中,再依次滴加配制好的0.1mol/L重铬酸钾溶液4mL于各试管中,并观察实验现象,记录如表6所示。
4.2 实验结论
从表6中可以得出,室温条件下0.1mol/L重铬酸钾溶液与金属单质无明显反应现象,表明0.1mol/L重铬酸钾溶液对金属单质无化学腐蚀作用;与非金属单质硫不反应,而与活性炭反应剧烈;对有机物而言,重铬酸钾与棉花、聚乙烯都无明显现象,而与橡胶、猪皮有反应现象,证明重铬酸钾溶液对橡胶、皮肤组织具有腐蚀性,因此在实验中因避免重铬酸钾溶液与皮肤接触,对于重铬酸钾溶液的保存不能使用橡胶塞。
5 重铬酸盐、铬酸盐的溶解性及沉淀转化实验
重铬酸钾(K2Cr2O7)为橙红色单斜晶系或三斜晶系结晶,稍溶于冷水,水溶液呈弱酸性,易溶于热水[5]。基于实验1存在的化学平衡,同为六价铬的重铬酸盐、铬酸盐溶解性是否有差异?我们设计如下实验进行探究。
实验仪器:量筒、试管、胶头滴管
实验试剂:0.1mol/L重铬酸钾溶液、稀盐酸、稀硫酸、稀硝酸、氢氧化钠溶液、氯化钡溶液、氯化钙溶液、氯化钠溶液、氯化铵溶液、氯化钾溶液、硝酸银溶液
5.1 实验步骤、现象
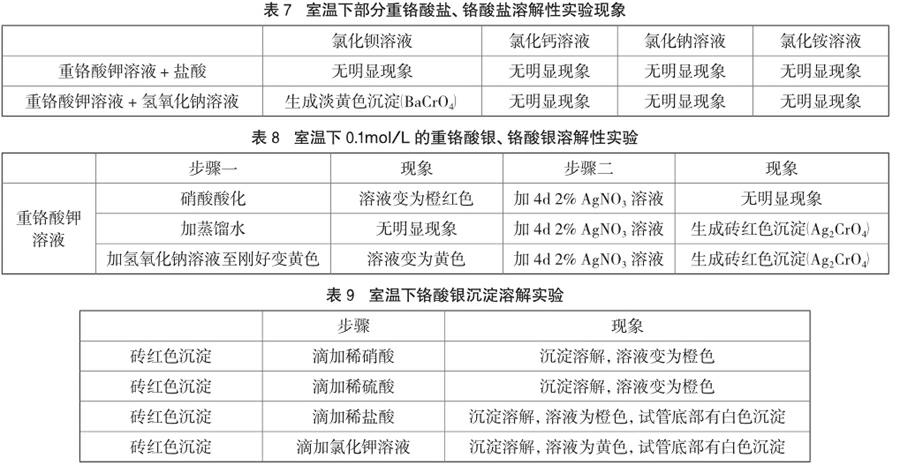
取0.1mol/L的重铬酸钾溶液20mL,加盐酸酸化(避免硫酸酸化,硫酸根的影响),分别取4mL于4支试管中;再取实验3中碱化的重铬酸钾溶液,分别取4mL于4支试管中。分别滴加氯化钡溶液、氯化钙溶液、氯化钠溶液、氯化铵溶液,观察实验现象,记录如表7。再分别取0.1mol/L的重铬酸钾溶液4mL于3支不同试管中,按照表8进行实验,观察记录实验现象。
将表8中生成的砖红色沉淀,均分成4份,分别滴加稀硝酸、稀硫酸、稀盐酸、氯化钾溶液,观察实验现象,并记录于表9。
5.2 实验结论

参考文献:
[1][8]赵雪.高考山东卷化学试题情境创设的统计与研究[J].化学教学,2016,(8):82~86.
[2]南照东,谭志诚,孙立贤.重铬酸钾晶体低温热容及热力学性质的研究[J].物理化学学报,2002,18(10):947~951.
[3][6][7]和玲,高敏,李银环.无机与分析化学(第二版)[M].西安:交通大学出版社,2013:193,422.
[4]武汉大学主编.分析化学(上册)(第五版)[M].北京:高等教育出版社,2006:244.
[5] http://kns.cnki.net/kns/brief/default_result.aspx.
[9]陈新华.化学高考深度复习的策略研究——有感于2016年全国卷理综化学试题答题情况[J].化学教学,2017,(1):83~86.