经腹膜外途径腹腔镜根治性膀胱切除Bricker术的初步体会
2021-07-30熊丙建陶光晶谢蛟魁
熊丙建,陶光晶,余 义,谢蛟魁,王 晓,江 铎
(安康市中心医院泌尿外科,陕西安康 725000)
膀胱癌是泌尿外科最常见的恶性肿瘤。对肌层浸润性膀胱癌(muscle invasive bladder cancer,MIBC)而言,根治性膀胱全切术(radical cystectomy,RC)是治疗的金标准[1]。RC同时行盆腔淋巴结清扫(pelvic lymph node dissection,PLND)是MIBC的标准治疗方式。其中RC包括3类术式:开放膀胱癌根治术(open radical cystectomy,ORC)、腹腔镜膀胱癌根治术(laparoscopic radical cystectomy,LRC)以及机器人辅助腹腔镜膀胱癌根治术(robot-assisted radical cystectomy,RARC)[2]。传统的根治性膀胱切除术通常采用经腹腔入路切除膀胱,随着微创技术的不断发展,LRC在许多大型临床医疗中心已经逐步代替传统的ORC,但经腹膜外途径腹腔镜膀胱根治性切除术(extraperitoneal laparoscopic radical cystectomy,ELRC)报道较少。安康市中心医院从2020年3月至2020年12月,共开展6例ELRC+ Bricker术,疗效满意,现报告如下。
1 资料与方法
1.1 患者的一般资料纳入研究的6例患者于2020年3—12月入院,均为男性,年龄65~84岁,平均(72.5±8.2)岁。主要临床表现为肉眼血尿,病史1个月至3年,首次就诊者2例,经尿道膀胱肿瘤电切术(transurethral resection of bladder tumor,TURBT)术后复发者4例(表1)。全部患者术前行腹部计算机断层扫描(computed tomography,CT)、胸片、膀胱镜检查明确诊断及了解盆腔有无淋巴结转移及远处转移。术前肿瘤活检病理提示为浸润性高级别尿路上皮癌。6例患者术前检查均无明显手术禁忌证,拟行ELRC+Bricker术。
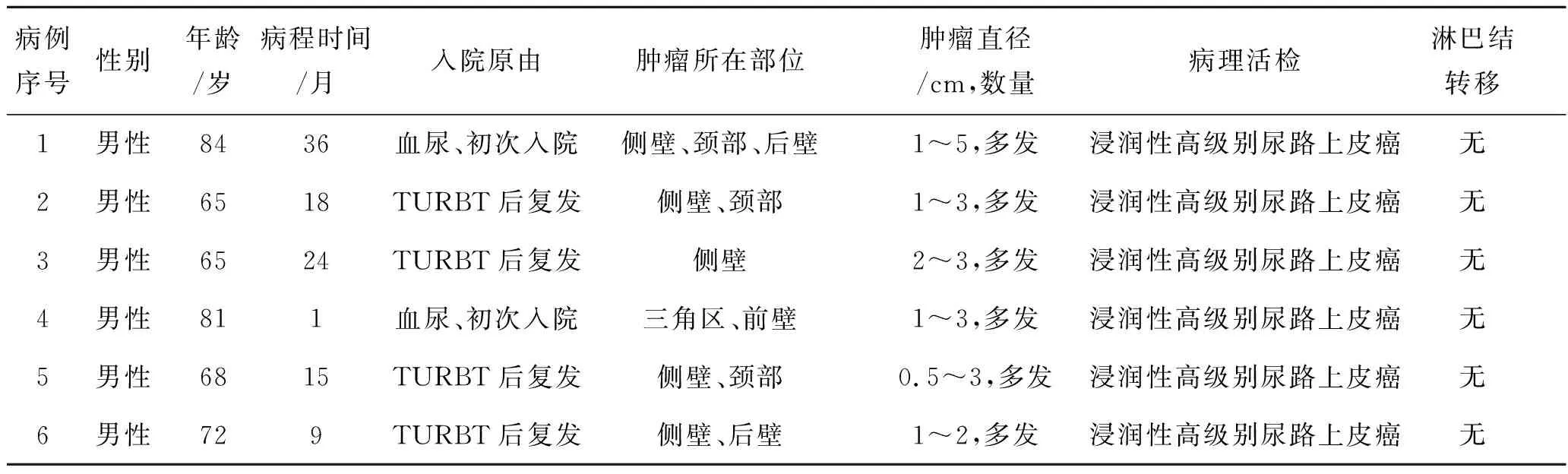
表1 患者的一般资料
TURBT:经尿道膀胱肿瘤电切术。
1.2 手术方法
1.2.1建立腹膜外腔隙 气管插管全身麻醉,臀部垫高5~10 cm,倾斜约20°。采用5孔法:脐下取2 cm长切口,逐层切开皮肤、皮下及腹直肌前鞘,在腹直肌后弓状线以下分离腹腔外间隙,置入自制气囊,充气800~1 000 mL,维持压力5 min,建立气腹。插入10 mm Trocar并放置腹腔镜,在屏幕直视下置入其他4个Trocar:第2、3穿刺点分别在左、右腹直肌旁平脐水平下2 cm处,置入10 mm Trocar;第4、5穿刺点分别在左、右骼前上棘内上方2 cm处,置入5 mm Trocar。气腹压力维持在1.734~1.867 kPa(13~14 mmHg)。
1.2.2腹膜外途径膀胱切除 分离粘连组织后进入耻骨后腹膜外间隙(图1A),先于右侧内环口附近找到精索并结扎切断,将腹膜推向头侧及左侧。于右侧髂外动脉起始部找到右侧输尿管并向下游离至膀胱,暂不切断。清扫右侧盆腔淋巴结(图1B),分别切除髂内、髂外动、静脉及闭孔神经周围的脂肪、淋巴组织,装入手指套内置于右髂窝处。同法清扫左侧盆腔淋巴结(图1C)。夹闭导尿管,生理盐水约200 mL充盈膀胱,找到膀胱与腹膜返折交界处,将腹膜与膀胱顶壁、后壁游离(图1D)。在Denon-villiers筋膜表面暴露精囊并切断双侧输精管,以精囊为标志向膀胱两侧游离,分别用Hem-O-lock结扎并切断膀胱侧韧带。切开前列腺两侧盆内筋膜(图1E),切断耻骨前列腺韧带,解剖出阴茎背深静脉复合体,2-0可吸收线缝扎(图1F)。靠近膀胱结扎并离断双侧输尿管,超声刀于背深静脉复合体结扎线近端切开前列腺前筋膜,解剖出尿道,用Hem-O-lock夹闭后切断。提起前列腺尖部,沿前列腺与直肠前间隙逆行游离至精囊,翻转前列腺,结扎离断前列腺韧带,完整切除膀胱及前列腺,装入标本袋移出术区。检查创面并彻底止血。
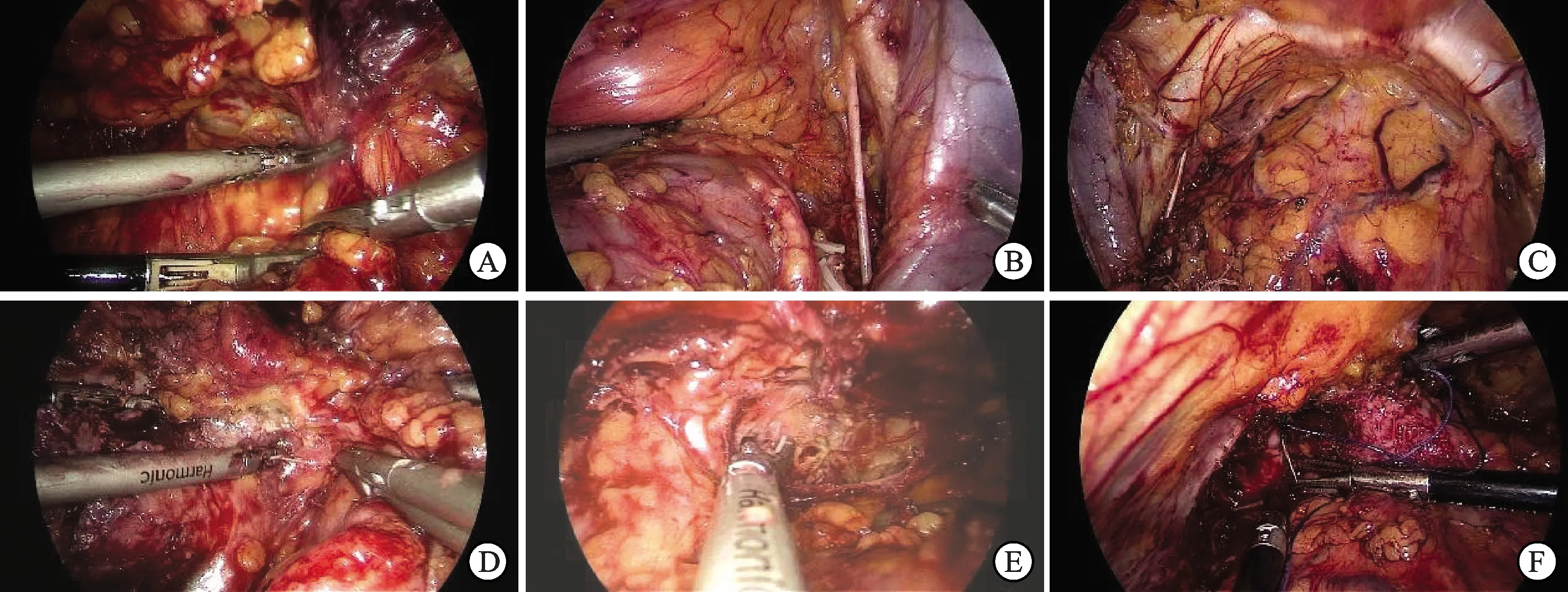
A:游离耻骨后腹膜外间隙;B:清扫右侧盆腔淋巴结;C:清扫左侧盆腔淋巴结;D:分离膀胱后壁与腹膜交界处层面,并沿此层面继续向后方游离并寻找精囊、输精管;E:切开盆内筋膜;F:缝扎阴茎背深静脉复合体。
1.2.3尿流改道 6例均行Bricker回肠膀胱术。延长正中切口约5 cm,取出标本袋。开放双侧输尿管断端并插入单J管引流尿液。切开腹膜,提出末段回肠,切除阑尾并包埋阑尾残端。距回盲部约15 cm处截取长15~20 cm回肠段,注意保护肠系膜动脉弓,于回肠段上方连续缝合回肠断端恢复肠道连续性。封闭回肠段近端,将输尿管断端与回肠段近端吻合,扩大右侧腹直肌旁Trocar孔,回肠段远端从孔内拖出,翻转回肠断端腹壁造口,固定单J管及回肠引流管。还纳回肠入腹腔,关闭肠系膜切口,缝合腹膜与肠系膜缘,将回肠段完全置于腹膜外。分层缝合腹壁切口,回肠造口贴造口袋。
1.3术中观察指标及术后随访 术中观察手术时间、出血量(测量吸引器中吸出的量)、肠功能恢复时间等指标,术后电话随访(每月1次)并返院行胸、腹、盆腔CT影像学检查及血常规等生化检查(第1年每3月1次,以后每半年1次)。
2 结 果
6例手术均成功,无中转开放手术。腹腔镜切除膀胱手术时间150~210 min,平均(174.0±23.0)min。术中出血量150~600 mL,平均(300.0±176.2)mL,术后肠功能恢复时间2~3 d,平均(2.2±0.5)d。术后病理肿瘤浸润深肌层4例(T2b),浸润膀胱外组织2例(T3a),切缘及淋巴结病理检查为阴性。所有患者已随访3~12个月,未见肿瘤局部复发、穿刺通道及远处转移,目前仍在进一步随访中。
3 讨 论
膀胱癌在男性全身恶性肿瘤中列第4位,在女性中列第11位[3]。据中国癌症统计数据显示,我国膀胱癌的发病率在全身肿瘤中列第12位,死亡率列第13位[4]。RC联合PLND已成为治疗MIBC的标准治疗术式,RC联合Bricker术又是最经典、并发症最少的术式。LRC开展以来,随着手术设备的不断发展和微创技术的提高,已被越来越多的泌尿外科医师采用。尽管LRC手术难度大、操作更为复杂,但创伤较小、术后恢复快、有较好的安全性和疗效,在我国已有逐步取代ORC术式的趋势[5]。目前对前列腺癌、膀胱癌根治性切除等复杂的盆腔手术,国内一流医疗中心已首选机器人辅助腹腔镜前列腺根治术(robot-assisted radical prostatectomy,RARP)及RARC。但机器人辅助系统设备昂贵,故LRC仍是目前国内主要医疗机构开展最多的术式,其中以TLRC为主流术式。近几年开始有ELRC的报道[5~8]。FENG等[6]认为腹腔镜经腹膜外入路比经腹腔入路能更好地改善围手术期结果,ZHAO等[9]发现经腹膜外ORC入路比TLRC患者肠功能恢复更快。大量的ELRP也证实建立腹膜外耻骨后间隙是安全可行的[10-11]。JENTZMIK等[12]对95例患者进行了对比研究,结果发现经腹膜外入路的肠梗阻发生率明显低于经腹腔入路,两组的肿瘤控制情况、手术时间、术中失血量等差异无统计学意义。魏强等[7]认为经腹膜外入路的优势是能更大程度地降低对腹内脏器的干扰,减少肿瘤腹腔种植转移的风险,保证腹腔内环境的稳定,减轻手术创面渗出及潜在漏尿对消化道的影响,术后恢复快,因此经腹膜外入路是安全和可行的。但因手术操作需要足够的腹膜外空间完成,腹型肥胖者不适宜行ELRC;另外,体型瘦小的人腹膜比较薄容易破损,术中容易出现皮下气肿,也不宜选择ELRC入路。
ELRC、TLRC两者手术过程类似,区别在于ELRC保留了完整的腹膜。ELRC优点:①手术期间无肠管干扰,更便于显露手术区域特别是分离膀胱后壁、精囊等优势明显,发生肠管损伤的可能性明显降低;②截取回肠段完全隔离于腹膜外,即使术后出现吻合口漏,尿液亦不会污染腹腔;③无需将左侧输尿管从乙状结肠后方移位于右侧;④创面产生的炎性物质对腹腔影响小,术后肠功能恢复时间短;⑤腹腔内炎症反应轻,术后肠粘连、肠梗阻发生率低。ELRC缺点:①手术空间相对狭小,解剖标志辨识度不高;②手术暴露难度更大,寻找输尿管、清扫盆腔淋巴结受到一定限制;③如果腹膜破损,气体进入腹腔,操作空间将进一步缩小;④寻找腹膜返折与膀胱顶部层面比较困难,容易误入膀胱肌层或切开腹膜。我们的经验是,在分离膀胱顶部时,经导尿管注入生理盐水200 mL充盈膀胱,寻找腹膜返折与膀胱顶部交界区相对容易。一旦找到正确层面后,分离到膀胱后壁时,与腹膜层面比较容易分离,同时因气腹压力作用,腹膜向头侧及后方推移,无肠管干扰,寻找精囊、输精管、结扎膀胱侧韧带更轻松。我们将输尿管保留在离断尿道前才结扎切断,好处在于将输尿管阻断时间降至最短,对肾功能影响降至最低。虽然在处理膀胱侧韧带时暴露难度有所增加,但影响甚微。
完成输尿管下段游离,常规进行盆腔淋巴结清扫(pelvic lymph node dissection,PLND)。研究表明膀胱癌淋巴转移最常出现的位置为闭孔、髂内淋巴结,其次髂外淋巴结,而骶前淋巴结和下腔静脉旁淋巴结转移少见。无法承受较大清扫范围的老年人,评估淋巴结阳性风险较低者,可行局限性淋巴结清扫[13-14]。在手术难度、手术并发症不增加的基础上,清扫淋巴结数量应根据预后最佳的手术方案进行[15]。因腹膜外操作空间相对较小,标准淋巴结清扫难度较大,我们对年龄>70岁、一般情况欠佳的患者仅行区域淋巴结清扫;年龄<70岁、一般情况较好者,在膀胱切除后行补充淋巴结清扫,但淋巴结数量少于标准淋巴结清扫,与FENG等[6]报道一致。如果空间狭小、显露不佳时,也可将清扫盆腔淋巴结放在膀胱切除之后进行。相信随着手术量增加、手术配合默契度的提高,清扫淋巴结数量会逐步接近标准淋巴结清扫。
腹腔镜手术阶段完成后,开放行Bricker术。还纳肠管入腹腔后,将腹膜缘与回肠段肠系膜缝合关闭腹腔,将回肠段完全置于腹膜外。避免了输尿管、回肠段对腹腔的干扰,降低了术后腹腔并发症的发生。
纳入研究的6例患者均手术成功,与2019年1月—2020年12月由同一术者施行的18例TLRC+Bricker术相比,在手术时间、术中出血量指标两组差异无统计学意义,但在术后肠功能恢复、腹腔并发症方面存在一定优势(P=0.004),与其他经腹或腹膜外途径LRC学者报道基本一致[5-9]。经腹膜外途径完整保留了腹膜,减少了对肠道的干扰及损伤,肠功能恢复快,有效降低了经腹腔途径可能引起的术后肠粘连、肠梗阻等并发症,有利于患者术后更快康复,符合目前微创手术及快速康复外科的理念。根据初期的手术经验和短期随访结果,ELRC+Bricker术在临床上安全可行。但手术病例数尚少,手术后随访时间较短,还需要积累更多的临床病例对其安全性进行全面评估。随着技术熟练程度的提高、手术团队配合默契度增强以及经验的不断积累,术中出血量将会进一步减少、手术时间将进一步缩短,让膀胱癌患者从ELRC中有更多获益。
