开放生化检测系统校准限值的设置与应用*
2021-07-29王志伟梅艳芳毛东英蔡永梅
王志伟,梅艳芳,毛东英,蔡永梅
宁夏医科大学总医院医学实验中心,宁夏银川 750004
全自动生化分析仪通过测定水空白和校准品吸光度,并根据给定的赋值(FV)计算校准因子(CF)、拟合校准曲线,计算样本中待测物浓度,同时监控校准过程和检测系统,如:检测试剂质量[1-2]、校准品(包括水空白)质量[3]及仪器工作状态[1]等。然而,开放生化检测系统使用第三方试剂和(或)校准品,校准监控相关参数设定一般采用系统默认的最大或最小值,但不能对校准过程进行监控,当出现试剂污染、水空白污染、校准品污染、试剂过期、校准品过期、试剂准备不当[1]、校准品准备不当、试剂加注异常(如气泡)、仪器工作欠佳等异常情况时[4],会通过校准引入系统误差,存在潜在质量风险[5]。因此,在进行开放生化检测系统参数设置时,有必要根据所使用第三方试剂的特点[6-7]和具体情况对校准相关参数进行必要配置[5-8]和优化,实现对开放生化检测系统的监控。本文探讨西门子ADVIA系列全自动生化分析仪组成开放系统时检测项目校准限值的设定方法及应用,其他制造商全自动生化分析仪组成开放检测系统时也应当根据仪器、试剂的特点对校准限值进行必要的设置。
1 材料与方法
1.1材料 常规生化二氧化碳(CO2)、肌酐(Cr)、尿素(UREA)、尿酸(UA)、葡萄糖(GLU)、钙(Ca)、无机磷(P)、铁(Fe)、不饱和(血清)铁结合能力(UIBC)、总胆固醇(CHOL)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、镁( Mg)、总蛋白(TP)、清蛋白(ALB)、天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、碱性磷酸酶(ALP)、γ-谷氨酰转移酶(GGT)、胆碱酯酶(CHE)、肌酸激酶(CK)、α-淀粉酶(AMY)、总胆红素(TBIL)、直接胆红素(DBIL)、乳酸脱氢酶(LDH)、α-羟丁酸脱氢酶(α-HBDH)、总胆汁酸(TBA)、腺苷脱氨酶(ADA)、α-L-岩藻糖苷酸(AFU)检测试剂及多项校准品,由北京利德曼生化股份有限公司提供;本实验室2018年7月至2019年6月上述项目校准结果; Microsoft Excel 2007和IBM SPSS Statistics19.0;西门子ADVIA 2400全自动生化分析仪。
1.2方法
1.2.1获取试剂空白初始限值 以去离子水为样本,测定30项常规生化项目20次,读取试剂空白(RB)吸光度,计算RB最大允许绝对偏差(Max Rep Deviation)、最大值(Max RB)和最小值(Min RB)。Max RB Deviation暂设为与Max Rep Deviation相同。
1.2.2获取校准品初始限值 以复合校准品为样本,测定30项常规生化项目20次,读取标准品吸光度值,计算最大允许绝对偏差(Max Rep Deviation),最大值和最小值,并根据标准品对应ADVIA 2400赋值FV计算校准因子CF最大值(Max CF),最小值(Min CF)和最大允许绝对偏差(Max CF Deviation)。
1.2.3校准限值的修正与优化 统计2018年7月至2019年6月30项常规生化项目校准结果,计算试剂空白吸光度值、校准品吸光度值及校准因子的均值和标准差,剔除离群值后计算RB和CF的最大值、最小值及最大允许绝对偏差,对所有项目Max RB、Min RB、Max RB Deviation,Max CF、Min CF、Max CF Deviation进行修正,并计算CF值的最大允许相对偏差。
1.2.4相同项目不同仪器校准差异 26个项目在两台ADVIA 2400上检测,将两台仪器各项目12个月校准结果试剂空白吸光度RB、校准品吸光度ABS-RB和CF值分组,先进行双样本方差齐性的F检验,然后进行双样本等方差假设的t检验或双样本异方差假设的t检验。
1.3统计学处理 所有数据均用Microsoft Excel 2007和IBM SPSS Statistics19.0进行统计分析,以P<0.05为差异有统计学意义。
2 结 果
西门子ADVIA 2400全自动生化分析仪和利德曼试剂组成的开放系统校准限值,见表1。MAX REP DEVIATION用于批内精密度监控,校准时水空白或校准品重复2次[4](或以上)测定吸光度绝对偏差大于限值时,校准不通过[4],试剂空白或校准精密度检查失败。MAX RB DEVIATION和MAX CF DEVIATION用于批间精密度监控,系统计算最近的3次校准的RB和CF均值,当本次校准RB或CF绝对偏差大于限值时,校准不通过(类似于即刻法室内质控),试剂空白或校准追踪检查失败。MAX RB、MIN RB、 MAX CF、MIN CF分别控制校准过程中RB和CF的最大值和最小值同,超过限值校准失败。项目校准时,系统按照表1所示的限值进行水空白和标准品吸光度精密度检查,并确保RB和CF值在允许的范围内变化,同时保证RB和CF值与近3次校准测定均值保持良好的离散度。由表1 可见,30个项目中,CF值的最大允许相对偏差最小为2.12%,最大为30.60%,除TBA为30.60%外,29项小于18.00%、27项小于15.00%、10项小于5.00%。
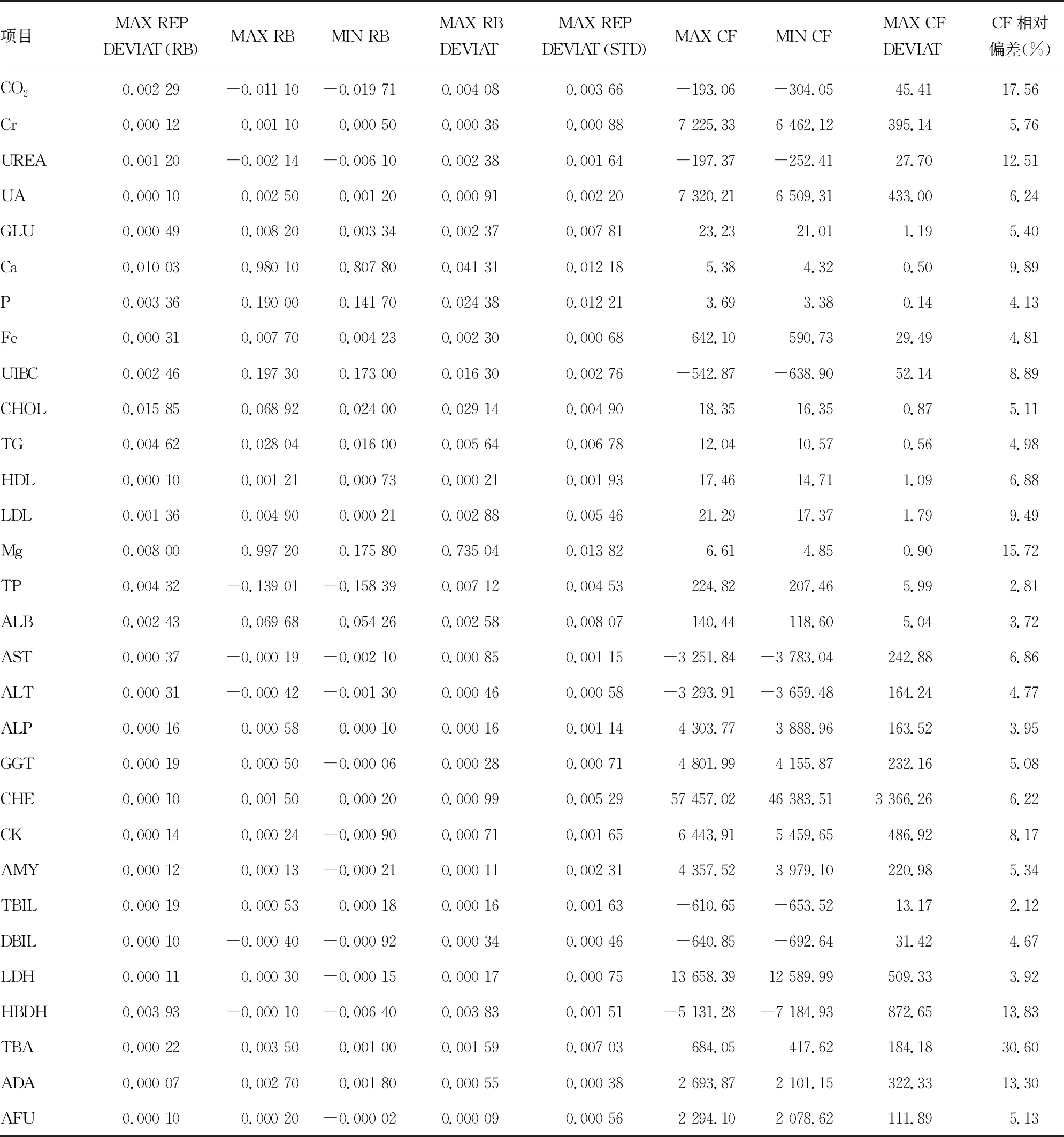
表1 ADVIA 2400使用利德曼生化试剂校准限值参数
两台ADVIA 2400 26个项目校准结果t检验如表2所示:试剂空白吸光度19个项目P值小于0.05占总数的73.00%;校准品吸光度21个项目P值小于0.05,占总数的81.00%;校准因子22个项目P值小于0.05,占总数的85.00%。两台仪器间校准结果差异有统计学意义(P<0.05)。

表2 同一项目不同仪器校准RB、ABS-RB、CF值t检验结果

续表2 同一项目不同仪器校准RB、ABS-RB、CF值t检验结果
3 讨 论
开放生化检测系统分析参数一般由试剂制造商工程技术人员负责设置,涉及不同仪器制造商、不同类型仪器及同一制造商不同规格型号的仪器,这些工程技术人员不可能做到面面俱到,往往只设置一些基本参数,诸如校准限值这类高级参数,要设计很多实验,操作非常繁琐,所以都不予以设置[9-10],均采用系统默认(最大或最小)值,导致检测系统存在潜在质量风险。
全自动生化检测系统的“自动化”不仅仅体现在高通量、快速检测上,还体现在对整个分析检测过程的自动监控上。设置开放生化检测系统校准限值,可实现对检测项目校准过程的监控,减少由校准引入的系统误差,进而监测整个分析检测系统,杜绝试剂[10]、校准品质量问题或仪器工作状态欠佳影响检测质量。不同检测项目校准限值存在差异,如表1所示,在进行校准限值设定时,应当根据所使用的试剂和分析仪器的特点设计实验方案,进行个性化设置[6]、优化。同一项目不同仪器测定时,校准结果也存在差异[11-12],如表2所示,在进行校准限值设定时应予以兼顾。试剂和/或校准品开瓶时间增加[13]、更换批号时[3,14],表征校准批间变异的限值Max RB、Min RB、Max RB Deviation、Max CF、Min CF、Max CF Deviation会在合理的区间变动,因此,根据一段时间(如12个月)的校准数据统计分析结果对这类限值进行优化、修正十分必要。如有必要,所设限值在后续使用过程中需做进一步动态调整,以便更好地兼容这种正常变化。速率法中,RB为去离子水与试剂反应时吸光度每分钟的变化率[3,12],因此,速率法校准限值设定还需考察试剂空白主波长吸光度值是否在允许范围内,如ADVIA 2400速率法还需正确设置BLANK(U)和BLANK(d)[15-16]。
许多临床实验室都认识到开放生化检测系统校准限值设定的重要性和必要性,但在进行设定时所有项目采用统一的限值,如CF相对偏差均设为±10.00%或±20.00%[4-5],这种方式不能反映如表1所示项目间的差异,存在一定的局限性。只有不同项目个性化地设置校准限值,才能灵敏地反馈检测系统(试剂、标准品、检测仪器)的异常变化。不同制造商生产的试剂亦存在差异[6,17],应当设计实验方案,在实验数据基础上设置校准限值。不同型号仪器乃至同一仪器的不同模块存在差异[11-12],也应当设置不同校准限值:同等条件下,由于不同仪器吸光度本底存在差异,如表2所示,即使同一型号仪器测得的试剂空白,校准品吸光度和校准因子均存在差异。因此,同一型号仪器可设置不同限值,设置相同校准限值时应当兼容仪器间的差异。由此可见,使用原装试剂的配套生化检测系统由制造商统一设置的校准限值也可以根据用户的实际情况进一步优化,以便对检测系统进行更有效的监控。
校准是实验室质量保证的首要环节,设置校准限值是实现监测校准过程和整个开放生化检测系统的必要手段,应当能够灵敏地反映试剂、校准品和检测仪器的异常变化,限值参数不宜设置过宽,否则达不到监控的目的;也不宜设置过严,导致校准不易通过,给正常工作带来不必要的困扰。校准限值需在使用过程中不断修正、优化、完善,实现对生化分析检测系统的有效监控,保证检测质量。
