中药复方861合剂对小鼠急性肝损伤的保护作用研究
2021-07-29赵小梅赵奎君马致洁
李 红,赵小梅,赵奎君,马致洁
(首都医科大学附属北京友谊医院中药剂科,北京 100050)
急性和慢性肝脏疾病是临床上的常见病、多发病,严重危害着人类健康。现有药物受疗效及不良反应等因素的影响,临床应用受到一定程度的限制,因此,寻找高效低毒的肝损伤治疗药物一直是新药研究领域的热点之一[1]。中药复方861合剂是首都医科大学附属北京友谊医院(以下简称“我院”)王宝恩教授根据中医药理论及多年临床经验总结开发的中药复方制剂(医疗机构制剂,批准文号:京药制字Z20063091),主要由黄芪、丹参等10味中药组成,主要功能为活性化瘀、益气健脾,具有保肝降酶、增强机体免疫功能等功效,在临床上被用于慢性肝纤维化和早期肝硬化的治疗,效果显著。10多年的临床应用结果亦表明,中药复方861合剂能有效改善肝病患者的症状、体征及肝功能[2-3]。为了进一步提供保肝降酶的临床用药依据,本实验分别采用四氯化碳(CCl4)和D-半乳糖胺(D-GalN)制备小鼠急性肝损伤模型[4],观察中药复方861合剂对小鼠肝损伤的保护作用,并通过小鼠急性毒性模型,了解中药复方861合剂的主要中毒症状及死亡情况,为中药复方861合剂的进一步深入研究和临床用药提供实验依据。
1 材料与方法
1.1 仪器
BS-224型生化分析测定仪(北京生化仪器厂);DG5030型酶联免疫检测仪(华东电子管厂)。
1.2 药品与试剂
中药复方861合剂(自制,由首都医科大学附属北京友谊医院药剂科按照原处方工艺制备,水煎液经浓缩制成每毫升含1 g生药的提取液)[3];联苯双酯(北京协和药厂,批准文号为国药准字H11020980);CCl4和D-GalN(中国人民解放军防化学院提供);丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)测定试剂盒(北京北化康泰临床试剂有限公司)。
1.3 实验动物
昆明种小鼠,体重18~20 g,雌雄各半,由军事医学科学院动物中心提供。动物饲养条件:按照清洁动物标准饲养;合格证号:军医动字第B98006。
1.4 方法
1.4.1 动物分组、给药及CCl4诱导小鼠急性肝损伤:取健康小鼠60只,体重(18±2) g,随机分为六组,即正常对照组、CCl4模型组(0.02 ml/kg)、阳性对照组(联苯双酯0.029 g/kg,联苯双酯是治疗肝损伤引起氨基转氨酶升高的常用药物,其保肝降酶作用效果明显,且毒性低副作用小,已有大量相关文献选用其作为阳性药[5-7])以及中药复方861合剂低、中及高剂量组(1.5、3及6 g/kg),每组10只。小鼠均每日灌胃给药2次,对照组及模型组小鼠给予相同容积的蒸馏水,连续给药7次后,除正常对照组外,各组小鼠腹腔注射0.1% CCl40.2 ml/10 g[8-9]。造模后40 h,于小鼠眶静脉采血,常规离心分离血清,按试剂盒操作说明检测ALT、AST水平,并迅速取肝组织,进行苏木精-伊红(hematoxylin and eosin,HE)染色。
1.4.2 动物分组、给药及D-GalN诱导小鼠急性肝损伤:取健康小鼠60只,体重(18±2) g,随机分为六组,即正常对照组、D-GalN模型组(0.8 g/kg)、阳性对照组(联苯双酯 0.029 g/kg)以及中药复方861合剂低、中及高剂量组(1.5、3及6 g/kg),每组10只。小鼠每日灌胃给药2次,对照组及模型组小鼠给予相同容积的蒸馏水,给药7次后,除正常对照组外,各组小鼠腹腔注射D-GalN 0.2 ml/10 g[10]。造模后20 h,于小鼠眶静脉采血,常规离心分离血清,按试剂盒操作说明检测ALT、AST水平,并迅速取肝组织,进行HE染色。
1.4.3 动物分组、给药及急性毒性实验:取健康小鼠40只,体重(18±2) g,雌雄各半,禁食12 h,按预实验结果,一次性以最大给药容量(1.0 ml/20 g)和最大给药浓度(1.2 g/ml)灌胃给药,剂量60 g/kg,记录14 d内小鼠各种中毒症状及死亡情况,对死亡动物进行尸检,分别在给药前、给药后第1、3、7及14日称量动物体重[11-12]。
1.5 统计学方法
所有实验数据均采用SPSS 11.0软件统计分析,组间均数差异采用单因素方差分析,P<0.05为差异有统计学意义,P<0.01为差异有极显著统计学意义。
2 结果
2.1 中药复方861合剂对CCl4致肝损伤小鼠血清ALT、AST及组织病理的影响
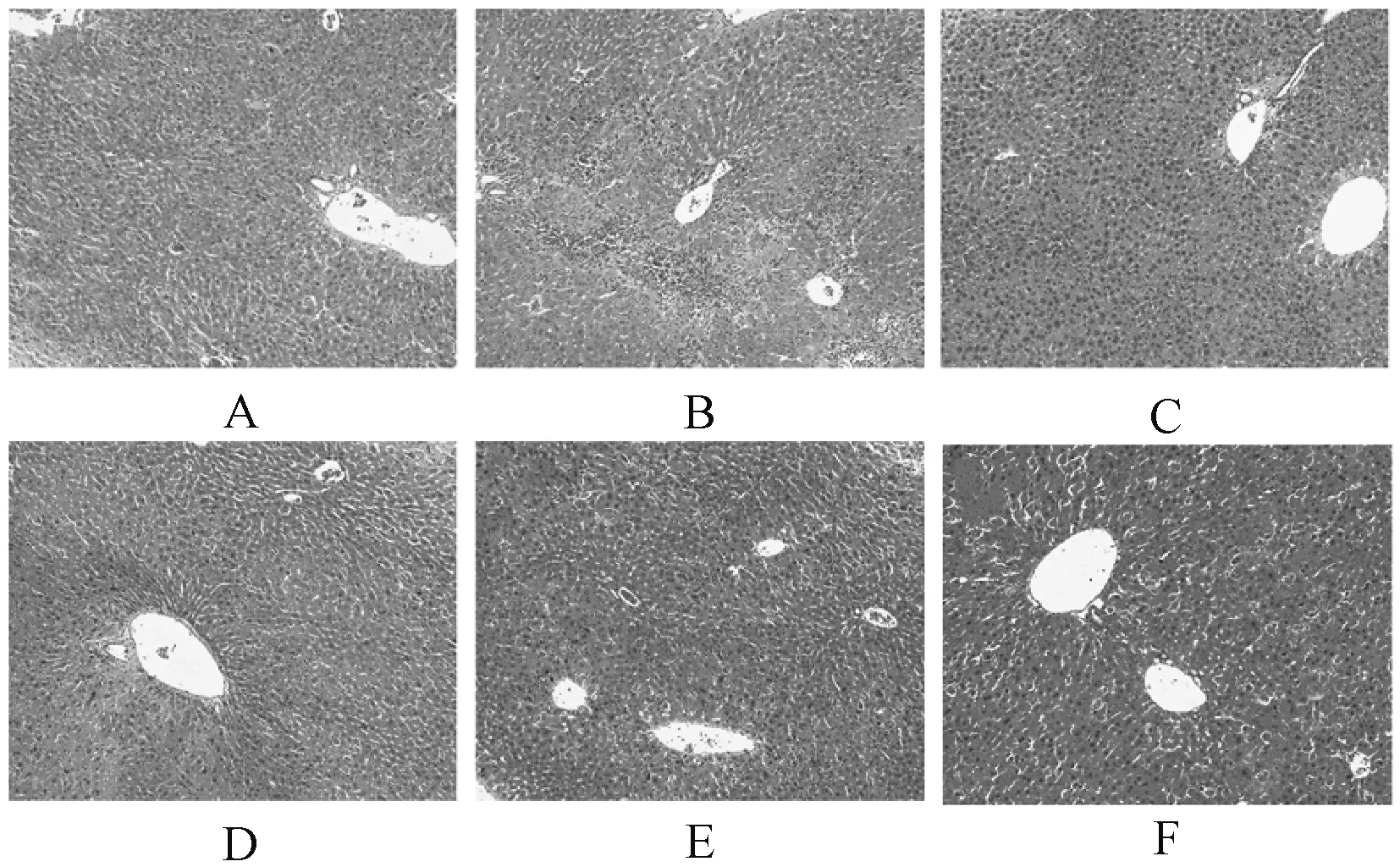
各给药组小鼠的血清ALT、AST水平均低于模型组;中药复方861合剂低、中及高剂量组小鼠血清ALT、AST水平与模型组的差异有统计学意义(P<0.05),说明中药复方861合剂对CCl4所致小鼠急性肝损伤具有明显的治疗作用,见表1。正常对照组小鼠肝小叶结构正常,肝细胞排列紧密,无小叶和汇管区炎症;模型组小鼠肝细胞可见明显脂肪样变,胞质疏松,胞浆内可见明显气球样病变,有的肝细胞核变形,被挤压偏向细胞周边,肝细胞呈灶状、桥状坏死,汇管区胆管增厚,可见密集的淋巴细胞及单核细胞浸润;阳性对照组小鼠肝组织排列紧密,无明显脂肪样变,有少量炎症细胞浸润;中药复方861合剂低剂量组小鼠部分肝细胞坏死,有少量炎症细胞浸润;中药复方861合剂中剂量组小鼠肝小叶未见明显脂肪样病变,肝细胞呈条索状分布,边缘清晰;中药复方861合剂高剂量组小鼠未见明显脂肪样变,汇管区可见炎症细胞浸润,见图1。
表1 中药复方861合剂对CCl4致急性肝损伤小鼠血清ALT、AST水平的影响Tab 1 Effects of herbal compound 861 on serum ALT and AST levels in mice with acute liver injury induced by
2.2 中药复方861合剂对D-GalN致肝损伤小鼠血清ALT、AST及组织病理的影响
各给药组小鼠的血清ALT、AST水平明显低于模型组;中药复方861合剂中、高剂量组与模型组小鼠血清ALT、AST水平与模型组的差异有统计学意义(P<0.05),说明中药复方861合剂对D-GalN所致小鼠急性肝损伤具有一定的治疗作用,见表2。正常对照组小鼠肝小叶结构正常,肝细胞排列紧密,无小叶和汇管区炎症;模型组小鼠肝细胞可见明显红细胞侵润,有的肝细胞核变形,被挤压偏向细胞周边,可见密集的淋巴细胞及单核细胞浸润;阳性对照组小鼠肝组织排列紧密,无明显脂肪样变,有少量炎症细胞浸润;中药复方861合剂低剂量组小鼠有少量炎症细胞浸润;中药复方861合剂中剂量组小鼠肝小叶未见明显脂肪样病变,边缘清晰;中药复方861合剂高剂量组小鼠肝细胞排列紧密,无小叶和汇管区炎症,见图2。
表2 中药复方861合剂对D-GalN致小鼠急性肝损伤的影响Tab 2 Effect of herbal compound 861 on liver histomathology of acute liver injury in mice induced by D-GalN

A.正常对照组;B.CCl4模型组;C.阳性对照组(0.029 g/kg);D.中药复方861合剂低剂量组(1.5 g/kg);E.中药复方861合剂中剂量组(3 g/kg);F.中药复方861合剂高剂量组(6 g/kg)A. normal control group; B. CCl4 model group; C. positive control group(0.029 g/kg); D. low-dose group of herbal compound 861(1.5 g/kg); E. medium-dose group of herbal compound 861(3 g/kg); F. high-dose group of herbal compound 861(6 g/kg)图1 中药复方861合剂对CCl4致急性肝损伤小鼠肝组织病理的影响(HE染色×200)Fig 1 Effect of herbal compound 861 on liver histomathology of acute liver injury in mice induced by CCl4(HE staining ×200)
2.3 急性毒性小鼠死亡及体重变化情况
小鼠急性毒性实验结果显示,小鼠无死亡,行为、活动如常,在以后的观察期内体重增长正常,未见明显异常症状,见表3。

表3 小鼠急性毒性实验的死亡情况和体重变化情况Tab 3 Death and body weight changes in acute toxicity test of mice
3 讨论
CCl4诱导小鼠急性肝损伤模型是目前研究保肝药物药效及作用机制最经典的模型,该模型指标明确、重复性好,能准确反映肝细胞功能、代谢及形态变化[13-14]。本实验采用CCl4诱导小鼠急性肝损伤经典模型研究中药复方861合剂对肝脏的保护作用,结果显示,经CCl4处理后,与正常对照组比较,模型组小鼠血清ALT和AST水平显著升高,差异均有统计学意义(P<0. 01);病理切片显示,肝细胞受损严重,表明模型建立成功。相比CCl4模型组,中药复方861合剂各剂量组小鼠的血清ALT和AST水平显著降低,差异均有统计学意义(P<0.05或P<0.01);病理切片显示,肝组织炎症病变程度明显减轻,且呈一定的剂量依赖性,提示中药复方861合剂对CCl4引起的急性肝损伤具有明显的保护作用。
A.正常对照组;B.D-GalN模型组;C.阳性对照组(0.029 g/kg);D.中药复方861合剂低剂量组(1.5 g/kg);E.中药复方861合剂中剂量组(3 g/kg);F.中药复方861合剂高剂量组(6 g/kg)A. normal control group; B. D-GalN model group; C. positive control group(0.029 g/kg); D. low-dose group of herbal compound 861(1.5 g/kg); E. medium-dose group of herbal compound 861(3 g/kg); F. high-dose group of herbal compound 861(6 g/kg)图2 中药复方861合剂对D-GalN致急性肝损伤小鼠肝组织病理的影响(HE染色×200)Fig 2 Effect of herbal compound 861 on liver histomathology of acute liver injury in mice induced by D-GalN(HE staining ×200)
D-GalN是肝细胞磷酸尿嘧啶核苷干扰剂,可造成肝弥漫性坏死和炎症[15]。D-GalN模型是目前公认较成熟的研究肝炎发病机制以及验证药物疗效的动物模型[16];且GalN诱发的动物肝组织损伤在形态学和功能学上与人类急性重症肝炎相似[17]。因此,D-GalN急性肝损伤模型是研究抗病毒性肝炎药物的理想模型[18]。本实验采用该模型确证中药复方861合剂对急性肝损伤小鼠的保护作用,结果显示,经D-GalN处理后,与正常对照组比较,模型组小鼠的血清ALT和AST水平显著升高,差异均有统计学意义(P<0.01);病理切片显示,肝细胞受损严重,表明模型建立成功。相比CCl4模型组,中药复方861合剂各剂量组小鼠的血清ALT和AST水平显著降低,差异均有统计学意义(P<0.05或P<0.01);病理切片显示,肝组织炎症病变程度明显减轻,且呈一定的剂量依赖性,提示中药复方861合剂对D-GalN引起的急性肝损伤具有明显的保护作用,但其保肝作用可能还与其他环节相关,具体作用机制需进一步深入研究。
本研究在考察中药复方861合剂对小鼠急性肝损伤的前提下,以最大给药容量和最大给药浓度考察了其对小鼠的急性毒性。小鼠给药剂量为60 g/kg(折合约400生药g/kg),约为临床上人日剂量的100倍,观察该剂量下小鼠14 d内的中毒状况,结果显示,观察期内未见小鼠死亡,亦未表现出明显中毒症状,且在观察期后继续观察动物的行为活动及体重增长状况,均未见异常现象,该结果明确了中药复方861合剂的安全性,为临床安全用药提供了有力的实验数据支持[19-20]。
