子宫内膜癌根治术联合腹腔热灌注化疗治疗子宫内膜癌的疗效及预后分析
2021-07-29杨佩贤黄少雅陈秋霞
杨佩贤 黄少雅 陈秋霞
子宫内膜癌是常见的女性生殖系统恶性肿瘤,多数患者可早期发现,可通过手术联合术后化疗进行治疗[1-2]。子宫内膜癌根治术只能清除肉眼可见的病灶组织,对于微小及游离于盆腹腔内部的癌细胞无法全部清除,故术后辅助化疗,最大程度杀死手术残留病灶及游离癌细胞,是保障患者术后生存时间的重要手段[3]。传统静脉化疗药物浓度低,临床应用效果不佳[4]。而腹腔热灌注化疗(Hyperthermic intraperitoneal chemotherapy,HIPEC)将化疗与热疗有效结合,通过将药物直接作用于腹腔,并进行腹腔加热,有效提高药物局部浓度与药物渗透率,优化静脉化疗疗效[5]。但目前,关于子宫内膜癌根治术后联合HIPEC治疗的相关报道较少,基于以上背景,我院开展如下研究。
1 资料与方法
1.1 一般资料
①纳入标准:患者符合开腹手术适应症,行扩大全子宫+双附件切除+盆腔淋巴结清扫术;术前临床分期为Ⅲ期~Ⅳ期;术后病理检查证实为子宫内膜癌。②排除标准:排除合并其他严重内科疾病者;合并其他恶性肿瘤者;手术或化疗禁忌症者。③病例资料:将医院2018年1月—2020年12月间收治的60例行子宫内膜根治术患者纳为研究对象,其均符合上述纳入及排除标准,根据患者术后辅助治疗意愿,将其分为观察组(行HIPEC治疗,n=33)与对照组(未行HIPEC治疗,n=27),两组一般资料无显著性差异(P>0.05),见表1。

表1 两组一般资料比较
1.2 方法
1.2.1 子宫内膜癌根治术 医护人员进行常规术前检查,术中采用气管插管全麻,麻醉后,患者取平卧位。消毒辅巾后,留置导尿管,取下腹正中行纵切口。逐层进腹,检查子宫大小、形态,按照常规步骤切除子宫双附件、盆腔或(和)腹主动脉旁淋巴结。
1.2.2 术后辅助治疗 根据患者意愿,采用不同的术后辅助治疗方式,其中观察组行腹腔灌注化疗,对照组行常规静脉化疗。
观察组患者术后即刻、第三天及第五天,使用BR-TRG-I型体腔热灌注治疗系统进行持续循环热灌注,将化疗药物(60 mg顺铂)混合NaCl注射液3 000 mL加入腹腔热灌注化疗袋,预热至43 ℃,灌注速度500 mL/min,分别连接盆腹腔及腹腔热灌注进出管,关闭出水管,开启治疗仪,调节水量,腹腔内液体量:1 500~2 500 mL,灌注1 h后,液体保留1 000 mL,化疗结束4 h后,将液体排出。连续进行3次腹腔热灌注后,将下腹引流管拔出。每次腹腔热灌注化疗后,行血常规、肝肾功能及电解质检查,评估有无骨髓抑制或肝肾功能损坏,同时给予持续心电监护、吸氧、抑酸、护胃、营养支持等对症支持治疗。第三次腹腔热灌注治疗完毕后第一天加用紫杉醇(135~175/m2)静脉滴注,三周后返院,给予联合TC方案常规全身经脉化疗,21 d为一个疗程,根据患者肿瘤分期,进行4~6个疗程。
对照组患者术后1周开始TC方案静脉化疗,连续化疗6~10个疗程。TC方案:紫杉醇135~175 mg/m2静脉滴注(静滴1次,3 h滴完),卡铂剂量按AUC=5计算,静滴1次化疗,21 d为一个疗程,化疗期间严格监测患者心电图、呼吸、血压、心率等指标,化疗期间进行保肝、护胃等对症支持治疗。
1.3 观察指标
①比较两组患者手术相关指标。②评估两组临床疗效:采用外周血CA125浓度作为晚期子宫内膜癌患者手术联合术后辅助治疗后疗效的判定标准。在两组患者化疗结束4周后测定其血清CA125水平,若患者CA125水平下降至正常水平,且维持时间超过4周,定义为完全缓解(CR),若CA125值下降幅度>治疗前50%,为部分缓解(PR),若CA125下降幅度<治疗前50%或无改变,为病情稳定(SD),若CA125水平升高则定义为进展(PD)。有效率=[(CR+PR)/n]×100%。③比较两组患者化疗毒副反应:化疗毒副反应评估参照美国国家癌症研究所(NCI)相关标准进行。④对患者进行门诊或电话随访,比较两组3年疾病无进展生存时间(PFS),PFS为患者治疗完成后到第一次出现疾病进展或任何原因死亡的时间。将无瘤存活者及失访患者列为删失病例。
1.4 统计学方法
2 结果
2.1 两组手术效果比较
两组手术时间、术中出血量、淋巴结清扫个数及术后并发症均无显著性差异(P>0.05),见表2。

表2 两组手术效果比较
2.2 两组化疗效果比较
观察组化疗有效率显著高于对照组,差异有统计学意义(P<0.05),见表3。

表3 两组化疗效果比较 n(%)
2.3 两组化疗毒副作用比较
两组骨髓抑制、肝功能受损、肾功能受损、周围神经损伤、心血管病变等毒副作用发生情况无显著性差异(P>0.05),观察组肠道反应较对照组严重,差异有统计学意义(P<0.05),见表4。

表4 两组化疗毒副作用比较 (n)
2.4 两组生存分析
观察组随访时间为6~35个月,3年内复发例数11例(局部转移4例,远处转移7例),无瘤存活者18例,失访4例。对照组随访时间6~34个月,3年复发例数17例(局部复发3例,远处转移14例),无瘤存活者5例,失访者5例。绘制生存曲线发现,观察组与对照组PFS差异显著(Rank2=11.681,P<0.05),见图1。
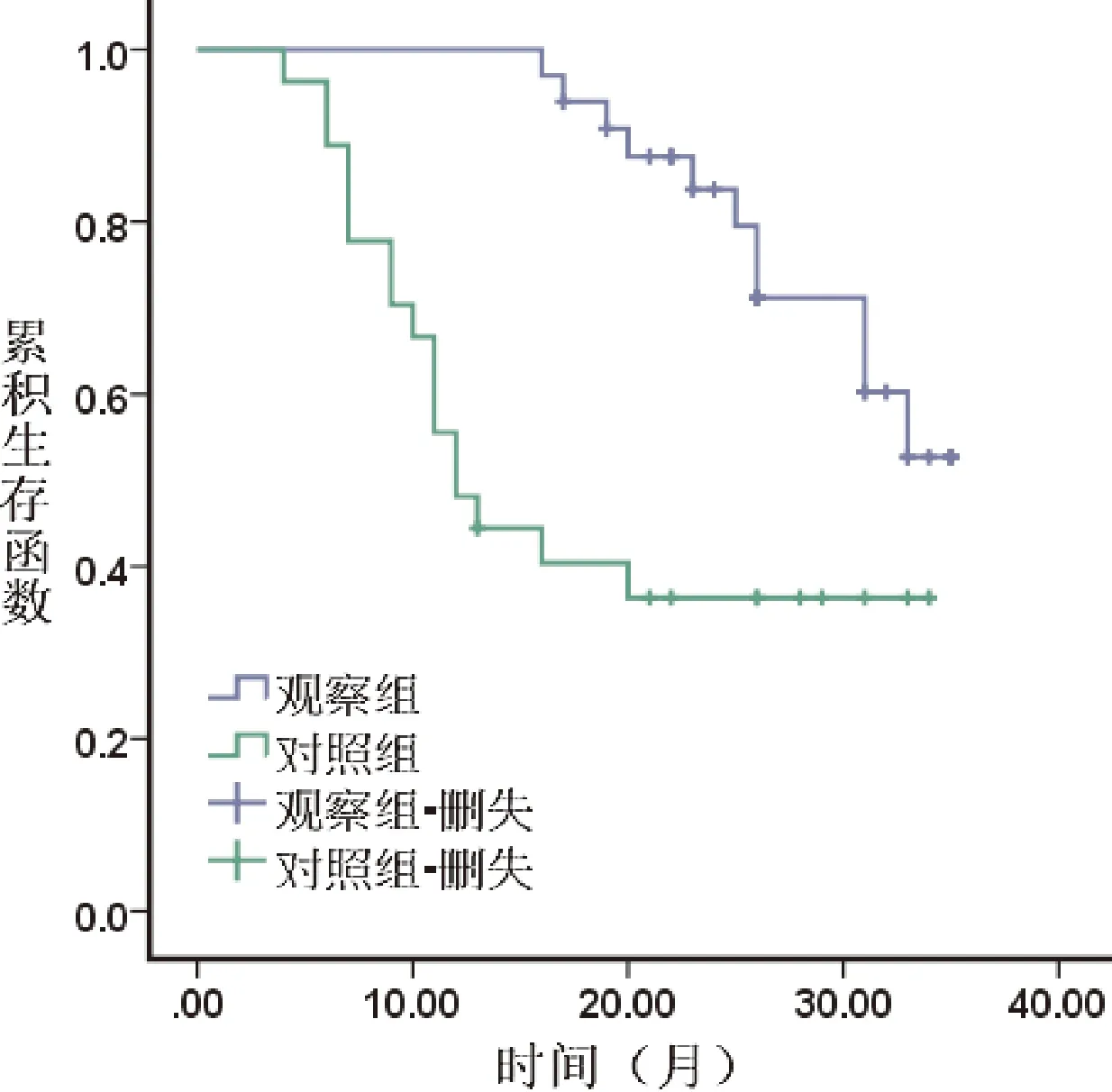
图1 两组疾病无进展生存分析
3 讨论
子宫内膜癌是女性三大恶性肿瘤之一,临床调查显示,子宫内膜癌约占女性生殖道恶性肿瘤的1/5~1/3左右,子宫内膜癌根治术联合术后辅助治疗,是子宫内膜癌的主要治疗方法[6-7]。子宫内膜癌根治术可有效切除病灶清扫淋巴结,防止病灶转移,延长患者生存时间。但手术只能有效切除肉眼可见的病灶与淋巴结,并不能彻底清除微小病灶及腹腔内游离癌细胞,此外,病理分期均集中在Ⅲ~Ⅳ期的晚期子宫内膜癌患者伴有大量腹水,以上因素均可能造成子宫内膜癌复发与转移[8-10]。
在根治术后加以辅助治疗抑制肿瘤转移,是保障患者治疗效果的有效措施。传统的全身静脉化疗不能保障腹腔内药物浓度,有效率低。腹腔灌注化疗(IPC)在常温下将药物直接灌注到腹腔内部,以提高腹腔内化疗药物浓度,使得药物与腹腔残余病灶及游离癌细胞间充分接触,并可保证腔内持久稳定的药物浓度,进而有效杀伤癌细胞,优化手术效果[11]。但IPC可能加重局部肠梗阻,并不能保障药物分布均匀。而将热疗与IPC相结合,可加强化疗药物热动力效应,提高肿瘤消灭效果[12-14]。
本研究将60例行根治术治疗的子宫内膜癌患者分为两组,观察组术后应用HIPEC,而对照组未使用HIPEC。由于CA125是子宫恶性病变的常见肿瘤标志物,血清CA125水平检测简单方便,本研究以患者化疗后血清CA125水平作为疗效评估的参考,结果显示,观察组患者化疗后疗效优于对照组,且疾病无进展中位生存时间更长,提示HIPEC能有效提高子宫内膜癌治疗效果。统计两组化疗毒副反应发现,观察组胃肠道不良反应较对照组有所增加,这可能与腹腔内直接灌注化疗药物,加重了胃肠道刺激有关,但并未出现肠梗阻等严重并发症,且两组骨髓抑制等其他毒副反应无显著性差异,提示HIPEC的安全性。
HIPEC能有效降低子宫内膜癌复发及转移风险,分析其作用机制可能是:肿瘤细胞耐热性较正常细胞差,当化疗药物加热至43 ℃时,对肿瘤细胞的杀伤力加强;且肿瘤细胞对高热敏感,化疗联合热疗能降低癌细胞膜的稳定性,增强药物渗透率,促进癌灶组织对药物的吸收;此外,热疗能促使化疗药物分布均匀,增加药物与腹腔的接触面积[15]。
综上所述,子宫内膜癌根治术联合HIPEC能有效提高子宫内膜癌治疗效果,减少癌灶术后转移,提高患者疾病无进展生存时间。
