基于FAERS数据库的质子泵抑制剂类药物不良事件信号挖掘研究*
2021-07-29白雪霏冉怡雯赵尹瑜赵锦霞陈力
白雪霏,冉怡雯,赵尹瑜,赵锦霞,陈力
(1.四川大学华西第二医院药学部/循证药学中心,成都 610041;2.出生缺陷与相关妇儿疾病教育部重点实验室,成都 610041;3.四川大学华西药学院,成都 610041)
近年来,质子泵抑制剂(proton pump inhibitors,PPIs)在临床中的使用率显著增加且不合理使用率较高[1],在PPIs纳入辅助用药药品目录后,其安全性受到广泛关注[2]。自1980年推出PPIs以来,其使用急剧增加,如今已成为世界上最常用的处方药之一[3]。英国每年分配使用的PPIs接近5900万张处方,且自2007年以来使用总量翻倍[4]。以中国重庆地区最大的教学医院为代表,在2004年至2013年间PPIs利用率提高10.4倍[5]。同时,PPIs过度使用问题也受到了诸多关注。在美国,25%~70%的PPIs处方没有适当的适应证[3,6];在中国45家医院的PPIs处方调查中[7],有32.6%~56.8%的PPIs处方用于未经批准的适应证;在2018年的一项中国上海地区某医院的单中心回顾性分析中[8],18 435例使用PPIs的患者中未经批准的适应证占47%;药物利用指数(DUI)通常用于评估PPIs使用的合理性,当DUI值>1.0表示存在不适当的使用,在该分析中,仅口服埃索美拉唑的DUI值低于1.0,表明PPIs存在滥用的现象。随着PPIs的过度使用,其安全性问题逐步显现,常见的药品不良反应(adverse drug reaction,ADR)与严重不良反应逐渐增多。
美国、欧盟药品监督管理部门先后发布了有关PPIs类药品的安全性信息,警示此类药品的骨折、低镁血症等风险以及与氯吡格雷的药物相互作用,并修订了药品说明书。我国国家药品监督管理局(NMPA)也在此基础上也针对其安全性问题进行分析评估发布了相关的药物警戒信息。如何合理使用PPIs,减少乃至避免PPIs导致的不良反应,是目前临床上应重视的问题。
FDA不良事件报告系统(FDA adverse event reporting system,FAERS)是美国FDA用于收集自发呈报的药物不良事件(adverse drug event,ADE)的数据库,其数据量大、数据信息多样,对公众免费开放,故常用于药品不良事件信号挖掘研究。
本研究基于FAERS系统,旨在对FAERS数据库收集的PPIs的不良事件信息进行分析对比,挖掘其潜在的不良反应信号,以期优化患者治疗方案,为临床安全合理用药提供参考依据。
1 资料与方法
1.1数据来源 本研究数据来源于2004年开始对外公开的FAERS数据库,不良事件数据每季度更新一次,以ASCII或XML形式存储。本研究选择了自2015年第1季度至2020年第4季度共24个季度的数据,包括患者的人口学和行政信息、药物/生物信息、不良事件、患者结果、报告来源、药物治疗的开始和结束日期等内容,将首要怀疑药物引起的ADE共27 335 800个,根据个人信息记录(DEMO)表进行去重处理后,导入MySQL5.7进行分析。
1.2数据筛选 FDA批准的PPIs包括奥美拉唑、兰索拉唑、右兰索拉唑、艾司奥美拉唑、泮托拉唑、雷贝拉唑6种,但由于右兰索拉唑并未在国内上市,本研究不作讨论。以FDA批准药品及不良反应公众数据库(public dashboard)中药品名称为标准,通过MySQL对以上药品的商品名和通用名在“drugname”字段进行模糊匹配,删除重复数据,筛选出首要怀疑药物为PPIs的所有报告:艾司奥美拉唑(“ESOMEPRAZOLE”“NEXIUM” “VIMOVO”),奥美拉唑(“OMEPRAZOLE”“PRILOSEC” “YOSPRALA” “TALICIA”),兰索拉唑(“LANSOPRAZOLE” “PREVACID” “PREVPAC”),雷贝拉唑(“RABEPRAZOLE”“ACIPHEX”),泮托拉唑(“PROTONIX” “PANTOPRAZOLE”)。
1.3数据处理 FAERS不良事件数据采用国际医学科学组织理事会《国际医学用语词典》(Medical Dictionary for Regulatory Activities,MedDRA)中首选语(preferred terms,PT)进行编码[9]。本研究中的ADE采用MedDRA药品不良反应术语集的首选系统器官分类(system organ class,SOC)和首选术语(preferred term,PT)。在MedDRA官方网站(https://www.meddra.org/)下载并运行网站提供的 MedDRA Desktop Browsers,将需要汉化的PT英文名导入,则系统自动输出中英文映射表,本文中SOC和PT的中英文表达均按照该映射表。
1.4数据分析 采用报告比值比法(reporting odds ratio,ROR)和综合标准法(MHRA法)分别计算ROR值、比例报告比值(proportional reporting ratio,PRR)和卡方(χ2),筛选潜在ADE信号,其基于比例失衡法四格表(表1),获取首要怀疑药物的目标ADE报告数及ADE发生的背景数等数据,根据公式(表2)计算ROR和PRR值[10-11]。ROR法中95%CI下限大于1且报告数不少于3例的事件和 MHRA法中 PRR ≥2、χ2≥4且报告数不少于3例的事件定义为ADE信号。所有统计分析采用Microsoft Excel 2016版软件完成。
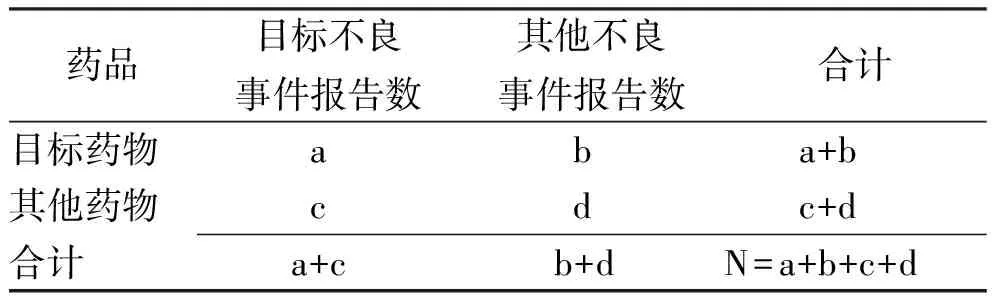
表1 比例失衡法四格表
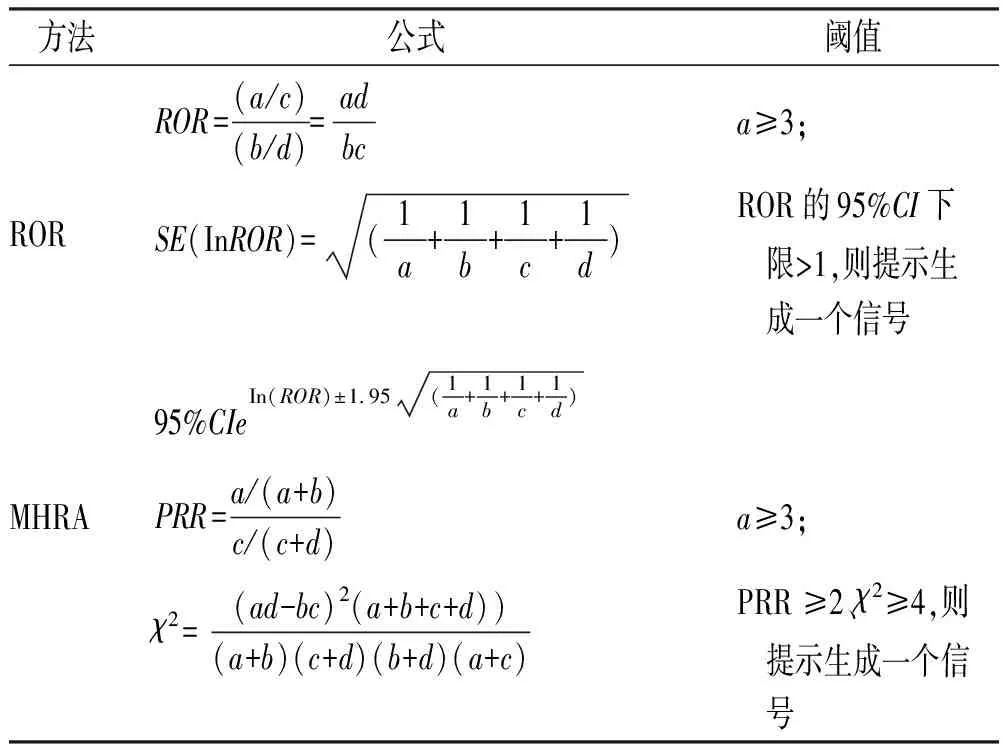
表2 ROR法与MHRA法公式及阈值
2 结果
2.1不良反应报告基本信息 FAERS数据库2015年第1季度至2020年第4季度共24个季度的不良事件数据,在删除重复报告后,共获得“首要怀疑药物”的相关报告2 733.58万例。其中首要怀疑药物为艾司奥美拉唑的ADE共98 563例,报告数45 748份;首要怀疑药物为奥美拉唑的ADE共31 874例,报告数20 822份;首要怀疑药物为兰索拉唑的ADE共64 739例,报告数28 626份;首要怀疑药物为泮托拉唑的ADE共36 155例,报告数22 666份;首要怀疑药物为雷贝拉唑的共1572例,报告数1364份。由于雷贝拉唑数据较少,且分布系统广泛,各系统涉及病例数很少,不具有明显大数据特征,故后续研究中未纳入。上报国家、患者性别与年龄等基本信息见表3。
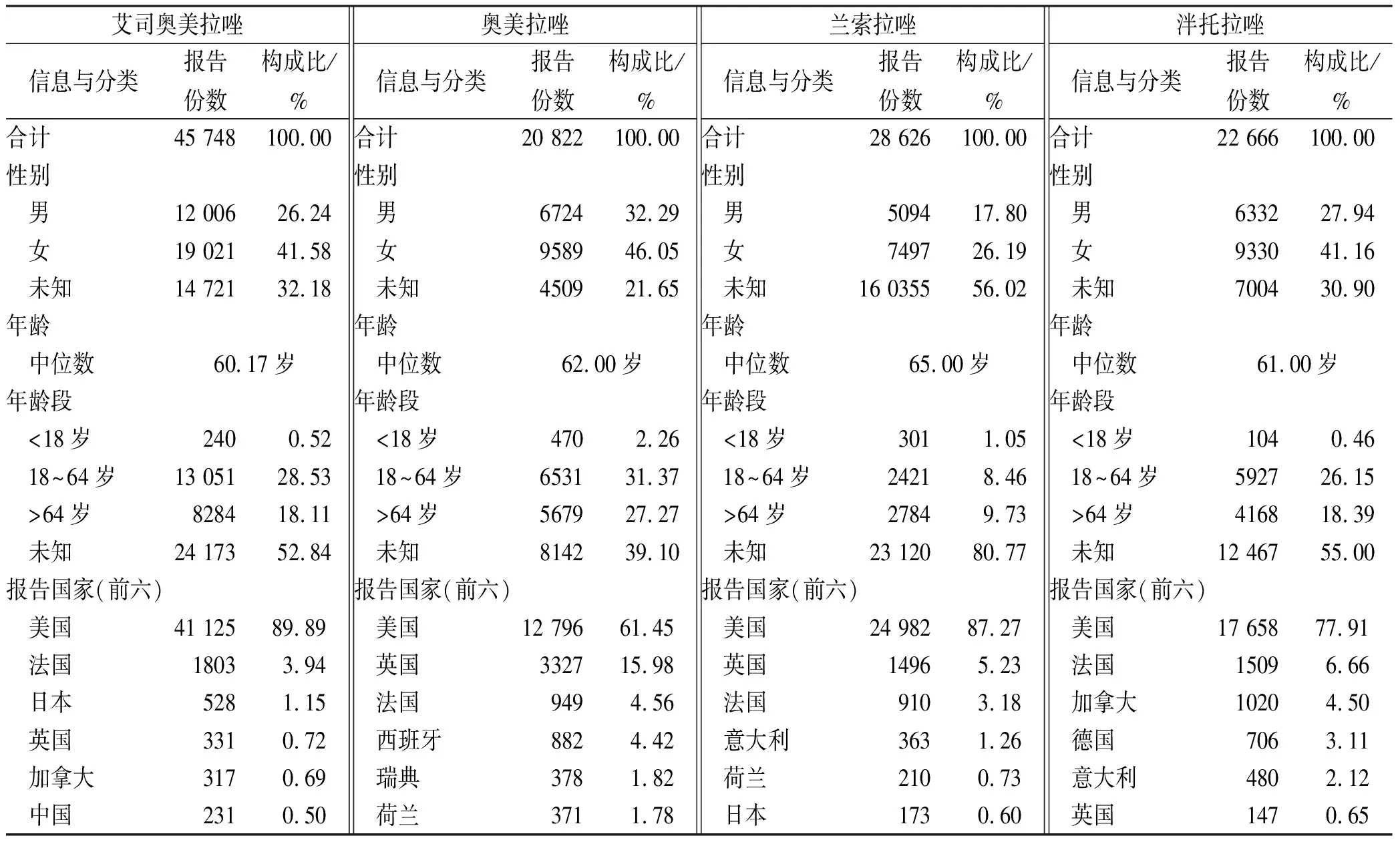
表3 4种PPIs不良事件报告的基本信息
2.2各系统器官分类不良事件报告及信号分类 将4种PPIs二次筛选后的ADE信号进行统计,使用MedDRA系统器官分类(system organ class,SOC)对有信号的PT进行分类,排除产品问题,各类损伤、中毒及操作并发症,各种手术及医疗操作和社会环境等与药物无关的信号,最终获得有效信号PT和累及系统(SOC)。
奥美拉唑是信号数最多的PPIs,累及23个系统,共540种信号;泮托拉唑共累及23个系统,共340种信号;艾司奥美拉唑累及22个系统,共239种信号;兰索拉唑累及22个系统,共298种信号。4种PPIs的ADE均主要累及“肾脏及泌尿系统疾病”( 艾司奥美拉唑:78 082 例、奥美拉唑:16 153例、兰索拉唑:54 008例、泮托拉唑:29 277例)和“胃肠系统疾病”(艾司奥美拉唑:9086 例、奥美拉唑:4303例、兰索拉唑:2097例、泮托拉唑:1947例)。
除此之外,艾司奥美拉唑主要集中于“血液及淋巴系统疾病”(2764例)和“内分泌系统疾病”(1381例),奥美拉唑主要集中于“代谢及营养类疾病”(2134例)和“全身性疾病及给药部位各种反应”(1 635例),兰索拉唑主要集中于“代谢及营养类疾病”(962例)和“全身性疾病及给药部位各种反应”(840例),泮托拉唑主要集中于“代谢及营养类疾病”(948例)和“皮肤及皮下组织类疾病”(561例)。各种PPIs的ADE涉及的系统有一定的差异,在使用过程中如果合并有该系统疾病应当换用其他的在该系统更加安全的药物。见表4,图1。
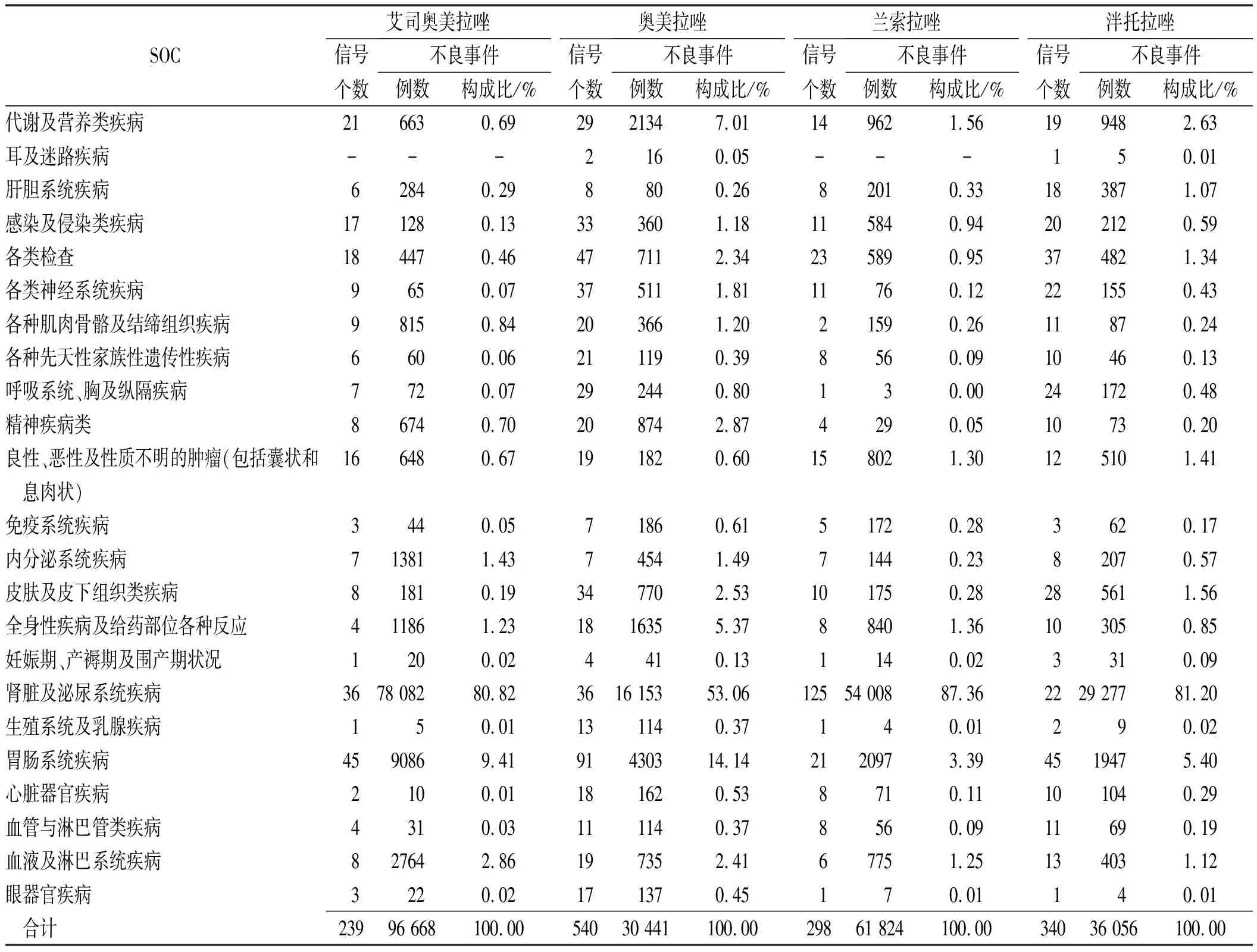
表4 4种PPIs累及系统信号数与不良事件数构成比
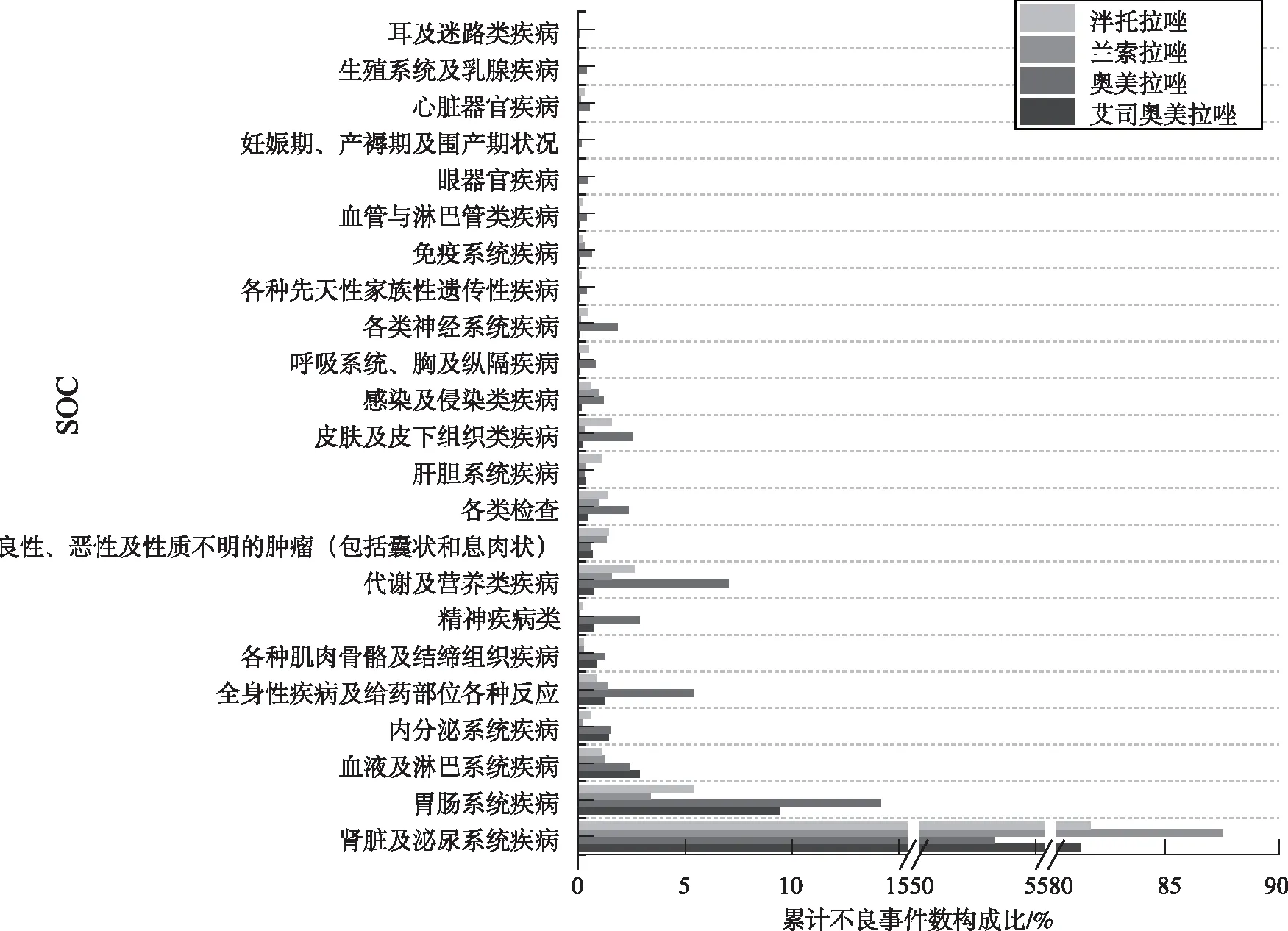
图1 四种PPIs累及系统不良事件数构成比
2.34种PPIs的ADE信号差别 对4种PPIs 的药品不良事件进行分析,排除与药物无关的信号,得到4种PPIs信号强度排序前20见表5。
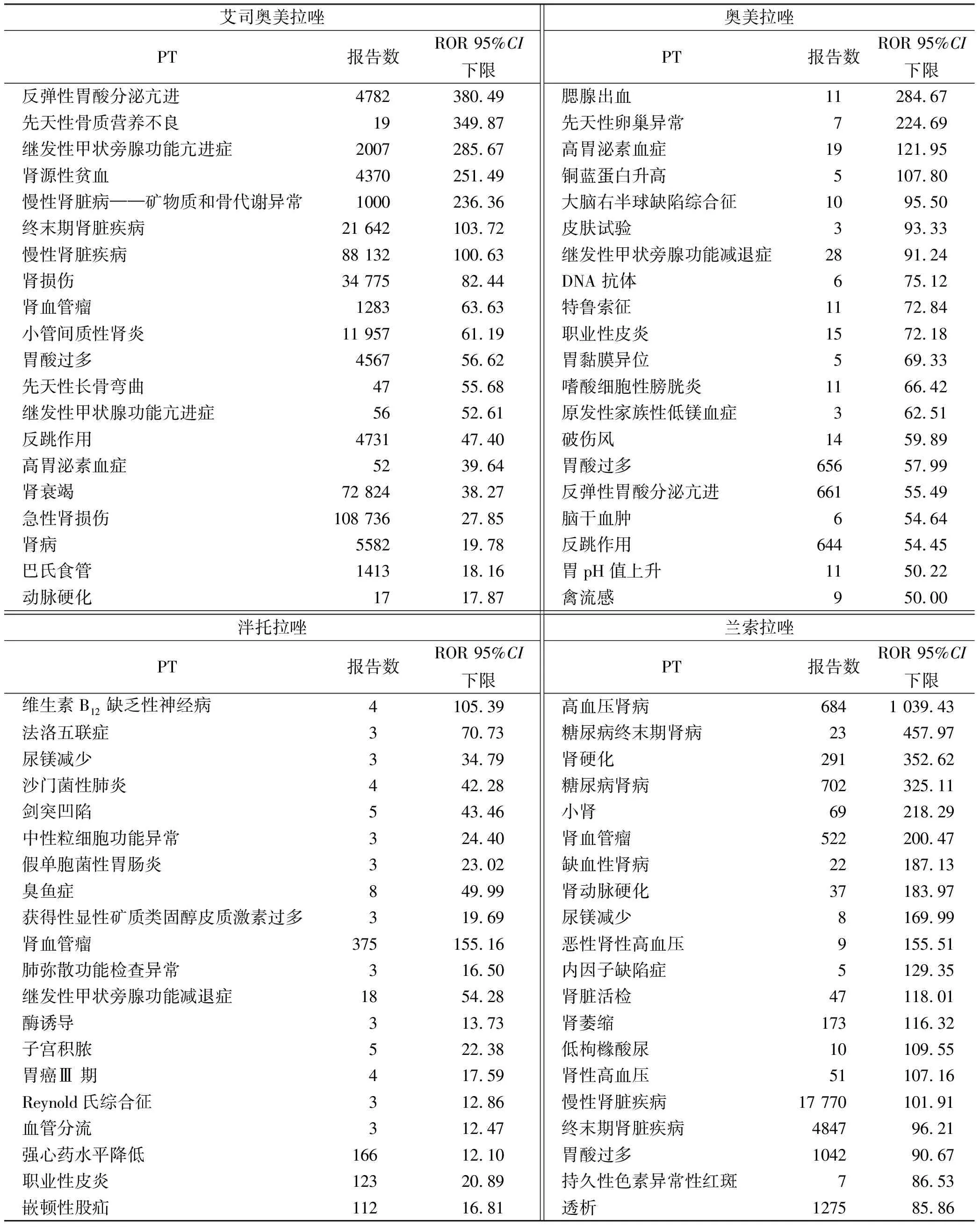
表5 4种PPIs信号强度前20
3 讨论
3.1PPIs类药物ADE发生的人口学特点 本次研究共纳入4种PPIs的ADE报告进行研究,获得首要怀疑药物为艾司奥美拉唑的报告45 748份;首要怀疑药物为奥美拉唑的报告20 822份;首要怀疑药物为兰索拉唑的报告28 626份;首要怀疑药物为泮托拉唑的报告22 666份,报告均主要来自于美国。由于上报的PPIs类药物ADE给药途径基本为口服,其他给药途径(注射等)报告数很少(奥美拉唑269份,泮托拉唑531份,兰索拉唑111份,艾司奥美拉唑268份),无法单独进行研究,因此本研究并未进行给药途径分类。在性别方面,4种PPIs均呈现出女性药品不良事件发生比例多于男性的现象,这提示PPIs的不良反应可能存在性别相关性。一项研究[12]指出,长期PPIs治疗中,男性患者和女性患者的空腹胃泌激素之间存在性别差异,且女性高于男性,其他不良反应的性别相关性有待继续研究。本次研究纳入的报告年龄<18岁的均不到3%,这可能与PPIs说明书中提到的不推荐用于儿童有一定的相关性。
3.2PPIs类药物 ADE累及系统和关联性的特点 本研究采用报告比值比法(reporting odds ratio,ROR)和综合标准法(MHRA法)作为信号检测方法,ROR和PRR值越大则表示该ADE信号强度越大,即目标ADE与目标药物关联性越强[13]。累及系统和关联性的分析可以为临床用药提供指导。说明书中提到的不良反应累及的系统如消化系统、神经系统、泌尿系统、肌肉骨骼系统等在本次研究中均有信号检出,证实了本研究的可靠性。且本次研究有新信号检出,可能为新发现的药品不良反应或新的常见药品不良反应,有待进一步研究,为说明书完善提供参考。消化系统ADE报告比例在4种PPIs中均排第二,但其常与原发疾病不易区分,所以暂不做讨论。本研究获得的雷贝拉唑报告共1572例,其中1178例集中在肾脏及泌尿系统系统,在《质子泵抑制剂临床应用指导原则(2020版)》中提到有肾功能损伤的患者使用雷贝拉唑时不需要调整剂量。除肾脏及泌尿系统外,雷贝拉唑在其他器官系统ADE分布很少,不具有大数据特征,故本研究对比结果均不包括雷贝拉唑。
4种PPIs的不良反应主要累及肾脏及泌尿系统,FDA说明书中的相关ADR只提到了“急性间质性肾炎”且频率为“罕见”,这与本次研究获得的数据不符。虽然并未获得使用人群的数据无法计算ADE发生率,大数据仍能提示PPIs在肾脏及泌尿系统的不良反应应当引起注意。研究结果显示,肾脏及泌尿系统疾病在PPIs的ADE总例数中构成比依次为:兰索拉唑>泮托拉唑>艾司奥美拉唑>奥美拉唑,发生例数依次为艾司奥美拉唑>兰索拉唑>泮托拉唑大>奥美拉唑,这提示除雷贝拉唑外,有肾脏疾病的患者使用奥美拉唑可能更加安全。除间质性肾炎外,此次发现的肾脏及泌尿系统ADE还包括慢性肾脏疾病(chronic kidney disease,CKD)、肾衰竭、肾损伤等。近年来,PPIs的肾毒性引起众多学者关注,SCHOENFELD等[14]研究证实PPIs与急性间质性肾炎(AIN)、肾小球滤过率降低和CKD的发生密切相关。值得注意的是,本研究中得到的肾脏及泌尿系统ADE的ROR值远大于已发表的几篇PPIs肾损伤研究[15-17]中ROR值,追溯时间发现肾损伤的报告主要集中在2019年,这正是PPI相关肾损伤问题研究的高热时期,所以有很大的过度报告风险。由于其他研究者纳入2004—2020年的总体数据,背景信号远高于本研究纳入的2015—2020年数据,造成被研究药物的信号强度偏低。同时其他研究者删除了非专业人士的报告,也造成了ROR值的低估。
奥美拉唑是临床上使用时间最久的PPIs类药物,并于1993年首次被报道与肾脏损伤相关[18]。在本研究中,与PPIs相关的AKI和CKD的最强信号分别是奥美拉唑和兰索拉唑。目前临床上尚缺乏对不同PPIs之间肾脏作用的横向对比。目前有研究显示[17],PPIs相关的肾脏事件平均发作时间存在显著差异,雷贝拉唑的最短中位发作时间为9 d,艾司奥美拉唑则为1221 d,即雷贝拉唑可在1个月内导致AKI,而暴露于艾司奥美拉唑的患者在几年后仍可能遭受AKI。提示临床上可在PPIs给药后进行个性化的监测策略,例如应用雷贝拉唑后可立即开展肾功能监测,停用艾司奥美拉唑后较长的一段时间内也应持续关注患者肾功能。目前CKD治疗指南中都没有患者使用PPIs的注意或警示,因此CKD治疗指南应当进行更新,提醒医师或患者谨慎使用PPIs。有肾脏疾病的患者如需使用PPIs,也应当尽量避免使用兰索拉唑,可换用相对较安全的PPIs,同时使用过程应注意监测肾功能。
在血液及淋巴系统疾病方面,奥美拉唑和艾司奥美拉唑发生此系统不良反应的比例相对另两种PPIs更高,这提示合并有血液及淋巴系统基础疾病的患者在使用PPIs时兰索拉唑和泮托拉唑可能是更安全的选择。4种PPIs可能导致各种类型的贫血(包括肾源性贫血、巨红细胞性贫血、恶性贫血等),肾源性贫血的发生次数和信号强度均较高,而说明书中并未提及。肾源性贫血是CKD的常见并发症,与PPIs导致CKD相关,表现为色素正细胞性、增生低下性贫血。因此在临床使用PPIs过程要注意贫血性疾病的预防,尤其是对于有肾脏疾病的患者和已经诱发肾脏的患者应当更加重视。除贫血外,奥美拉唑和泮托拉唑还会导致脾脏疾病,在患者使用过程中应当注意脾脏功能的保护;艾司奥美拉唑和奥美拉唑均检测出血小板疾病,使用这两种PPIs时要注意预防出血性疾病的发生。
内分泌系统疾病中,奥美拉唑和艾司奥美拉唑发生此系统不良反应的比例相对更高,且甲状旁腺功能障碍,尤其是继发性甲状旁腺功能亢进在4种PPIs中均有较强的信号。一项回顾性队列研究[19]显示PPIs使用与甲状旁腺功能亢进相关。其可能机制为PPIs抑制钙离子吸收、导致高胃泌素血症,这两种作用都会引起甲状旁腺激素分泌增加。而甲状旁腺激素分泌增加又会进一步干扰钙磷代谢,增强破骨或骨丢失过程,降低骨密度和骨强度,这也是PPIs导致骨质疏松的机制之一[20]。临床应避免长期使用PPIs,并在使用过程中注意监测患者骨密度监测,避免发生骨折和骨质疏松的风险。
在肿瘤方面,兰索拉唑、泮托拉唑、艾司奥美拉唑主要集中于肾脏肿瘤和胃肠系统肿瘤,而奥美拉唑则主要集中于各种消化道肿瘤和子宫、胰腺、横纹肌肿瘤等,构成比和发生次数相对于其他3种PPIs更少,但分布系统更广。PPIs可促进幽门螺杆菌的定植并导致高胃泌素血症,进而可能增加胃肠道恶性肿瘤的风险[21]。GARCIA RODRIGUEZ等[22]研究发现,长期应用PPIs,患者罹患食管癌的风险增加5倍,胃癌风险增加4倍,但长期PPIs治疗可能只是癌症的预警标志,并非危险因素。因此,长期使用PPIs的患者应定期进行癌症筛查。
奥美拉唑还在精神疾病类、代谢及营养疾病、神经系统疾病方面比较其他PPIs具有较大报告比例,合并有以上几个系统疾病的患者在治疗过程中应谨慎选用奥美拉唑。
3.3特殊人群用药 4种PPIs在妊娠期、产褥期及围产期状况均有信号检出,这提示妊娠和哺乳期妇女使用PPIs可能存在风险,应当谨慎使用。目前多个队列研究[23-24]表明PPIs并不增加胎儿出生缺陷的风险,但是临床研究资料有限,因此PPIs不作为妊娠期妇女常规抑酸剂使用。国家卫生健康委员会印发的《质子泵抑制剂临床应用指导原则(2020版)》建议妊娠期妇女应在抗酸剂、H2RA和胃黏膜保护剂疗效不佳时,评估效益风险后使用,且在妊娠前3个月应当避免使用任何PPIs。研究表明[25],PPIs会通过乳汁分泌,不推荐用于哺乳期妇女,但泮托拉唑在乳汁中极不稳定,在乳儿吸收前即被破坏失活,因此哺乳期妇女若无法避免使用PPIs,可选用泮托拉唑进行治疗,且应暂停哺乳4~5个半衰期。
3.4PPIs类药物不良反应分析与临床应用 PPIs按ADE报告数量排序依次是艾司奥美拉唑、兰索拉唑、泮托拉唑、奥美拉唑。这与一项回顾性队列研究[26]所得结论基本一致。
根据中国45家医院的PPIs处方调查[8],最常用的口服PPIs是雷贝拉唑,其次是泮托拉唑、兰索拉唑、艾司奥美拉唑和奥美拉唑。本研究未纳入雷贝拉唑是因为其不良反应报告数过少,较大的使用量和较少的不良反应报告数提示雷贝拉唑可能是目前相对安全性较高的PPIs。黄伟等[27]评价 5 种PPIs治疗幽门螺杆菌(Hp)引起的消化性溃疡的疗效及经济效果,结果发现,PPIs有效率依次为艾司奥美拉唑>雷贝拉唑>泮托拉唑=兰索拉唑>奥美拉唑,经济学效益最好的是雷贝拉唑,其后依次为艾司奥美拉唑>泮托拉唑=兰索拉唑>艾司奥美拉唑。医师在开具PPIs处方时,可优选雷贝拉唑,当无法开具雷贝拉唑时可以综合疗效、费用等问题选择合适的PPIs。
PPIs作为最广泛使用的处方药之一,有着重要的临床地位。但临床使用中并非所有PPIs都遵循循证指南规定。不恰当的PPIs使用是目前临床上面临的主要问题,探索PPIs的合理使用成为临床关注的重点之一。要确保PPIs的合理选择,促进合理用药,需要医师定期评估使用PPIs治疗的必要性。当有明确证据表明需要使用PPIs时,医师应保证其使用的疗程,同时应将其限制在最低有效剂量,不过度使用,规避不良反应的发生,促进临床合理用药。
3.5局限性 本研究采用FAERS的大数据进行分析,可以有效弥补临床试验样本量少、观察时间短等缺陷,获得真实世界下的结果,外推性强。但仍存在一定的局限性,FAERS数据库来报告来源大多为美国,不同国家和地区存在药物使用情况、人种、地域等存在差异,因此本研究的分析结果不一定完全适用于中国人群,可能存在一定偏差。其次,由于FAERS是ADE自发呈报系统,不可避免发生少报、漏报、报告不准确的现象,可能导致研究结果产生偏倚。本研究中性别、年龄、用药剂量等项目缺项太多,无法进行PPIs不良反应与这些项目之间的关联性分析;缺少用药人群的信息,没有分母,不能计算ADE发生率[28]。同时,ROR和MHRA法虽然计算简便,灵敏度高,但在特定条件下易出现假阳性。因为不同PPIs数据量差异大,本研究无法纳入雷贝拉唑的数据,而雷贝拉唑在临床应用较多,因此本研究存在一定局限性。
4 结论
本次研究对FAERS数据库2015—2020年不良事件报告进行分析,利用比例失衡法中ROR和MHRA方法进行PPIs不良事件数据挖掘,数据与说明书一致证明本研究的可靠性,为临床安全用药提供参考。4种PPIs的主要ADR具有一定的差异性。研究结果显示,奥美拉唑、艾司奥美拉唑、泮托拉唑、兰索拉唑不良反应均主要集中于肾脏及泌尿系统疾病,包括间质性肾炎、慢性肾脏疾病、肾衰竭等,奥美拉唑发生构成比和累计例数均最低,可能提示除雷贝拉唑外对于肾脏疾病的患者奥美拉唑是相对较安全的PPIs,使用过程要注意肾功能监测。PPIs还会致肾源性贫血等各种类型的贫血,发生例数和关联性都较大,但在说明书中未并未提到,临床应用时应引起注意。患者使用奥美拉唑和泮托拉唑过程中应当注意脾脏功能的保护;使用艾司奥美拉唑和奥美拉唑时要注意预防出血性疾病的发生。合并有精神疾病、代谢及营养疾病、神经系统疾病的患者在抗酸治疗治疗过程中应谨慎选用奥美拉唑。长期使用PPIs还应进行癌筛查。
