壳聚糖杂化吴茱萸碱复合纳米粒的药动学研究*
2021-07-29向晓燕余忠姝谢佳希施宇涛张景勍赵华
向晓燕,余忠姝,谢佳希,施宇涛,张景勍,赵华
(1.重庆医科大学药学院重庆高校药物工程研究中心,重庆 400016;2.重庆市巴南区人民医院药剂科,重庆 401320)
吴茱萸碱(evodiamine,ED)是分离自吴茱萸的一种主要活性生物碱。研究报道ED能与多靶点相互作用,发挥广泛的生物活性,如胃肠道调节、心血管保护等,还能通过阻滞细胞周期、诱导细胞凋亡、抑制迁移和侵袭等多种机制发挥抗肿瘤疗效,是一种有前景的天然药物[1]。但是ED的水溶性差、半衰期短、口服生物利用度低等缺陷阻碍了其临床应用[2]。目前文献报道的ED制剂包括复合物[3]、脂质体[4]、纳米乳[2]等,这些剂型分别存在改善口服生物利用度效果不明显、安全性不高等不足,不能很好地满足需求。因此高效、安全的ED新剂型的研究和开发具有重要意义。
磷脂和环糊精是安全有效的辅料,用于提高药物溶解度和透膜能力,两者同时与药物络合形成三元体系,显著改善药物的溶解性、增强药物口服吸收[5]。生物相容的天然多糖壳聚糖和透明质酸是低毒、可降解的载体材料,壳聚糖阳离子可与带负电荷的肠黏膜相互作用,打开细胞间隙,促进ED吸收[6];亲水性透明质酸增加药物溶解、延长其血液循环,也通过主动靶向肿瘤细胞CD44受体,改善药物在肿瘤部位的积累[7]。壳聚糖和透明质酸通过正负电荷相互吸引制备聚电解质纳米粒,用于改善药物体内代谢和分布特征[8]。本研究首先将ED与磷脂、羟丙基-β-环糊精制成三元复合物,辅以富勒醇包载,随后将含药复合物包纳进壳聚糖/透明质酸载体外层中,制备了壳聚糖杂化吴茱萸碱复合纳米粒(chitosan hybrid evodiamine composite nanoparticles,CENP),希望结合药物复合技术和纳米技术的优势,以达到显著增加ED水溶性、提高ED的口服生物利用度的效果。通过考察CENP和ED在大鼠体内的药动学特征,为ED后续抗肿瘤研究提供方向,并奠定其临床应用的基础。
1 材料与方法
1.1材料
1.1.1试剂 ED(含量>99%,武汉远城科技发展有限公司);羟丙基-β-环糊精(HP-β-CD)(含量99.8%,淄博千汇生物科技有限公司);磷脂(PC)(Lipoid S 100,Phospholipid Gmbh,Nattermannllee,Germany);壳聚糖(CS)(浙江金壳生物化学有限公司);透明质酸(HA)(曲阜市广龙生物制品厂);CENP(实验室自制);和厚朴酚(西安小草植物科技有限公司);甲醇、乙腈(色谱纯,美国天地有限公司);其他试剂均为分析纯。
1.1.2仪器 岛津LC-20A型液相色谱仪(日本岛津公司);旋转蒸发器(型号:RE-52AA,上海亚荣生化仪器厂);电子天平(感量:0.1 mg,型号:FA1004A,上海精天电子仪器有限公司);TGL-16B台式高速离心机(上海安亭科学仪器厂);DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限公司);Zetasizer Nano zs90激光粒度电位仪(日本岛津公司)。
1.1.3实验动物 清洁级SD大鼠,雄性,体质量(230±20) g,由重庆医科大学实验动物中心提供,许可证号:SCXK-(渝)2017-0001。饲养环境:温度(20±2) ℃、相对湿度(60±10)%、明暗交替12 h/12 h。
1.2方法
1.2.1CENP的制备及表征 采用离子凝胶法制备CENP[9]。称取处方量ED、羟丙基-β-环糊精、磷脂溶于乙醇中,水浴中磁力搅拌3.5 h,40 ℃旋转蒸发除去无水乙醇得淡黄色复合物。取适量复合物,将处方量的透明质酸溶液、富勒醇溶液逐滴、缓慢加入壳聚糖溶液,磁力搅拌30 min得CENP。取适量CENP,用超纯水稀释10倍,采用马尔文激光粒度仪测定其粒径和Zeta电位。
1.2.2给药方案及样品采集 12只SD大鼠采用随机数字表法分为游离药ED组和制剂CENP组(n=6),禁食12 h后,分别灌胃相应药物(剂量均以ED 100 mg·kg-1计)。分别于给药后5,10,15,30,45 min、1,2,4,6,8,12,24,48,72,96 h采集血样体积500 μL,随后6000 r·min-1,离心10 min,后取上清液,-80 ℃冻存,待下一步处理。
1.2.3血浆样品的处理 取待测血浆样品100 μL,加入1 μg·mL-1内标和厚朴酚溶液20 μL和乙腈500 μL,3000 r·min-1涡旋1 min,静置30 s后重复涡旋1次。将样品离心(12 000 r·min-1,10 min)取上清液,氮气吹干,随后加入乙腈100 μL复溶,涡旋30 s,8000 r·min-1,离心5 min,取上清液40 μL进样。
1.2.4色谱条件 色谱柱:COSMOSIL 5C18-MS-II柱(250 mm × 4.6 mm,5 μm);流动相:10 mmol·L-1乙酸铵:乙腈=40:60;柱温:30 ℃;流速:1.0 mL·min-1;检测波长:225 nm;进样体积:40 μL。
1.2.5方法学考察 按照“2.4项”下的色谱条件,通过专属性、线性关系、精密度、回收率和稳定性等试验,考察ED体内含量测定方法的合理性[10]。
1.2.6数据处理 以血药浓度为纵坐标、时间为横坐标绘制血药浓度-时间曲线。使用DAS2.1.1 版软件处理数据,计算并比较CENP和ED的主要药动学参数,以P<0.05为差异有统计学意义。
1.2.7生物等效性评价 采用DAS软件将AUC(0-∞)和Cmax经对数转换后进行方差分析、单双侧t检验和[1-2α]90%置信区间考察;利用非参数统计Wilcoxon秩和检验考察CENP和ED的tmax,比较CENP和ED的生物等效性。
2 结果
2.1CENP的粒径和Zeta电位 CENP的粒径和Zeta电位分别为(423.90±26.12) nm和(43.47±1.20) mV。
2.2CENP的药动学参数 CENP和ED灌胃大鼠后的体内药时曲线图见图1。结果显示,CENP的整体血药浓度水平较ED增加,CENP的Cmax约为ED的3倍,表明CENP增加了ED的口服吸收。CENP的血药浓度达峰时间较ED延迟。当ED在给药后24 h浓度已接近于0时,CENP仍保持较高浓度值,说明CENP延长了药物的体内滞留时间,能发挥更长时间的作用。

图1 大鼠口服CENP和ED后的平均血药浓度-时间曲线
CENP和ED的主要药代参数结果分别见表1和表2。分析非房室模型参数可知,与ED比较,CENP的AUC(0-∞)和Cmax分别增加了约3.57倍和1.92倍。MRT(0-96 h)增加了约7.59 h,CL降低了78.57%,分析房室模型参数可知,CENP的AUC(0-∞)和Cmax分别约为ED的4.18倍和2.92倍。与ED比较,CENP的相对生物利用度AUC(0-∞)在非房室模型和房室模型中分别为457.46%和417.80%,两种模型分析结果相差不大。
2.3生物等效性评价 CENP和ED的药代动力学参数及生物等效性结果,见表3。由表可知,AUC(0-∞)和Cmax的[1-2α]90%置信区间分别为(79.9,82.8)%和(78.3,84.6)%,均不在标准范围内;两者的tmax差异有统计学意义(P=0.01)。综上所述,CENP和ED生物不等效。
3 讨论
本实验成功制备壳聚糖杂化吴茱萸碱复合纳米粒CENP,研究其在大鼠体内的药代动力学特征。CENP的粒径为(423.90±26.12) nm,属于纳米范围。CENP的Zeta电位为(43.47±1.20) mV,> 30 mV,粒子间的反作用力可以避免絮结和凝集,从而保持CENP的稳定性[11]。ED的体内含量测定方法符合要求。药动学结果表明,CENP可以明显改善ED的体内药动学行为,促进ED的口服吸收,减缓药物的清除,延长ED的体内作用时间,增加ED的AUC约3.57倍。CENP增加ED的口服生物利用度的原因可能是:ED与磷脂、环糊精形成三元复合体系,环糊精包纳ED的同时,磷脂也部分伸入环糊精空腔,改善ED的水溶性、稳定性和生物膜透过能力,进而促进ED的口服吸收[5];纳米载体壳聚糖和透明质酸进一步提高ED的溶解性和胃肠道吸收,改善药物释放行为,同时延长ED的体内循环,减缓清除[12]。与文献[3,13]报道的磷脂复合物、环糊精包合物比较较,CENP改善ED的AUC能力更强。此外,虽然已报道的ED纳米乳分别提高了ED的AUC约3.66和5.30倍[2,14],略强于CENP提高AUC的能力。但是由于纳米乳的形成需要大量的表面活性剂(如泊洛沙姆188、聚山梨酯80、RH40等),而这些非离子型表面活性剂可能导致溶血、过敏、神经毒性等不良反应,使纳米乳的临床应用受到了限制[15]。反之,CENP的载体材料具有生物相容性、可降解性和低免疫原性,递送系统安全性更高,具有应用潜力。CENP具有安全有效的特性,它是递送抗癌药物的有前景的平台,具有通过以下多种机制发挥抗肿瘤作用的潜力:CENP具有EPR效应[16];环糊精能抑制P糖蛋白(P-gp)改善药物吸收并减轻耐药[17];透明质酸具有控释和主动靶向肿瘤的作用[7];富勒醇具有自由基清除能力,还可以通过调控肿瘤微环境、抑制血管生成等作用增强药物抗肿瘤疗效[18]。综上所述,本实验首次制备的复合纳米粒CENP是可改善ED药动学行为的新制剂,为提高ED生物利用度的剂型研究提供了一定的参考依据,同时也为后续体内外研究及临床应用奠定基础。
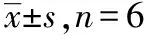
表1 大鼠单剂量口服CENP和ED的非房室模型药动学参数
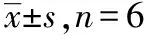
表2 大鼠单剂量口服CENP和ED后的房室模型药动学参数
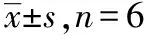
表3 大鼠单剂量口服CENP和ED的生物等效性评价
(志谢:本实验在重庆医科大学重庆高校药物工程研究中心完成,在此真诚感谢实验室的所有老师和同学。)
