FeF2@C球形核壳复合结构的制备及其电化学性能 ①
2021-07-28张艳丽王晶鑫谢乐琼谢英鹏郝永胜何向明
张艳丽,张 强,王晶鑫,谢乐琼,王 莉,谢英鹏,郝永胜,何向明*
(1.沈阳化工大学材料科学与工程学院,辽宁 沈阳 110142;2.清华大学核能与新能源技术研究院,北京 100084)
1 引言
锂离子电池是重要的能量存储器件,目前已经广泛应用于笔记本电脑等便携领域。为了在清洁能源存储和电动汽车领域中推广应用,需要具有更高的能量密度。提高锂离子电池能量密度的关键在于寻找具有更高能量密度的电极材料。金属氟化物通过多电子转化反应而具有较高理论比容量,且因金属-氟化学键具有较高的离子性成分而具有较高电势[1]。在各种金属氟化物中,氟化亚铁(FeF2)是一种潜在的理论高比能量的锂离子电池正极材料[2]。FeF2属金红石晶体结构,空间群为P42/mnm。作为锂离子电池正极材料时,随着放电的进行,在2.66 V电压附近,会发生如下转化反应:FeF2+2Li++2e-=Fe+2LiF,FeF2被还原成金属单质Fe,并形成锂合物LiF;充电过程中LiF发生分解,Fe重新被氧化为FeF2。理论放电比容量为571 mAh g-1,理论放电比能量为1 519 Wh kg-1。但氟化亚铁带隙较大、电子导电率低;在电化学转化反应过程中存在结构和形貌的不断改变和重排、难以保持结构稳定、电极反应动力学缓慢[3];表现在电化学性能上即为较大极化和电压滞后、循环寿命短、倍率性能较差,阻碍了它的实际应用。
为了克服上述问题,研究者探索了各种改善的途径,如合成固溶体[4-7]、合成纳米孔结构[8]、构建复合材料[9-24]。碳是一种具有极好导电性的材料,已经有多种碳-FeF2复合材料被合成出来。如以CFx为前驱体,采用热解、电化学插层等方式合成“FeF2纳米颗粒位于碳层中的结构”[11,14,21,22,25]、“FeF2纳米颗粒位于多孔碳中的结构”[15,16,18]、“碳管包覆FeF2纳米棒结构”[19]。在这些结构中,碳组分不仅增加了导电性,而且缓冲了FeF2转化反应中的体积变化,FeF2性能得到了提高。
在我们之前的研究中,曾用二茂铁和PVDF作为前驱体,合成了棒状的碳层包覆氟化亚铁的壳核复合结构[20]。在本研究中,我们提出通过将二茂铁和NH4F混合、在一定温度和时间下反应,原位得到球形的碳包覆氟化亚铁的壳核复合结构。通过XRD、SEM、TG对所得复合结构的形貌、结构、碳含量进行了表征,并测试了恒流充放电循环性能。
2 实验部分
2.1 FeF2@C核壳球形复合结构的制备
按化学式计量比Fe∶F=1∶2称取二茂铁和NH4F粉末,通过行星球磨(500 rpm,30 min)混合均匀。将混合物置于不锈钢反应容器中,而后将容器中填充纯净氩气并密封。将不锈钢反应容器置于马弗炉中,以10 ℃/min的速度升温至600 ℃,在此温度下保温5 h,而后待温度自然冷却至室温后取出。打开反应容器,见容器内沉积有黑色、松软的粉末,即为所制得的碳包覆氟化亚铁纳米颗粒。
2.2 FeF2@C核壳球形复合结构的表征
采用X射线衍射仪(D8 ADVANCE 3W,Cu K射线源)、扫描电镜(JSM-7100F)、透射电镜(FEI Technai G2 F30)、对产物的形貌和结构进行表征。热重测试在NETZSCH STA 409C型热分析仪上进行,升温速率为10 ℃/min,温度区间为50-850 ℃,空气流速为50 mL/min。
2.3 FeF2@C核壳球形复合结构的电化学性能测试
工作电极是按照FeF2@C活性物质90 wt.%,黏结剂(PTFE)10 wt.%的比率混合均匀后压制成直径10 mm的小圆片,真空干燥箱中80 ℃下烘6 h。以金属锂片为负极,采用Celgard 2400聚丙烯隔膜,1 mol/L LiPF6的EC+DMC+EMC(体积比1∶1∶1)溶液作为电解液。在Ar气氛手套箱中组装2032扣式电池。恒流充放电测试在蓝电测试仪上进行,充放电电流密度为30 mA g-1,充放电电压范围为1.3 V-4.2 V。作为对比,购买了粒度为微米级的FeF2粉末,按FeF2∶黏结剂∶乙炔黑=80∶10∶10 wt.%的比率制备电极片,电池制备及电化学测试采用与FeF2@C相同的工艺与程序。
3 结果与讨论
3.1 FeF2@C核壳球形复合结构的物相、形貌、组分
图1为所得产物样品的XRD图谱,所有的峰均可标定为JCPDS-45-1062,表明样品中物相均为纯净的正方氟化亚铁(FeF2)。
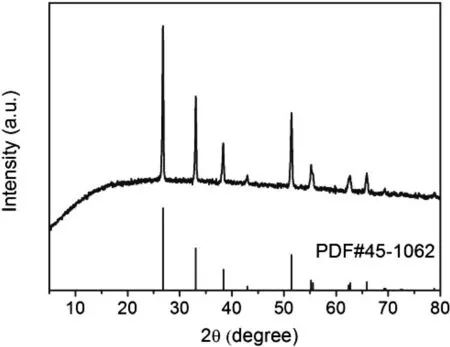
图1 FeF2@C核壳球形复合结构的XRD图Fig.1 XRD pattern of the FeF2@C core-shell spherical nanostructure.
图2为样品的SEM图片(a、b)、TEM图片(c、d)和能谱(e)。SEM图片显示大量近球形颗粒,颗粒的尺寸分布在100 nm-1 μm之间,仔细观察发现,颗粒的边缘区域与内部区域具有不同的衬度。TEM图片进一步揭示颗粒为壳核结构,内核物质的面间距为0.264 nm,对应正方FeF2的(101)晶面,结合XRD结果,认为内核物质为FeF2。外壳层厚度分布在10 nm-20 nm之间,外壳层中大部分为无定形态,其中含有少量的晶态区域,测量晶格间距约为0.34 nm,与石墨的面间距类似。能谱显示颗粒由Fe、F和C三种元素构成,其中Cu来自微栅。

图2 FeF2@C核壳球形复合结构的扫描电子显微镜图片(a)(b)、透射电子显微镜图片(c)(d)及相应的能谱分析(e)Fig.2 SEM images (a,b),TEM images (c,d) and EDS spectrum (e) of the FeF2@C core-shell spherical nanostructure.
图3为样品的热重图谱。通过观察热重图谱可见,在热重测试过程中,自升温开始到350 ℃之间的温度范围内,样品几乎没有失重或增重;自350 ℃开始,样品开始失重,对应碳包覆氟化亚铁纳米颗粒的外壳层碳层开始逐渐被氧化掉;当温度到达约543 ℃时,外壳层碳层几乎完全被氧化掉,暴露出来的氟化亚铁内核开始被氧化,对应热重曲线上的缓慢失重;当温度达到819 ℃时,样品重量不再变化,说明经过升温过程,碳包覆氟化亚铁纳米颗粒最终氧化为三氧化二铁,可由此来估测碳包覆氟化亚铁纳米颗粒中氟化亚铁的相对含量。由TG曲线得出样品中残余三氧化二铁的重量百分比为51.4%,经换算得,样品中氟化亚铁的重量百分比为61.1 wt.%。
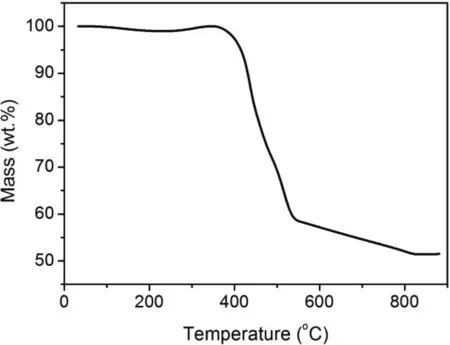
图3 FeF2@C核壳球形复合结构的热重曲线Fig.3 TG analysis of the FeF2@C core-shell spherical nanostructure.
3.2 FeF2@C核壳球形复合结构的电化学性能
图4为样品的恒流充放电曲线,充放电电流密度为30 mA g-1,电压范围为1.3 V-4.2 V。在第一个充放电循环中,样品的首次放电比容量为279 mAh g-1,可逆充电比容量为266 mAh g-1,相应的首次库伦效率为95.4%。首次放电曲线可以分为两个放电区域:第一个放电区域中,电压从开路电压逐渐降至1.87 V,相应放电比容量为50 mAh g-1;第二个放电区域中,电压从1.87 V逐渐降至1.3 V。第一个放电区域对应锂离子在氟化亚铁中的插入过程,相应的生成化合物LixFe1-xF2。第二个放电区域涉及到转化反应,伴随着Fe和LiF的生成。在首次循环之后的循环过程之中,充放电曲线的形状与首次的类似,不同之处在于电压略有增高,这归因于在转化反应中生成的铁纳米颗粒进一步改善了材料的导电性。此处壳核球形样品的充放电比容量比我们之间报道的壳核棒状样品[20]的略低,推测原因在于:不同于棒状样品中碳包覆层结晶性良好的状况,此处球形样品中的碳包覆层大部分为无定形态,只有少量结晶态,尽管对内核FeF2转化过程中的电子导电性有一定促进作用,但导电效果不及前者,这导致了比容量偏低。从图4可得,第10个、第20个、第30个循环中的放电比容量分别为263、228、188 mAh g-1。
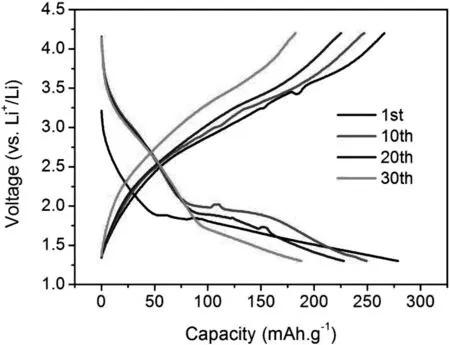
图4 FeF2@C核壳球形复合结构的充放电曲线(第1、10、20、30次循环)Fig.4 1st,10th,20th and 30th discharge-charge curves of the FeF2@C core-shell spherical nanostructure measured at a current density of 30 mAg-1 between 1.3 V-4.2 V (vs Li+/Li).
图5显示样品的循环性能及库伦效率随循环次数的变化。可逆充放电比容量随着循环的进行逐渐衰减,30次循环后的比容量保持率为67.4%,衰减率为1.09%每个循环。自第二个循环之后,库伦效率的波动范围为89.5%-106.7%。

图5 FeF2@C核壳球形复合结构的循环性能与倍率性能Fig.5 Cycling performance and columbic efficiency of the FeF2@C core-shell spherical nanostructure.
图6和图7分别为纯净FeF2的恒流充放电曲线及循环性能。表面无碳包覆层的纯净FeF2在充放电电流密度为30 mA g-1,电压范围为1.3 V-4.2 V下的首次放电比容量为560 mAh g-1,第10个、第20个、第30个循环中的放电比容量分别为199、83、34 mAh g-1。30次循环后的比容量保持率仅为6.1%。推测无碳包覆层的纯净FeF2在首次充放电转化反应后,生成的Fe纳米颗粒因缺少了碳层的包覆而直接接触电解液并溶解于其中,造成了比容量逐渐损失。且缺少了碳层的导电子作用,电子导电性下降,也在一定程度上阻碍了充放电反应进行,导致比容量进一步降低。而上述有碳包覆层的FeF2@C样品在充放电过程中,碳层起到传输电子及隔离电解液、防止Fe损失的作用,故有较稳定的充放电性能。

图6 FeF2的充放电曲线(第1、10、20、30次循环)Fig.6 1st,10th,20th and 30th discharge-charge curves of FeF2at a current density of 30 mAg-1 between 1.3-4.2 V (vs Li+/Li).
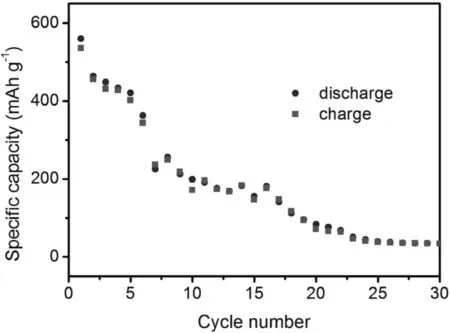
图7 FeF2的循环性能Fig.7 Cycling performance of FeF2.
4 结语
采用一步热反应法,以二茂铁和NH4F的混合物为原料,制备了一种新型的球形碳包覆氟化亚铁壳核纳米颗粒。纳米颗粒的内核为晶态氟化亚铁,外包覆层为具有少量结晶态的碳层。近球形颗粒的尺寸在100 nm-1 μm之间,碳包覆层厚度分布在10 nm-20 nm之间。碳层的重量百分含量为39 wt.%。测试了所得FeF2@C壳核结构的充放电性能。首次放电比容量为279 mAh g-1,第10个、第20个、第30个循环中的放电比容量分别为263、228、188 mAh g-1。衰减率为1.09%每个循环;自第二个循环之后,库伦效率的波动范围为89.5%-106.7%。良好的电化学性能归因于碳包覆层增加了FeF2的电子导电性,缓冲了FeF2转化反应过程中的体积变化,并且防止了与电解液之间的接触。
