氧化铝作为热电池电解质流动抑制剂的应用研究 ①
2021-07-28赵彦龙张小龙王天宝常文涛
赵彦龙,张小龙,王天宝,张 飞,常文涛
(1.西安北方庆华机电有限公司,陕西 西安 710025;2.陆军装备部驻西安地区军代局驻西安地区第一军代室,陕西 西安 71002)
1 引言
热电池是以热能为初始激活能源的电池,它的电解质是常温下呈现为固体,无导电性的熔融盐,工作时热能使熔融盐转化为具有导电性的离子导体,电池激活并开始向用电系统放电。该熔融盐电解质电池与水溶液电解质相比,具有许多特点,例如比电导很大、大功率放电能力强、体积(质量)比能量和体积(质量)比功率高,以及宽泛的环境温度、优良的贮存寿命、激活速度快、可靠性高、核心结构紧凑、制造工艺简便、造价低廉、无需维护等特点。因此热电池是近现代武器(如导弹、火箭弹、炮射导弹、鱼雷等)十分重要的电源之一,在军用电源系统中占有非常重要的位置[1]。
在热电池中,电解质主要起两种作用:一种作用是导电介质(离子导体);另一种作用是隔离正负极并将其电极反应产物部分溶解,因此所选用的材料必须具有良好的电导率和化学稳定性[2]。当工作温度高于电解质熔点时,电解质变熔化、流动。电解质的流动产生电噪声,加快自放电,严重时造成电池短路,对电池放电具有十分不利的影响。为了减缓电解质的非常规流动,常通过使用比表面积大的化学惰性物质(即不与电解质和电极材料发生化学反应)添加到电解质中以抑制电解质的流动[3]。
常用的抑制剂有二氧化硅和氧化镁,但是二氧化硅会与锂合金发生化学反应,只适用于在以钙系材料作为阴极的热电池中充当电解质流动抑制剂。锂系热电池一般使用氧化镁作为电解质流动的抑制剂。在熔融盐电解质中,氧化镁毛细管作用能够有效抑制电解质的流动。氧化镁添加到电解质中的质量百分比范围为35%~60%[3]。国内MgO 吸附能力不足的问题随着热电池性能要求的不断提升,已经开始展现出来,需要开发能够适应超高比能量热电池的高吸附能力黏合剂材料。
活性Al2O3是一种具有多孔结构的高比表面物质,广泛应用于橡胶、石油等化学工业的吸附剂、催化剂或载体,为了提升电解质中黏结剂对共晶盐的吸附能力,本文基于LiSi/LiCl-KCl/FeS2电化学体系,考察研究了两种温度下制备的氧化铝添加剂对热电池放电效率的影响,获得了许多重要的数据,对今后提高热电池电解质中有效导电成分的含量,降低成本具有重要意义。
2 实验部分
2.1 材料制备
本实验所氧化镁及氧化铝添加剂均参照热电池用轻质活性氧化镁处理工艺进行预处理,氧化镁在马弗炉中500 ℃灼烧4 h,氧化铝分两种灼烧温度进行处理,500 ℃灼烧4 h获得Al2O3,800 ℃灼烧4 h获得Al2O3*。所用电解质材料均参照热电池用电解质纸杯工艺进行,按所述比例将电解质抑制剂与LiCl-KCl共熔粉混合后再马弗炉中550 ℃灼烧4 h后,经冷却、粉碎、烘干后获得。
2.2 材料表征
本文使用扫描电子显微镜(捷克Tescan公司,VEGA ⅡXMU)对氧化镁和氧化铝的微观形貌进行了观测,系统的观察了样品的表面形貌;采用溶剂吸附法对二者的比表面积进行测试(美国麦克公司,Tristar Ⅱ 3020);采用斯科特容量法对其堆积密度进行测试(北京佳航博创科技有限公司,HYL-103)。
2.3 实验操作
采用特制单体电池放电反应炉进行单体电池放电实验。实验用单体电池直径为Φ24 mm,正极材料为FeS2,负极材料为LiSi,电解质材料为加入不同添加剂的自制电解质。单体电池压制采用常规叠层压制方法。具体放电过程为单体电池与集流体装配好后,再与加热装置及数据采集仪连接,加热放电。放电温度通过高温炉的温度控制器进行调节,电压和时间通过数据采集仪进行采集。数据取值为3次平行试验的平均值。单体电池放电采用恒阻、恒温方式进行,比能量计算截至电压1.6 V。
3 结果与讨论
3.1 材料表征
3.1.1 材料形貌
图1为氧化镁、氧化铝样品的扫描电子显微镜(SEM)照片。由图1可知,MgO颗粒为球形,粒子的平均粒径约为50 nm,颗粒之间存在大小不等的微孔。氧化铝的为近球形颗粒,平均粒径约为30 nm~50 nm,同样是通过颗粒间的连结搭建的多孔结构。
3.1.2 比表面积
表1为氧化镁、氧化铝的比表面积测试结果。由表1可知,不同方法处理所得的氧化铝比表面积比氧化镁高出2~3倍,Al2O3*的比表面积更是达到了198 m2/g。由于热电池电解质流动抑制剂对电解质流动的抑制能力主要与比表面积相关且成正比关系,即抑制剂的比表面积越大抑制能力越强,由此可以得出氧化铝作为流动抑制剂应具有比氧化镁更强的吸附能力。

表1 氧化镁、氧化铝的比表面积Table 1 Specific surface area of magnesium oxide and alumina.
3.1.3 堆积密度
表2为氧化镁、氧化铝的堆积密度测试结果。由表1可知,不同处理方法所得氧化铝的堆积密度均大于氧化镁,分别为0.68 g/mL和0.85 g/mL,这与扫描电镜和比表面积测试结果相一致,即氧化铝的粒径比氧化镁的小,而比表面均比氧化镁的大,为其以更小的使用量代替氧化镁成为热电池电解质流动抑制剂提供了理论基础。

图1 氧化镁、氧化铝的扫描电子显微镜图像。(a) MgO;(b) Al2O3;(c) Al2O3*Fig.1 SEM images of magnesium oxide and alumina.(a) MgO;(b) Al2O3;(c) Al2O3*.

表2 氧化镁、氧化铝的堆积密度Table 2 Stacking density of magnesium oxide and alumina.
3.1.4 单元电池的放电性能
针对以氧化铝作为热电池电解质流动抑制剂的LiSi/LiCl-KCl/FeS2电化学体系,系统研究氧化铝作为热电池电解质流动抑制剂对电池性能影响,首先通过试验确定氧化铝抑制剂体系在1.5 Ω、3 Ω负载条件下的最优工作温度。
Al2O3作为流动抑制剂的性能试验
表3为添加25% Al2O3作为流动抑制剂,不同放电条件下单元电池的电性能数据。由表3可知,在不同的负载条件下,随着工作温度的逐渐升高,单体电池的工作电压逐渐升高,但其放电时间呈先延长后缩短的趋势。工作时间缩短的主要原因为随着温度的升高,其单体电池内部的活性物质衰减急剧增加,导致放电时间缩短[8]。由实验结果可知,在1.5 Ω负载条件下,其最优工作温度为500 ℃;在3.0 Ω负载条件下,其最优工作温度为450 ℃。
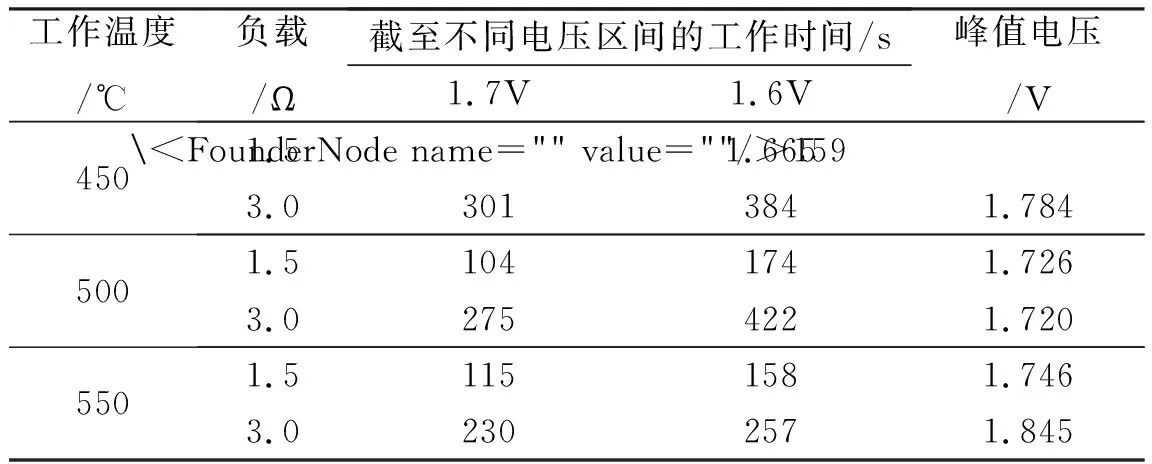
表3 不同温度下添加25% Al2O3的单体电池放电数据Table 3 Discharge data of battery cells with 25% Al2O3at different temperatures.
图2为最优放电条件下不同比例氧化铝和氧化镁作为电解质流动抑制剂的单元电池放电曲线。由图可知,不论是氧化镁还是氧化铝作为电解质流动抑制剂,单元电池的放电时间和最高电压都随其含量的增加而降低,因为随着流动抑制剂含量的增加,电解质熔融时流动能力变差,内阻增大,致使电池中活性物质的利用率降低。由图2可以看出,抑制剂为35% MgO时,单元电池的电性能最好,25% Al2O3*的单元电池电性能次之,这也与上述理论相吻合,但含35% MgO的电解质热稳定性能较差,不能满足热电池装备使用要求,这点我们将在下一小节中进行讨论。
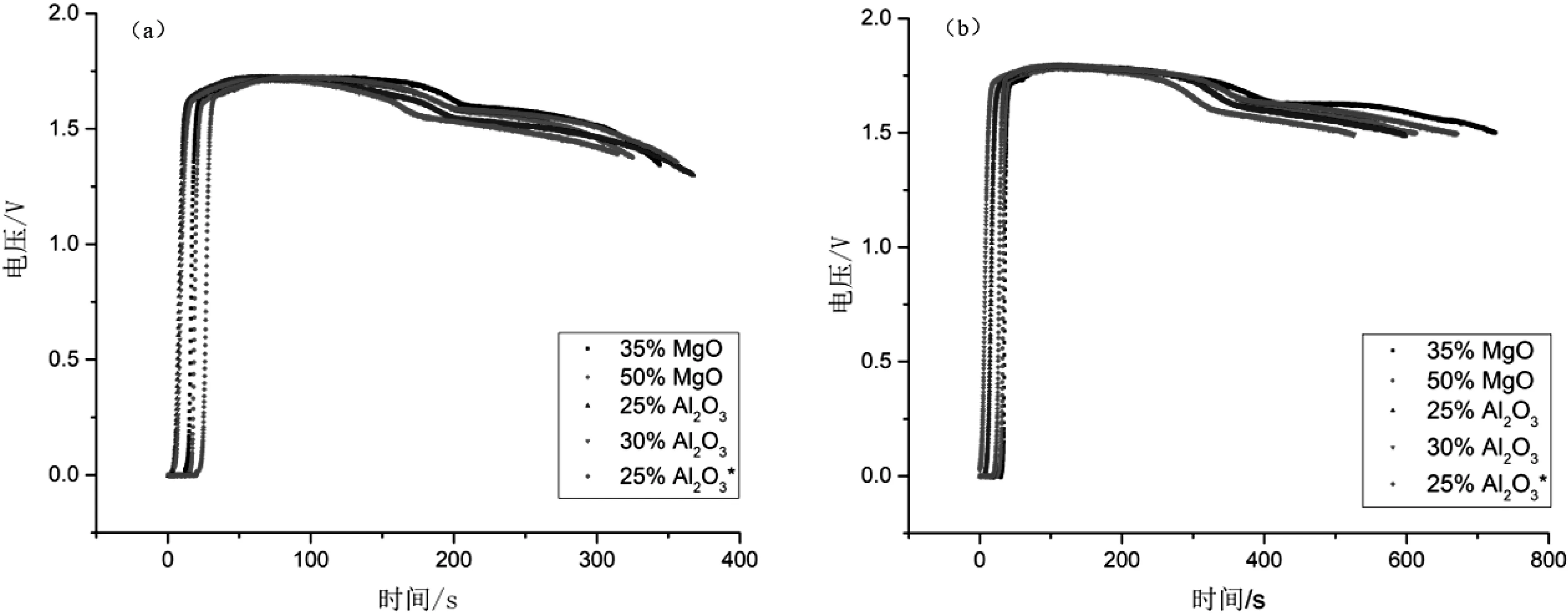
图2 不同比例氧化铝和氧化镁作为电抑制剂的放电数据。(a)负载1.5 Ω,500 ℃;(b)负载3.0 Ω,450 ℃Fig.2 Discharge data of different proportions of alumina and magnesium oxide as electrodepressants.(a) discharge at 500 ℃ with 1.5 Ω;(b) discharge at 450 ℃ with 3.0 Ω.
3.2 电解质的热稳定性
称取3 g电解质样品,以7 MPa的压力将电解质粉末压制成具有一定强度的圆柱体,然后向其施加1 kPa的作用力,放进温度为500 ℃的马弗炉中保温30 min,取出后室温条件下冷却,所得结果如图3所示。
由图3可知,50% MgO和25% Al2O3的电解质型变量相当,但50% MgO 已经失去了起初圆柱形的轮廓;25% Al2O3*形变较小,且依然保持较为规则的圆形轮廓,初步说明电解质的稳定性顺序为:30% Al2O3*>25% Al2O3>50% MgO。
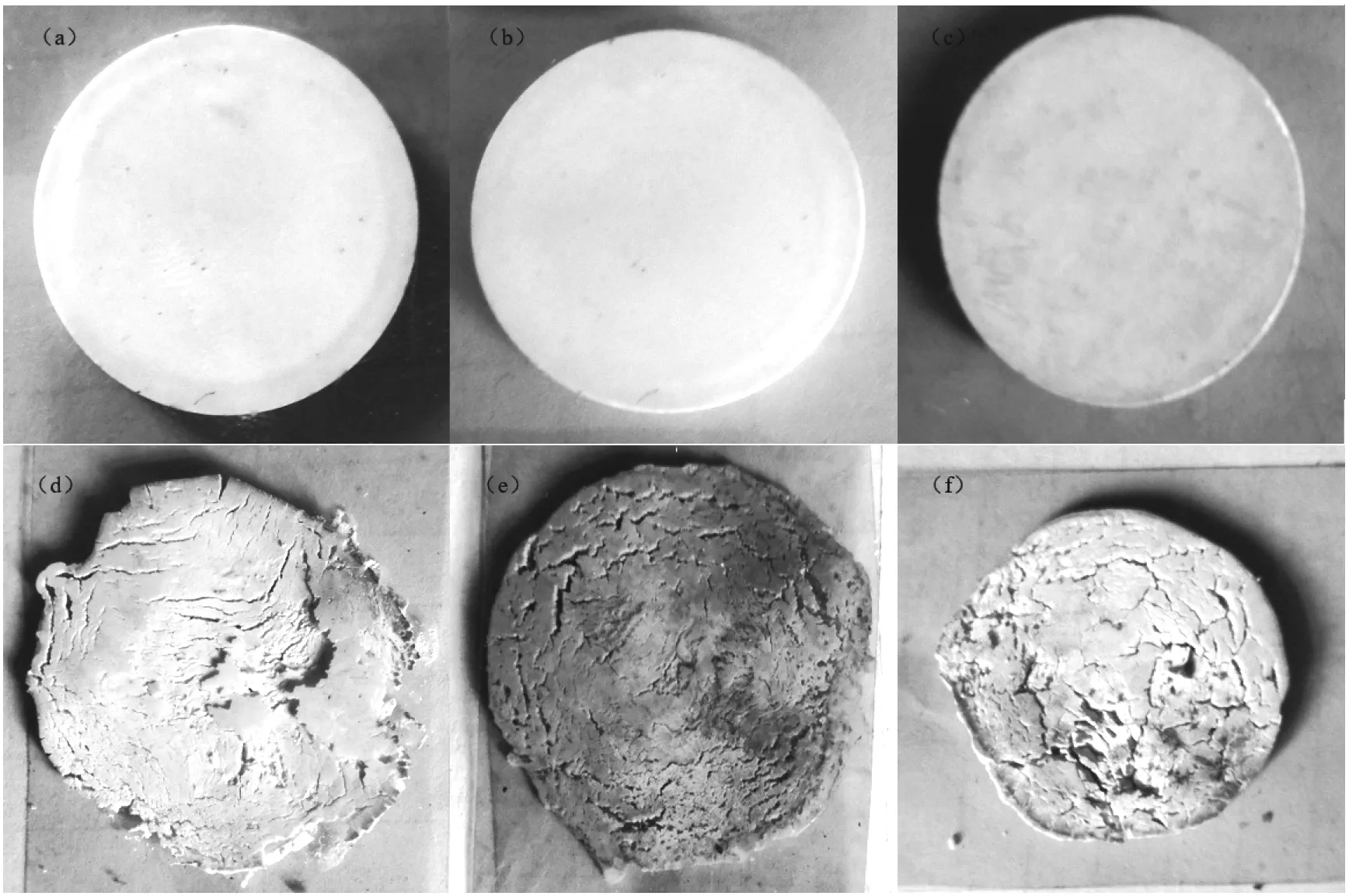
图3 电解质的机械稳定性。(a)含50% MgO电解质片灼烧前;(b)含25% Al2O3电解质片灼烧前;(c)含25% Al2O3*电解质片灼烧前;(d)含50% MgO电解质片灼烧后;(e)含25% Al2O3电解质片灼烧后;(f)含25% Al2O3*电解质片灼烧后Fig.3 Mechanical stability of electrolytes.(a) Tablets containing 50% MgO electrolyte before burning;(b) Tablets containing 25% Al2O3 electrolyte before burning; (c) Tablets containing 25% Al2O3* electrolyte before burning; (d) The tablets containing 50% MgO electrolyte were burned; (e) The tablets containing 25% Al2O3 electrolyte were burned; (f) The tablets containing 25% Al2O3* electrolyte were burned.
通过铺大面的放方法(即在制备单元电池过程中压制电解质层时不加入阻流环)在接近热电池极限温度条件(550 ℃,放电负载为3.0 Ω)下放电对电解质的热稳定进行测试,其结果如图4所示。由图3可知,35% MgO在42 s时单元电池发生短路,通过放电结束后对单元电池的观察,短路原因为电解质外流使正负极接通,因此35% MgO作为电解质流动抑制剂不能满足热电池在较高温度的正常工作需求,而其他几种配比的抑制剂均无短路现象出现,尤以氧化铝的性能突出,在Al2O3和Al2O3*加入量为25%时即可达到50% MgO添加量的效果,进一步体现出氧化铝作为电解质流动抑制剂的优势。
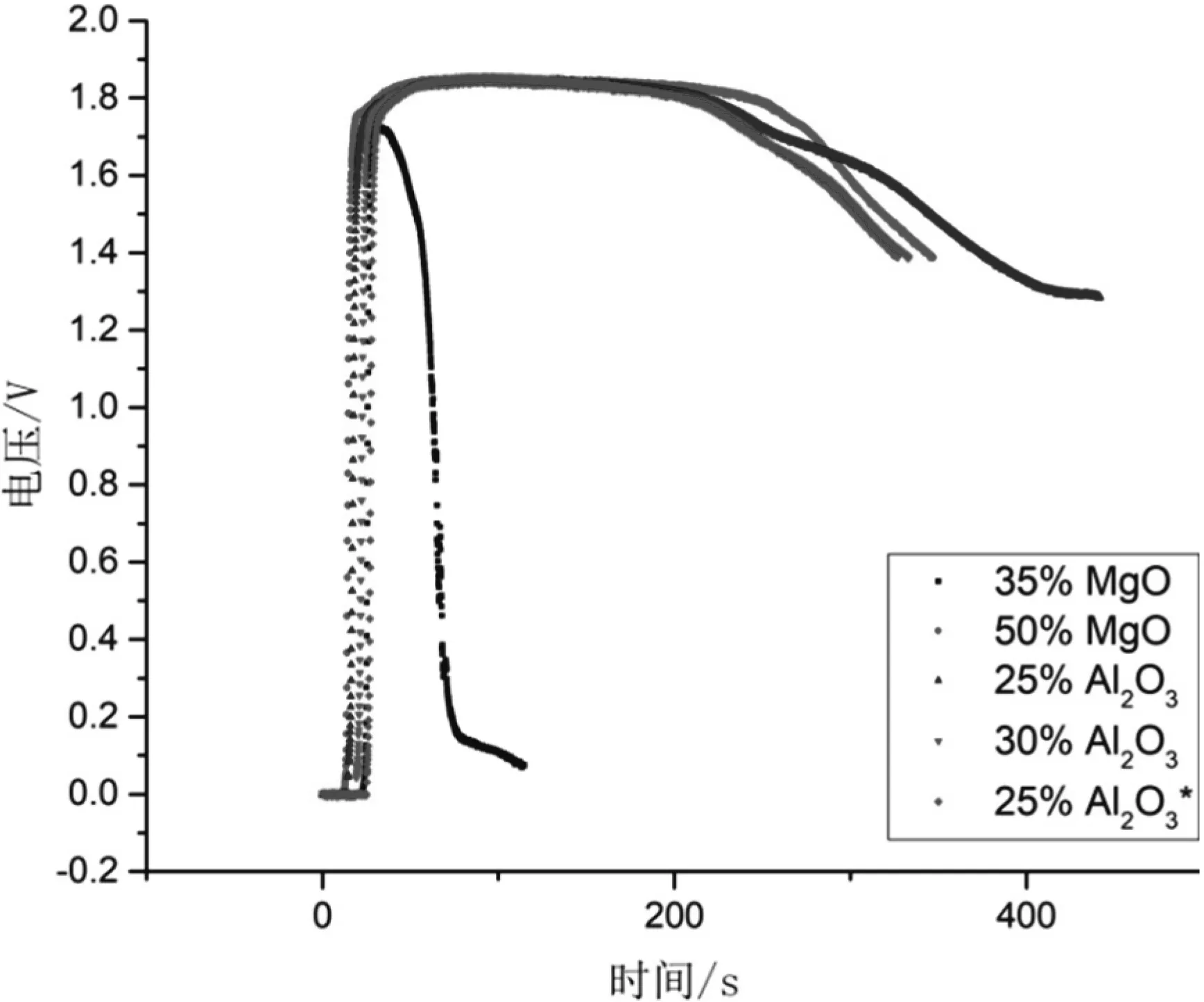
图4 氧化镁、氧化铝在3.0 Ω、550 ℃条件下的热稳定性曲线Fig.4 Thermal stability curves of magnesium oxide and alumina at 3.0 Ω and 550 ℃.
4 结论
本文针对热电池LiCl-KCl二元电解质,研究了不同添加剂对其流动抑制性能的强弱,在相同的工艺过程及添加比例下,由研究结果发现:
(1)氧化铝的平均粒径、比表面积及堆积密度在作为流动抑制剂方面的性能均优于氧化镁,尤其是将其使用高温电阻炉在800 ℃烧制后性能能更加优良,为其作为热电池电解质流动抑制剂提供了基础理论依据;
(2)通过在不同的负载和温度下单元电池进行放电,可以看出,在Al2O3*加入量仅为25%的情况下,单元电池就可达到以MgO作为流动抑制剂时添加量为50%的效果,说明Al2O3*对电解质的流动抑制能力强于MgO,且氧化铝抑制剂制备电池的电性能满足热电池的使用要求,即氧化铝作为热电池电解质流动抑制剂在热电池中的应用具有相当大的潜力。
