TACE联合微波消融术治疗特殊部位原发性肝癌的临床研究
2021-07-28余海滨
余海滨
(南昌市第九医院肝五科,江西 南昌 330002)
原发性肝癌(primary liver cancer)是临床常见恶性肿瘤之一,其中特殊部位的病灶治疗是临床治疗难题[1]。特殊部位原发性肝癌是指距肝门静脉一、二级分支或肝静脉、下腔静脉主干<5 mm,与肝周围脏器毗邻[2]。临床治疗原发性肝癌多采用手术切除,经肝动脉化疗栓塞(TACE)在临床治疗原发性肝癌具有一定疗效,并得到证实,但治疗特殊部位肿瘤较困难[3-4]。微波消融术是临床治疗原发性肝癌的常用方式,是临床治疗肝癌的有效方式[5]。但目前临床关于TACE联合微波消融治疗特殊部位原发性肝癌的报道较少。基于此,本研究旨在探讨特殊部位原发性肝癌采用TACE联合微波消融术治疗的效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2018年5月至2019年2月本院收治的特殊部位原发性肝癌患者60例,随机分为两组,各30例。对照组男22例,女8例;年龄32~82岁,平均年龄(60.23±5.48)岁;病灶毗邻部位:胆囊5例,肝门部9例,膈肌8例,心脏2例,肠胃3例,大血管3例;Child肝功能分级:A级13例,B级17例。观察组男21例,女9例;年龄33~81岁,平均年龄(60.46±5.74)岁;病灶毗邻部位:胆囊3例,肝门部8例,膈肌9例,心脏4例,肠胃2例,大血管4例;Child肝功能分级:A级12例,B级18例。两组临床资料比较差异无统计学意义,具有可比性。本研究经本院医学伦理委员会审核批准。患者及家属均知情同意并签署知情同意书。纳入标准:均符合《原发性肝癌诊断规范》[6]中关于特殊部位原发性肝癌的相关诊断标准;病灶数量≤3个,或肿瘤单发,最大直径≤5 cm;肿瘤毗邻胆囊、大血管(最短间距≤0.5 cm)、肝门部、膈肌等;患者无法采用外科手术切除肿瘤。排除标准:肿瘤肝外转移;合并其他恶性肿瘤;依从性较差。
1.2 方法 对照组采用TACE术治疗:局麻,采用Seldinger法对股动脉进行穿刺插管,经动脉鞘将5F RH导管送入腹腔动脉干及肠系膜上动脉后进行数字减影血管造影技术(DSA)检查,确定肿瘤供血动脉位置,经导管灌注奥沙利铂100~150 mg,并将吡柔比星混悬乳液与碘化油(1∶1)注入进行栓塞,加固采用栓塞微粒球,并在此采用DSA确定肿瘤血供阻断情况,如阻断后拔出导管,对穿刺点进行按压止血,加压包扎。观察组采用TACE联合微波消融术,TACE术同对照组,术后1~2周进行微波消融术,治疗前禁食禁饮8 h,采用局麻与静脉辅助麻醉,超声引导下进行微波消融术,消融肿瘤顺序为先深后浅,特殊高风险区域病灶靠近重要部位处应消融至边缘。对靠近膈顶受肺气干扰的病灶可使用人工胸水,待肿瘤清楚显影后行消融治疗。根据肿瘤情况选择功率,多为40~60 W,多以40 W为主,作用时间3~8 min。术后20 min复查超声,若病灶区域仍有残留则再次补充消融治疗。两组术后均随访1年。
1.3 观察指标 ①比较两组临床疗效,术后4周复查,根据实体瘤mRECIST评价标准[7]评估肝癌局部疗效:完全缓解(complete response,CR),病灶完全消失,且维持4周以上;部分缓解(partial response,PR),患者病灶最大直径减少>50%;疾病稳定(stabledisease,SD):患者最大直径病灶减少25%~50%,且4周以上无新病灶出现;疾病进展(progressive disease,PD):患者最大直径病灶增加25%以上,或出现新病灶。总有效率=(CR+PR+SD)/总例数×100%。②比较两组并发症发生情况,包括恶心、呕吐、肝区疼痛、发热、肝功能异常。③术后随访6个月、1年,比较两组生存率。
1.4 统计学方法 采用SPSS 25.0统计软件进行数据分析,计数资料以[n(%)]表示,比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组治疗总有效率为96.67%,高于对照组的73.33%,差异有统计学意义(P<0.05),见表1。

表1 两组临床疗效比较[n(%)]Table 1 Comparison of clinical efficacy between the two groups[n(%)]
2.2 两组并发症发生率比较 两组恶心呕吐、肝区疼痛、发热、肝功能异常发生率比较差异无统计学意义,见表2。
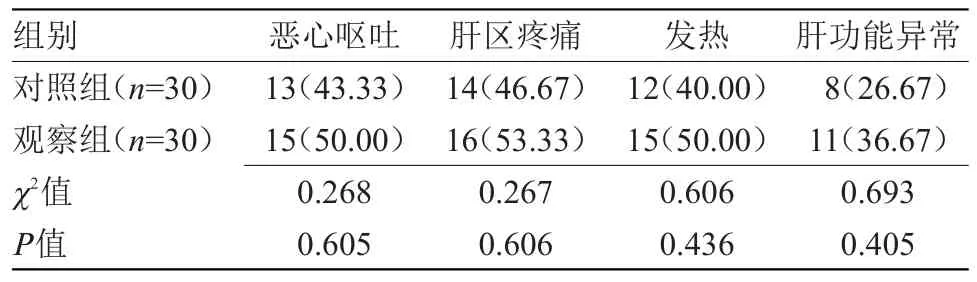
表2 两组并发症发生率比较[n(%)]Table 2 Comparison of the incidence of complications between the two groups[n(%)]
2.3 两组生存率比较 术后6个月、1年,观察组生存率均高于对照组,差异有统计学意义(P<0.05),见表3。
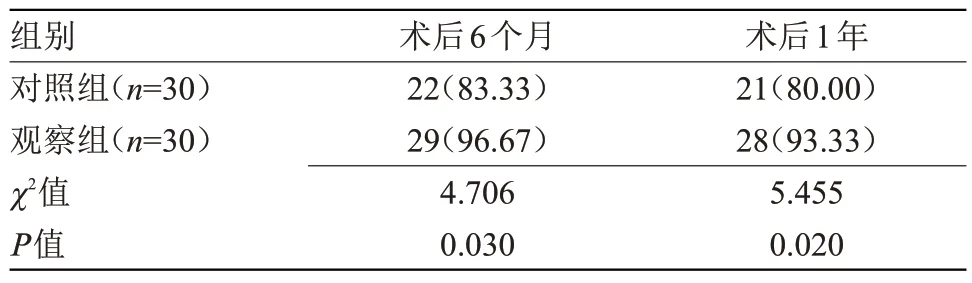
表3 两组生存率比较[n(%)]Table 3 Comparison of survival rates between the two groups[n(%)]
3 讨论
TACE是临床治疗肝癌的常用手术方式,通过股动脉穿刺将化疗药物及栓塞剂注入肿瘤血管及肿瘤供血动脉,进而杀死肿瘤,具有一定的微创效果,有利于患者术后恢复,且可重复操作[3,8]。但患者的肿瘤供血来源、肿瘤位置等因素影响TACE疗效[9]。因此,仅采用TACE治疗特殊部位肝癌患者治疗效果不理想,因此,需配合其他治疗方式进行治疗[10]。微波消融术是临床常用于治疗肝癌的微创治疗方式,且相关研究[11]指出,微波消融术可有效治疗毗邻重要器官的肝癌。
本研究结果显示,观察组治疗总有效率高于对照组(P<0.05);术后随访6个月、1年,观察组生存率均高于对照组(P<0.05);两组恶心呕吐、肝区疼痛、发热、肝功能异常发生率比较差异无统计学意义。表明特殊部位原发性肝癌患者采用TACE联合微波消融术治疗效果显著,可明显提升生存率。TACE可栓塞患者的肿瘤动脉血供,减轻血液循环产生的热针效应,扩大消融范围[12]。而TACE术后进行微波消融术,可同时进行多针消融、病灶温度较高,且受血流散热的影响较小,可增强杀死肿瘤的效果;还可清除TACE术后残留的肿瘤组织,直接覆盖消融血供不足的肝癌,提升清除效果。同时,TACE联合微波消融可有效减少化疗药物用量,减少对肝功能的损伤,利于患者术后肝功能恢复[13]。此外,TACE后患者的肿瘤血供减少,降低微波消融术时的病灶及周围血管产生的热效应,其还可直接损毁TACE后形成的细小新生血管及微小病灶,有效预防残余病灶。相关研究[14]指出,一般情况下,TACE后进行微波消融术,要求消融范围至少为0.5~1.0 cm,但由于有效距离<0.5 cm的特殊部位肿瘤,应消融至肿瘤边缘,布针方式应谨慎选择,微波消融范围采用椭圆形区域,因此,对血管及胆囊旁边的病灶进针应与邻近组织长轴方向尽可能一致,但如微波针需要进行垂直进针,应将针尖贴紧胆囊或血管壁,以不刺破原则进行进针。鉴于本研究样本量有限,随访时间较短,后期应加大样本量,延长随访时间,进一步分析TACE联合微波消融术对特殊部位原发性肝癌患者的效果。
综上所述,TACE联合微波消融术治疗特殊部位原发性肝癌患者效果显著,可明显提升生存率。
