基于SERS技术快速检测“瘦肉精”硫酸特步他林
2021-07-27李志成郑晓冬刘雪梅闫新焕曹宁周大森宋烨
李志成,郑晓冬,刘雪梅,闫新焕,曹宁,周大森,宋烨
(中华全国供销合作总社济南果品研究院,山东济南 250014)
“瘦肉精”是一类具有相似化学结构物质的统称,属于苯乙醇胺类,都具有苯乙胺结构,根据含取代基的不同可进一步分为三种,即苯胺型、苯酚型和苯二酚型。硫酸特步他林(TS),又名间羟舒喘灵(分子式(C12H19NO3)2·H2SO4),属于苯二酚型β受体激动剂类物质,是医疗领域用于治疗哮喘、哮喘型支气管炎以及慢性支气管炎的有效药物,由于和臭名昭著的瘦肉精盐酸克仑特罗同属于肾上腺素受体激动剂类物质,具有增加瘦肉率,降低骨骼肌脂肪含量的功效,因此被非法添加在动物饲料中,消费者食用该类饲料喂养的动物产品后,会出现肌肉振颤、心慌头疼、恶心呕吐等不适症状,特别是对具有高血压、心脏病、糖尿病、等基础类疾病的消费者危害更大,严重者可导致死亡。农业部等国家部委先后下发文件,命令禁止使用β激动剂类药物作为兽药和饲料添加剂,并加大了对盐酸克仑特罗、莱克多巴胺和沙丁胺醇等常见瘦肉精的监管力度,但受到利益驱使,仍有不法养殖户违禁使用硫酸特步他林代替盐酸克仑特罗加入饲料中企图逃避监管[1]。
目前,我国已制定发布β受体激动剂检测方法标准共14个。其中包括HPLC法(1项)、LC-MS/MS法(6项)、GC-MS法(6项)、ELISA法(1项)及胶体金试纸条法(1项)。其中液相色谱串联质谱法(LC-MS/MS)及气相色谱串联质谱法(GC-MS)是我国官方检测β受体激动剂的半确证和确证方法[2],该方法虽然具有精密度高和灵敏度高的优点,但样品前处理方法较复杂、耗时长,设备昂贵操作难度大[3]。难以满足现场大量样品的筛查要求。酶联免疫法(ELISA)虽然可以在一定程度上克服上述缺点,但易受多种因素影响,出现假阳性结果,干扰检测准确性。
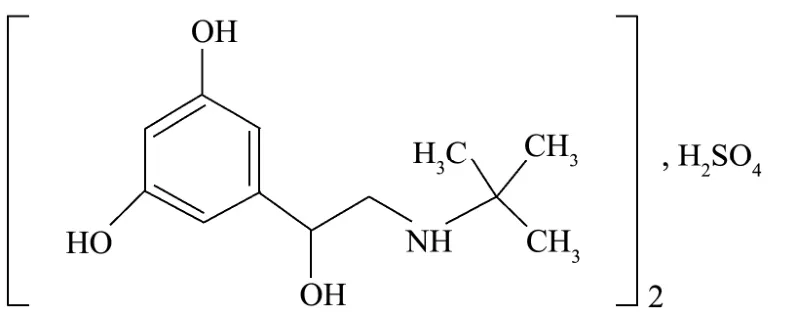
图1 硫酸特步他林结构式图Fig.1 Structural diagram of terbutaline sulfate
SERS技术具有样品制备前处理简单、便于携带、高通量、检测快的特点,目前已经在食品以及农产品农药残留的快速检测中得到应用。本文基于表面增强拉曼光谱技术(SERS)快速检测水溶液、尿液中的硫酸特步他林,为瘦肉精的现场快速检测打下了良好的基础。该方法重现性良好,检测时间短,设备便于携带,检测时间和经济成本低,能够满足牲畜养殖现场的快速筛查使用[4-6]。
1 实验部分
1.1 仪器与试剂
OPAL-3000型便携式拉曼光谱仪(激发功率400 mW,激发光785 nm,分辨率4.5 cm-1),英国Metage公司;透射电镜(H7650),日本日立公司;电磁加热搅拌器(最大转速:1400 r/min;转速精度:±1%)德国Heidolph MR Hei-End。
硫酸特步他林(TS)(C12H19NO3)2·H2SO4,99.9%,中国药品生物制品检定所;氯酸金(HAuCl4·4H2O,99.9%)、柠檬酸三钠(Na3C6H5O7·2H2O,99.8%)、硝酸银(AgNO3),国药集团化学试剂北京有限公司。
1.2 金溶胶的制备
参考杨德红[7]柠檬酸钠还原法制备金溶胶的方法:准确称取10 mg氯金酸粉末,加入少量去离子水将其溶解,然后移至100 mL容量瓶中,再用去离子水定容至100 mL,制成浓度为10-4g/mL的氯金酸溶液备用。
将圆底烧瓶中加入氯酸金溶液25 mL。加热圆底烧瓶,待氯金酸溶液沸腾后,缓慢添加170 mmol/L柠檬酸钠溶液0.11 mL。滴加完成后继续磁力搅拌使两种物质能够充分反应,保持加热状态使得溶液微沸20 min,待溶液颜色变为紫红色时停止加热。制得的胶体金溶液置于4 ℃的冰箱里避光保存备用。
1.3 银溶胶的制备
参考许丽梅[8]等人的制备方法,精确称取精确称取36 mg的硝酸银试剂,用去离子水定容至200 mL制成硝酸银溶液,将配置好的硝酸银溶液置于三孔圆底烧瓶内,在磁力搅拌器上不断搅拌并将其加热至微沸状态。快速添加4 mL 1%柠檬酸钠水溶液,保持沸腾状态,继续加热搅拌60 min,然后冷却至常温待用。
1.4 样品的制备
硫酸特步他林水溶液的制备:用去离子水溶解硫酸特步他林(TS)标准品配置成10 mg/mL水溶液,量取4 mL转移至石英比色皿中。
尿液中硫酸特步他待测样品的制备:准确量取银纳米颗粒溶胶1 mL,和待测尿样1 mL,置石英比色皿中,用稀硝酸调至pH 5.2,加入氯化钠8.775 mg作为凝聚剂,分别加入浓度为1 mg/L、3 mg/L、5 mg/L、7 mg/L的硫酸特步他林水溶液2 mL配置成不同浓度梯度的硫酸特步他林尿液溶液待测样。
1.5 光谱检测与数据处理
拉曼光谱设置检测条件为激光功率为400 mW,光谱范围是500~2000 cm-1,扫描时间60 s,连续扫描3次获得稳定光谱。使用仪器配套的essential FTIR数据处理软件对得到的拉曼光谱进行处理,获得清晰的拉曼光谱图并进行数据分析。
1.6 建立标准曲线
经过方法优化后,在最优实验条件下,获得梯度浓度的硫酸特步他林拉曼谱图。以标准硫酸特步他林溶液的浓度为横坐标,表面增强拉曼光谱特征峰信号强度为纵坐标建立线性回归曲线。
2 结果与讨论
2.1 金溶胶和银溶胶的电镜表征
从纳米颗粒形态方面进行观察和分析,使用电子显微镜透射法(TEM)对所制备的金溶胶和银溶胶进行表征,观察纳米颗粒粒径大小、形状和分布情况。结果如图3、图4所示。结果显示在20万倍电子显微镜放大条件下,金溶胶中颗粒形状不如银溶胶规则,金溶胶中既有球形颗粒也有棒状颗粒的出现。银溶胶颗粒主要呈球形,颗粒大小和分布较为均匀,颗粒直径大多在30~40 nm之间,因此判断银溶胶有更好的吸附放大效应。

图3 银溶胶透射电镜图Fig.3 TEM image of silver colloids
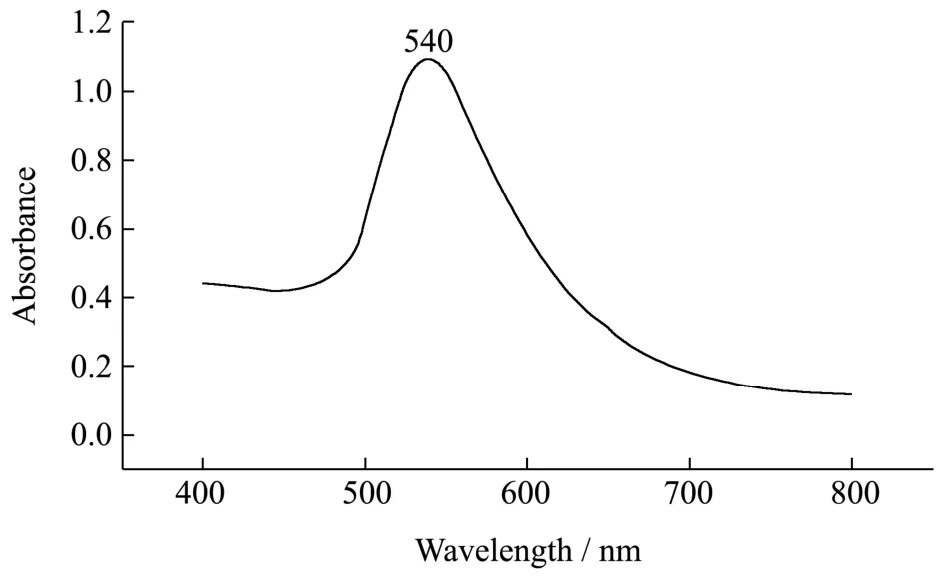
图4 金溶胶紫外-可见吸收光谱图Fig.4 UV-Vis spectrum of gold colloidal

图2 金溶胶透射电镜图Fig.2 TEM image of gold colloids
2.2 银溶胶的紫外-可见吸收光谱
金属纳米粒子在紫外-可见吸收光谱中会发生共振这种共振现象具有产生紫外光谱带间跃迁的特殊性质,表现为紫外可见区出现特定的吸收峰。该吸收光谱的峰型与金属颗粒的大小、形状以及分布情况有关。最大紫外吸收峰的位置与纳米颗粒的粒径大小具有对应关系,金属纳米颗粒的粒径大小与吸收峰波长的长度正相关,即最大吸收峰波长越长说明金属颗粒的粒径越大。这时因为分子轨道能级之间的宽度即能隙会随颗粒直径的增大而减小决定的,粒径越大在紫外-可见吸收光谱上的反应是光吸收带向短波方向移动[9-11]。
峰型与峰宽则能反应出纳米颗粒溶胶的均匀性以及分别情况。一般来说,半宽峰偏窄说明粒子的粒径分布也较窄,意味着纳米颗粒大小较均匀。同时颗粒大小不均匀还会影响吸收谱线的形状,反应在形状上为长波长方向出现吸收拖尾[12,13]。
图4 是金溶胶的紫外-可见吸收光谱图。金溶胶的吸收峰在540 nm处说明其金属颗粒大于银溶胶,与电镜观察结果一致。金溶胶的的吸收曲线对称性不如银溶胶,说明粒子形状不均匀,正如电镜观察的球型、棒状颗粒对应。金溶胶紫外-可见吸收光谱存在拖尾现象表示其颗粒均匀度不佳。
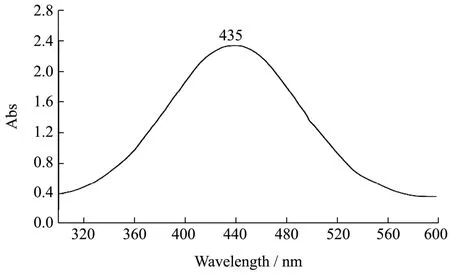
图5 银溶胶紫外-可见吸收光谱图Fig.5 UV-Vis spectrum of silver colloidal
通过观测银溶胶的紫外-可见吸收光谱图可以发现,银纳米颗粒溶胶在435 nm处出现紫外吸收峰,且该峰对称性好,半峰宽较窄,无拖尾现象。说明该溶胶大小较为均一,分布均匀。该结果与电镜结果相互印证。因此最终选择银溶胶作为表面增强剂对硫酸特步他林进行研究。
2.3 溶胶的稳定性
通过对制备出的金属溶胶进行存放观察实验发现,银溶胶不耐保存,银胶在室温条件下3 d开始出现颜色和形态改变,7~10 d内沉降失活。银溶胶在4 ℃冰箱冷藏存放21 d后产生沉淀现象。金溶胶性质较为稳定,在4 ℃的冰箱内冷藏存放90 d颜色和形态没有改变。这是由于制备过程中加入的柠檬酸三钠中的柠檬酸根离子有三个羧基基团对银粒子的表面吸附作用远强于金粒子[14]。
金属溶胶的存放温度和时间对其稳定性产生重要影响,常温下金属颗粒之间运动频率高,产生碰撞的几率大,导致出现聚集沉淀现象,不利于胶体的分散。存放时间过长导致溶胶的稳定性下降,产生自凝聚现象。因此,金溶胶能较长时间保存,银溶胶不易长时间保存,制备后低温保存尽快使用。
2.4 硫酸特步他林水溶液的拉曼光谱
设置检测条件为激光功率400 mW,拉曼光谱扫描范围500~2000 cm-1,扫描时间60 s,连续进行3次,得到稳定光谱。采用同样条件获得去离子水的稳定拉曼光谱,结果如下:
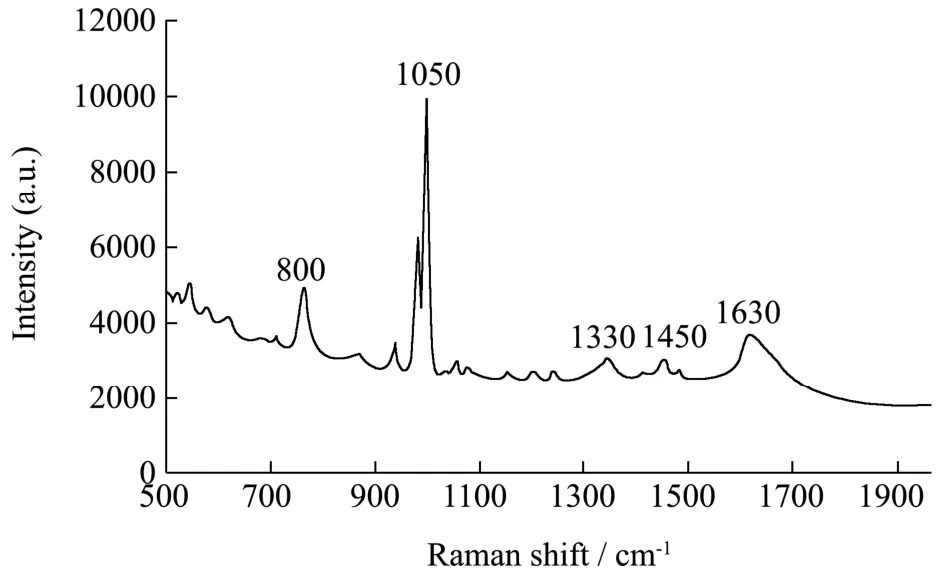
图6 硫酸特步他林水溶液拉曼光谱Fig.6 Terbutaline sulfate Raman spectroscopy
观察发现硫酸特步他林水溶液的在800 cm-1、1050 cm-1、1330 cm-1、1450 cm-1、1630 cm-1处出现五个明显的拉曼信号。去离子水在1630 cm-1处出现拉曼信号峰,因此扣除去离子水在1630 cm-1处出现拉曼信号,硫酸特步他林的拉曼信号峰应为800 cm-1、1050 cm-1、1330 cm-1、1450 cm-1四处。其中800 cm-1、1450 cm-1、1050 cm-1三处是由β受体激动剂类药物分子共有特征结构苯乙胺结构存在导致,1330 cm-1处拉曼特征峰是由于硫酸特步他林苯环上的C=C键拉伸振动引起的,可作为识别硫酸特步他林的特征峰进行分析
[15,16]。
由图7观察可知,银纳米溶胶与β受体激动剂混合后相比金纳米溶胶混合产生更强的表面增强效果。这是因为在可见光区内,金纳米的表面增强因子比银纳米的小,根据实验发现银纳米溶胶与目标分子结合后往往能产生更为强烈的共振现象,也就是说银溶胶与金溶胶相比具有更强的表面增强活性。这与已经知道的金、银溶胶放大其他待测物分子结果一致。说明在通常条件下银溶胶在与目标分子结合后往往能表现出更强的放大效果,是更为合适的表面增强剂。
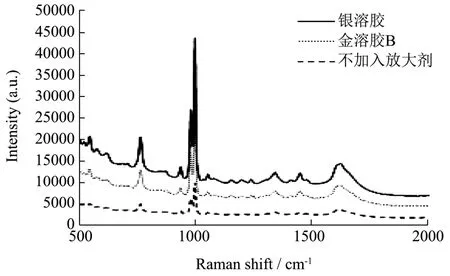
图7 金、银溶胶与TS溶液混合Fig.7 Gold, silver colloids add TS
2.5 尿液中硫酸特步他林的拉曼光谱检测
拉曼光谱对尿液中硫酸特步他林的检测无需前处理,测样速度快,仅需后期在图谱处理时扣除尿液拉曼信号的影响,图8为尿液经过离心后直接进行拉曼光谱检测的图谱。
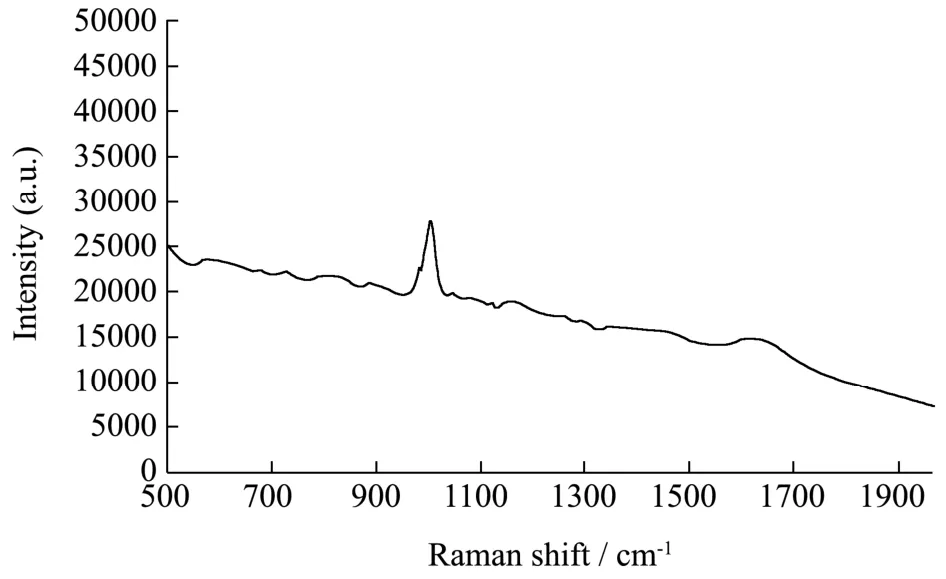
图8 尿液拉曼光谱Fig.8 Raman spectra of urine
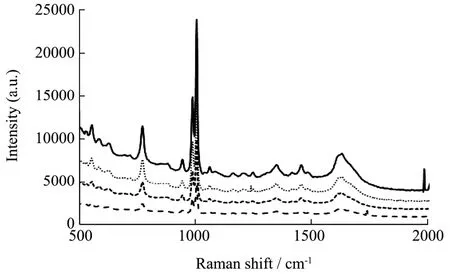
图9 梯度浓度尿液中硫酸特步他林的SERSFig.9 SERS spectra of TS in urine
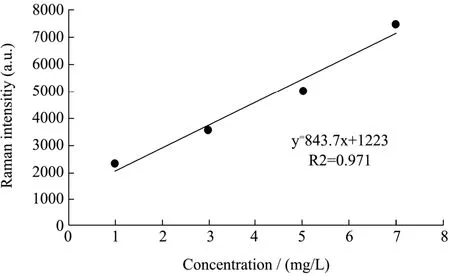
图10 尿液中硫酸特步他林标准曲线Fig.10 Calibration curve of TS in urine
由图8可知尿液仅在1005 cm-1附近出现拉曼特征峰,其他拉曼位移处无明显拉曼特征峰,因此对检测样品干扰小,此时空白尿液在1005 cm-1附近出现的拉曼峰是由于尿液中尿素分子中C-N键伸缩振动引起的。
对位于1330 cm-1处的特征峰强度硫酸特步他林尿液溶液浓度的变化进行线性拟合。
尿液中硫酸特步他林的浓度与拉曼特征峰信号强度之间存在良好的线性关系,硫酸特步他林在浓度1~10 mg/L范围内,满足回归方程Y=843.75X+1223.80,相关系数为R2=0.97。
为了探究尿液中硫酸特步他林的检出限,继续稀释尿液中硫酸特步他林后进行表面增强拉曼上机检测。当溶液浓度为0.5 mg/L时,硫酸特别他林的拉曼特征峰信噪比大约达到3,故最低检出限为0.5 mg/L。
为了验证该方法的可靠性,取100 mL空白尿液添加盐酸特步他林,添加水平为0.5 mg、1 mg、10 mg 3个浓度水平进行加标回收实验,每个添加浓度在前述的最佳表面增强拉曼光谱条件下进行SERS扫描,每个加标浓度重复测定3次,测定测定结果如表1。
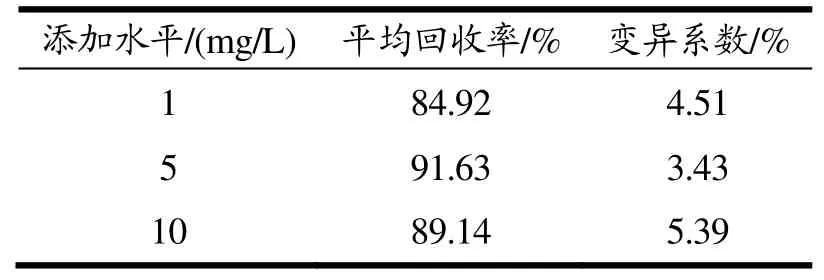
表1 回收率和精密度测定结果Table 1 The result of recoveries and precision tests (n=5)
从表中数据可以看出,回收率可满足样品的分析要求。
2.6 SERS样品测定结果与HPLC检测方法的比较
为验证本试验建立的SERS方法对硫酸特步他林的快速检测方法的可靠性,分别采用本法和HPLC法对目标物进行检测,并加以比较,检测结果如表2。
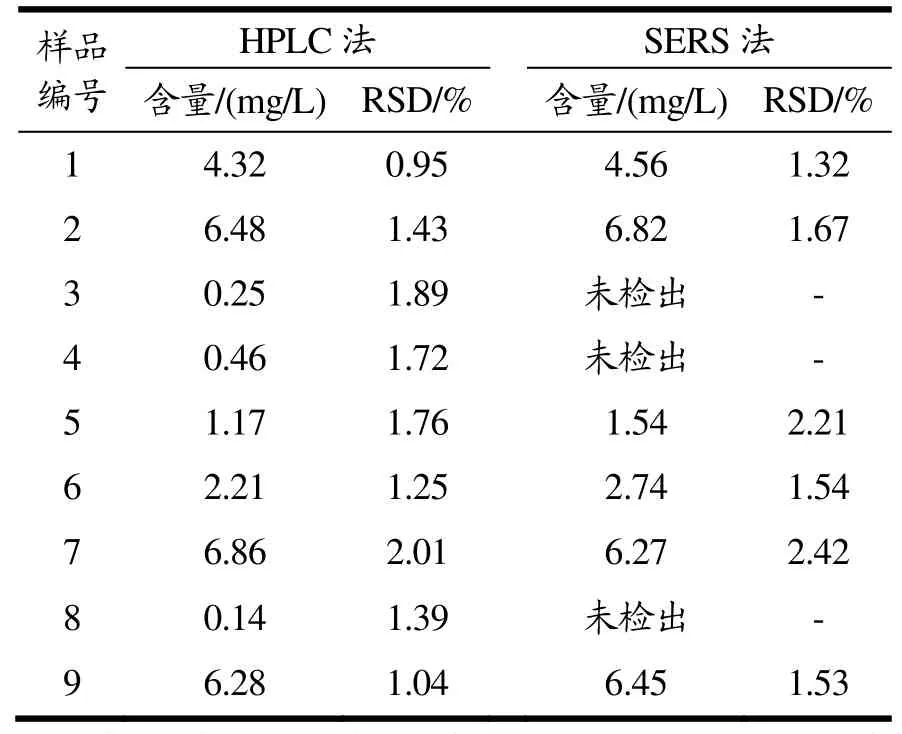
表2 SERS与HPLC检测结果对比Table 2 Comparison of results between SERS and HPLC methods
由表2结果可以得出结论如下,用SERS方法检测九个盲样中硫酸特步他林的含量结果与HPLC测得的结果基本相符,具有较高的可信度,其中3号、4号、8号样品由于浓度低于SERS方法检出限的原因,导致表面增强拉曼光谱方法没有检出,说明传统实验室大型仪器HPLC在痕量检测方面优于SERS检测方法,通过对比两种检测方法可以得出在一定浓度范围内SERS检测方法与HPLC测得的结果基本相符。
如果考虑两种检测方法的前处理过程,HPLC方法前处理复杂。从前处理到上机检测分析所需时间在1 h以上,且需要在实验室环境下进行。而SERS方法所需时间小于15 min,且不受场地限制。特别是在大量样品需要检测的情况下,SERS方法的优势会更加明显,相对于HPLC方法,SERS方法对操作人员要求低、检测时间短、检测效率高,能达到快速分析检测的目的。前处理操作方面,高效液相色谱法需要先用有机溶剂多次萃取,然后将溶剂蒸干,最后溶解过膜后上样,步骤繁琐,耗时长。因此SERS方法在样品量大,检测环境受限时优势明显,适合用于对大量样品的筛查。
3 结论
本实验开发一种利用表面增强拉曼光谱技术快速检测硫酸特步他林的方法。首先制备了金溶胶和银溶胶两种表面增强剂。对两种增强剂进行表征和比较分析,然后选择银溶胶作为活性基底,对水溶液和尿液中的硫酸特步他林进行检测,获得800 cm-1、1050 cm-1、1330 cm-1、1450 cm-1处作为硫酸特步他林拉曼信号特征峰。进而建立表面增强拉曼光谱法检测硫酸特步他林的方法,结果显示在浓度1~10 mg/L范围内,满足回归方程Y=843.75X+1223.80,相关系数为R2=0.97。该方法具有快速、准确、无损、操作简便等优点,为水溶液、尿液中瘦肉精成分硫酸特步他林的现场快速检测奠定了良好的基础。
