牛乳酪蛋白源ACE抑制肽对大鼠的降血压作用
2021-07-27刘飞苗建银杨余语何泽琪乔子骄刘果杜洁宁德山曹庸
刘飞,苗建银,杨余语,何泽琪,乔子骄,刘果,3,杜洁,宁德山,曹庸
(1.广州绿萃生物科技有限公司,广东广州 510663)(2.华南农业大学食品学院,广东省功能食品活性物重点实验室,广东省天然活性物工程技术研究中心,广东广州 510642)(3.华南农业大学园艺学院,广东广州 510642)(4.无限极(中国)有限公司,广东广州 510665)
高血压指动脉血压持续升高,是心血管疾病中极为危险的因素[1],高血压会增加冠心病、中风的发病率[2],在国内成年人高血压发病率高达31%~35%,但在患病人群中自身知晓率、治疗率较低[3-5]。据全国卫生部门统计资料显示,我国现有高血压病患者已超过1.6亿人,每年新增300万人以上。高血压的发病率已经达到了23.2%。尤其北方高血压发病率特别高,北方地区高血压的发病率达到了32%~33%。血管紧张素转化酶抑制肽(Angiotensin I-converting enzyme inhibitory peptides,ACEI),也称为降血压肽,是通过抑制血管紧张素转换酶(Angiotensin-I converting enzyme,ACE)活性从而抑制血管紧张素Ⅰ转为血管紧张素Ⅱ,以此达到降低血压[6-8]。目前用于临床治疗高血压和心脏衰竭的合成ACE抑制剂已有许多,如卡托普利、培哚普利、依那普利、赖诺普利和雷米普利,但是,这些药物可能产生低血压、钾水平上升、肾功能降低、咳嗽、味觉异常等副作用,不适长期服用[9-16]。而食物蛋白来源的ACE抑制肽通常由蛋白酶在温和条件下水解蛋白质而获得[17-19]。而食物蛋白来源的ACE抑制肽通常由蛋白酶在温和条件下水解蛋白质而获得,食用安全性高,无毒副作用,对高血压患者可以起到降压作用而对血压正常者无降压作用,同时还具有免疫调节、减肥和易消化吸收等功能,有着合成化学药物不可比拟的优越性[20-36]。
本文利用牛乳酪蛋白为原料,经过胰蛋白酶水解、超滤膜处理得到分子量小于5000 u的降血压肽(ACE抑制肽),通过自发性高血压大鼠(SHR)检测ACE抑制肽的降血压功效。酪蛋白为重要的乳源蛋白,原料安全、无毒副作用,有较高的营养价值,具有良好的研发背景,本文为酪蛋白的深加工和具有降血压作用的乳源活性肽进一步应用提供参考。
1 材料与方法
1.1 材料、试剂与仪器设备
1.1.1 原料与试剂
降血压肽(ACE抑制肽),批次20190326J,纯度30%,广州绿萃生物科技有限公司提供。
1.1.2 主要仪器设备
BS223S天平,德国Sartorius公司;BP-2010A无创血压计,北京软隆生物技术有限公司。
1.1.3 实验动物
(SD)血压正常大鼠,SPF级,8只,雄性;实验开始时动物体重:195.6~216.8 g,广东省医学实验动物中心,广东省实验动物质量合格证号:44007200009225;动物许可证号:SYXK(粤)2013-0002。
(SHR)自发性高血压大鼠,SPF级,40只,雄性;实验开始时动物体重:189.40~224.00 g,北京维通利华实验动物技术有限公司,北京市实验动物质量合格证号11400700044184;(动物许可证号:SCXK(京)2012-0001。
1.2 实验方法
1.2.1 剂量设计依据[35]
根据《保健食品功能评价程序和检验方法规范》(2003年版)进行剂量设计,以人推荐剂量的5倍作为大鼠给予受试产品的剂量(低剂量每天115 mg/kg、中剂量1165 mg/kg、高剂量2335 mg/kg)。根据人服用卡托普利的剂量,换算大鼠等效剂量作为卡托普利的大鼠给药剂量(每天3.94 mg/kg,用于2周内给药,15.75 mg/kg,用于2周后给药)。
1.2.2 药物配制和给予样品方法[31-36]
分别配置233.50 mg/mL(高剂量)、116.50 mg/mL(中剂量)、11.50 mg/mL(低剂量)的ACE抑制肽溶液。前2周阳性对照组剂量:卡托普利浓度为0.39 mg/mL。第3~4周阳性对照组剂量:卡托普利浓度为1.58 mg/mL。
将检疫合格的8只SD血压正常大鼠作为正常对照高剂量组(给予ACE抑制肽高剂量干预),8只/组;另将检疫合格的40只SHR自发性高血压大鼠按照血压基础值随机分为模型对照组、ACE抑制肽高剂量组、中剂量组、低剂量组、卡托普利阳性对照组,8只/组。所有大鼠按照1 mL/100 g给予样品,1次/d,连续30 d。
1.2.3 标本的采集与处理[21,31-36]
1.2.3.1 尿液收集
实验结束前1 d收集12 h尿液。
1.2.3.2 血清采集
实验结束当天,麻醉处死大鼠,腹主动脉取血,离心取血清进行相关测定。
1.2.4 检测指标
1.2.4.1 观察
从实验开始至实验结束每天观察动物1次。
1.2.4.2 体重
从实验开始至实验结束每周称量大鼠体重1次。
1.2.4.3 血压、心率测定
从实验前及实验开始后每周测定大鼠血压、心率1次[21]。
1.2.4.4 采用ELISA测定
试剂盒检测血清血管紧张素Ⅱ浓度(Angiotensin-Ⅱ,ANG-Ⅱ)、一氧化氮(Nitric Oxide,NO)、内皮素(ET)、降钙素基因相关肽(CGRP)水平[21]。
1.2.4.5 采用生化分析仪测定
血清中血糖(GLU)、K+、Na+、Ca2+、总胆固醇(CHOL)、甘油三脂(Triglyceride,TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(Low density lipoprotein cholesterin,LDL-C)、血尿酸(UA)水平检测[34]。
1.2.4.6 尿微量白蛋白检测
测定收集尿液中尿微量白蛋白(ALB)的含量[21]。
1.2.5 统计分析
采用SPSS 13.0软件对数据进行统计分析;计量资料以均数±标准差(±s)表示,以α=0.05为检验水平;采用重复测量资料方差分析方法对重复测量的数据进行统计分析;采用单因素方差分析方法对单次测量的数据进行统计分析。
2 结果与讨论
2.1 体重
各组大鼠的体重随着时间的变化而增加(表1)。投喂4周后,模型对照组(252.90 g)、阳性组(254.40 g)、ACE抑制肽低(245.70 g)、中(248.00 g)和高剂量组(252.90 g)的体重均无统计学差异,并且在各测定时间点的体重均无统计学差异(p>0.05)。说明本实验所用的大鼠符合建动物模型条件。
表1 干预30 d大鼠的体重变化Table 1 The weight change of rats after 30 days of intervention (± s , n=8, ♂, g)

表1 干预30 d大鼠的体重变化Table 1 The weight change of rats after 30 days of intervention (± s , n=8, ♂, g)
注:与模型对照组相比,“**”p<0.01。
?
表2 干预大鼠前和干预后的血压和心率Table 2 Blood pressure and heart rate before and after intervention in rats (± s , n=8, ♂)

表2 干预大鼠前和干预后的血压和心率Table 2 Blood pressure and heart rate before and after intervention in rats (± s , n=8, ♂)
注:与模型对照组相比,“*”p<0.05,“**”p<0.01。下表同。
?
2.2 血压和心率
在观察期内,模型对照组的血压(包括收缩压、舒张压和平均压)始终高于正常对照高剂量组,具有统计学差异(p<0.01),说明本实验所用SHR大鼠是良好的高血压动物模型。给予样品前,ACE抑制肽低、中、高剂量组和阳性对照组的基础血压(包括收缩压、舒张压和平均压)、心率与模型对照组比较均无统计学差异(p>0.05)。干预30 d后,模型对照组心率(次/分)、收缩压(mm Hg)分别是446、186,ACE抑制肽中、低剂量组和阳性对照组的心率(次/分)分别398、402、395,与模型对照组相比,差异具有统计学意义(p<0.05,p<0.01);ACE抑制肽高、低剂量组和阳性对照组的收缩压(mm Hg)分别为175、175、172,与模型对照组相比,差异具有统计学意义(p<0.01),说明ACE抑制肽能有缓解大鼠心率过速[33],且不同剂量的ACE抑制肽对SHR大鼠初始血压均有显著降低效果[32];正常对照高剂量组在干预前后收缩压分别为124 mm Hg、122 mm Hg,无明显差异,说明本实验的ACE抑制肽对血压正常的大鼠无降压作用,与夏磊等人研究结果一致[20]。
2.3 血清检测及尿液检测
除了收缩压、心率是判断高血压的依据,血清中的ANG-II、ETI、NO等指标浓度变化同样也会引发高血压病。本实验给予样品30 d后,与模型对照组相比,ACE抑制肽高剂量组血清的CGRP(10.09 pg/mL)与模型对照组(7.47 pg/mL)相比,明显升高(p<0.05);ACE抑制肽高剂量组ET1浓度(8.69 pg/mL)与模型对照组(10.26 pg/mL)相比,明显降低(p<0.05),说明ACE抑制肽可在一定程度上改善肾血管性高血压大鼠血清生化指标,与模型对照组相比,ACE抑制肽高剂量组ALB含量明显升高(p<0.05),说明ACE抑制肽可在一定程度上改善SHR大鼠的肾功能指标[21,34],见表3。
表3 干预后的大鼠血清及尿检结果Table 3 Serum and urine test results of rats after intervention (± s , n=8, ♂)
?
2.4 血生化
由表4可见,给予样品30 d后,与模型对照组相比,ACE抑制肽高剂量组的GLU(6.41 mmol/L)、CHOL(1.13 mmol/L)、HDLC(0.29 mmol/L)、血UA(108.20 μmol/L),具有统计学差异(p<0.05,p<0.01),而TG含量没有统计学差异(p>0.05);阳性对照组的血清TG和血UA浓度都明显升高,具有统计学差异(p<0.05,p<0.01)。这说明在连续灌胃30 d后,ACE抑制肽对血糖、尿酸以及胆固醇有一定控制作用[33]。
表4 干预30 d的大鼠血生化结果Table 4 Blood biochemical results of rats after 30 days of intervention (± s , n=8, ♂)

表4 干预30 d的大鼠血生化结果Table 4 Blood biochemical results of rats after 30 days of intervention (± s , n=8, ♂)
?
2.5 血电解质
由表5可见,给予样品30 d后,与模型对照组血清TCa(2.13 mmol/L)相比,ACE抑制肽高剂量组的血清TCa(2.06 mmol/L)都明显降低,具有统计学差异(p<0.05),而K、Na、Cl和iCa都没有统计学差异(p>0.05),ACE抑制肽通过降低钙离子浓度,降低总钙的浓度,说明ACE抑制肽能促进离子吸收,从而影响血钙的浓度。
表5 干预30 d的大鼠血电解质结果Table 5 Results of blood electrolytes in rats after 30 days of intervention (± s , n=8, ♂)
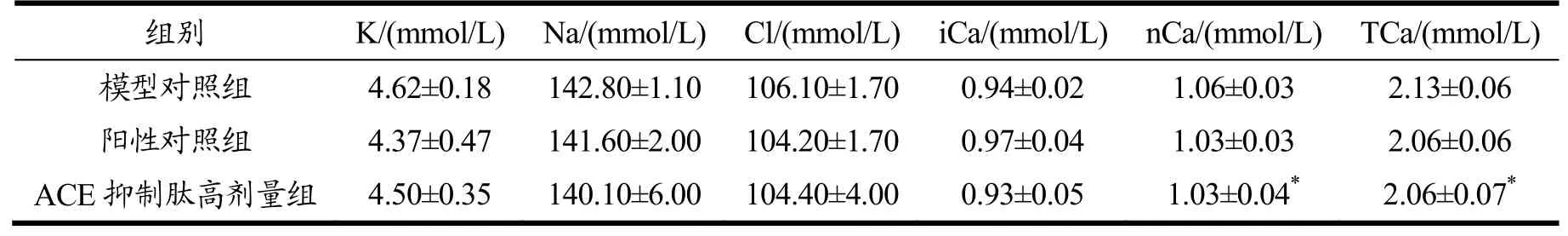
表5 干预30 d的大鼠血电解质结果Table 5 Results of blood electrolytes in rats after 30 days of intervention (± s , n=8, ♂)
?
3 结论
在本实验条件下,干预30 d后,模型对照组心率(次/分)、收缩压(mm Hg)分别是446、186,ACE抑制肽中、低剂量组和阳性对照组的心率(次/分)分别398、402、395,与模型对照组相比,差异具有统计学意义(p<0.05,p<0.01);ACE抑制肽高、低剂量组和阳性对照组的收缩压(mm Hg)分别为175、175、172,与模型对照组相比,差异具有统计学意义(p<0.01),说明牛乳酪蛋白源ACE抑制肽能有缓解大鼠心率过速,并且对SHR大鼠初始血压均有显著降低效果;本实验给予样品30 d后,ACE抑制肽高剂量组血清的CGRP浓度10.09 pg/mL,与模型对照组相比,明显升高(p<0.05);ET1浓度8.69 pg/mL、GLU浓度6.41 mmol/L、CHOL浓度1.13 mmol/L、HDLC浓度0.29 mmol/L、血UA浓度108.2 μmol/L、血清TCa浓度2.06 mmol/L,与模型对照组相比,明显降低(p<0.05),说明ACE抑制肽可在一定程度上改善肾血管性高血压大鼠血清生化指标及肾功能指标。同时对血糖及胆固醇有一定控制作用。ACE抑制肽可能通过升高血液CGRP、抑制ET1、降低血钙水平起到降血压作用。
