双胎妊娠一胎21-三体综合征的妊娠结局
2021-07-23冀清方陈建平邹刚
冀清方 陈建平 邹刚
(同济大学附属第一妇婴保健院 胎儿医学科,上海 201204)
辅助生殖技术的发展和孕妇生育年龄的高龄化增加了双胎和多胎妊娠的发生率。多胎妊娠与母体并发症(如子痫前期等)、胎儿畸形(包括染色体异常)、不良妊娠结局及围产期死亡率发生风险增加相关[1]。双胎产前筛查的方案包括早孕期胎儿颈项透明层厚度(nuchal translucency,NT)、孕妇外周血胎儿游离DNA检测及超声筛查等。对于筛查高危的孕妇需要进行合理的入侵性产前诊断。当介入性产前诊断结果发现双胎之一发生非整倍体异常时,可通过选择性减胎术减去异常胎儿来避免一个严重出生缺陷的胎儿出生。本文对45例双胎之一21-三体综合征的孕妇临床资料进行回顾性分析,着重评估减胎效果及妊娠结局,为进一步临床治疗方案的制定提供参考。
1 资料与方法
1.1 研究对象 回顾性分析2011~2020年在同济大学附属第一妇婴保健院胎儿医学科进行产前诊断咨询,并确诊为双胎之一21-三体综合征的45例孕妇的临床资料,44例为双绒毛膜双羊膜囊双胎(简称双绒双胎),经遗传咨询后均行氯化钾减胎术,1例为单绒毛膜双羊膜囊双胎(简称单绒双胎),自愿放弃选择性减胎并决定继续妊娠。接受减胎的病例均为双绒双胎,减胎指征为双胎一胎为21-三体(或21-三体嵌合型)。提前告知夫妻双方手术相关风险,在无先兆流产、凝血障碍及感染等手术禁忌证的前提下签署选择性减胎手术知情同意书。孕妇的一般资料见表1。

表1 双胎一胎21三体综合征孕妇一般资料
1.2 手术方法
1.2.1 术前准备 术前超声结合羊膜腔穿刺精确标记待减灭胎儿,明确绒毛膜性,确定目标胎儿是否存活,并预估手术路径。完成术前常规检查:血尿常规、凝血功能、肝肾功能、心电图检查及明确血型和排除乙肝、艾滋、梅毒等传染病。
1.2.2 手术步骤 44例减胎病例均为双绒双胎,采取胎儿心脏氯化钾注射法。孕妇取仰卧位,常规腹部消毒铺巾,局部麻醉穿刺部位皮肤。超声显示目标胎儿心脏最大平面,在超声引导下,将21G穿刺针透过孕妇腹壁穿入胎儿心脏搏动处,回抽见心脏血,留取2ml送染色体核型分析(验证),然后快速注入10%KCl 2~6 ml,密切观察目标胎儿胎心情况,确认心脏停跳后,再拔出穿刺针。术中注意监测保留胎儿胎心。
1.2.3 术后处理 ①术后孕妇卧床休息加安胎治疗,注意术后有无腹痛、阴道流液、流血等;②术后1d复查B超,如无异常可出院;定期B超追踪,检查凝血功能,随访有无流产、早产等;③抗生素预防感染,注意外阴清洁,禁止性生活。
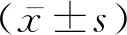
2 结果
2.1 孕妇一般情况 孕妇年龄21~42岁,平均(33.0±4.1)岁,其中≥35岁的孕妇占比33.3%(15/45)。孕妇均为汉族,受孕方式主要为辅助生殖技术(assisted reproductive technology,ART),其中体外受精-胚胎移植(in vitro fertilization/intracytoplasmic sperm injection-embryo transfer,IVF/ICSI-ET) 22例(48.9%),卵胞浆内单精子显微注射技术(intracytoplasmic sperm injection,ICSI)15例(33.3%),自然受孕仅占17.9%。44例为双绒双胎,1 例为单绒毛膜双胎。宫颈长度平均(34.2±8.1)mm,减胎孕周平均为(24.0±3.2)周,选择在17~24周行减胎术的患者比例为54.5%,24~27+6周进行减胎的占45.5%。
2.2 研究病例接受介入性产前诊断的指征 双胎羊膜腔穿刺平均孕周为(19.7±2.9)周,羊水穿刺指征中,无创产前检测(non-invasive prenatal testing,NIPT)高风险最常见,其次为NT增厚、高龄和其他结构异常(如鼻骨缺失、法洛四联征等)。有15例是在外院进行羊穿后发现一胎21-三体,因外院无减胎能力转诊至本院。由于未提供区分胎儿的信息,标记系统不明确,均在本院重做羊穿。1例单绒双胎的羊穿指征是一胎儿颈部水囊瘤。所有的双绒双胎经短串联重复序列(short tandem repeat,STR)验证均为双卵双胎。单绒双胎亦经验证为单卵双胎。表2。

表2 44例双绒双胎一胎21-三体综合征接受羊水穿刺的指征(n=44)
2.3 孕妇及家属的妊娠选择 羊穿结果提示双胎一胎21-三体后,所有的孕妇均接受了遗传咨询,告知21-三体综合征的预后,并提供了继续妊娠、减胎术、引产3个不同选择方案。告知双绒双胎的氯化钾减胎方法和单绒双胎的射频消融术方案。44例双绒双胎病例均接受了氯化钾减胎术。1例单绒双胎因担心射频消融术对另一胎儿的影响,决定不做减胎,顺其自然。
2.4 选择性减胎术后妊娠结局 本研究中44例氯化钾减胎孕妇,手术均一次性成功,术中KCl平均用量为(4.3±1.4)ml。术中没有孕妇出现胸闷气急及心律失常。仅1例术后1周流产,后行引产。术后进行被减胎儿心脏血染色体验证,核型均提示为21-三体,再次确认减灭胎儿为术前标记的目标胎儿。44例减胎孕妇母体无严重并发症,术后保留胎儿活产率为97.7%,预后良好。分娩孕周平均为(36.4±3.7)周,足月产(≥37周)比例为65.9%(29/44);分娩方式主要为剖宫产38例,阴道分娩6例(包括1例引产)。整体新生儿平均出生体重为 (2798.6±673.0)g,Apgar评分均在7分以上,其中4例新生儿出现新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome,NRDS),经积极治疗预后良好。电话随访43例存活儿,身高、体重、智力发育等各项指标均正常。
2.5 不同减胎时机妊娠结局比较 本研究中,17~24周进行选择性减胎术的有24例,其中1例术后1周引产,早产率为16.7%,其中最早分娩孕周为28周,28~34周和34~37周分娩的病例分别为3例(12.5%)和1例(4.2%);24周后进行减胎的早产率为45.0%,其中最早分娩孕周为29周,28~34周和34~37周分娩的病例分别为5例(25.0%)和4例(20.0%)。二者早产率经统计学分析,P=0.04,差异具有统计学意义;经t检验后发现,17~24周和≥24周行减胎术后,分娩孕周和新生儿出生体重的差异性无统计学意义。表3。

表3 不同孕周选择性减胎妊娠结局比较
3 讨论
3.1 双胎一胎21-三体进行选择性减胎临床疗效良好、安全性可靠 21-三体综合征又叫唐氏综合征,是最常见的染色体异常。该缺陷主要是由于第一次或第二次减数分裂过程中21号染色体随机不分离导致的,为导致患儿智力障碍最主要的原因[2]。21-三体患儿会给家庭和社会带来沉重的经济和精神负担,因此必要的产前诊断及有效处理是非常重要的。产前诊断主要包括超声和染色体检查,对于21-三体胎儿的检出率可高达99%。一项研究显示[3],鼻骨发育异常、心脏畸形和羊水偏多与21-三体综合征关联度高,本研究汇总的双胎之一21-三体进行羊水穿刺最主要的指征为NIPT高风险,其次为NT增厚、高龄和其他结构异常(如鼻骨缺失、法洛四联征、足内翻等)。
以往受限于胎儿医学的发展局限性,对于双胎之一非整倍体异常的主要处理原则是引产。随着胎儿医学的发展完善,现在大家对于双胎之一非整倍体胎儿的态度主要有两种,一种是选择性减胎,另一种是继续妊娠。随着技术的逐渐成熟,选择性减胎术妊娠结局良好,已经成为大多数家庭的选择,且符合国家优生优育的政策要求。选择性减胎最初被用来终止受遗传变异影响的胎儿[4],后来发展为以消除多胎妊娠中的一个或多个正常或异常胎儿,同时保证其他胎儿存活。对于双绒双胎,KCl减胎术是最常用的,单绒双胎主要选择射频消融减胎术。对于双胎一胎21-三体几乎多为双绒双胎,采用的氯化钾减胎方案是安全有效的手术方案。本研究中,44例氯化钾减胎病例中仅有1例流产胎儿丢失,其余均为活产,总体临床疗效好。中华医学会生殖医学分会推荐减胎术中KCl规范用量为1.1~7.5ml[5]。孕16周以上的孕妇行减胎术,一个胎儿KCl用量约为3~7ml[6],但由于部分胎儿对药物不敏感或胎儿体重较大,KCl用量酌情增加,但一般不超过10ml,否则会危及母体及保留胎儿。本研究中,KCl用量平均为(4.26±1.38)ml,符合国内外推荐规范用量范围。术中无患者出现严重的母体并发症,如胸闷、气急、心律失常等。
在临床实践中,我们要给孕妇提供所有相关的信息咨询,为患者制定出最佳方案,并充分尊重患者本人意愿。本研究中有1例单绒双胎,因一胎早孕期水囊瘤行羊水穿刺,结果提示水囊瘤胎儿为21-三体胎儿,同时STR亦证实两胎儿为单卵双胎。已有研究指出[7],在16~28周进行射频消融选择性减胎的复杂性单绒双胎的围产期结局,主要与减胎指征相关。其中选择性宫内生长受限(selective intrauterine growth restriction,sIUGR)、双胎反向动脉灌注序列综合征(twin reversed arterial perfusion sequence syndrome,TRAP)的妊娠结局要好于双胎输血综合征(twin-to-twin transfusion syndrome,TTTS)及严重胎儿异常,但该实验未对21-三体的情况进行研究。单卵双胎发生一胎儿21-三体的概率非常低,可能与1个受精卵分裂成2个同卵双胎时,其中一胎儿又发生21号染色体的不分离所致。2个胎儿胎盘之间存在血管吻合,血脉相连,宫内治疗风险要高于双绒双胎,在我们与孕妇咨询了单绒双胎射频消融术的风险后,孕妇及家属表示不能接受一胎减灭,另一胎儿同时死亡的风险,决定继续妊娠。该双胎分娩后外周血提示两婴儿核型均正常,但一婴儿表现为21-三体面容、肌张力低,后来对该胎儿进行口腔颊黏膜的染色体检查证实其为21-三体。这可能由于21-三体婴儿的血液在母体子宫内与同胞双胎的血液存在交换,这也提示我们进行产前诊断时,如果发现羊水细胞异常而脐血正常,需要警惕脐血其实并不能代替羊水细胞的产前诊断,因为羊水代表了3个胚层,而脐血仅代表中胚层。对于复杂性单绒双胎的减胎方案,需要更多的临床数据支撑,以便进一步优化。
3.2 减胎时机对妊娠结局的影响 相关研究表明[8],选择性减胎能够有效避免多胎妊娠导致的各种母胎并发症及不良妊娠结局的发生,但其也可导致一定的流产风险。KCl减胎术后的流产率一般在5%~10%,大量研究共识,减胎时间越早,操作越简单,对孕妇及保留胎儿的影响越小。此外,有研究指出[9],射频消融术(radiofrequency ablation,RFA)是16周后单绒双胎孕妇选择性减胎的有效途径。4个及以上的射频周期是导致胎儿丢失的最重要的独立因素(P=0.024,OR=5.56),而RFA的指征、胎儿数量、羊膜性及RFA减胎孕周则不是导致流产的主要原因。Evans等[10]对来自多中心的402例多胎妊娠孕妇进行选择性减胎术后评估,所有孕妇均未为发生严重术后并发症,且不同孕周进行减胎术的流产率分别为:孕9~12周,5.4%;孕13~18周,8.7%;孕19~24周,6.8%;孕25周及以上,9.1%。孕早期和孕中期减胎术后流产率无统计学差异。该研究进而提出,只要经验丰富,在整个孕期都可进行选择性减胎,且90%以上的病例预后良好。本研究中,44例减胎孕妇术后仅1例引产(减胎孕周为22+5周),流产率仅为2.3%。由此我们有理由相信,随着减胎术的成熟,选择性减胎术后流产率会继续降低,从而获得更好的预后。
另有国外研究表明,妊娠15周后行选择性减胎,早产(≤34周)的发生率升高,可能是由于较大孕周的胎儿减灭后占据宫内更多空间,从而使保留胎儿的生长发育在一定程度上受到影响[11]。但另一项基于173例减胎病例的国内研究表明[12],孕早期(6.3%)和孕中期(17.0%)的早产率无统计学差异。本研究中,减胎孕周最早为17周,17~24周和≥24周进行减胎的早产率分别为16.7%和45.0%,P=0.04(<0.05),差异具有统计学意义,提示减胎孕周越早,早产概率越低;分娩孕周和出生体重均无统计学差异。
不同研究结果的得出,可能由于国内外对流产和早产的孕周定义有所差异,不同研究中样本量和研究对象,及减胎操作的熟练程度也有差别,尚无法准确得出减胎时机对妊娠结局的影响。在条件允许的情况下,我们仍倾向于尽早进行减胎术,可以避开多胎妊娠的自发性流产期,且可通过超声及羊穿等对目标胎儿进行准确定位。如果孕周已经在24周之后,亦可与孕妇讨论可以期待至27~27+6周之间减胎,此时减胎后一旦发生胎膜早破或早产,保留胎儿亦可以有一定的存活能力。但需要与患者讨论,随着孕周的增大,胎儿和母体的不可控因素会增加,之前羊穿的定位标记随着孕周的增大可能会变得难以区分,可能会加大手术的难度。孕28周之后的减胎需要伦理委员进行讨论。
3.3 介入性产前诊断需要在有“精准减胎”能力的胎儿医学中心进行 双胎妊娠的产前筛查指征和方式与单胎无较大差别,但双胎的羊水穿刺质控要求较高,涉及到术前“精确”标记,以便后续“精准”的宫内干预。介入性产前诊断前,需要借助超声软指标以辨别拟取样的目标胎儿,当超声标记物无法满足穿刺要求时,可能存在穿刺错误的风险。本研究中有15例病人因外院羊穿提示一胎21-三体转诊,对于这些病例,由于没有良好的术前标记系统,我们又重新给孕妇进行了羊穿并重新定位,3天内出具荧光原位杂交(fluorescent in situ hybridization,FISH)报告,以明确哪个胎儿为21-三体后再实施减胎。由于术前精准的标记定位,经过术后被减胎儿的心脏血核型验证,没有发生减胎目标胎儿选择错误的情况。
如果孕妇在一所不具备“宫内干预”能力的产前诊断中心进行穿刺,结果提示一胎儿染色体异常,但无法进行精确标记和区分。此情况下,患者就要转至有“宫内干预”能力的胎儿医学中心,再次进行羊膜腔穿刺,重新定位和区分,以利于后续精准减胎。如此,不仅增加了患者再次穿刺的痛苦和流产的风险,还需承担额外的治疗费用,甚至错过最佳治疗时间。所以,介入性产前诊断需要在有“精准减胎”能力的胎儿医学中心进行[13]。
