HPLC-CAD法分离测定三金片中同分异构体积雪草苷B和羟基积雪草苷
2021-07-21闵建国吴敏菊钟小清周艳林邹节明
邹 准,闵建国,吴敏菊,钟小清,周艳林,邹节明
桂林三金药业股份有限公司,广西 桂林 541004
三金片由积雪草、金樱根、金沙藤等5味中药组成,具有清热解毒、利湿通淋、益肾之功效,临床应用于治疗急、慢性肾盂肾炎,膀胱炎、尿路感染及慢性非细菌性前列腺炎等泌尿系感染疾病,临床疗效确切,成长为中药大品种之一。
自《中国药典》2000年版收载以来,质量标准不断提升完善,现行标准【含量测定】采用HPLCELSD法测定处方药味积雪草的主要药效成分羟基积雪草苷含量[1]。研究进展发现,按照《中国药典》2020年版方法检测的羟基积雪草苷,实际混杂有难以分离的同分异构体积雪草苷B[2]。有关二者的分离测定研究,一直是制药行业的难点,特别是在处方中含积雪草药材的中成药制剂中二者的准确定量分析[3-4]和纯化分离研究富有挑战性[5],2个成分的化学结构式如图1所示。
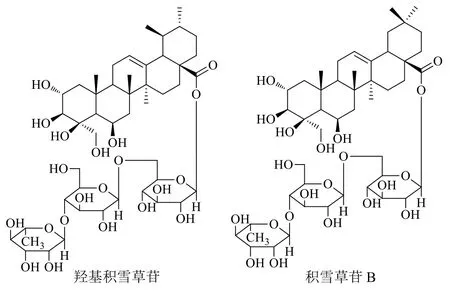
图1 羟基积雪草苷和积雪草苷B的化学结构式Fig.1 Chemical structures of madecassoside and asiaticoside B
为了真实反映其内在质量属性,本实验创新性地利用C30色谱柱进行分离,并结合近年来发展应用于无紫外吸收物质检测的新型通用型电喷雾检测器(CAD)分析测定了其中积雪草苷B和羟基积雪草苷的含量[6],结果表明该方法具有灵敏度高、专属性强、重现性好的特点,可用于本品药典质量标准的提升研究。
1 仪器、药品与试剂
1.1 仪器
赛默飞Dionex Ultimate 3000高效液相色谱仪,配三元泵、Corona Veo电喷雾检测器和变色龙色谱软件(7.1版),美国赛默飞世尔科技公司;BG-60超声仪,必能信(上海)有限公司。
1.2 对照品来源及纯度
羟基积雪草苷,中国食品药品检定研究院,批号110893-201403,质量分数91.4%;积雪草苷B为自制,并按《中药新药质量标准研究用对照品研究技术要求》进行了结构确证和纯度检查。
1.2.1 积雪草苷B结构鉴定 白色无定形粉末。mp 217~220 ℃;UV (CH3OH)λmax: 192 nm;IR (KBr)cm-1: 3 418.3 (OH), 2 935.8 (C-H), 1 732.2 (COO-),1 644.3 (C=C), 1 460.3, 1 382.4, 1 262.6, 1 238.0,1 062.9 (C-O), 1 033.8, 812.5;ESI-MSm/z: 1019, 974,503;1H-NMR (400 MHz, C5D3N)δ: 6.32 (1H, d,J=8.0 Hz, -C=CH), 5.12 (12H, 4-CH2OH), 0.98 (3H, d,J= 8.0 Hz), 1.29 (3H, s), 1.83, 1.93 (6H, s), 1.99 (3H,s), 2.17 (3H, s);13C-NMR (125 MHz, C5D3N)δ: 47.5(C-1), 69.4 (C-2), 78.7 (C-3), 43.2 (C-4), 49.2 (C-5), 68(C-6), 42.1 (C-7), 39.8 (C-8), 49.2 (C-9), 38.6 (C-10),24 (C-11), 123.5 (C-12), 143.9 (C-13), 44.9 (C-14),28.7 (C-15), 24.4 (C-16), 44.9 (C-17), 42.1 (C-18), 47.4(C-19), 31.1 (C-20), 33.4 (C-21), 32.9 (C-22), 66.6 (C-23), 16.4 (C-24), 18.9 (C-25), 19.5 (C-26), 26.4 (C-27),176.9 (C-28), 33.4 (C-29), 24 (C-30), 96.1 (Glu C-1′),74.4 (Glu C-2′), 78.6 (Glu C-3′), 70.7 (Glu C-4′), 76.9(Glu C-5′), 70.7 (Glu C-6′), 105.2 (Glu C-1′′), 75.7 (Glu C-2′′), 76.9 (Glu C-3′′), 78.3 (Glu C-4′′), 76.9 (Glu C-5′′), 61.7 (Glu C-6′′), 103.1 (Rha C-1′′′), 72.9 (Rha C-2′′′), 73.1 (Rha C-3′′′), 74.4 (Rha C-4′′′), 69.4 (Rha C-5′′′), 19.2 (Rha C-6′′′)。上述波谱数据与文献报道的积雪草苷B数据一致[7]。
1.2.2 积雪草苷B纯度检测 精密称取干燥至恒定质量的积雪草苷B对照品适量,用甲醇溶解并稀释至刻度,摇匀,制成含1 mg/mL积雪草苷B对照品溶液,精密吸取10 μL,注入液相色谱仪,连续测定3次,用归一化法计算平均质量分数为98.0%,RSD为0.22%,符合定量用对照品纯度要求,色谱图如图2所示。

图2 积雪草苷B纯度检测色谱图Fig.2 HPLC chromatography of asiaticoside B
1.3 药品与试剂
三金片由桂林三金药业股份有限公司提供,批号分别为170320、170501、170910、180402、180409、180420、181208、190936、191001、191005、191102。流动相甲醇和乙腈为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
采用Thermo AcclaimTMC30色谱柱(250 mm×4.6 mm,5 μm),甲醇-乙腈-水(35∶8∶57)为流动相,柱温为35 ℃,体积流量为1 mL/min,电喷雾检测器(corona veo)的气化温度为50 ℃。供试品溶液、对照品溶液及缺积雪草阴性溶液的色谱图如图3所示。

图3 积雪草苷B (a)、三金片样品 (b)、羟基积雪草苷 (c)及缺积雪草阴性样品 (d) 的HPLC图Fig.3 HPLC of asiaticoside B (a), Sanjin Tablets sample (b),madecassoside (c), and negative sample without Centella asiatica (d)
2.2 溶液的制备
2.2.1 对照品溶液制备 精密称取干燥至恒定质量的积雪草苷B和羟基积雪草苷对照品适量,加甲醇溶解并分别稀释至25、10 mL,配制成质量浓度分别为1.228、3.135 mg/mL的对照品溶液。
2.2.2 供试品溶液的制备 取三金片30片(小片)或20片(大片),研细,取约1.0 g,精密称定,精密加入甲醇50 mL,称定质量,超声处理(功率250 W、频率40 kHz)45 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过。精密量取续滤液25 mL,回收溶剂至干,残渣加流动相溶解并稀释至刻度,摇匀,即得。
2.3 线性关系考察
取“2.2.1”项下各对照品溶液,按5、10、20、25、50倍稀释配制系列质量浓度的对照品溶液。分别精密吸取上述对照品溶液各10 μL,注入液相色谱仪,测定。以各对照品的进样量为横坐标(X),峰面积积分值为纵坐标(Y),绘制标准曲线,进行线性回归,得回归方程为积雪草苷BY=33.654 3X-0.034 0,r=0.999 3;羟基积雪草苷Y=30.674 8X+0.768 6,r=0.998 4。结果表明,积雪草苷B在进样量0.240 7~2.406 9 μg、羟基积雪草苷在进样量0.573 1~5.730 8 μg与峰面积呈良好线性关系。
2.4 精密度试验
取同一批号样品(批号181208),按“2.2.2”项下方法制备供试品溶液,进样10 μL,连续进样6次,计算积雪草苷B和羟基积雪草苷的含量。结果积雪草苷B的平均质量分数为1.80 mg/g,RSD为0.80%,羟基积雪草苷的平均质量分数为4.06 mg/g,RSD为1.78%。
2.5 重复性试验
取同一批号样品(批号181208),平行制备6份,按“2.2.2”项下方法制备供试品溶液,分别测定,结果积雪草苷B的平均质量分数为1.77 mg/g,RSD为1.37%;羟基积雪草苷的平均质量分数为3.98 mg/g,RSD为1.49%。
2.6 稳定性试验
取供试品溶液(批号181208),分别于制备后0、3、6、9、12、24、48 h的时间间隔测定,结果积雪草苷B平均质量分数为1.79 mg/g,RSD为1.48%;羟基积雪草苷的平均质量分数为3.98 mg/g,RSD为1.11%。
2.7 加样回收率试验
取重复性试验同一批号样品(批号181208),平行取6份,各约0.5 g,精密称定,分别精密加入积雪草苷B对照品溶液(质量浓度为1.228 mg/mL)0.6 mL和羟基积雪草苷对照品溶液(质量浓度为3.135 mg/mL)0.7 mL,按“2.2.2”项下方法制备加样回收供试品溶液,并分别测定和计算加样回收率。结果积雪草苷B、羟基积雪草苷平均加样回收率分别为100.26%、98.32%,RSD分别为0.69%、1.78%。
2.8 方法耐用性试验
取重复性试验同一批号样品(批号181208),经不同体积流量(1±0.1)mL/min、不同色谱柱温(35±4)℃和流动相中乙腈比例(8±1)%单因素影响实验,以及不同厂家色谱柱(YMC carotenoid C30250 mm×4.6 mm,5 μm;Welch Ultimate®XBC30250 mm×4.6 mm,5 μm和Thermo Scientific AcclaimTMC30250 mm×4.6 mm,5 μm)考察,上述各测定结果与重复性测定样品中2指标成分测定结果无显著性差异,RSD小于3%。
2.9 定量限考察
取“2.3”项下羟基积雪草苷和积雪草苷B对照品溶液,加甲醇依次稀释成适宜的质量浓度,精密吸取10 μL,注入液相色谱仪,记录色谱图,使信噪比为10∶1,结果测得羟基积雪草苷和积雪草苷B的定量限分别为57.308 ng和60.172 ng(羟基积雪草苷对照品溶液的质量浓度为5.730 8 μg/mL,积雪草苷B对照品溶液的质量浓度为6.017 2 μg/mL)。
2.10 样品测定
取各批次三金片样品,按“2.2.2”项方法制备供试品溶液和“2.1”色谱条件测定,结果见表1。可见,11批样品中积雪草苷B在1.65~3.18 mg/g,羟基积雪草苷在3.49~7.90 mg/g,二者总量在5.14~11.08 mg/g。上述检测结果表明,三金片中2个指标成分较稳定,低含量批次与高含量批次范围在2倍以内,且表现出同增同减的关联性。

表1 11批三金片样品含量测定结果 (n = 2)Table 1 Determination results of 11 batches of Sanjin Tablets (n = 2)
3 讨论
三金片为《中国药典》2020年版收载品种,其【含量测定】项以羟基积雪草苷作为测定指标,经实验发现,常规C18色谱柱未能将互为同分异构体的积雪草苷B和羟基积雪草苷有效分离。据文献报道[8-9],在流动相添加β-环糊精(β-CD)可以实现二者有效分离,但添加β-CD的流动相存在显著缺陷,积雪草苷B色谱峰容易受到流动相中β-CD的浓度变化而发生保留时间飘移,且β-CD易导致色谱柱柱压升高及损耗色谱柱[10]。C30色谱柱采用聚合型的键合方式方法,在硅胶表面形成致密的多层C30烷基链,因而有比常规单层键合的C18色谱柱更长的烷基链,有更强的疏水性,因而对非极性溶质的保留能力和分辨率更高,同时对长链的异构体有非常好的分离能力,故而张勇等[11]利用C30色谱柱分离齐墩果酸同分异构体有较好的表现。本实验通过系列研究筛选出C30色谱柱,采用常规流动相,即可实现有效分离并准确评价三金片中积雪草苷B和羟基积雪草苷含量,可供齐墩果烷型和乌苏烷型同分异构体皂苷的分离测定提供参考,相关的分离原理有待下一步深入研究。
三金片成分复杂,对比了超声提取、加热回流提取等不同提取方法,超声处理30、45、60 min及回流2 h不同提取时间,甲醇、无水乙醇、95%乙醇不同提取溶液的效果,结果表明甲醇50 mL,超声处理(功率250 W,频率40 kHz)45 min为最简便高效提取条件。
原标准采用正丁醇提取纯化皂苷成分,实际操作繁琐,且易产生操作误差,现改进为甲醇超声处理得到提取液,蒸干后直接采用流动相(甲醇-乙腈-水混合溶剂)进行沉淀除杂纯化,能有效富集目标成分,具有效果好、经济环保、简单快捷的特点。
本实验比较了相同液相条件下,C30色谱柱联合不同类型检测器(UV、ELSD和CAD)测定二者含量的方法。结果表明,UV检测法中,检测波长为210 nm时,色谱图中的2个目标成分难以达到基线分离,无法进行有效积分;ELSD检测法中,平行进样中2个目标成分积分面积偏差较大(重复性实验RSD为8.5%),特别对含量较低的积雪草苷B影响更为显著。CAD检测法具有灵敏度高的特点[12],适用于紫外吸收较弱的成分检测,较目前常用的蒸发光散射检测器灵敏度显著提高,较紫外检测器基线干扰小,可以为此类含量偏低吸收偏弱成分的定量检测提供更好的选择。
利益冲突所有作者均声明不存在利益冲突
