葛根中1个新的6a,11a-脱氢紫檀素
2021-07-21田梦茹盛丹阳袁明昊王琰琰李梦园支燕乐马金莲薛贵民孙彦君冯卫生
杜 锟 ,田梦茹,盛丹阳,袁明昊,王琰琰,李梦园,支燕乐 ,马金莲,薛贵民 ,陈 辉 ,孙彦君 ,冯卫生
1.河南中医药大学药学院,河南 郑州 450046
2.河南中医药大学呼吸疾病诊疗与新药研发河南省协同创新中心,河南 郑州 450046
3.河南中医药大学中医药科学院,河南 郑州 450046
野葛Pueraria lobata(Willd.) Ohwi系豆科(Leguminosae)葛属PuerariaDC.植物,主产于河南、湖南、浙江、四川等地,药用其根茎。葛根是我国的常用中药,被《中国药典》2015年版记载,其味甘、辛,性凉。归脾、胃、肺经,具有解肌退热、生津止渴、透疹、升阳止泻、通经活络、解酒毒的功效[1]。现代药理研究表明葛根在调血脂、抗氧化和抗抑郁活性等方面具有显著的药用价值[2-4]。目前报道的葛根化学成分主要有黄酮类、葛酚苷类、香豆素类、三萜及其皂苷类化合物[5]。其中,异黄酮类化合物为葛根的主要化学成分。为进一步丰富葛根化学成分的研究,完善其药效物质基础,本实验从葛根中分离得到11个化合物,分别鉴定为葛檀素(pueracarpanin,1)、芒柄花苷(ononin,2)、大豆苷(daidzin,3)、大豆素(daidzein,4)、4′,8-dimethoxy-7-O-β-D-glucopyranosylisoflavone,5)、异芒柄花苷(isoononin,6)、染料木素(genistein,7)、formononetin-7-O-β-D-apiofuranosyl-(1→6)-O-β-Dglucopyranoside(8)、7,2′,4′-trihydroxyisoflavone(9)、3′-methoxydaidzein(10)和芒柄花素(formononetin,11)。其中化合物1为1个新的6a,11a-脱氢紫檀素,化合物8和9为首次从葛属植物中分离得到。
1 仪器与材料
Bruker AVANCE III 500型核磁共振仪、Bruker maxis HD型飞行时间质谱(德国Bruker公司);Autopol IV全自动旋光仪(美国鲁道夫公司);Flexa型中压制备液相色谱仪(博纳艾杰尔公司,含FL-H050G型半制备型高压输液泵,HP-Q-UV100型紫外检测器,检测波长:210 nm和254 nm;Agela technologies型色谱工作站)。LC52型高压制备液相色谱仪(赛谱锐思北京科技有限公司,SP-5030型半制备型高压输液泵,UV200型紫外检测器,检测波长:210 nm和254 nm;Easychrom型色谱工作站;色谱柱为YMC-Pack ODS-A,250 mm×20 mm,5 μm)。薄层色谱硅胶GF254、柱色谱硅胶(200~300目,青岛海洋化工厂);Sephadex LH-20(Pharmacia Biotech公司);RP-C18(40~60 μm,YMC公司);大孔树脂Diaion HP-20(日本三菱化学);甲醇(色谱纯,天津市四友精细化学品有限公司);其他试剂均为分析级。
葛根于2018年5月购自郑州市药材市场,经河南中医药大学药学院董诚明教授鉴定为豆科葛属植物野葛P.lobata(Willd.) Ohwi的根茎。凭证样本(ID-20180520)存于河南中医药大学中药化学研究室。
2 提取与分离
葛根干燥根茎10 kg,醋酸乙酯和甲醇依次浸泡提取2次,滤过,合并提取液,减压浓缩,分别得到醋酸乙酯浸膏35 g和甲醇浸膏320 g。甲醇浸膏(100 g)经大孔吸附树脂Dianion柱色谱(70 cm×8 cm)分离,依次用水-乙醇(10∶0、8∶2、6∶4、4∶6、2∶8、0∶10)梯度洗脱,并经硅胶薄层色谱检识,合并相同流分得到6个组分(Fr.A~F)。Fr.C(25 g)经中低压RP-C18柱色谱(25 cm×5 cm)分离,依次用10%~100%甲醇(体积流量10 mL/min)梯度洗脱,得到9个亚流分(Fr.C-1~C-9)。Fr.C-9重结晶得到化合物3(505 mg)。Fr.E(32 g)经Sephadex LH-20凝胶柱色谱纯化(甲醇),并经硅胶薄层色谱检识,合并相同流分得到9个组分(Fr.E-1~E-9)。Fr.E-2(5 g)经中低压RP-C18柱色谱(19 cm×3 cm)分离,依次用甲醇-水(10%→100%甲醇,体积流量10 mL/min)梯度洗脱,得到9个亚流分(Fr.E-2-1~E-2-9)。Fr.E-2-2(2 g)经硅胶柱色谱分离,依次用二氯甲烷-甲醇(25∶1、15∶1、10∶1)洗脱,得到组分10个亚流分(Fr.E-2-2-1~E-2-2-10)。Fr.E-2-2-6经制备型HPLC制备(65%甲醇,体积流量3 mL/min)得到化合物2(20.5 mg,tR=11.5 min)、6(10.6 mg,tR=12.5 min)。Fr.E-2-2-9经制备型HPLC制备(30%乙腈,体积流量3 mL/min)得到化合物8(5.5 mg,tR=10.5 min)。Fr.E-2-3(700 mg)经硅胶柱色谱分离,依次用二氯甲烷-甲醇(25∶1、20∶1、15∶1、10∶1)梯度洗脱,得到8个组分(Fr.E-2-3-1~E-2-3-8)。Fr.E-2-3-8经制备型HPLC制备(25%乙腈,体积流量3 mL/min)分离得到化合物5(15.2 mg,tR=23.0 min)。Fr.E-5(500 mg)经中低压RP-C18柱色谱(19 cm×3 cm)分离,依次用10%~100%甲醇(体积流量10 mL/min)梯度洗脱,得到16个亚流分(Fr.E-5-1~E-5-16)。Fr.E-5-3、Fr.E-5-7和Fr.E-5-10经制备型HPLC制备(溶剂分别为30%乙腈、80%甲醇、75%乙腈,体积流量3 mL/min)分别得到化合物9(4.5 mg,tR=11.5 min)、4(10.3 mg,tR=12.0 min)和1(2.5 mg,tR=34.5 min)。Fr.E-7(1 g)经中低压RP-C18柱色谱(19 cm×3 cm)分离,依次用10%~100%甲醇(体积流量10 mL/min)梯度洗脱,得到18个亚流分(Fr.E-7-1~E-7-18)。Fr.E-7-8经硅胶柱色谱分离,依次用二氯甲烷-甲醇(25∶1、20∶1、15∶1、10∶1)洗脱,得到化合物7(6.5 mg)。葛根甲醇浸膏(100 g)加水混悬,用醋酸乙酯萃取,减压回收溶剂,得醋酸乙酯部位(40 g)。醋酸乙酯部位(35 g)经硅胶柱色谱分离,依次用二氯甲烷-甲醇(30∶1、25∶1、15∶1、10∶1)洗脱,得到组分5个亚流分(Fr.1~5)。Fr.3(5 g)经中低压RP-C18柱色谱(19 cm×3 cm)分离,依次用10%~100%甲醇(体积流量10 mL/min)梯度洗脱,得到18个亚流分(Fr.3-1~3-18)。Fr.3-15重结晶得到化合物10(6.6 mg)。Fr.3-20经制备型HPLC制备(80%甲醇,体积流量3 mL/min)得到化合物11(10.5 mg,tR=13.5 min)。
3 结构鉴定
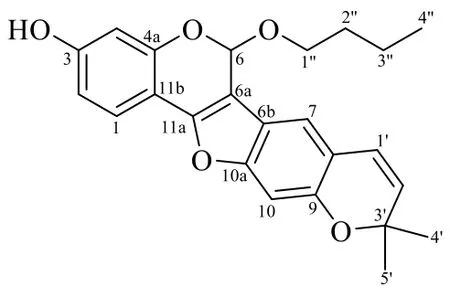
图2 化合物1的结构Fig.2 Structure of compound 1

表1 化合物1的1H-NMR和13C-NMR波谱数据 (500/125 MHz, DMSO-d6)Table 1 1H-NMR and 13C-NMR data of compound 1(500/125 MHz, DMSO-d6)

图1 化合物1的关键1H-1H COSY和HMBC相关Fig.1 Key 1H-1H COSY and HMBC correlations of compound 1
化合物1属于紫檀素类化合物,该类化合物具有抗菌、抗肿瘤等生物活性[7-8],并且从天然产物中发现的较少,2012—2017年仅有32个新紫檀素类化合物被报道[8]。化合物1的发现进一步丰富了紫檀素类化合物的结构类型。
化合物2:白色无定形粉末,易溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.43 (1H, s, H-2),8.05 (1H, d,J= 8.8 Hz, H-5), 7.53 (2H, d,J= 8.5 Hz,H-2′, 6′), 7.24 (1H, d,J= 1.4 Hz, H-8), 7.15 (1H, dd,J= 8.8, 1.4 Hz, H-6), 6.99 (2H, d,J= 8.5 Hz, H-3′,5′), 5.10 (1H, d,J= 7.1 Hz, H-1′′), 3.78 (3H, s,OCH3);13C-NMR (125 MHz, DMSO-d6)δ: 174.7(C-4), 161.4 (C-7), 159.0 (C-4′), 157.0 (C-9), 153.6(C-2), 130.1 (C-2′, 6′), 126.9 (C-3), 124.0 (C-1′),123.4 (C-5), 118.4 (C-10), 115.6 (C-6), 113.6 (C-3′,5′), 103.4 (C-8), 100.0 (C-1′′), 77.2 (C-5′′), 76.4(C-3′′), 73.1 (C-2′′), 69.6 (C-4′′), 60.6 (C-6′′), 55.1(4′-OCH3)。以上数据与文献报道一致[9],故鉴定化合物2为芒柄花苷。
化合物3:白色无定形粉末,易溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.38 (1H, s, H-2),8.04 (1H, d,J= 8.8 Hz, H-5), 7.40 (2H, d,J= 8.4 Hz,H-2′, 6′), 7.23 (1H, d,J= 1.7 Hz, H-8), 7.14 (1H, dd,J= 8.8, 1.7 Hz, H-6), 6.81 (2H, d,J= 8.4 Hz, H-3′,5′), 5.10 (1H, d,J= 7.1 Hz, H-1′′);13C-NMR (125 MHz, DMSO-d6)δ: 174.7 (C-4), 161.4 (C-7), 157.2(C-4′), 157.0 (C-9), 153.3 (C-2), 130.0 (C-2′, 6′), 126.9(C-3), 123.7 (C-1′), 122.3 (C-5), 118.4 (C-10), 115.5(C-6), 114.9 (C-3′, 5′), 103.3 (C-8), 100.0 (C-1′), 77.2(C-5′′), 76.4 (C-3′), 73.1 (C-2′′), 69.6 (C-4′′), 60.6(C-6′′)。以上数据与文献报道一致[10],故鉴定化合物3为大豆苷。
化合物4:白色无定形粉末,溶于甲醇。1H-NMR(500 MHz, DMSO-d6)δ: 8.27 (1H, s, H-2), 7.94 (1H,d,J= 8.8 Hz, H-5), 7.37 (2H, d,J= 8.5 Hz, H-2′, 6′),6.91 (1H, dd,J= 8.8, 1.8 Hz, H-6), 6.83 (1H, d,J=1.8 Hz, H-8), 6.80 (2H, d,J= 8.5 Hz, H-3′, 5′);13C-NMR (125 MHz, DMSO-d6)δ: 174.6 (C-4), 162.6(C-7), 157.4 (C-4′), 157.1 (C-9), 152.7 (C-2), 130.0(C-2′, 6′), 127.2 (C-3), 123.4 (C-1′), 122.5 (C-5),116.5 (C-10), 115.1 (C-6), 114.9 (C-3′, 5′), 102.0(C-8)。以上数据与文献报道一致[11],故鉴定化合物4为大豆素。
化合物5:白色无定形粉末,易溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.48 (1H, s, H-2),7.80 (1H, d,J= 9.0 Hz, H-5), 7.52 (2H, d,J= 8.7 Hz,H-2′, 6′), 7.36 (1H, d,J= 9.0 Hz, H-6), 7.00 (2H, d,J= 8.7 Hz, H-3′, 5′), 5.10 (1H, overlapped d,J= 7.2 Hz, H-1′′), 3.94 (3H, s, 8-OCH3), 3.78 (3H, s,4′-OCH3), 3.18~3.74 (6H, m, Glc-H-2′′~6′′);13C-NMR (125 MHz, DMSO-d6)δ: 174.8 (C-4), 159.0(C-4′′), 154.0 (C-7), 153.6 (C-2), 150.0 (C-9), 136.8(C-8), 130.0 (C-2′, 6′), 123.9 (C-1′), 123.0 (C-3),120.3 (C-5), 119.3 (C-10), 113.9 (C-6), 113.6 (C-3′,5′), 100.4 (C-1′′), 77.2 (C-5′′), 76.6 (C-3′′), 73.2(C-2′′), 69.5 (C-4′′), 61.2 (8-OCH3), 60.5 (C-6′′), 55.1(4′-OCH3)。以上数据与文献报道一致[12],故鉴定化合物5为4′,8-dimethoxy-7-O-β-D-glucopyranosylisoflavone。
化合物6:白色无定形粉末,易溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.43 (1H, s, H-2),8.03 (1H, d,J= 8.8 Hz, H-5), 7.51 (2H, d,J=8.5 Hz,H-2′, 6′), 7.16 (1H, d,J= 2.0 Hz, H-8), 7.08 (1H,overlapped, H-6), 7.08 (2H, d,J= 8.5 Hz, H-3′, 5′),4.90 (1H, d,J= 7.3 Hz, H-1″), 3.90 (3H, s, 7-OCH3);13C-NMR (125 MHz, DMSO-d6) δ: 174.7 (C-4), 163.8(C-7), 157.5 (C-9), 157.2 (C-4′), 153.7 (C-2), 130.0(C-2′, 6′), 127.0 (C-5), 125.3 (C-3), 123.4 (C-1′),117.6 (C-10), 116.0 (C-6), 114.9 (C-3′, 5′), 100.6(C-8), 100.4 (C-1″), 77.1 (C-5″), 76.6 (C-3″), 73.3(C-2″), 69.7 (C-4″), 60.7 (C-6″), 56.2 (7-OCH3)。以上数据与文献报道一致[13],故鉴定化合物6为异芒柄花苷。
化合物7:淡黄色无定形粉末,溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 12.94 (1H, s,5-OH), 8.30 (1H, s, H-2), 7.36 (2H, d,J= 8.5 Hz,H-2′, 6′), 6.81 (2H, d,J= 8.5 Hz, H-3′, 5′), 6.36 (1H,d,J= 1.4 Hz, H-6), 6.20 (1H, d,J= 1.4 Hz, H-8)。13C-NMR (125 MHz, DMSO-d6)δ: 180.1 (C-4), 164.7(C-7), 161.9 (C-5), 157.6 (C-4′), 157.4 (C-9), 153.8(C-2), 130.1 (C-2′, 6′), 122.2 (C-3), 121.2 (C-1′),115.0 (C-3′, 5′), 104.3 (C-10), 99.0 (C-6), 93.7 (C-8)。以上数据与文献报道一致[14],故鉴定化合物7为染料木素。
化合物8:白色无定形粉末,易溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.39 (1H, s, H-2),8.07 (1H, d,J= 8.9 Hz, H-5), 7.53 (2H, d,J= 8.8 Hz,H-2′, 6′), 7.24 (1H, d,J= 1.9 Hz, H-8), 7.15 (1H, dd,J= 8.9, 1.9 Hz, H-6), 7.00 (2H, d,J= 8.8 Hz, H-3′,5′), 5.04 (1H, d,J= 6.4 Hz, H-1″), 4.82 (1H, d,J= 2.8 Hz, H-1′′′), 3.79 (3H, s, 4′-OCH3), 4.47~5.51 (6H, m,glc, api-OH), 3.07~3.96 (m, glc, api-H);13C-NMR(125 MHz, DMSO-d6)δ: 174.6 (C-4), 161.3 (C-7),159.0 (C-4′), 157.0 (C-9), 153.6 (C-2), 130.0 (C-2′,6′), 127.0 (C-5), 124.0 (C-1′), 123.3 (C-3), 118.5(C-10), 115.4 (C-6), 113.6 (C-3′, 5′), 109.3 (C-1′′′),103.6 (C-8), 100.0 (C-1′′), 78.6 (C-3′′′), 76.4 (C-3′′),75.9 (C-2′′′), 75.6 (C-5′′), 73.2 (C-4′″), 73.0 (C-2″),69.9 (C-4″), 67.7 (C-6″), 63.1 (C-5″′), 55.1(4′-OCH3)。以上数据与文献报道一致[15],故鉴定化合物8为formononetin-7-O-β-D-apiofuranosyl-(1→6)-O-β-D-glucopyranoside。
化合物9:白色无定形粉末,溶于甲醇。1H-NMR(500 MHz, DMSO-d6)δ: 8.13 (1H, s, H-2), 7.92 (1H,d,J= 8.7 Hz, H-5), 6.97 (1H, d,J= 8.2 Hz, H-6′),6.91 (1H, brd,J= 8.7 Hz, H-6), 6.83 (1H, brs, H-8),6.35 (1H, brs, H-3′), 6.26 (1H, brd,J= 8.2 Hz, H-5′)。13C-NMR (125 MHz, DMSO-d6)δ: 175.2 (C-4), 162.9(C-7), 158.3 (C-4′), 157.5 (C-9), 156.4 (C-2′), 154.2(C-2), 132.0 (C-6′), 127.1 (C-5), 121.7 (C-3), 116.3(C-10), 115.2 (C-6), 110.2 (C-1′), 106.3 (C-5′), 102.9(C-3′), 102.0 (C-8)。以上数据与文献报道一致[16],故鉴定化合物9为7,2′,4′-trihydroxyisoflavone。
化合物10:白色无定形粉末,溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.31 (1H, s, H-2),7.96 (1H, d,J= 8.7 Hz, H-5), 7.16 (1H, d,J= 1.8 Hz,H-2′), 6.98 (1H, dd,J= 8.2, 1.8 Hz, H-6′), 6.93 (1H,dd,J= 8.7, 2.1 Hz, H-6), 6.85 (1H, d,J= 2.1 Hz,H-8), 6.81 (1H, d,J= 8.2 Hz, H-5′), 3.79 (3H, s,OCH3);13C-NMR (125 MHz, DMSO-d6)δ: 174.8(C-4), 162.5 (C-7), 157.3 (C-9), 153.0 (C-2), 147.1(C-3′), 146.4 (C-4′), 127.3 (C-5), 123.5 (C-3), 123.0(C-1′), 121.5 (C-5′), 116.6 (C-10), 115.2 (C-6), 115.1(C-6′), 113.2 (C-2′), 102.1 (C-8), 55.6 (3′-OCH3)。以上数据与文献报道一致[17],故鉴定化合物10为3′-methoxydaidzein。
化合物11:白色无定形粉末,溶于甲醇。1H-NMR (500 MHz, DMSO-d6)δ: 8.33 (1H, s, H-2),7.96 (1H, d,J= 8.7 Hz, H-5), 7.50 (2H, d,J= 8.5 Hz,H-2′, 6′), 6.98 (2H, d,J= 8.5 Hz, H-3′, 5′), 6.93 (1H,dd,J= 8.7, 2.0 Hz, H-6), 6.86 (1H, d,J= 2.0 Hz,H-8), 3.78 (3H, s, OCH3);13C-NMR (125 MHz,DMSO-d6)δ: 174.5 (C-4), 162.6 (C-7), 158.9 (C-4′),157.4 (C-9), 153.1 (C-2), 130.0 (C-2′, 6′), 127.2 (C-5),124.2 (C-1′), 123.1 (C-3), 116.5 (C-10), 115.2 (C-6),113.5 (C-3′, 5′), 102.1 (C-8), 55.6 (4′-OCH3)。以上数据与文献报道一致[10],故鉴定化合物11为芒柄花素。
利益冲突所有作者均声明不存在利益冲突