二氢丹参酮Ⅰ标准样品的研制
2021-07-16俞佳妮贾巧君叶子弘杨东风侯卓妮张晓丹
俞佳妮,贾巧君,叶子弘,杨东风,侯卓妮,肖 艺,张晓丹
(1.浙江理工大学 生命科学与医药学院 浙江省植物次生代谢调控重点实验室,浙江 杭州 310018;2.中国计量大学 生命科学学院,浙江 杭州 310018;3.宁波易中禾药用植物研究院有限公司,浙江 宁波 315122)
二氢丹参酮Ⅰ,作为丹参有效物质丹参酮类物质的重要组分,在抗炎、抗癌[1-4]、抗肿瘤、心血管防治等方面均具有显著疗效[5-6],是检验丹参药效的重要指标成分之一。近年来对于中药指纹图谱的研究逐渐受到瞩目,作为丹参有效成分之一的二氢丹参酮Ⅰ是作为丹参质量评价的重要指标,在研究中常需要测定其含量[7-9]。然而目前国内外对二氢丹参酮Ⅰ标准样品研制方法的报道较少,且市面上无可购买的二氢丹参酮Ⅰ标准样品,由于其标准样品的缺乏,不仅制约了二氢丹参酮Ⅰ的产业化发展,也限制了国内外研究者对二氢丹参酮Ⅰ药理药效的进一步研究与二氢丹参酮Ⅰ产品的开发。因此全国标准样品技术委员会批准了二氢丹参酮Ⅰ国家标准样品的研制。本文以ISO Guide 35:2017作为参照,依据GB/T 15000.3—2008标准样品系列工作导则[8],研制了二氢丹参酮Ⅰ的国家标准样品。
1 材料与方法
1.1 仪器与试剂
旋转蒸发仪(Buchi Rotavapor R-3)、冷冻干燥仪(Scientz-12N)、液相色谱仪(Waters e2695)、中压制备液相色谱仪(Buchi Pure C-815)、Waters快速纯化制备色谱(Waters Prep 150 LC System)、傅里叶红外光谱分析仪FT-IR(Necolit iS5)、紫外吸收图谱分析仪(UV-2500PC series)、HYG-B恒温摇床(太仓市实验仪器厂)、AB204-N电子天平(瑞士梅特勒公司)、乙酸乙酯和石油醚等分析纯试剂(杭州常青化工有限公司),以及乙腈、甲醇、乙醇(色谱纯,Merck公司),200~300目硅胶(青岛海洋化工厂)和GF254硅胶板(山东烟台汇友硅胶有限公司)。
1.2 二氢丹参酮Ⅰ样品的制备
原料为采集于丹参道地产区陕西商洛丹参(SalviaMiltiorrhiza)的根(根为红色),将其粉碎后经乙醇溶剂回流提取3次,2~5 ℃静置析晶后抽滤得总丹参酮粗品。采用正相硅胶柱层析进一步纯化样品,以石油醚-乙酸乙酯梯度洗脱,合并收集二氢丹参酮Ⅰ斑点段。浓缩干燥后利用中压液相色谱进行第二次纯化,以乙腈-去离子水梯度洗脱,最后用甲醇洗脱,经薄层层析检测后根据Rf值合并相同组分进行真空浓缩,得到纯度为90%的二氢丹参酮Ⅰ粗品。将上述粗品继续采用Waters快速纯化制备色谱,以乙腈-去离子水梯度洗脱,经薄层层析检测后根据Rf值合并相同组分进行真空浓缩,经过2次重结晶(结晶溶剂为二氯甲烷-甲醚),过滤结晶,冷冻干燥后得到纯度高于99%的二氢丹参酮Ⅰ样品。制备过程中二氢丹参酮Ⅰ纯品纯度确认采用TLC分析与HPLC检测。
1.3 分装与储存
在相对清洁且独立的环境中,用电子天平精确称量,分别将100份10 mg二氢丹参酮Ⅰ样品装入100个4 mL的棕色小瓶中,并且以1到100进行编号,密封后于4 ℃保存。
1.4 杂质分析
采用库伦电位滴定法:瑞士万通KF915水分测定仪,卡尔费休试剂滴定,以纯水标定所制备的二氢丹参酮Ⅰ样品水分。采用EXPEC 7000型电感耦合等离子体质谱仪测定二氢丹参酮Ⅰ样品无机杂质。为测定无机杂质,准确称取5.32 mg样品,溶于20 mL甲醇,完全溶解后,定容至50 mL容量瓶,摇匀待测。用校准液进行半定量曲线校准,建立半定量工作曲线,以质量数为横坐标,半定量因子为纵坐标,建立校准曲线,分析样品。
1.5 定性分析
采用熔点与元素分析样品水分与灰分。紫外光谱(UV)、红外光谱(IR)、液质联用(HPLC-MS)、核磁共振(NMR)进行定性分析,对制备的样品进行结构确认,分析条件如下。
紫外光谱(UV):溶剂为乙醇,紫外可见光区(200~600 nm)全波长扫描。
红外光谱(IR):溴化钾压片后对吸收峰进行分析。
液质联用(HPLC-MS):仪器为布鲁克microTOF-Q,质谱条件为电离方式ESI+,毛细管电压4.5 kV,载气用普氮,载气流速为4.0 L/min,载气温度180 ℃,扫描范围为m/z=50~800。
核磁共振(NMR):以氘代丙酮为溶剂,四甲基硅烷(TMS)为内标进行测定。
1.6 均匀性检验
均匀性是用于衡量标准样品空间分布特征的基本属性。对于二氢丹参酮Ⅰ标准样品来说,具有一定规格的标准样品,在同一批次或同一瓶内的样品的二氢丹参酮Ⅰ的纯度都应是均匀的,在检测时其定值应在规定的不确定范围内,该标准样品才能被定义为均匀的。
为了对所制备的二氢丹参酮Ⅰ样品进行均匀性检验,首先需要对所制备的同一批样品进行分装,抽样标准按标准样品工作导则[10]中对均匀性研究的要求进行。抽样数目确定为10个,取10瓶样品并以1~10进行编号,从10瓶样品中以3种不同程序从上述编号的样品分别各称取0.25 mg样品3份,并以1.0 ml色谱乙醇作为溶剂溶解后进行HPLC分析,样品纯度值以HPLC面积归一法进行测定。HPLC条件为:仪器用Waters e2695型高效液相色谱仪。色谱柱为Sunfire-C18色谱柱(4.6 mm×250 mm,5 μm)。流动相是乙腈/(0.2%乙酸)水=50/50。流速1.0 mL/min。柱温30 ℃。检测波长254 nm。进样量10 μL。
3次的抽样样品编号顺序为1,3,5,7,9,2,4,6,8,10号瓶;10,9,8,7,6,5,4,3,2,1号瓶;2,4,6,8,10,1,3,5,7,9号瓶。对每个样品重复测定3次。标准样品均匀性情况通过对测得数据使用方差分析法来判断。
1.7 稳定性检验
标准样品的稳定性是用来描述标准样品的特性值随时间的变化。本文设置了实验将所制备样品在0~4 ℃条件下放置24个月来检验其稳定性,分别于0,1,2,3,6,9,12,18,24个月时取3个样品,按照1.6项下色谱条件,每份试样以测定3次的平均值为其定值结果,用峰面积归一化法计算纯度。
1.8 定值分析
1.8.1 定值分析方法
根据GB/T 15000—2008规定,对所制备样品的定值需由多个权威实验室进行联合定制分析,所选实验室需要获得国家或部门认可的具备资质。本实验选取共8个具备资质的权威实验室,从所制备样品中随机抽取24瓶,随机送3瓶去往各实验室,每瓶样品进行平行实验测定2次。送去的样品在各定值实验室使用高效液相色谱仪测定其纯度,并采用HPLC面积归一化法对纯度进行定值,色谱条件与1.6项下一致,并将检测报告从各实验室收集起来进行进一步分析。
1.8.2 样品溶液制备
本实验室以色谱乙醇溶解样品,过0.22 μm微孔滤膜,获得质量浓度为0.25 mg/mL的样品溶液。
2 结果与讨论
2.1 二氢丹参酮Ⅰ的杂质分析


2.2 二氢丹参酮Ⅰ的结构鉴定
2.2.1 熔点和元素分析
使用仪器为梅特勒熔点仪MP50,其测得所制备样品的熔点为216~217 ℃。根据JY/T 017—1996元素分析仪方法通则进行测试,平行测试三次。根据元素分析结果可得所制备样品的分子式为C18H14O3,计算值:C 77.69%,H 5.036%。实际测定值:C(77.68±0.007)%,H(5.062±0.005)%。
2.2.2 紫外(UV)光谱分析
扫描结果为在410.40 nm,290.40 nm,240.80 nm,215.20 nm处有吸收。
2.2.3 红外(IR)光谱分析

2.2.4 液质联用(HPLC-MS)分析
ESI-MS模式下测量值m/z=301.083 9[M+Na]+,理论计算值m/z=301.083 5[M+Na]+,测得二氢丹参酮Ⅰ分子量为278.30,分子式为C18H14O3。
2.2.5 核磁共振(NMR)分析
核磁数据归属见表1与表2。
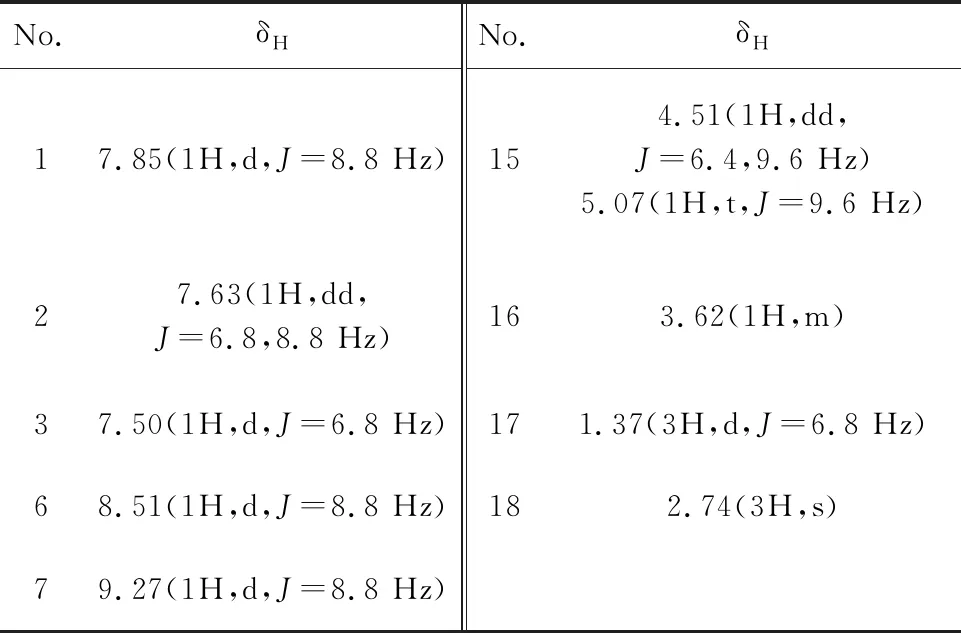
表1 二氢丹参酮Ⅰ的氢谱核磁共振数据(600 MHz,氘代丙酮)

表2 二氢丹参酮Ⅰ的碳谱核磁共振数据(150 MHz,acetone-d6)
由上述液质联用分析结果与核磁共振分析结果与已发表文献对比可知,所制备样品种化合物的HPLC-MS和NMR数据均与二氢丹参酮Ⅰ结构相关的文献报道一致[11-12],证明该化合物确为二氢丹参酮Ⅰ,结构式见图1。
治疗前两组患者NIHSS、3MS、BI评分比较无显著性差异;治疗后两组患者NIHSS评分显著降低,3MS、BI评分均显著升高,同组治疗前后比较差异有统计学意义(P<0.05);治疗后观察组患者NIHSS、3MS、BI评分改善情况均显著优于对照组,两组比较存在显著性差异(P<0.05),见表2。
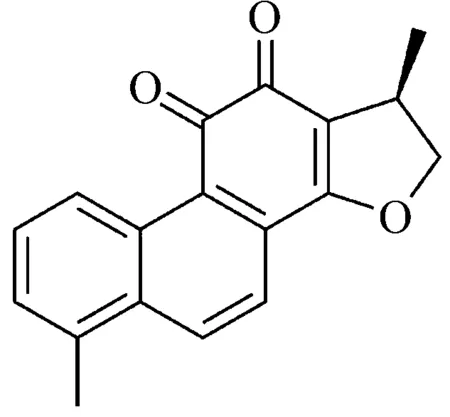
图1 二氢丹参酮Ⅰ结构式Figure 1 Chemical structure of dihydrotanshinone Ⅰ
2.3 均匀性试验
标准样品的均匀性性检验是标准样品研制过程中不可缺少的程序。因此在对样品进行分装后,对二氢丹参酮Ⅰ标准样品进行纯度均匀性检验,均匀性检验结果见表3与表4。

表3 二氢丹参酮Ⅰ标准品纯度均匀性检验结果
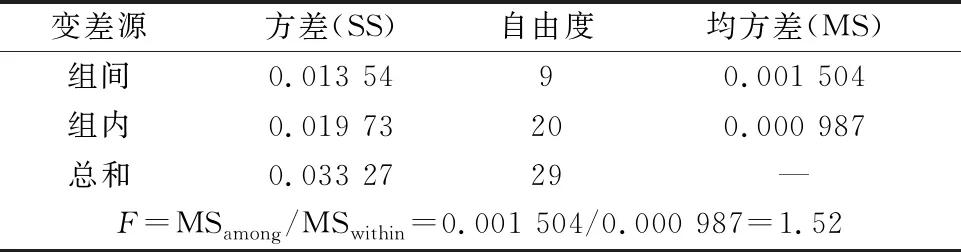
表4 方差分析结果
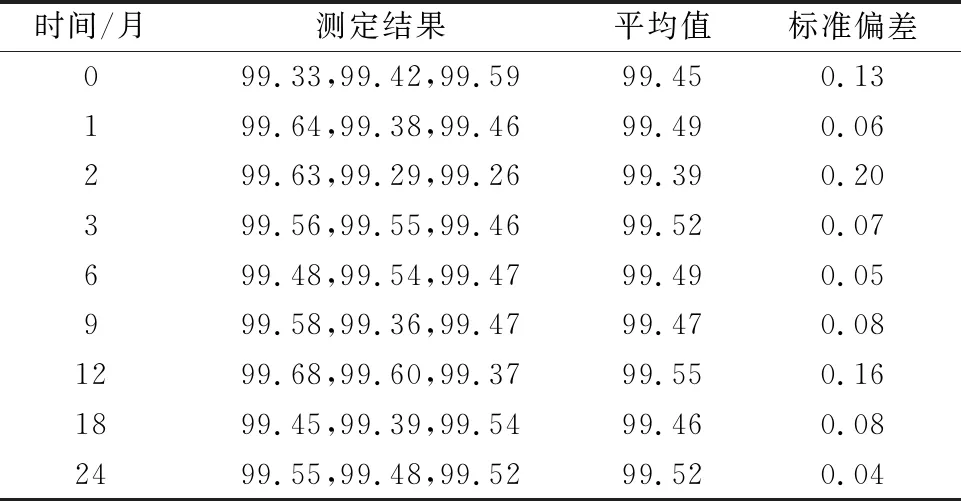
从上表4可见,以υ1(即组间)=9及υ2(即组内)=20,F=MS间/MS内=1.52 0,1,2,3,6,9,12,18,24个月样品纯度统计结果见表5。 表5 稳定性检验试验结果 从表5可见,在24个月中,不同时间测得的样品纯度平均值并在没有随时间的变化而明显的改变,同时根据GB/T 15000—2008中对标准样品稳定性分析的要求,选取直线模型作为经验模型,采用F检验与t检验对不同时间测得的样品纯度平均值数据进行分析,分析过程如下。 t检验斜率计算: |b1| 因此,斜率的变化是不显著的。因而二氢丹参酮Ⅰ样品在两年内未观测到显著的不稳定性。有效期t=24个月的长期稳定性的不确定度的贡献为u=sb·t=0.002 003×24=0.048 072。 因此可以确定在0~4 ℃的储存条件下,所制备的标准样品在24个月内是稳定的。 2.5.1 定值结果 二氢丹参酮Ⅰ纯度定值结果汇总表如表6。 表6 8家实验室二氢丹参酮Ⅰ纯度定值数据 表7 8家实验室定值数据方差分析 2.5.2 定值分析的不确定度评定 根据GB/T 15000.3—2008标准可知,定值结果由标准值和不确定度组成。标准值定值实验引入的不确定度uchar、均匀性检验引入的不确定度ubb和稳定性检验引入的不确定度ults组成了标准样品特性标准值的测量不确定度u。依据全部测定结果,计算二氢丹参酮Ⅰ标准样品的不确定度。 由上述分析结果可知,本文所制备二氢丹参酮Ⅰ标准样品的不确定度由uchar=0.062 5%,ubb=0.013 128%,ults=0.048 072%,此外还有杂质检验中水分引入的不确定度u水分=0.230 77%,灰分引入的不确定度u灰分=0.029 557组成。 则其扩展不确定度为 因此二氢丹参酮Ⅰ标准样品的定值结果为:二氢丹参酮Ⅰ标准样品的纯度为99.835%。二氢丹参酮Ⅰ标准样品扩展不确定度按只进不舍原则处理并统一小数点位数后为0.50%。 本文以标准样品工作导则作为参照,研制了二氢丹参酮Ⅰ的标准样品。经检验,所研制的二氢丹参酮Ⅰ标准样品的均匀性与稳定性均符合国家对标准样品的要求,所制备的样品的纯度定值结果为(99.835±0.50)%,达到了天然产物国家标准样品的要求。该标准样品可用于丹参等药材中的二氢丹参酮Ⅰ含量的测定,有利于对丹参产业的质量控制,与进一步的药效研究。同时也可用于一些抗衰老护肤产品的开发研制。2.4 稳定性试验

2.5 定值结果及其不确定度评定




3 结 语
