大气NO2长期暴露与中国成人慢性肾脏病的关联:基于中国慢性肾脏病流行病学调查
2021-07-15梁琛瑜王万州马麟梁泽王玥瑶李鹏飞杨超李双成张路霞
梁琛瑜,王万州,马麟,梁泽,王玥瑶,李鹏飞,杨超,李双成,张路霞,,5
1.北京大学 a.地表过程分析与模拟教育部重点实验室 b.城市与环境学院,北京 100871
2.北京大学公共卫生学院,北京 100191
3.浙江省北大信息技术高等研究院,浙江 杭州 311215
4.北京大学第一医院肾内科,北京大学肾脏病研究所,北京 100034
5.北京大学健康医疗大数据国家研究院,北京 100191
慢性肾脏病(chronic kidney disease,CKD)是当前全球重要的健康问题。2017年,全球CKD患者数目已达到6.98亿,因CKD导致的死亡人数达到120余万[1]。一项全球疾病负担研究(Global Burden of Disease Study,GBD)结果提示,CKD是2019年全球伤残调整寿命年(disability adjusted life year,DALY)的第18 位危险因素,且近年来呈现患病逐渐增加的趋势,是继糖尿病与获得性免疫缺陷综合征(acquired immune deficiency syndrome,AIDS)后疾病负担增加趋势最明显的慢性疾病[2]。据2007—2010年“中国慢性肾脏病流行病学调查”(China National Survey of Chronic Kidney Disease,CNSCKD)结果显示,我国18岁以上成人的CKD患病率约为10.8%[3]。然而,当前研究提示,除高血压、糖尿病、代谢性疾病等疾病因素的影响外,其他CKD 相关的发生发展机制仍不明晰[4-6]。
多项全球流行病学研究提示,空气污染对人群健康具有不可忽视的危害。GBD 2019 研究显示,空气污染是全球204 个国家和地区人群DALYs 的第7 位危险因素[7]。空气污染物可分为颗粒物与气态污染物两类。近年来,已有来自美国、韩国和中国等国家的数项研究指出,大气细颗粒物(fine particulate matter with median aerodynamic diameter ≤2.5 μm,PM2.5)长期暴露会导致人群CKD 患病风险增加[8-10]。目前对气态污染物健康危害的相关研究仍然有限,但在近年来也呈现日渐增加的趋势,如研究发现二氧化氮(nitrogen dioxide,NO2)的长期暴露可能增加人群心血管、呼吸系统等疾病的患病以及死亡风险[11-13]。然而,当前对NO2与CKD 关联的研究尚缺乏,且相关结果因地理区域、人群特征、研究设计不同等影响而存在差异[8,14-16]。此外,目前尚无基于我国人群开展的全国性相关研究。为此,本研究借助CNSCKD 全国性调查数据,探究大气NO2长期暴露与我国成人CKD 患病风险的关联,从而为空气污染的肾脏健康影响研究提供科学依据。
1 对象与方法
1.1 研究对象
本研究为横断面调查。人群健康数据来源于2007—2010年期间的CNSCKD 全国性调查数据。研究对象均为18 岁以上成年人(n=47 204),覆盖我国13 个省、直辖市或自治区的城乡地区,调查员均具备医学专业背景。该调查采集了研究对象的人口学资料(年龄、性别、收入、受教育程度)、健康资料(高血压、糖尿病、心血管疾病史)、生活方式(吸烟、饮酒情况)以及实验室检查指标等,详尽内容可见既往研究[3]。本研究已通过北京大学生物医学伦理委员会审批(批准号:IRB00001052-20030)。
1.2 环境暴露数据
本研究利用卫星遥感反演数据提取2002—2009年的年近地表NO2和PM2.5质量浓度(后简称“浓度”)数据,这是弥补大气污染地面监测覆盖不足最有效的方式,具有空间分辨率高、空间覆盖范围广、连续的优点。本研究利用全球臭氧监测实验(Global Ozone Monitoring Experiment,GOME)、大气制图扫描成像吸收光谱仪(Scanning Imaging Absorption Spectrometer for Atmospheric Chartography,SCIAMACHY)和GOME-2卫星的对流层NO2柱密度反演年地表NO2浓度,使用GEOS-Chem 化学传输模型(https://sedac.ciesin.columbia.edu/data/set/sdei-global-3-year-running-meanno2-gome-sciamachy-gome2)将对流层NO2柱密度与地面NO2浓度联系起来[17-18]。同时,本研究通过美国宇航局中分辨率成像光谱仪(Moderate-resolution Imaging Spectroradiometer,MODIS)、多角度成像光谱仪(Multi-angle Imaging Spectrometer,MISR)和海洋观察宽视场敏感器(Sea-viewing Wide Field-of-view Sensor,SeaWiFS)的气溶胶光学厚度(aerosol optical depth,AOD)反演得到PM2.5网格数据集,同样利用GEOS-Chem化学传输模型和地理加权回归(geographically weighted regression,GWR)模型将AOD与近地表PM2.5浓度联系起来(https://sedac.ciesin.columbia.edu/data/set/sdei-global-annualgwr-pm2-5-modis-misr-seawifs-aod)[19-20]。使用双线性插值的重采样方法将初始空间分辨率分别为0.1°和0.01°的NO2网格和PM2.5网格重采样至1 km网格。
中国气象强迫数据集(China Meteorological Forcing Dataset,CMFD)是中国首个专为研究陆面过程而开发的高时空分辨率近地面气象数据集,提供了2 m气温、比湿、降水率等7个近地表气象要素[21-22]。该数据集通过遥感产品、再分析数据集和站点数据融合而成,记录时间为1979年至今,时间分辨率为3 h,空间分辨率为0.1°[21-22]。该数据集较国际上广泛使用的全球陆面数据同化系统(Global Land Data Assimilation System,GLDAS)数据集具有更高精度,由于其时间的连续性和较高的质量,CMFD 成为中国使用最广泛的气候数据集之一。本研究利用该数据集的近地面气温、近地面空气比湿计算2002—2009年的年平均温度和年平均比湿,并使用双线性插值的重采样方法获取1 km分辨率的气象数据。
此后,依据调查中研究对象记录的对应街道经纬度,设立10 km 缓冲区半径以提取栅格均值,并根据研究对象实际调查年份,匹配各研究对象于调查时间前5年的环境暴露数据。
1.3 健康指标定义
本研究中,CKD 定义为肾小球滤过率(estimated glomerular filtration rate,eGFR)低于60 mL·min-1·(1.73 m2)-1或尿蛋白肌酐比大于30 mg·g-1;高血压定义为收缩压≥140 mmHg 或舒张压≥90 mmHg,或在过去2 周内使用降压药,或自报有高血压病史;糖尿病定义为空腹血糖浓度≥7.0 mmol·L-1,或使用降糖药,或自报有糖尿病病史;心血管事件定义为心肌梗死或脑卒中发病;高尿酸血症定义为血尿酸浓度男性>422 mol·L-1,女性>363 mol·L-1[3]。
1.4 统计学分析
分析研究对象暴露于大气NO2浓度1~5年时间窗滑动平均值与慢性肾病患病的关联。利用logit 函数连接的广义相加模型(generalized additive model,GAM)分析大气NO2浓度与人群CKD 患病的关联,并控制性别,年龄,体重指数(body mass index,BMI),受教育程度,人月均收入,城乡,吸烟、饮酒情况,高血压、糖尿病、心肌梗死/脑卒中病史等因素,以控制相关变量的混杂[23]。此外,研究将同时间窗温度与空气比湿的立方样条函数纳入模型,以控制气象因素对污染物健康效应的非线性混杂。样条函数的自由度基于广义交叉验证(generalized cross validation,GCV)最小值原则进行选取,以提升效应值估测的准确性[24-25]。
为探索不同个体特征和地区因素对NO2长期暴露与CKD患病关联差异的影响,研究进一步将NO2浓度与性别,年龄,BMI,受教育程度,人月均收入,城乡,吸烟、饮酒情况,高血压、糖尿病、心肌梗死/脑卒中病史的乘积交互项纳入模型,以分析上述因素的修饰效应是否有统计学意义,并进行相应亚组分析[9,15,26]。此外,本研究将同时间窗的PM2.5浓度作为协变量进行敏感性分析,以分析PM2.5对NO2的估计效应是否存在混杂。
研究结果以NO2浓度每增加10 μg·m-3,人群CKD患病风险比值比(odds ratio,OR)及其95%可信区间(confidence interval,CI)表示。本研究检验水准为α=0.05(双侧)。统计学分析借助R 3.6.1进行。
2 结果
2.1 描述性分析结果
在47 204名研究对象中,CKD的患病率为10.8%。其中,男性为20 148人(42.7%),女性为27 056人(57.3%),年龄为(49.6±15.2)岁,BMI 为(23.9±3.7)kg·m-2。有高血压、糖尿病及心肌梗死/脑卒中病史病者分别为16 691人(35.4%)、3 488人(7.4%)及1 220人(2.6%)。研究对象的其他人群基线信息可见既往研究[3]。
研究对象在调查前5年时间窗内的NO2与温度、空气比湿的暴露情况见表1。其中,各研究对象NO2、温度及空气比湿暴露的中位数M及四分位数间距(interquartile range,IQR)分别为13.4(16.6)μg·m-3、16.4(5.0)℃、9.0(4.4)g·kg-1。
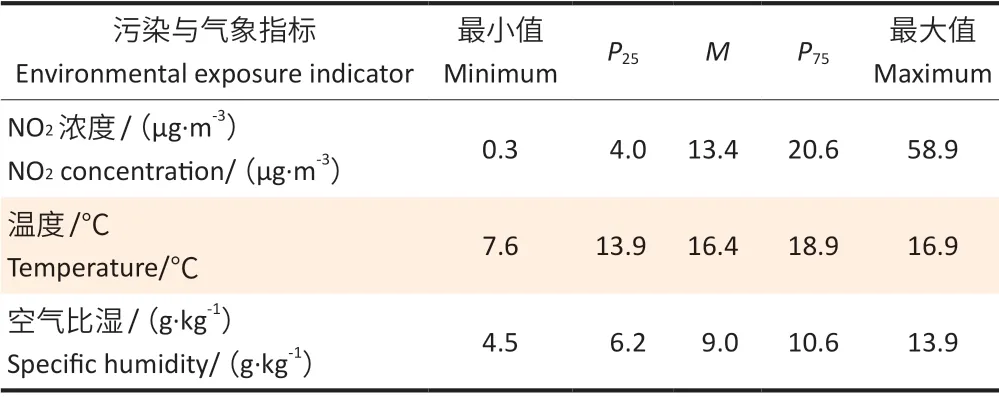
表1 研究对象调查前5年(2002—2009年)期间的环境暴露情况Table 1 Environmental exposure of study participants over the preceding 5 years (2002—2009)
2.2 NO2与我国人群CKD 患病的关联
结果显示:大气NO2长期暴露与我国成人CKD 患病风险增加的关联具有统计学意义。总体而言,NO2暴露浓度的升高与CKD 患病风险在1、4、5年滑动平均内均有正向关联,在5年时达到最大。NO2的5年滑动平均值每增加10 μg·m-3,CKD 患病的OR为1.15(95%CI:1.11~1.19)。见图1。敏感性分析结果提示,在控制同期PM2.5的混杂后,NO2长期暴露与CKD 患病风险的关联仍然稳定。
使用NO2的五年滑动平均值进行亚组分析,基于人群基本信息、人群行为特征和慢性疾病患病情况的亚组分析结果分别见于图2。基本信息方面:男性、≥65 岁、超重(24 kg·m-2≤BMI<28 kg·m-2)及肥胖(BMI ≥28 kg·m-2)、受教育程度较高、人月均收入较低及农村地区人群对NO2的相关健康效应更为敏感。NO2暴露每增加10 μg·m-3:男性人群CKD患病的OR为1.30(95%CI:1.24~1.37),高于女性(OR=1.04,95%CI:1.00~1.09)(交互项P<0.01);农村地区人群CKD患病的OR为1.57(95%CI:1.33~1.85),高于城市人群(OR=1.09,95%CI:0.99~1.21)(交互项P<0.01)。行为特征方面:相比于不吸烟、偶尔吸烟与基本不饮酒者,每天吸烟、偶尔或经常饮酒的人群患CKD与NO2的关联更高。慢性疾病患病方面:未患有高血压、糖尿病、心肌梗死/脑卒中者相比于患相关疾病的人群对于NO2的效应更为敏感。其中,非糖尿病患病人群NO2暴露每增加10 μg·m-3,CKD患病的OR为1.21(95%CI:1.16~1.26),高于糖尿病患病人群(OR=1.01,95%CI:0.95~1.07)(交互项P<0.01)。

图2 NO2每增加10 μg·m-3对中国成人CKD效应OR 及95% CI 的亚组分析(5年移动平均)Figure 2 Estimated odd ratios (ORs) and 95% confidence intervals(CIs) for the prevalence of chronic kidney disease (CKD) associated with a 10 μg·m-3 increase in NO2 exposure in Chinese adults in stratified analysis (5-year moving average)
3 讨论
本研究基于CNSCKD 全国性横断面调查数据发现:NO2长期暴露与我国成人CKD 患病风险增加的关联具有统计学意义(P<0.05),且在男性、≥65 岁、超重及肥胖、受教育程度较高、人月均收入较低、农村、每天吸烟、偶尔或经常饮酒、无慢性疾病史的人群中风险更高。
不断有证据表明,大气污染物暴露对于人群肾脏健康具有不可忽视的负面影响[9,14-15,27-28]。Mehta等[9]基于美国波士顿地区退伍军人研究首次报告了PM2.5暴露对CKD 患病风险的提升作用。此后,空气污染对CKD 的负面效应也得到了来自不同地区人群的证据支持[23,29-32]。一项基于中国台湾人群的研究发现,肾病综合征患病风险的增加与NO2和PM2.5浓度的增加密切关联[33]。一项基于韩国人群的研究指出,PM10和NO2暴露与eGFR水平下降的关联具有统计学意义(P<0.05)[8]。NO2对CKD 影响的生物学机制尚不清楚,现有的研究提示,NO2等污染物可能经肺泡进入血液,造成炎症反应[34]、氧化应激损伤[35]、肾脏组织DNA损伤[36]、肾脏血管血液流变学改变[27]、热应激与脱水[37]等,进而对肾脏功能造成负面影响[38-40]。
本研究结果提示,NO2长期暴露与CKD患病风险的增大密切关联:NO2的5年滑动平均值每增加10 μg·m-3,CKD 患病的OR为1.15(95%CI:1.11~1.19)。Bowe 等[14]基于美国退伍军人的纵向研究发现,NO2每增加一个IQR(16.9 μg·m-3),CKD 患病的风险比(hazard ratio,HR)为1.09(95%CI:1.08~1.11)。Chen 等[15]基于我国台北市8 497 名65 岁以上老年人群的横断面研究发现,NO2每上升一个IQR(7.0 μg·m-3),CKD 患病的OR为1.07(95%CI:1.01~1.14)。本研究结果与上述研究的发现一致,即NO2暴露可能会增加人群CKD的风险,但效应值略高于既往研究,可能与研究设计、地理特征、人群易感性等因素的差异有关[41-43]。此外,既往研究提示,不同地区污染物浓度水平具有差异,这亦可能是气态污染物健康效应差异的原因[44-45]。修饰效应结果提示,在排除同期PM2.5的潜在混杂影响后,长期大气NO2暴露与CKD 的正向关联仍然稳定。因此,NO2与CKD的关联尚需进一步深入关注。
亚组分析结果提示,男性、≥65 岁、超重及肥胖、受教育程度较高、人月均收入较低、农村、每天吸烟、偶尔或经常饮酒、无高血压/糖尿病/心肌梗死/脑卒中的人群可能是NO2相关健康影响的易感人群。Mehta 等[9]发现,PM2.5与eGFR 降低的关联则在非糖尿病患者的老年人群中更为明显。Chen等[15]也发现,PM2.5、NO2与eGFR降低的关联在非糖尿病人群中更为明显。本研究与多项研究均显示,≥65岁以及非糖尿病人群可能是空气污染相关效应的易感人群。但Yang等[32]基于中国台湾成年人的研究发现,颗粒物暴露与<65 岁人群肾功能的关联相比于≥65 岁者更为明显。当前,空气污染对不同年龄阶段人群肾脏健康影响的相关研究较为缺乏,相关结果尚需得到进一步验证。
本研究的局限性包括:(1)研究使用的CNSCKD数据调查时间为2007—2010年期间,未能捕捉此后近10年我国大气NO2暴露与人群CKD的潜在关联。然而,CNSCKD 是当前我国时限最新的全国性流行病学调查,具有较好的人群代表性与科学性。(2)本研究基于横断面设计,研究证据强度有限,未来研究可进一步基于前瞻性分析方法,估测NO2对CKD 的影响。(3)人群健康调查数据可能存在一定的信息偏倚,但本研究的调查人员均具有医学背景,在一定程度上能够提升数据的准确性。(4)本研究中,空气污染暴露数据是基于卫星遥感反演获取,可能存在一定的“暴露错分”问题,进而对NO2相关健康效应估测造成偏差。
综上,大气NO2长期暴露可能提升中国成人CKD患病风险,且此关联关系可能因人口学基本特征、行为习惯、慢性疾病病史不同而存在差异。我国尚需对NO2等污染物采取严格防控措施,从而为人群肾脏健康促进提供有益支持。当前,气态污染物与肾脏健康的关联研究较缺乏,相关论题尚需进一步探索和阐明,从而为进一步制订针对空气污染健康影响的防控措施提供科学依据。
