MRI术前鉴别诊断肠型和胰胆管型壶腹周围癌的价值研究
2021-07-06祝琼洁严陈晨
祝琼洁,张 冰,黎 琪,何 健,严陈晨*
1南京大学医学院附属鼓楼医院医学影像科,2病理科,3核医学科,江苏 南京 210008
壶腹周围癌(periampullary carcinoma,PAC)是指发生在十二指肠大乳头周围2 cm 范围内的恶性肿瘤。传统的分类方法依据肿瘤的起源部位将PAC分为以下4种类型:起源于Vater壶腹本身的壶腹癌,起源于十二指肠的十二指肠癌,起源于胆总管远端的胆管癌以及起源于胰头和/或钩突部的胰腺癌。近年来基于组织学和分子特征的新型分型方法将PAC 分为以胰胆管型和肠型为主的两种病理亚型[1]。临床研究表明,肠型PAC 的预后要明显好于胰胆管型,PAC 的病理亚型可以作为判断预后的一个独立预测指标[2-3]。此外,这两种亚型对不同化疗方案的反应不同,胰胆管型PAC治疗相似于胰胆管癌,可以从吉西他滨化疗中获益,而肠型患者主要从5-氟尿嘧啶为基础的化疗中获益[4]。因此相对于传统分型,新的病理亚型分型对PAC预后的判断和临床治疗方案的制订都具有重要意义。
现阶段,PAC 病理亚型的诊断主要依靠术后病理,而一些晚期患者可能无法通过手术切除取得病理组织。内镜下逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)可以直接观察十二指肠内侧壁和壶腹乳头区,并可切开十二指肠乳头进行活组织检查,对PAC的诊断具有较高的敏感性和特异性,然而由于肿瘤内部存在异质性,活检取到的有限组织并不能代表肿瘤的整体状态。另外因其为有创的介入式检查,术中存在发生多种并发症的风险,从而限制了ERCP 在临床诊断中的应用[5]。因此需要一种无创的术前诊断方法来鉴别PAC病理亚型。
影像学检查作为临床普遍应用的一种术前检查手段,目前有多种成像技术用于Vater壶腹及其周围组织的显示。常规超声检查(ultrasongraphy,US)因无创、简便、高效、经济而成为PAC的首选检查方法,但因受腹壁脂肪及肠道内气体的干扰,US 对壶腹区病变显示欠佳,只能作为黄疸待查或可疑壶腹区病例的初筛检查手段[6]。计算机断层扫描(computed tomography,CT)是诊断PAC的常用方法,具有扫描速度快、层面薄、可以进行多期增强扫描及图像后处理的优势,有助于准确地显示肿瘤的形态、强化特点、周围脏器及血管的侵犯情况、淋巴结转移情况等,但CT 检查具有放射性,对病灶检出的敏感性低于磁共振成像(magnetic resonance imaging,MRI)[7]。MRI 有良好的软组织对比度和无电离辐射[8],磁共振胰胆管水成像(magnetic resonance cholangiopancreatography,MRCP)可以直观清楚地显示胰胆管全貌、扩张及梗阻的部位,使得磁共振多模态成像成为评价PAC的主要手段[9]。但目前术前应用MRI 来鉴别诊断PAC 新型病理亚型的国内外研究相对较少[10-12]。本研究回顾性分析肠型和胰胆管型PAC的MRI图像资料,旨在探讨MRI在术前区分PAC 病理亚型的价值,从而为术前诊断及治疗方案的选择提供帮助。
1 对象和方法
1.1 对象
回顾性分析南京鼓楼医院2017年1月—2020年7月怀疑患有PAC患者的临床资料及MRI图像。纳入标准:①经手术病理证实为PAC,且有明确的病理学亚型结果(肠型或胰胆管型);②术前完成磁共振检查(包括常规MRI序列、MRCP序列以及MRI弥散加权成像),MRI 检查时间与手术时间间隔小于2 周。排除标准:诊断时患者同时患有其他部位的恶性肿瘤;在接受MRI检查前进行过壶腹部有创操作或抗肿瘤治疗;MRI图像伪影较大,影响观察。最终59 例患者纳入研究,肠型21 例,胰胆管型38 例,男32例,女27例,年龄37~80岁,患者主要以黄疸及腹痛为首发症状就诊。本研究属回顾性研究,医院伦理委员会豁免伦理审查。所有患者及其监护人知情同意。
1.2 方法
1.2.1 检查
所有患者在MRI 检查前需禁食6~8 h,并在扫描前进行呼吸训练,采用荷兰Philips Ingenia 3.0T MRI 扫描仪及腹部相控阵线圈进行成像。取仰卧位,双臂上举过顶。扫描范围为肝脏膈顶部至十二指肠水平部。扫描主要序列和参数包括:①MRI 平扫:常规横断位、矢状位、冠状位定位扫描后,行横断位T1WI脂肪抑制序列扫描(TR 3.2 ms,TE 1.5 ms,层厚4.4 mm,层间距-2.2 mm,视野400 mm×352 mm×220 mm,矩阵268×235,翻转角10°,NAS 1次),横断位T2WI 脂肪抑制序列扫描(TR 724 ms,TE 70 ms,层厚5 mm,层间距1.5mm,视野400 mm×328 mm×206 mm,矩阵288×208,翻转角90°,NAS 1 次)及冠状位T2WI 扫描(TR 515 ms,TE 70 ms,层厚5 mm,层间距1 mm,视野300 mm×354 mm×143 mm,矩阵200×208,翻转角90°,NAS 1 次)。②DWI 扫描:TR 1 446 ms,TE 59 ms,层厚5 mm,层间距1.5 mm,视野310 mm×365 mm×206 mm,矩阵116×128,翻转角90°,NAS 2 次,b=0、1 000 s/mm2。MRCP 薄层:TR 2 500 ms,TE 556 ms,层厚2 mm,层间距-1 mm,视野260 mm×291 mm×80 mm,矩阵260×291,翻转角80°,NAS 1次,采用MIP重建3D图像。
1.2.2 图像分析
由2名分别具有4年和11年腹部MRI诊断经验的放射科医师共同对MRI图像进行独立分析,意见不一致时请教上级医师(在腹部MRI诊断方面有12年经验)取得共识。读片者对患者临床、病理结果均不知晓。评价内容包括定性评价和定量评价。
定性评价。①病灶类型:肿块型或浸润型;②位置:十二指肠腔内、跨壁生长或十二指肠外(肿块主体相对十二指肠肠壁位置,50%为界,位于中间定为跨壁生长);③十二指肠乳头形态:扁平、半圆形或结节;④主胰管扩张:>4 mm为扩张;⑤胆总管扩张:>10 mm 为扩张;⑥胆总管狭窄形态:截断性或渐进性;⑦胆总管远端内是否可见类圆形充盈缺损;⑧截断胰管周围是否有扩张侧枝;⑨管征:双管征、三管征或四管征;⑩病灶信号:低、等或高信号(分别在T1WI 平扫脂肪抑制序列及T2WI 平扫脂肪抑制序列图像上,以正常胰腺信号作为参照);⑪DWI:弥散受限或不受限,弥散受限指病变在DWI 图像上表现为高信号,同时在ADC 图上表现为低信号。
定量评价。①病灶大小:测量最大径;②主胰管、胆总管管径:测量最宽处;③十二指肠乳头至截断的胰胆管末端的距离;④胰胆管角度:测量梗阻端以上胰胆管延长线形成的夹角。每一项指标由2名医师分别测量,取2次测量的平均值。
1.2.3 病理分析
标本取材后,按病理常规方法制片及HE 染色。免疫组织化学采用常规SP 法。对所有患者的组织病理学报告进行分析并记录:肿瘤大小、分化程度(高分化、中分化和低分化)、浸润深度(T 分期)、有无淋巴结转移(N分期)、有无远处转移(M分期)、有无神经侵犯以及脉管侵犯。由一位具有7年病理学诊断经验的医生综合形态学标准和免疫组织化学诊断PAC病理亚型。
形态学标准:根据Kimura 等[13]提出的形态学标准进行分类,肠型由形状良好的管状腺体、复杂的筛状区和实巢组成的肿瘤,肿瘤细胞高大,常呈假层状柱状,细胞核呈椭圆形或雪茄状,常含有黏液。胰胆管型是由简单的或分支状的腺体和被密集的间质所包围的小的实性细胞巢组成的肿瘤,肿瘤细胞呈立方至低柱状排列,呈单层,胞核呈圆型,大小和形态各不相同。
免疫组织化学标准:国际上已有多位学者报道了应用免疫组织化学标志物鉴定PAC 病理亚型的研究,但未有统一的明确结论。本研究采用Ang等[14]提出的诊断标准肠型的主要标志物为CK20、CDX2、MUC2,胰胆管型的主要标志物为MUC1。
1.3 统计学方法
使用SPSS 25.0 及Medcalc 19.5 软件进行统计分析。本研究的连续变量采用Shapiro-Wilk 检验来验证数据是否符合正态分布,符合正态分布的采用独立样本t检验进行比较分析,不符合正态分布的计量资料采用Mann-WhitneyU检验进行比较分析。符合正态分布的计量资料用均值±标准差()表示,不符合正态分布的计量资料以中位数(四分位数间距)[M(IQR)]表示。分类变量通过χ2检验或Fisher精确概率法进行比较分析。对单因素分析有意义的变量(P<0.05)采用向前逐步法进行多因素二元Logistic回归分析,确定区分PAC病理亚型的重要预测因素。采用受试者操作特征(receiver operating characteristic,ROC)曲线来评价有意义指标的诊断效能,计算ROC 曲线下面积(area under curve,AUC)、灵敏度、特异度、阳性预测值及阴性预测值。AUC 比较采用DeLong 检验。采用Kappa 检验评估2 名医师MRI 图像评估的一致性。P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料
肠型和胰胆管型PAC 患者在有无淋巴结转移(N 分期)、神经侵犯方面的差异具有统计学意义(P<0.05),而在性别、年龄、症状等其他临床及病理资料间的差异均无统计学意义(表1)。
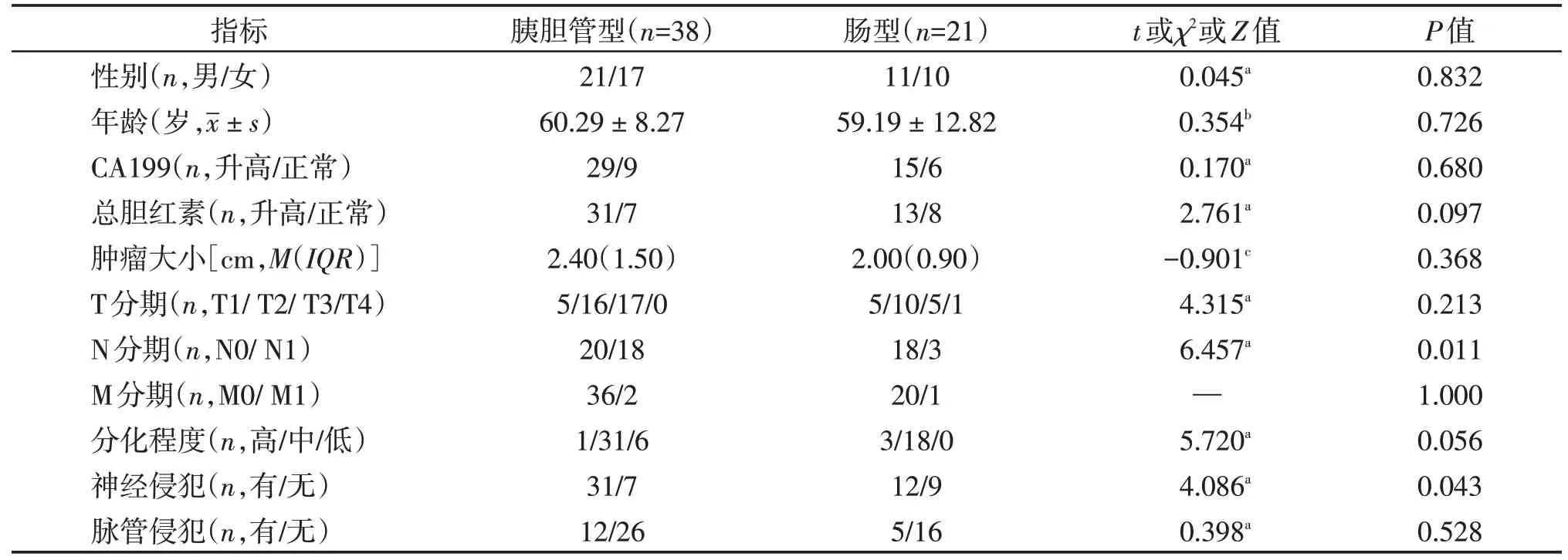
表1 两组患者一般情况比较
2.2 MRI常规平扫图像分析
肠型和胰胆管型PAC患者在病灶位置、十二指肠乳头形态、T2WI信号特点方面差异有统计学意义(P<0.05)。在59 例患者中,肠型PAC 病灶较多位于十二指肠腔内,在T2WI 上相对正常胰腺信号主要表现为等信号(图1),而胰胆管型PAC 病灶多位于十二指肠腔外(P<0.001),在T2WI上主要表现为等信号及高信号(P=0.013,图2,表2)。相对胰胆管型PAC,肠型PAC十二指肠乳头表现为结节型的比例更高(P<0.001),而两组在病灶类型、最大径、T1WI 信号、DWI信号方面差异无统计学意义(表2)。
分析“do/does/did+v.”构式的语域分布特点,对于理解和掌握该构式有实际意义。通过检索分析,发现该构式语域分布特点如表5所示,口语语域占比最大,为47.4%;其次为小说,百分比为16.7%;接着依次为杂志、报纸和学术,其中学术占比最小,仅9.5%。结合构式语义分析,该构式核心构式义为强调人的意识,带有主观性,因此在口语体出现频率较高,因为对话中,说话者往往需要表达自身意识,同样地,小说中塑造人物也需要通过表达人的意识来完成,也充满了人物的主观性,因此该构式也使用较多,但是对于杂志、报纸和学术,语域较为正式,内容多为客观事实,因此该构式出现频率相对较低。该分布特点与构式语义相吻合。
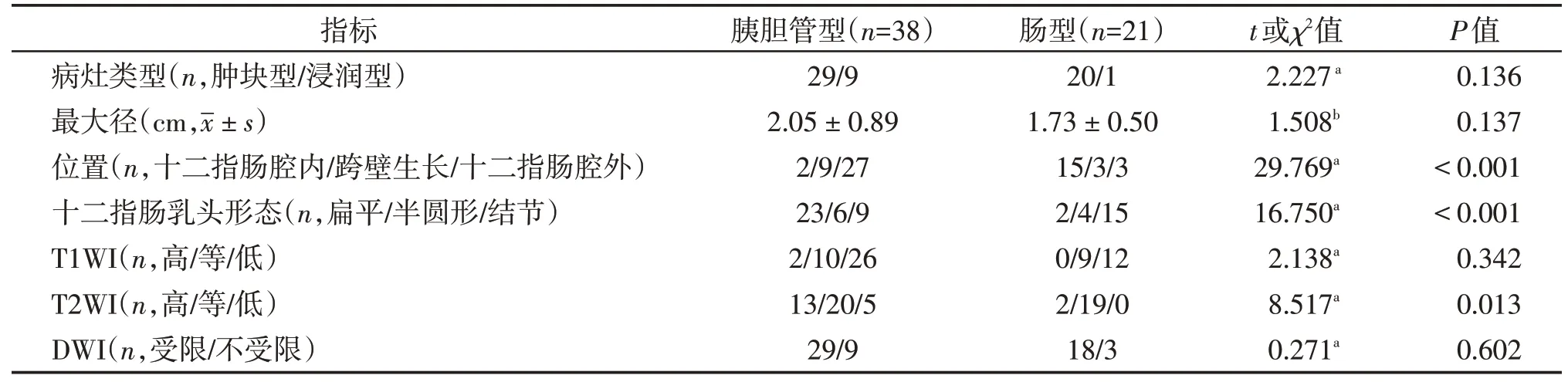
表2 两组MRI常规平扫特征比较

图1 肠型PAC MRI平扫图像、MRCP图像及病理图片
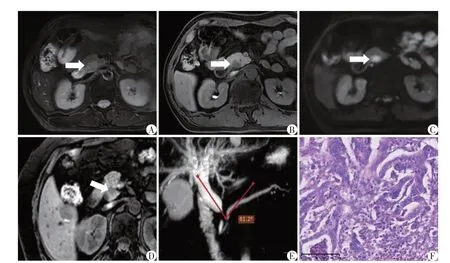
图2 胰胆管型PAC MRI平扫图像、MRCP图像及病理图片
2.3 MRCP图像分析
在MRCP 图像上,两组在胆总管远端内有无类圆形充盈缺损影、十二指肠乳头至截断胰管末端的距离、胰胆管角度间的差异有统计学意义(P<0.05)。在MRCP图像上,肠型PAC胆总管远端出现类圆形充盈缺损的比例高于胰胆管型PAC(P=0.013)。肠型PAC的十二指肠乳头至截断胰管末端的距离及胰胆管角度均小于胰胆管型(P=0.009,P<0.001,表3)。两组在胆总管及胰管是否扩张及定量分析、胆总管远端狭窄形态、管征、截断胰管周围是否有扩张侧枝、十二指肠乳头至截断胆管末端的距离间的差异无统计学意义(表3)。本研究中,κ值均超过0.8,表示研究者之间的诊断结果具有高度一致性。
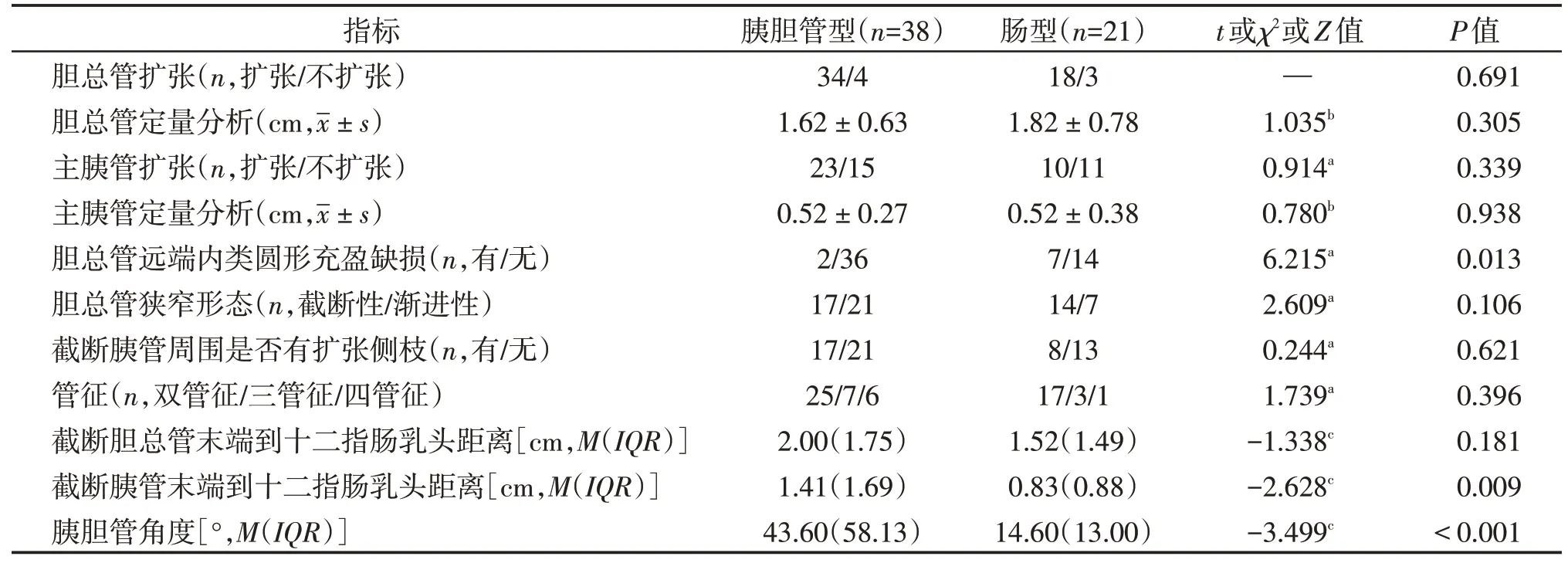
表3 两组MRCP特征比较
2.4 多因素二元Logistic回归分析及ROC曲线分析
将单因素分析结果差异有统计学意义的指标:病灶位置、十二指肠乳头形态、胆总管远端内类圆形充盈缺损、截断胰管到十二指肠乳头的距离、胰胆管角度、平扫T2WI 脂肪抑制图像上病灶信号特点纳入多因素Logistic 回归分析,显示病灶位置[OR=0.002,95%CI:0.001~0.220,P<0.001]和胆总管远端内类圆形充盈缺损[OR=0.016,95%CI:0.000~0.044,P=0.002]为鉴别肠型和胰胆管型PAC的独立预测指标,评价病灶位置、胆总管远端内类圆形充盈缺损及两者联合模型的诊断效能(表4),两者联合变量模型的AUC 更大(图3),差异具有统计学意义(P均<0.05)。
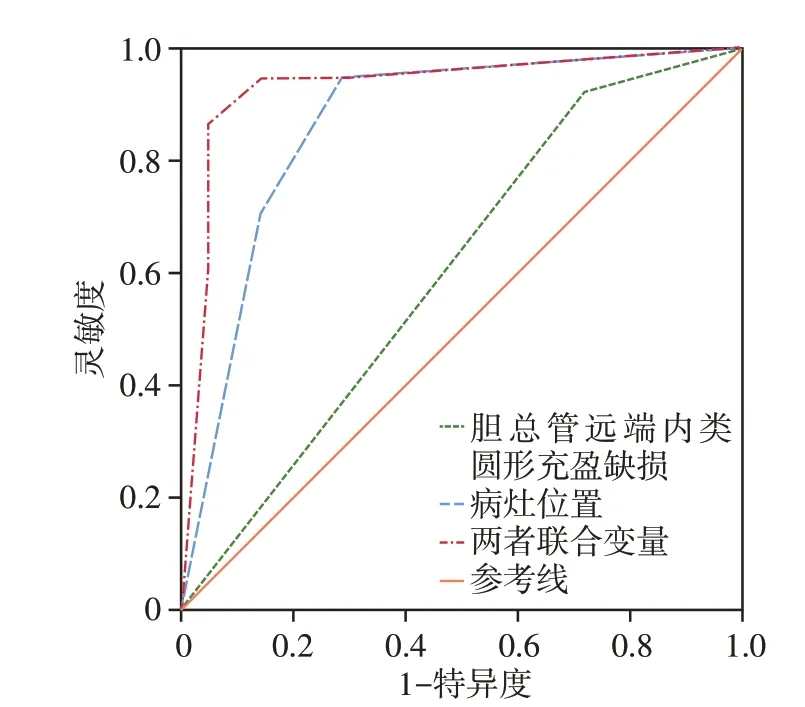
图3 单因素及联合指标诊断PAC病理亚型的ROC曲线
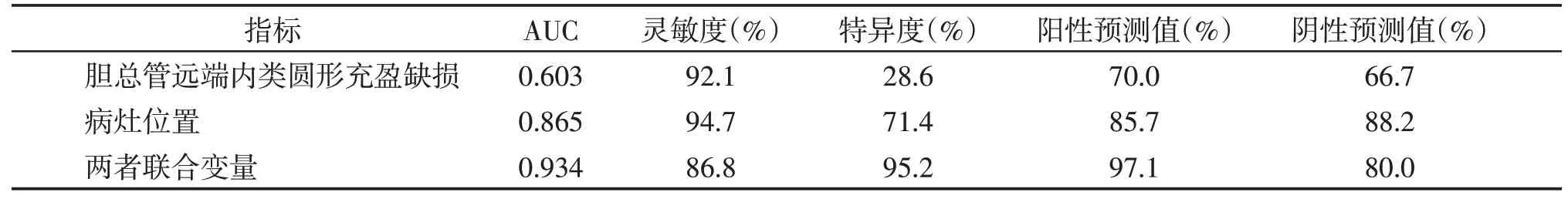
表4 独立预测因子及联合模型对PAC病理亚型的诊断价值
3 讨论
本研究发现,肠型及胰胆管型PAC在MRI图像上的表现有显著差异,相对胰胆管型PAC 而言,肠型PAC 病灶多位于十二指肠腔内,在平扫T2WI 脂肪抑制图像上病灶信号多为等信号,较少表现为高信号和低信号,十二指肠乳头多表现为结节型,胆总管远端常出现类圆形充盈缺损,截断胰管到十二指肠乳头距离较短,胰胆管角度偏小。
在59例患者中,肠型PAC病灶较多位于十二指肠腔内(15/21,71%),而胰胆管型PAC 病灶多位于十二指肠腔外(27/38,71%)。但在Chung 等的[11]研究中,壶腹癌的位置对肠型和胰胆型PAC的鉴别没有帮助。我们考虑壶腹癌作为PAC的一种,仅代表了起源于壶腹部的肿瘤特征,而不能代表还包括十二指肠癌、远端胆管癌、胰腺癌在内的PAC。
在T2WI 平扫脂肪抑制序列上,对照正常胰腺组织,两种病理亚型病灶均主要表现为等信号,胰胆管型PAC还表现为高信号(13/38,34%)及低信号(5/38,13%),而肠型较少表现为高信号(2/21,10%),未有病灶表现为低信号。结合文献报道[15],我们考虑胰胆管型PAC可能由于肿瘤内纤维基质增生表现为低信号,肿瘤出现坏死而表现为高信号。
本研究将十二指肠乳头形态分为扁平、半圆形或结节3 种类型,肠型PAC 十二指肠乳头主要表现为结节型(15/21,71%),胰胆管型PAC 主要表现为扁平型(23/38,61%)。在Chung 等[11]的壶腹癌病理亚型MRI 成像研究中,MRI 图像未表现出乳头膨出的7例患者中有6例为胰胆型。另外一项对PAC病理亚型的MDCT成像研究发现18例胰胆管亚型PAC中14例显示乳头回缩,而14例肠型中13例呈乳头膨出[16],这些文献报道结果与本研究结果相一致。造成这一差异的原因是胰胆管型PAC 病灶多位于十二指肠腔外,且大体形态上多为浸润性生长,引起十二指肠乳头回缩呈扁平状,而肠型PAC病灶多位于十二指肠腔内,大体形态上呈结节样生长,使十二指肠乳头呈结节型较多。
在MRCP 图像其他指标的定量分析中,两组在十二指肠乳头至截断胰管末端的距离及胰胆管角度间的差异有统计学意义(P<0.05)。肠型PAC的十二指肠乳头至截断胰管末端的距离及胰胆管角度均小于胰胆管型。多篇文献报道,胰头癌和胆总管下段癌的胆总管梗阻末端及主胰管梗阻末端到十二指肠主乳头的距离、胰胆管汇合角度大于壶腹癌及十二指肠乳头组[17-18],但未有对新的病理亚型的研究报道。本研究中十二指肠乳头至截断胰管末端的距离更短,可能与病灶位置有关,肠型PAC 的病灶位置多位于十二指肠腔内,较胰胆管型引起梗阻的位置更低,从而使十二指肠乳头至截断胰管末端的距离更短。另外肠型病灶的长径[(1.73±0.50)cm]小于胰胆管型[(2.05±0.89)cm],当病灶位于胰胆管之间时,引起的占位效应更小,可能使胰胆管角度更小。
本研究多因素Logistic 回归分析显示病灶位置和胆总管远端内类圆形充盈缺损为鉴别肠型和胰胆管型PAC的独立预测指标,并将病灶位置和胆总管远端内类圆形充盈缺损相结合,构建了两者联合的Logistic 回归模型。结果显示两者联合可进一步提高诊断准确性,为临床制定治疗方案和预后评估提供客观的影像学依据。
本研究存在以下不足:第一,晚期及不能接受手术的患者不包括在内,这可能会导致选择偏倚;第二,入组样本量较小;第三,只采用了MRI常规平扫及MRCP图像,未对MRI增强图像进行研究,存在一定局限性。今后以期进一步采用影像组学中的纹理分析,使得到的信息更全面、准确,从而具有更高的预测效能。
综上所述,MRI 检查可术前鉴别肠型及胰胆管型PAC,特别是病灶位置、胆总管远端内类圆形充盈缺损及两者联合变量模型对PAC 病理亚型具有较高的预测价值。
