沙库巴曲缬沙坦钠缓释片的制备与释药机制研究
2021-07-03程曼曼施沁青王菁华尹莉芳秦超韩晓鹏中国药科大学药学院药剂系南京210009
程曼曼,施沁青,王菁华,尹莉芳,秦超,韩晓鹏(中国药科大学药学院药剂系,南京 210009)
心力衰竭(heart failure,HF)是由心室充盈或射血的任何结构或功能受损所致的一种复杂的临床综合征[1]。心力衰竭是一类患病率高、再住院率高、死亡率高的疾病,其严重影响患者的生活质量和生命,是一个日益严重的公共卫生问题。据统计,全球心力衰竭患者的数量已高达2300万,仅在美国就有约650万患者,并且大约50%的病例是射血分数降低的心力衰竭[2]。尽管目前心力衰竭的治疗有了较大的进展,但其发病率和死亡率仍非常高(患者的5年生存率为50%,10年生存率为10%),医疗支出仍较高(全球每年用于心力衰竭上的费用为1080亿美元,2012年美国用于心力衰竭的费用约为300亿美元[3])。沙库巴曲缬沙坦钠(sacubitril/valsartan,LCZ696)是由诺华制药公司开发的治疗慢性心力衰竭的创新药物,与依那普利相比,其使心血管疾病死亡率和首次住院率降低了20%,是首个也是唯一一个较标准治疗显著改善心力衰竭患者预后的药物[4-5]。2015年7月沙库巴曲缬沙坦钠通过FDA和欧盟审批上市,于2017年和2020年进入中国和日本市场,目前已被各国心力衰竭治疗指南推荐为慢性心力衰竭的一线治疗药物。
LCZ696由沙库巴曲和缬沙坦按物质的量1∶1共结晶形成,是FDA批准的第一个药物共晶体,有效提高了缬沙坦的生物利用度[6]。LCZ696具有同时阻断血管紧张素受体和抑制脑啡肽酶的双重作用机制,沙库巴曲(AHU377,前药)可由酯酶快速代谢为活性成分脑啡肽酶抑制剂(LBQ657),起到排钠利尿、舒张血管等作用;缬沙坦是一种血管紧张素Ⅱ受体阻滞剂,起到改善水钠潴留、减轻心脏负荷等作用[7-8]。2017年沙库巴曲缬沙坦钠片(Entresto,诺欣妥)全球销售额为5.07亿美元,2018年全球销售额为10.28亿美元,处于飞速增长期,临床需求量大。目前仅有原研厂家诺华上市的普通片剂型,规格分别为50 mg、100 mg和200 mg,日服2次。而慢性心力衰竭患者需长期服药,给药顺应性差,且其临床试验表明患者服用该药物后有低血压、高血钾等不良反应。因此将沙库巴曲缬沙坦钠制备成日服一次的缓释骨架片,可在体内缓慢平稳的释放药物,从而有效避免血压过度波动,发挥最佳治疗效果。
1 试药与仪器
1.1 试药
沙库巴曲缬沙坦钠原料药(含量:100.8%,山东四环药业股份有限公司);羟丙甲基纤维素(HPMC)、聚氧乙烯(PEO N60K)、欧巴代ambⅡ薄膜包衣预混剂(卡乐康包衣技术有限公司);羟丙基纤维素(HPC MXF,亚什兰公司);卡波姆(971PNF,路博润特种化工有限公司);海藻酸钠(500~800 mPa·s,青岛明月海藻有限公司);羧甲基纤维素钠(CMC-Na,亚什兰公司);无水乳糖(德国美剂乐公司);甘露醇(法国罗盖特公司);微晶纤维素(德国JRS药用辅料公司);硬脂酸镁(安徽山河药用辅料股份有限公司);微粉硅胶(上海风泓药用辅料技术有限公司);乙腈(美国天地,色谱纯);三氟乙酸(阿拉丁,色谱纯);其余试剂均为分析纯。
1.2 仪器
AR223CN千分之一天平(OHAUS公司);XS105DU十万分之一天平[梅特勒-托利多(常州)精密仪器有限公司];pH计(北京赛多利斯科技仪器有限公司);LC-20AT高效液相色谱仪(SHIMADZU公司);FADT-1200RC溶出仪(上海富科思分析仪器有限公司);电热鼓风干燥箱(上海一恒科学仪器有限公司);旋转压片机(北京新龙立科技有限公司);YPD-200C片剂硬度测定仪(上海黄海药检仪器有限公司)。
2 方法与结果
2.1 释放度测定方法的建立
2.1.1 色谱条件 色谱柱:以十八烷基硅烷键合硅胶为填充剂(GL Inertsil ODS-3,4.6 mm×150 mm,3 μm);流动相:水-乙腈-三氟乙酸(500∶500∶1);检测波长:255 nm;流速:2.0 mL·min-1;进样温度:25℃;柱温:30℃;进样体积:10 μL。
2.1.2 释放度的测定 按照2020年版《中国药典》四部通则0931第二法(桨法)[9],以pH 6.8的磷酸盐缓冲液为溶出介质,体积为900 mL,转速为50 r·min-1,温度(37.5±0.5)℃,依法操作,分别于1、2、4、6、8 h取样10 mL,并及时补加同温等体积溶出介质,经0.45 μm 微孔滤膜过滤,取续滤液作为供试品溶液。按外标法分别计算不同时间点样品中沙库巴曲和缬沙坦的浓度,并计算沙库巴曲和缬沙坦的累积释放度。
2.1.3 系统适用性 按“2.1.1”项下色谱条件,取“2.1.2”项下供试品溶液进样检测,结果缬沙坦的保留时间为3.908 min,理论板数为10 772,拖尾因子为1.120;沙库巴曲的保留时间为5.170 min,理论塔板数为12 858,拖尾因子为1.100。取供试品溶液连续进样6次,记录峰面积,结果缬沙坦峰面积RSD为0.030%,沙库巴曲峰面积RSD为0.15%,精密度符合要求。
2.2 原料药在各介质中平衡溶解度的测定
缬沙坦是BCS Ⅱ类(低溶高渗)的弱酸性药物,其在不同pH值介质中的平衡溶解度结果见表1,结果显示缬沙坦在水中几乎不溶,在不同pH值介质中的平衡溶解度具有pH依赖性,随着pH值升高缬沙坦平衡溶解度增大。共晶中缬沙坦在不同pH值介质中的平衡溶解度均大于缬沙坦单药。
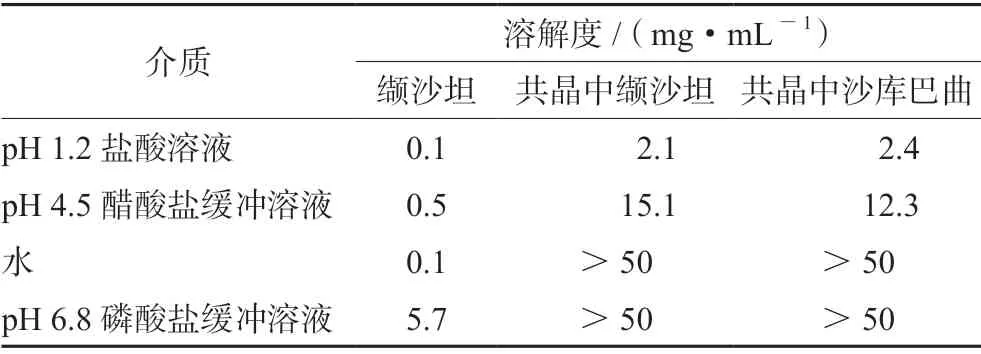
表1 缬沙坦和沙库巴曲缬沙坦钠在不同pH值介质中的平衡溶解度Tab 1 Equilibrium solubility of valsartan and sacubitril/valsartan in media with different pH values
2.3 原料药稳定性
按《化学药物(原料药和制剂)稳定性研究技术指导原则》要求开展原料药影响因素试验。将沙库巴曲缬沙坦钠原料药平铺于敞口称量瓶中,厚度小于3 mm,分别放置在高温60℃、高湿92.5% RH和光照[照度(4500±500)Lx]条件下,于10 d、30 d取样,观察性状,测定有关物质变化情况(有关物质方法参照沙库巴曲缬沙坦钠片进口药品注册标准JX20150417),结果见表2。结果表明,沙库巴曲缬沙坦钠在上述条件下化学性质稳定,有关物质无明显变化;高湿92.5%RH条件下药物吸湿明显,原料药应在干燥密封条件下储存。

表2 原料药稳定性结果Tab 2 Stability of drug substance
2.4 制备工艺考察
沙库巴曲缬沙坦钠原料药易潮解、流动性较差,且在处方中比例较大,不易采取粉末直压工艺,因此考虑湿法制粒和干法制粒工艺制备缓释片。由于沙库巴曲缬沙坦钠为共晶药物,在制备过程中可能会使原料药晶型发生转变,因此测定不同制粒方式下颗粒的X射线粉末衍射,见图1。结果显示自制缓释片(干法制粒、湿法制粒)和原料药在相同位置有明显衍射峰,表明制备工艺未引起原料药晶型改变。此外不同制粒工艺制得缓释片在pH 6.8磷酸盐缓冲溶液中缬沙坦和沙库巴曲的释放均无明显差异(见图2)。由于干法制粒颗粒得率低,且颗粒流动性差,因此最终选择湿法制粒工艺为缓释片制备工艺,其制备工艺如下:按处方用量称取沙库巴曲缬沙坦钠原料药、无水乳糖、HPMC K4M和HPMC K100LV,按等量递增法混合均匀。加入适量无水乙醇,制软材,过20目筛湿整粒,经40℃干燥2 h后,过20目筛干整粒,按照处方量称取硬脂酸镁和微粉硅胶,混合均匀后,将总混颗粒用旋转压片机压制成硬度在8~10 kg·cm-2的片芯。采用amb Ⅱ型薄膜包衣粉进行包衣,物料温度约40~45 ℃,包衣锅转速15 r·min-1,喷液速度约1 g·min-1,薄膜衣增重4%~5%。

图1 原料药、空白辅料和缓释片的X-射线粉末衍射测定图Fig 1 X-ray diffraction of API,the blank excipient and sustainedrelease tablets

图2 不同制备工艺对药物释放行为的影响Fig 2 Effect of different preparation methods on drug release behaviors A.缬沙坦(valsartan);B.沙库巴曲(sacubitril)
2.5 处方单因素考察
2.5.1 骨架材料的考察 本研究选择6种缓释材料作为亲水凝胶骨架材料,分别为羟丙甲基纤维素(HPMC K100LV)、卡波姆971PNF、海藻酸钠、CMC-Na、PEO N60K、HPC MXF,用量占片芯质量的25%,按照“2.4”项下方法制备缓释片,缬沙坦释放曲线见图3A,沙库巴曲释放曲线见图4A。结果显示,骨架材料种类相同时,缬沙坦的释放较沙库巴曲的释放略快。当缓释材料用量固定为25%时,6种骨架材料均有不同程度的缓释作用,卡波姆971PNF的缓释效果最明显,CMC-Na的缓释效果次之,HPC MXF 和PEO N60K缓释效果相当,HPMC K100LV和海藻酸钠的缓释效果最小。因HPC MXF、PEO N60K和CMC-Na形成的凝胶层较厚,缬沙坦和沙库巴曲的8 h释放约60%左右,使用过程中可能存在释放不完全的问题。当使用卡波姆971PNF作为骨架材料时,物性太黏,使用低比例就能产生较强的缓释效果,在工业放大生产时耐用性较差;HPMC是一种全能型的缓控释聚合物材料,作为亲水凝胶骨架材料在骨架片中应用较为广泛,目前HPMC有多种黏度型号可供选择,具有安全无毒、价格低廉、成型性好、释放易调节等诸多优点,因此本研究选用HPMC作为骨架材料。
2.5.2 HPMC型号的考察 分别选用4种不同黏度型号的羟丙甲基纤维素(K100LV、K4M、K15M、K100M)作为骨架材料,用量占片芯质量的25%,按照“2.4”项下方法制备缓释片,缬沙坦释放曲线见图3B,沙库巴曲释放曲线见图4B。结果显示,黏度型号相同时,缬沙坦的释放较沙库巴曲的释放略快。当骨架材料为低黏度型号K100LV时,由于其黏度较低,骨架片溶蚀较快,药物释放也较快,骨架在试验过程中不能保持完整,缓释效果较差;当骨架材料为高黏度型号K100M、K15M、K4M时,由于高黏度的HPMC形成的凝胶层的分子链较长,形成凝胶层较厚,骨架溶蚀较长,药物的释放依次变快。
2.5.3 HPMC用量的考察 本研究考察单独使用HPMC K100LV和HPMC K4M时,不同HPMC用量对药物释放的影响,缬沙坦释放曲线见图3C,沙库巴曲释放曲线见图4C。结果显示,在研究用量范围内,单独使用HPMC K100LV作为骨架材料时,缬沙坦和沙库巴曲在前期释放均较快,产生突释现象,骨架不能保持完整的外形,缓释效果较差;当单独使用HPMC K4M作为骨架材料时,随着用量的增加,缬沙坦和沙库巴曲的释放均减慢,在研究用量范围内8 h缬沙坦和沙库巴曲累计释放度低于80%,释放不完全。单一规格的HPMC在一定程度上能使许多药物缓慢释放,但是很难达到平稳释药且释药速率调节不够灵活[10-12],因此本研究联合使用HPMC K4M和HPMC K100LV作为二元骨架材料制备沙库巴曲缬沙坦缓释片。
2.5.4 填充剂种类的考察 分别选用无水乳糖、甘露醇和微晶纤维素为填充剂,用量为25%,保持其他条件不变,按“2.4”项下方法制备缓释片,缬沙坦曲线结果见图3D,沙库巴曲释放曲线见图4D。结果显示,填充剂相同时,缬沙坦的释放较沙库巴曲的释放略快,填充剂的种类对缬沙坦和沙库巴曲的释放几乎无影响。因无水乳糖可压性和流动性好,性质稳定,压成的药片光洁美观,选择无水乳糖为填充剂。
2.5.5 润滑剂用量的考察 为了增加颗粒的流动性,防止压片过程中出现黏冲,本研究选用硬脂酸镁和微粉硅胶作为润滑剂,润滑剂用量分别为片重的2%、3%、4%,保持其他条件不变,按“2.4”项下方法制备缓释片,缬沙坦释放曲线见图3E,沙库巴曲释放曲线见图4E。结果显示,润滑剂用量对缬沙坦和沙库巴曲的释放几乎无影响,当润滑剂用量2%,压片过程中出现轻微黏冲现象,当润滑剂用量为3%时可起到较好的润滑作用,故将润滑剂用量定为3%。
2.5.6 硬度的考察 分别选用5~7 kg·cm-2、8~10 kg·cm-2、11~13 kg·cm-2的硬度制备缓释片,缬沙坦释放曲线见图3F,沙库巴曲释放曲线见图4F。结果显示,在研究范围内片芯硬度对药物的释放影响较小,硬度在5~7 kg·cm-2时,片剂表面粗糙且脆碎度较大,不利于后续薄膜包衣;硬度在8~10 kg·cm-2时,片剂光滑美观且脆碎度满足要求,因此,本研究将片剂硬度范围定为8~10 kg·cm-2。

图3 不同因素对缬沙坦释放行为的影响Fig 3 Effect of different factors on the release behaviors of valsartan

图4 不同因素对沙库巴曲释放行为的影响Fig 4 Effect of different factors on the release behaviors of sacubitril
2.6 中心复合设计-效应面法优化处方
2.6.1 试验设计 经单因素考察可知,联合应用HPMC K100LV和HPMC K4M能更好地控制药物释放。因此,本文以HPMC用量(X1,%)和HPMC K100LV占HPMC的比例(X2,%)为考察对象,选取各处方缬沙坦在pH 6.8磷酸盐缓冲溶液中2、6、8 h 的累积释放度作为评价指标,利用二因素五水平中心复合设计-效应面法筛选沙库巴曲缬沙坦钠缓释片最优处方,因素水平见表3,试验结果见表4。

表3 中心复合设计试验中的变量水平Tab 3 Variable levels in central composite design test

表4 中心复合设计试验中的自变量(X)和因变量(Y)Tab 4 Independent variable (X) and dependent variable (Y) in central composite design test
2.6.2 二次回归模型的建立 利用软件Design-Expert 10.0对表4试验数据进行回归分析,得二次多元回归模型。模型①Y2h=27.22-11.24X1+2.62X2-2.78X1X2+7.29X1
2-0.064X22(r=0.9257);模型②Y6h=64.61-17.13X1+5.86X2-0.97X1X2+5.81X12+2.30X22(r=0.9651);模型③Y8h=78.97-13.58X1+4.80X2+2.35X1X2+1.41X12+1.49X22(r=0.8994)。各方程对应的3D效应面图见图5。

图5 自变量X1、X2与因变量Y2 h、Y6 h、Y8 h的3D效应面图Fig 5 Response surface plot showing the effect of X1 and X2 on Y2 h,Y6 h, and Y8 h
2.6.3 方差分析和显著性检验 由以上3个拟合方程的相关系数可知模型拟合程度良好,可以用此模型对沙库巴曲缬沙坦钠缓释片处方进行分析和预测。从表5回归系数的显著性检验可知,模型①中X1、X2、X12项显著,其他项不显著;模型②中X1、X2、X12项显著,其他项不显著;模型③中X1、X2项显著,其他项不显著。
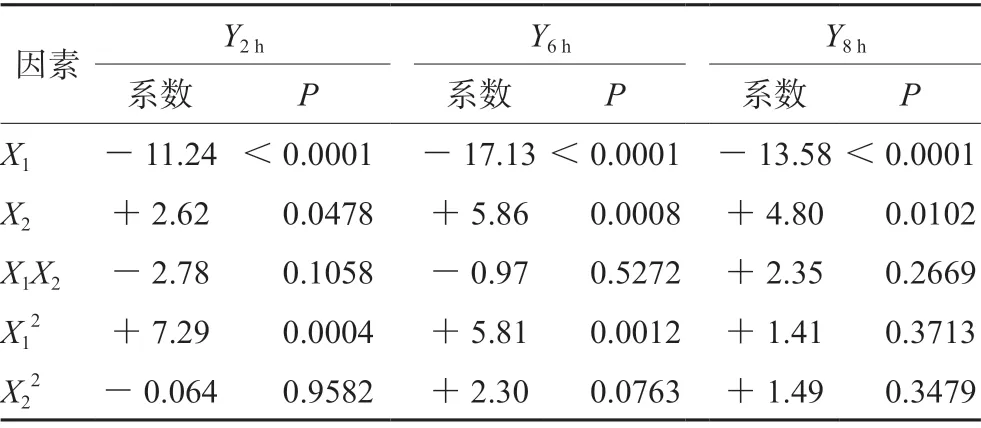
表5 方差分析结果Tab 5 ANOVA
2.6.4 效应面优化与预测 根据《化学药物口服缓释制剂药学研究技术指导原则》规定缓释片的体外释放要求,选取各处方缬沙坦在 2、6、8 h共3个点的累积释放度作为评价指标,释放度标准分别为2 h:25%~35%;6 h:65%~80%;8 h:不低于85%。设定处方的优化条件为:25%≤Y2h≤35%,65%≤Y6h≤80%,Y8h≥85%,软件综合评价后给出的最佳处方:HPMC用量(X1)为25%,HPMC K100LV比例(X2)为71%,即最优处方为沙库巴曲/缬沙坦 400 mg,HPMC K100LV 用量18%,HPMC K4M用量7%,无水乳糖用量25%,硬脂酸镁用量1.5%,微粉硅胶用量1.5%,按照“2.4”项下方法制备3批缓释片,并按照“2.1”项下方法测定各时间点缬沙坦的累积释放度,结果见表6,释放度的预测差值小于5%,说明模型预测性良好。

表6 优化处方缬沙坦释放度的预测值与观测值Tab 6 Optimal formulation of predicted and observed values of valsartan release
2.7 不同释放介质对药物释放的影响
沙库巴曲在低pH介质中易降解(12 h大约降解6%),而缓释片的释放度试验往往持续时间较长,因此为了避免药物降解产生误差,本文仅考察最优处方制备的骨架缓释片在pH 4.5醋酸盐缓冲溶液、pH 6.8磷酸盐缓冲溶液、水介质中的释药行为,缬沙坦释放结果见图6A,沙库巴曲释放结果见图6B。结果显示,相同介质条件下缬沙坦的释放比沙库巴曲略快,在不同介质中,缬沙坦和沙库巴曲在水中的释放最快,pH 6.8磷酸盐缓冲溶液次之、pH 4.5醋酸盐缓冲液中最慢,药物在不同介质中的释放行为差异可能由于是共晶中药物溶解性具有pH依赖性。

图6 不同释放介质对药物释放行为的影响Fig 6 Effect of different dissolution media on the drug release
2.8 释药模型
缓释制剂的释药机制与其所用的缓释材料具有密切关系,其释药过程是缓释材料、水和药物复杂的相互作用的结果。缓释骨架片中药物的释放机制主要是药物在凝胶层中的扩散和凝胶层的溶蚀。溶解度大的药物,释药机制主要表现为扩散;溶解度小的药物,释药机制主要表现为凝胶层的溶蚀,因此药物在水中的溶解性影响骨架片的释药过程[13]。本文对处方优化后的沙库巴曲缬沙坦钠缓释片各指标成分在pH 6.8磷酸盐缓冲溶液中的体外释放度数据进行零级动力学方程、一级动力学方程、Higuchi方程和Ritger-Peppas方程拟合,研究沙库巴曲缬沙坦钠缓释片的体外释药机制,结果见表7。
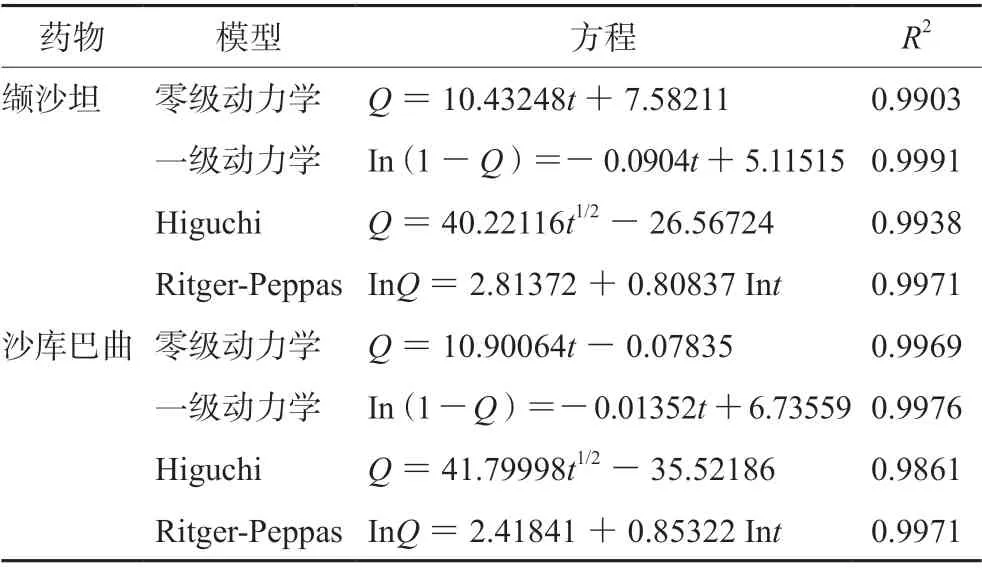
表7 沙库巴曲缬沙坦钠缓释片释药曲线拟合Tab 7 Release pattern of sacubitril/valsartan sustained-release tablets
结果显示,沙库巴曲缬沙坦钠缓释片各指标成分体外释放度数据与一级动力学模型拟合程度最高,相关系数最大;根据Ritger-Peppas方程,缬沙坦和沙库巴曲扩散指数分别为0.8084和0.8532(介于0.45~0.89),表明沙库巴曲缬沙坦缓释片的释放符合non-Fick扩散机制,即药物既具有骨架结构的扩散,也具有骨架的溶蚀瓦解而释放药物的特点。
3 讨论
目前国内外最常用的亲水凝胶骨架材料是HPMC,其遇水后水化形成凝胶层,凝胶层的性质直接影响药物的释放速率,是控制药物释放的重要因素。不同型号的HPMC水化和溶蚀速度不同,因而控制药物释放的效果不同。本研究通过对HPMC的型号和用量进行筛选,最终确定以HPMC K4M和HPMC K100LV作为骨架材料制备沙库巴曲缬沙坦钠缓释片。采用中心复合设计-效应面法优化处方并量化各因素之间的相互影响,通过Design-Expert 10.0软件综合分析后得到了沙库巴曲缬沙坦钠缓释片的最佳组成,其释放度的预测值和实测值基本一致,说明模型预测性良好,可用于优化处方。本试验优化后的处方体外释放结果表明,HPMC K4M和HPMC K100LV作为沙库巴曲缬沙坦钠的二元亲水凝胶骨架,可有效地控制药物的释放速度。
本研究制备的沙库巴曲缬沙坦缓释片工艺简单,研发和生产成本较低,适合工业化生产,具有较大的临床应用价值,但其体内外相关性仍需进一步研究。
