复方藏茴香治疗功能性消化不良作用机制及药效验证研究*
2021-07-02朱慧明冯小龙
朱慧明,乔 莉,冯小龙
(石家庄学院化工学院 石家庄 050035)
FD又称消化不良,基于功能性胃肠病罗马Ⅳ标准[1],FD临床以上腹部疼痛或烧灼感、餐后饱胀、早饱、过度嗳气等上消化道症状为主要表现,世界范围内广泛流行,西方国家发病率为9.8%-20.2%,中国大陆地区为11.8%-23.8%[2]。临床上无特效治疗方案,目前临床上常见治疗方法多为促进胃肠动力、抑制胃酸分泌及胃粘膜保护药物疗法,如胃复安、吗丁啉、西沙必利等,上述药物的治疗作用单一,且副作用较多。因此,研究开发用于治疗FD的药物具有十分重要的意义,近年来,用中成药治疗FD的临床报道增多,并显示出一定优势[3]。
复方藏茴香[4]是正在研发的中药5类新药,目前处于III期临床实验阶段,适应症为FD,主要由薄荷油[5,6](Peppermint Oil)和藏茴香油[7](Caraway Oil)组成。
薄荷油系从唇形科植物薄荷(Menthɑhɑplocɑlyx Briq)中提取的挥发油,具有清凉止痒、解痉、利胆、溶石、抗炎镇痛作用,可治疗头痛、晕船、反胃、胃肠气胀等,主要含有薄荷醇、薄荷酮及薄荷酯类化学成分[8]。薄荷醇和薄荷酮是药典收载薄荷油的含量测定指标性成分,具有较强的利胆作用,可促进胆汁排出[9]。薄荷油在欧洲也具有较长的药用历史,是一种安全有效的肠易激综合征(IBS)治疗用药[10],瑞士Tillotts Pharma公司生产的薄荷油肠溶包衣胶囊[11,12](Colpermin,含薄荷油约187 mg)已在欧盟多个国家上市销售。
藏茴香油系从藏茴香(Cɑrum cɑrvi L.)药材中提取的挥发油,该药性温、味微辛,有芳香健胃驱风理气之功,用于治疗食欲不振、胃脘疼痛、腹胀、消化不良及小肠疝气等症[13],主要含香芹酮(carvone)、柠檬烯(limonene)及β蒎烯等萜烯化学成分[14]。香芹酮能延长豚鼠组胺、乙酰胆碱性哮喘的引喘潜伏期,对豚鼠气管有直接松弛作用,并有抗氨甲酰胆碱作用,可抑制豚鼠离体气管Schultz-Dale反应,抑制过敏介质释放和拮抗过敏介质引起气道收缩,发挥呼吸道抗过敏作用[15]。柠檬烯具有祛痰、止咳、平喘,溶解胆结石,镇静中枢神经等作用,以柠檬烯为主要成分的复方柠檬烯胶囊,具有利胆溶石,理气开胃,消炎止痛的功效[16]。
现有临床实验结果表明,复方藏茴香治疗FD安全有效,疗效持续至停药2周后[4]。但由于其化学成分复杂、作用广泛,在FD治疗中发挥作用的有效成分及其相关作用分子机制尚不清楚,因此,本研究将采用网络药学方法,对该药潜在活性成分及其作用靶点进行预测分析,同时采用部分实验验证其活性,明确药物的药效物质基础及作用机制,为该药临床研究、后期推广及同类药物的开发提供参考。
1 材料与方法
1.1 化学成分库的构建
检索中药系统药理学分析平台数据库(TCMSP,http://tcmspw.com/index.php)及查阅相关文献收集薄荷油和藏茴香主要化学成分,利用PubChem数据为库(https://pubchem.ncbi.nlm.nih.gov/)对其分子结构进行确认,结合Chemdraw软件获取主要成分、CAS号、分子式、分子量、化学结构式、SMILES等信息,并将每个化学成分的结构式保存为mol格式,用于后继分析。
1.2 化合物靶点筛选
分别用STITCH,Swiss TargetPredict,TCMSP数据库预测化学成分的靶点[17],对TCMSP预测结果保留“validated”的靶点,对STITCH和SwisstargetPredict预测结果选取有结合性的靶点,将获得的靶点进一步在Uniport(https://www.uniprot.org/)数据库上获取标准化命名,最终得到化学成分作用靶点数据库。
1.3 FD相关靶点筛选
通过在DrugBank[18]数据库(https://go.drugbank.com/)和OMIM[19]数据库(https://omim.org/)中输入关键词Functional dyspepsia搜索已报道的与FD相关的基因,去除重复基因,得到FD疾病相关靶点数据库。
1.4 网络构建与分析
将化学成分作用靶点和FD疾病相关靶点进行匹配,得到复方藏茴香治疗FD的潜在作用靶点,将复方藏茴香化学成分和潜在作用靶点导入Cysopscape 3.7.2软件,构建化学成分-潜在作用靶点网络,利用NetworkAnalyzer工具计算网络拓扑参数,包括度值(Degree)、介数(Betweenness centrality,BC)[20],确定关键节点,分析潜在活性成分和关键作用靶点。
1.5 基因功能和信号通路分析
将潜在作用靶点导入DAVID数据库,Select identifier设置为Official gene symbol,List type设置为Gene list,限定物种为人,根据P<0.05作为筛选条件,对复方藏茴香作用靶点进行GO功能富集,并获得KEGG通路富集结果[21]。
1.6 活性化合物的筛选
采用ADMET Predictor 9.5软件[22],对作用于潜在作用靶点的化学成分进行药代动力学预测研究,选择人体的吸收分数%Fa≥40%和人体口服生物利用度%Fb≥30%作为筛选指标[23],结合文献中化学成分的含量信息,以化学成分的含量≥1%为指标,最终筛选出药物中主要活性成分。
1.7 药效学验证
1.7.1 醋酸扭体法观察复方藏茴香对小鼠的镇痛作用
选取健康昆明种小鼠,体重23-25 g,雌雄各半,按性别、体重随机分为对照组、复方藏茴香35、70、140 mg·kg-1、阳性药阿司匹林200 mg·kg-1剂量组,共5组,每组10只,灌胃给药,给药容积均为0.1 mL/10g体重,小鼠给药后1 h,均腹腔注射0.6%醋酸溶液0.01 mL·g-1体重,记录15 min内小鼠的扭体次数。
1.7.2 对大鼠血清胃泌素含量的影响
选取健康Wistar种大鼠,体重200-250 g,雌雄兼用,按性别、体重随机分为对照组、复方藏茴香25、50、100 mg·kg-1、阳性药硫酸阿托品2.5 mg·kg-1剂量组,共5组,每组8-11只,灌胃给药,灌胃容积均为0.01 mL·g-1体重,对照组给予等容量对照液。大鼠禁食供水24 h后,再灌胃给药1次(共2次),末次灌胃给药1 h后,眼眶取血2 mL,立即3500 rpm离心10 min,分离血清置-20℃冰箱待测,采用放免法进行胃泌素的测定。
1.7.3 对多巴胺致小鼠胃排空抑制的影响
选取健康昆明种小鼠,体重20-23 g,雌雄各半,按性别、体重随机分为空白对照组、盐酸多巴胺模型对照组、复方藏茴香35、70、140 mg·kg-1及阳性药硫酸阿托品5 mg·kg-1剂量组,共6组,每组10只,小鼠禁食供水18 h后,灌胃给药,给药容积为0.01 mL·g-1体重,模型对照组和空白对照组分别给予等容量对照液和蒸馏水,于给药后1 h,除空白对照组外,其余各组均腹腔注射盐酸多巴胺2.54 mg·kg-,并同时灌胃给予营养性半固体糊0.8 mL/只,20 min后脱颈处死动物,剖腹、取胃、称量胃全重和净重,计算胃内残留率。
2 结果
2.1 复方藏茴香中活性成分和作用靶点
通过TCMSP数据库并检索相关文献[24-26]共收集到72个化学成分,主要为小分子化合物,对72个化学成分的作用靶点进行检索,其中有作用靶点的化学成分为68个,共获得作用靶点180个。
运用Cytoscape软件构建化学成分-靶点网络,如图1所示,红色节点为活性化合物,绿色为靶点,网络拓扑学分析显示,化合物的平均度数为16.82,说明复方藏茴香中潜在化学成分具有多靶点属性,其中度数较大(度数>17)的化合物共29个,藏茴香中含量较高的主要成分香芹酮和柠檬烯的度数分别为39和15,薄荷油中含量较高的主要成分薄荷醇和薄荷酮的度数分别为24和14。

图1 复方藏茴香活性成分-作用靶点网络图
2.2 潜在作用靶点网络分析
将化学成分作用靶点和FD疾病相关靶点(共341个)进行匹配,共获得14个潜在作用靶点,通过String获得14个潜在靶点的蛋白相互作用关系,导入Cytoscape软件绘制蛋白相互作用网络(图2),节点大小表示度值的大小,对网络拓扑学特征进行分析,发现14个靶点组成2个作用网络,γ-氨基丁酸-多巴胺网络和激素受体网络。
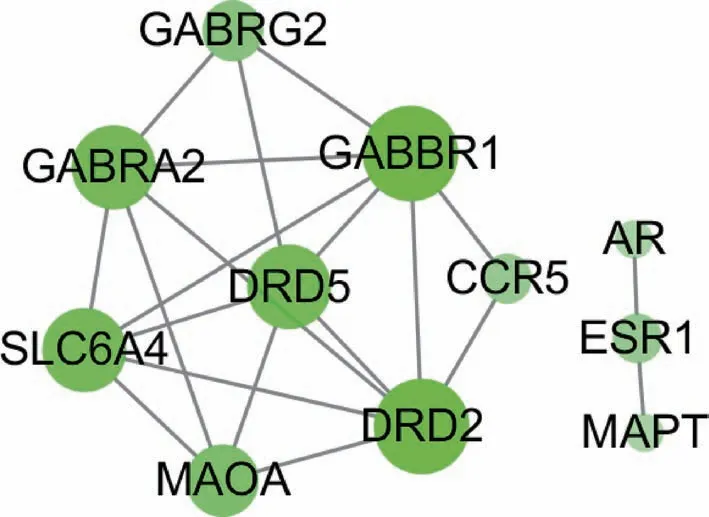
图2 潜在作用靶点蛋白质-蛋白质相互作用网络图
运用Cytoscape软件构建潜在化学成分-潜在作用靶点网络,如图3所示,红色节点为活性化合物,绿色为靶点,网络拓扑学分析显示,共有42个化学成分作用于潜在作用靶点,平均度数为2.85,其中最大度值为6,表明复方藏茴香中成分具有多靶点属性,且多个成分均可以作用于潜在作用靶点;潜在作用靶点的平均度数为8.57,度数较大的靶点有4个,分别为AR(度数38)、ESR1(度数26)、SLC6A4(度数17)和GABBR1(度数13),14个潜在作用靶点信息见表1。
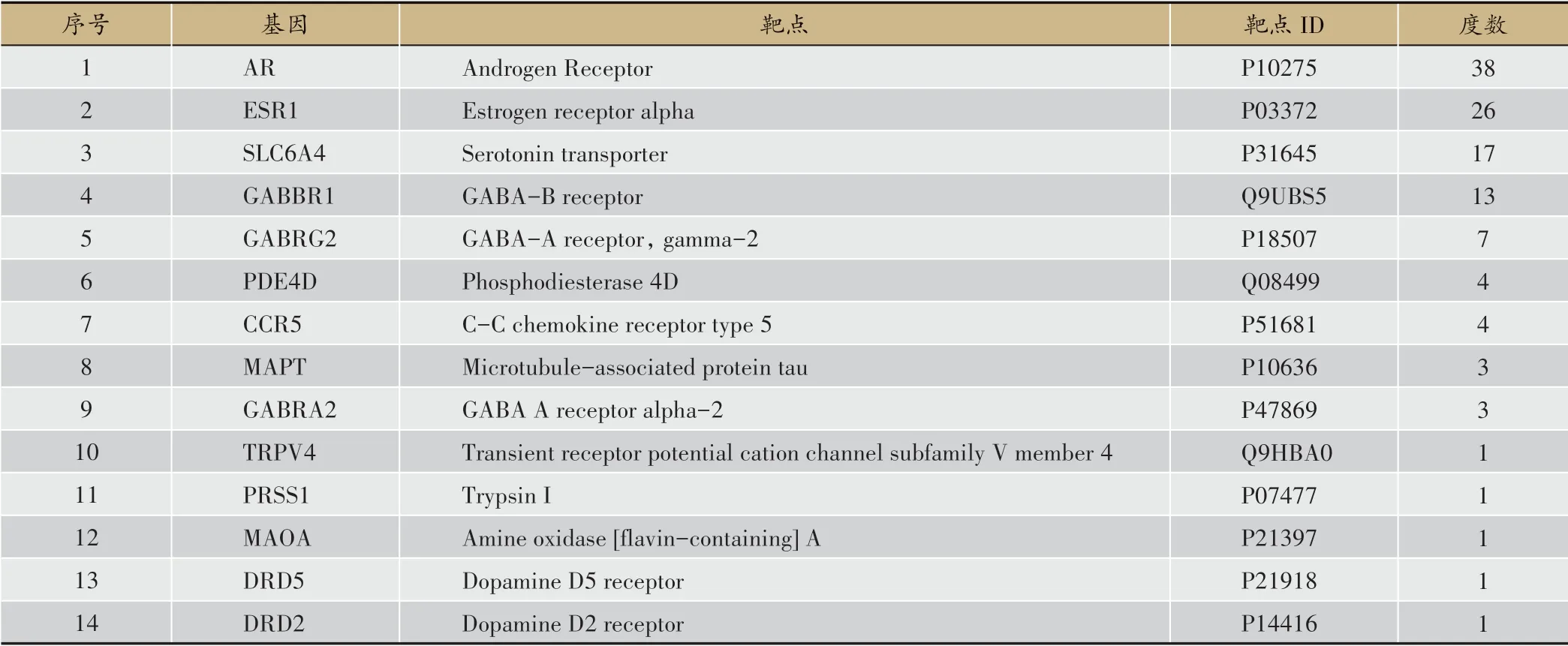
表1 活性成分潜在靶点信息
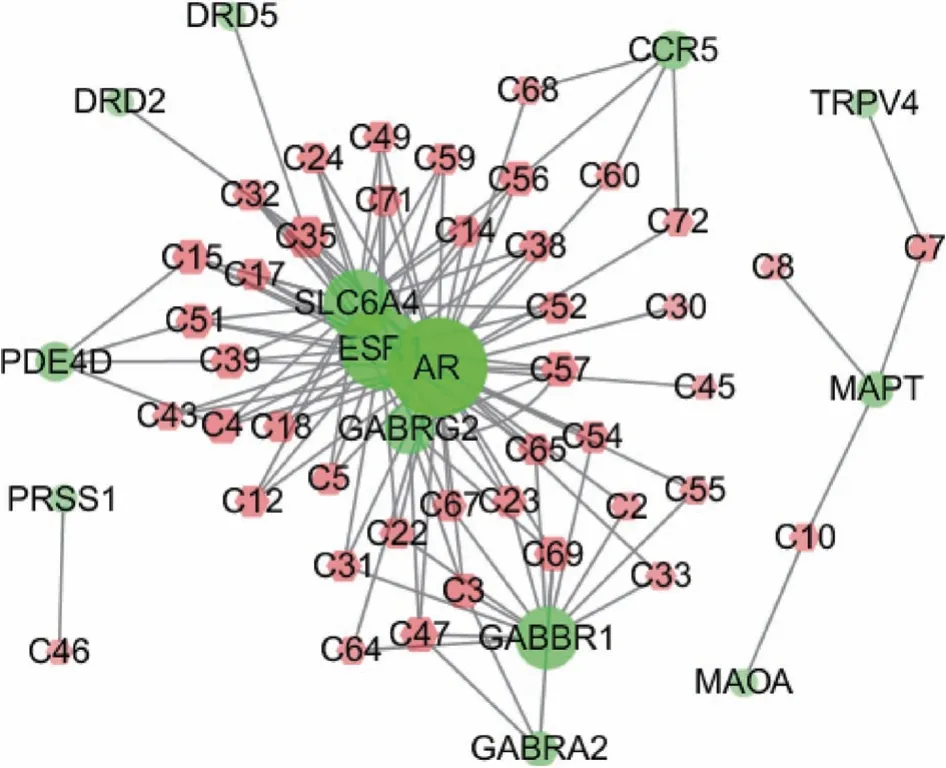
图3 复方藏茴香活性成分-潜在作用靶点网络图
2.3 潜在作用靶点生物学功能分析
将14个潜在作用靶点映射到DAVID数据库中,设定P≤0.05,进行GO功能富集分析和信号通过分析,共发现9个富集分析结果和1个信号通路(表2)。富集分析结果涉及到的生物过程有4个,主要是氯化物运输、γ-氨基丁酸信号通路、多巴胺能突触传递和磷脂酶C激活多巴胺受体信号通路;分子功能有3个,包括多巴胺结合、GABA-A受体活性和细胞外配体门控离子通道活性;细胞组成2个,包括GABA-A受体复合物和质膜的组成成分。通路富集分析表明神经活性配体-受体相互作用(Neuroactive ligand-receptor interaction)是复方藏茴香的主要作用通路。

表2 复方藏茴香作用靶点基因功能和蛋白通路
2.4 主要活性成分分析
为进一步确定主要活性成分,对42个作用于潜在作用靶点的化学成分进行预测筛选,结合化学成分在药物中的含量[25-26],采用ADMET Predictor软件中人体生物利用度预测评估系统,选择1 mg和10 mg 2个剂量,以%Fa≥40%和%Fb≥30%作为筛选指标,共筛选出潜在活性成分共17个,藏茴香油中4个,薄荷油中13个,其中,香芹酮和薄荷醇分别是藏茴香油和薄荷油中含量最高的成分,预测结果见表3。
表3可见,化合物平均分子量156.43,最大分子量为257.42,均为小分子化合物,所有化合物在不同剂量(1.0 mg和10 mg)下的吸收分数%Fa值均较高,表明此类药物在肠道内渗透性良好,且生物利用度值均在40%以上,文献报道,两种挥发油中含量较高的香芹酮和薄荷醇在人体内吸收良好[27],表明此类小分子化合物口服给药后在人体内可以被吸收利用。
2.5 药效学验证
2.5.1 镇痛作用
通过以上研究发现,复方藏茴香可影响神经活性配体-受体相互作用,可能具有止痛作用,因此在动物体内进行了验证实验(表4)。
由表4可见,与对照组比较,阳性药阿司匹林有明显镇痛作用,复方藏茴香70、140 mg·kg-1剂量组明显减少醋酸致小鼠的扭体次数,与空白对照组相比具有统计学差异。此结果表明,复方藏茴香有明显的镇痛作用,起效剂量为70 mg·kg-1,随剂量增加作用增强。
表4 复方藏茴香对小鼠的镇痛作用(±s,n=10)
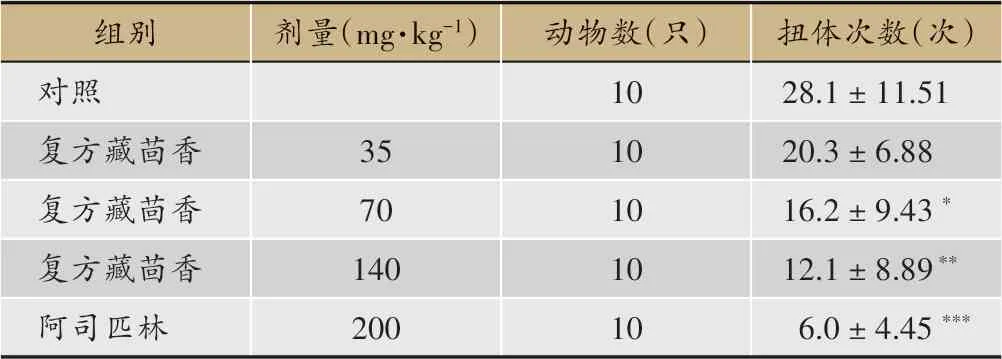
表4 复方藏茴香对小鼠的镇痛作用(±s,n=10)
注:*P<0.05,**P<0.01,***P<0.001(与对照组比较)
组别对照复方藏茴香复方藏茴香复方藏茴香阿司匹林剂量(mg·kg-1)35 70 140 200动物数(只)10 10 10 10 10扭体次数(次)28.1±11.51 20.3±6.88 16.2±9.43*12.1±8.89**6.0±4.45***
2.5.2 血清胃泌素含量影响
复方藏茴香对大鼠内分泌的影响,结果见表5。
表5 复方藏茴香对正常大鼠血清胃泌素含量的影响(±s)
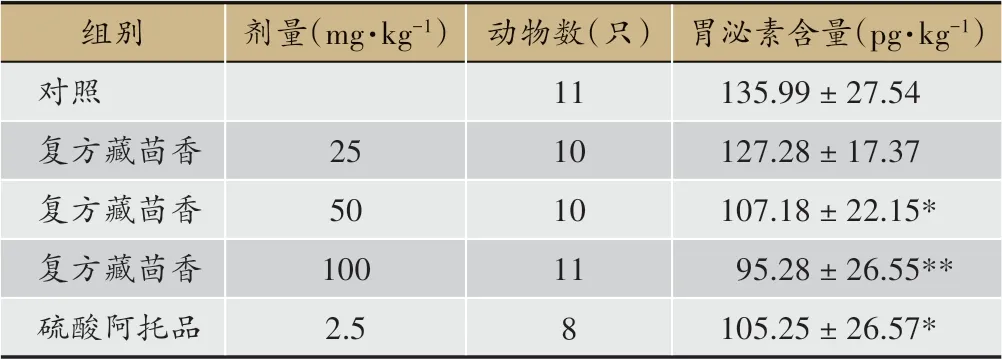
表5 复方藏茴香对正常大鼠血清胃泌素含量的影响(±s)
注:*P<0.05,**P<0.01(与对照组比较)
组别对照复方藏茴香复方藏茴香复方藏茴香硫酸阿托品剂量(mg·kg-1)25 50 100 2.5动物数(只)11 10 10 11 8胃泌素含量(pg·kg-1)135.99±27.54 127.28±17.37 107.18±22.15*95.28±26.55**105.25±26.57*
结果表明,复方藏茴香50、100 mg·kg-1灌胃给药能降低正常大鼠血清胃泌素含量,并随剂量增加,作用增强,阳性药硫酸阿托品亦有明显作用。
2.5.3 对多巴胺致小鼠胃排空抑制的影响
复方藏茴香对多巴胺致小鼠胃排空的影响,结果见表6。
表6 复方藏茴香对多巴胺致小鼠胃排空抑制的影响(±s)
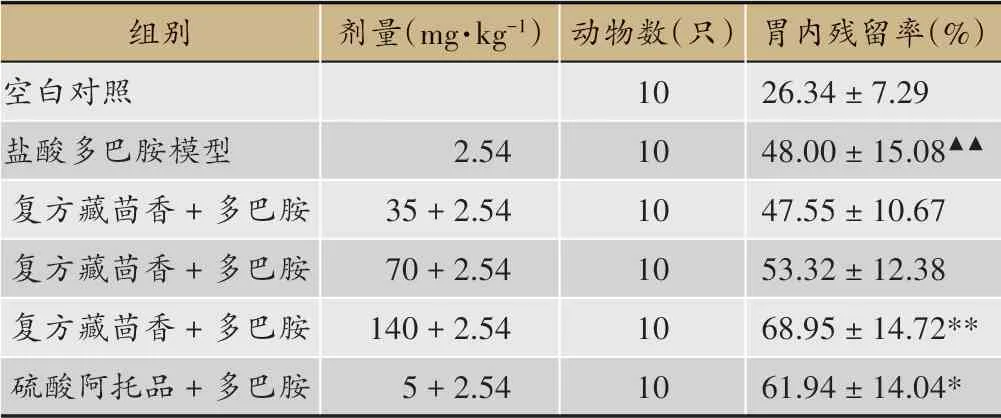
表6 复方藏茴香对多巴胺致小鼠胃排空抑制的影响(±s)
注:△P<0.05(与空白对照组比较),*P<0.05,**P<0.01(与多巴胺模型组比较)
组别空白对照盐酸多巴胺模型复方藏茴香+多巴胺复方藏茴香+多巴胺复方藏茴香+多巴胺硫酸阿托品+多巴胺剂量(mg·kg-1)2.54 35+2.54 70+2.54 140+2.54 5+2.54动物数(只)10 10 10 10 10 10胃内残留率(%)26.34±7.29 48.00±15.08▲▲47.55±10.67 53.32±12.38 68.95±14.72**61.94±14.04*
结果表明,复方藏茴香140 mg·kg-1可增加多巴胺致小鼠胃排空抑制作用,并随剂量增加,作用增强。阳性药硫酸阿托品也有增加多巴胺致小鼠胃排空抑制作用。
3 讨论
FD虽然为常见病,但其发病机制暂不明确,相关机制包括胃肠运动功能障碍、内脏高敏感、胃酸、Hp感染、精神心理因素、脑肠肽等[28]。功能性胃肠病罗马系列标准的推出,促进了FD的基础及临床研究,逐渐明确FD的发生与胃肠道动力异常、内脏高敏感性有关,与胃肠黏膜炎症、局部免疫功能异常及肠道菌群改变等可能有关,脑-肠轴异常在FD的发病机制中占有重要地位[29]。传统的脑-肠轴从肠神经系统的局部调控、自主神经系统和中枢神经系统三各层面影响肠道功能,同时肠道和大脑之间还可以通过内分泌、脑肠肽、肠道菌群等体液途径实现双向调节,从而维持正常的胃肠功能,病理情况下,脑肠相互作用的外周和中枢改变可能是慢性腹痛和胃肠道功能障碍症状的基础[30]。本研究中发现,复方藏茴香具有多成分多靶点的特点,通过氯化物运输、γ-氨基丁酸信号通路、多巴胺能突触传递、磷脂酶C激活多巴胺受体信号通路等生物过程,影响GABA-A受体复合物、质膜的组成成分,作用于神经活性配体受体相互作用信号通路,从而实现对消化道肠神经系统、神经内分泌、间质细胞和平滑肌细胞等消化道动力系统的调节,从而发挥综合治疗作用,药效学研究结果表明,复方藏茴香具有镇痛,降低正常大鼠血清胃泌素含量,影响胃排空等作用。
在活性化合物预测研究中,目前多采用药物相似性(drug-likeness,DL)[21]结合口服生物利用度(oral bioavailability,OB)作为的筛选指标,当DL≥0.18(整个相似度的平均值)则认为该化合物与Drugbank数据库中药物具有一定的相似,成药性较好。本研究发现,所有化合DL的平均值为0.05,均小于0.18,此指标不适合用于挥发油类小分子化合物的筛选。因此药代动力学指标发挥着重要作用,中药化学成分复杂,口服给药后在体内需经过吸收、分布、代谢及排泄过程到达靶点器官和组织发挥作用,为了提高预测研究结果的准确性,本研究中运用ADMETPredictor软件中人体生物利用度预测评估系统,建立了以表示活性成分在肠道内渗透性的%Fa≥40%和人体口服生物利用度%Fb≥30%[23]的筛选标准,同时为减少了微量成分对作用机制的干扰,结合以化学成分含量≥1%组成综合指标,提高了预测结果的准确性,共确定以香芹酮和薄荷醇为代表的主要活性成分的17个。
网络药理学是以系统生物学理论为基础,融合多向药理学、生物信息学和计算机技术,具有整体性和系统性的特点,与中医药整体观的原则相一致[31]。通过构建蛋白相互作用网络,探索药物与疾病间的关联,阐明中药作用机制,并可以指导新药研发。本研究构建了复方藏茴香“活性成分-靶点”等网络,从整体角度对药物进行了系统研究,网络分析结果表明,AR、ESR1、SLC6A4和GABBR1可能为复方藏茴香关键作用靶点。已有研究表明,AR并不在肠道上皮细胞内表达,却在肠道固有层的间充质细胞表达,间充质细胞在接收雄激素信号后,会分泌大量Bmp信号的抑制分子,减少Wnt拮抗信号分子的分泌,Bmp信号具有抑制肠干细胞分化的作用,Wnt有促进肠干细胞增殖的作用,两种信号协同维持肠干细胞自我增殖的稳态[32],AR与肠道相关疾病密切相关。雌激素及其受体与胃肠道疾病的发生及预后存在相关性,尤其在胃食管反流病、食管癌、消化性溃疡、胃癌、炎症性肠病、肠易激综合征和结肠癌的发生、发展中起到了不同的作用[33],肠道中雌激素受体的对正常的上皮结构具有维持作用,同时具有抑制肠道炎症作用,ESR1信号通路可能与胃黏膜肠上皮化生过程有关,并在其中发挥重要作用[34]。5-羟色胺转运体SLC6A4在中枢和外周均能通过调控5-羟色胺的表达影响肠道的病理生理功能,在肠道疾病中发挥重要作用[35],经验方痛泻安脾肠可通过调节大鼠5-羟色胺和5-羟色胺转运体水平,缓解腹痛、腹泻、腹胀等不适症状[36]。GABA能信号系统在小肠上皮细胞功能性表达,可通过GABA受体影响小肠液体分泌[37],GABA能信号系统激活后,破坏结肠粘膜屏障,增加肠通通透性,加重肠道有害细菌入侵,加重结肠粘膜炎症反应[38],GABA通过不同受体调节不同共存递质的释放而在胃肠动力的兴奋与抑制中发挥协调作用[39],GABA可通过改善肠黏膜屏障损伤,缓解TNBS-乙醇溶液诱导的实验性结肠炎[40]。
综上所述,FD多有胃肠运动功能紊乱、迷走神经功能亢进,体内乙酰胆碱、组胺等物质释放增多现象,导致胃肠运动与分泌亢进而出现胃肠道痉挛、疼痛、胀气、胀满等消化道症状,复方藏茴香中以香芹酮和薄荷醇为代表的主要活性成分,通过作用于AR、ESR1、SLC6A4和GABBR1等关键靶点,影响神经、神经内分泌、脑肠肽等途径调控脑-肠轴系统,影响胃肠道动力系统并产生镇痛等作用,达到治疗FD的目的。
FD临床治疗无特效药,复方藏茴香临床实验已显示了一定的治疗优势,但其成分复杂,作用机制不明确。本研究采用网络药理学方法对复方藏茴香主要药效成分、药物作用靶点、药物与疾病相互作用通路进行了研究,并通过动物体内实验验证了网络药理学的结论,明确了复方藏茴香多成分-多靶点-多通路的治疗FD的作用特点,加深了对复方藏茴香用于治疗FD的认识,为复方藏茴香分子机制的深入研究奠定了基础,同时为后期临床研究中观察指标的选择,临床方案的制定提供参考,并为加快此类药物开发,提高药物临床应用的科学性合理性提供理论依据。
