改良单针法纵向套叠显微输精管附睾吻合术(“大家泌尿网”观看手术视频)
2021-07-01涂响安廖武源吕坤龙龙世颖庄锦涛周明宽邓春华
涂响安,廖武源,吕坤龙,龙世颖,庄锦涛,周明宽,邓春华
(1.中山大学附属第一医院男科,广东广州 510070;2.郑州大学第一附属医院男科,河南郑州 450000)
不孕不育症在全球范围内已受到越来越多的关注,据文献报道,全球不孕不育症的发病率约为15%,其中男性因素占50%[1]。在过去数十年里,伴随着男性精子数量的下降,男性不育症的发病率有所上升,而梗阻性无精子症(obstructive azoospermia,OA)是男性不育的一个重要原因。梗阻性无精子症可由男性精子流出道(包括睾丸输出小管、附睾、输精管、射精管)任意一处的双侧梗阻导致,其中又以输精管/附睾梗阻最为常见,占55%~67%[2]。引起附睾梗阻的原因主要有输精管结扎术、特发性因素、感染、医源性因素和肿瘤性病变等。在欧美,输精管结扎术为附睾梗阻发生的主要原因[3],而在我国则以特发性因素为主[4],近些年也有多篇文献研究表明,约50%~70%的附睾梗阻患者有附睾炎病史[5-6],这提示感染亦是我国附睾梗阻的重要病因之一。
得益于显微输精管附睾吻合术(microsurgical vasoepididymostomy,MVE)的发展,附睾梗阻可以通过手术重建的方式使之复通。MVE不仅需要手术医师进行严格的显微外科系统学习,并积累足够多的显微外科手术经验,还要求手术医师要有足够的耐心来完成精细准确的手术操作。因此,MVE通常被认为是最具技术挑战的男性不育显微外科手术。输精管附睾吻合术的出现可溯及上世纪初,然而,在引入显微外科技术之前,输精管附睾吻合术不仅成功率不高,术后的复通率及妊娠率也很低。随着显微技术的发展,美国的SILBER教授在1978年首次报道了显微镜下输精管附睾(端-端)吻合术治疗附睾梗阻性无精症,术后复通率可超过50%。此后,又经历了三针套叠和横向套叠缝合技术的改进,特别是康奈尔大学CHAN等[7]于2003年报道了纵向套叠的缝合方式,该缝合方式使得附睾小管到输精管的吻合口管腔更大,而这种纵向套叠显微输精管附睾吻合术(longitudinal intussusception microsurgical vasoepididymostomy,LIVE)的复通率也更高;康奈尔大学MONOSKI等首次报道了一种单针输精管附睾吻合缝合技术,不同于昂贵且需要特制的双针缝合线,这种单针缝线易于获得,且临床试验证明,使用双针缝线与单针缝线的MVE术后复通率差异无统计学意义[7-11]。正是在前辈们的努力下,MVE蓬勃发展,成为了附睾梗阻手术治疗的“金标准”。而我们团队则在康奈尔大学团队的纵向套叠技术以及单针缝合技术的启发下,将二者结合,对MVE进行了创新性的改良,开创了改良单针法纵向套叠MVE,不仅能保证术后复通率,而且能缩短手术时间、避免交叉缝合,效果令人满意[6,11,13]。本文将结合自身经验,对改良单针法纵向套叠MVE的手术步骤及操作要点等方面进行阐述。
1 术前准备
配合手术良好的患者,可使用腰硬联合麻醉;如果预计手术时间较长、患者无法配合或在其他复杂情况下可使用全身麻醉。体位取平卧位。消毒后可于阴囊下垫一团夹纱或治疗巾以抬高阴囊,便于手术时对阴囊进行操作。由于手术时间较长,且术后须绝对卧床休息,一般术前常规留置尿管。
2 手术步骤
2.1 输精管的准备在阴囊纵隔旁取适宜长度的纵切口,一般为3 cm,用尖刀依次切开皮肤、皮下组织、肉膜等结构,直至睾丸鞘膜层表面,自切口处将睾丸及精索提出并暴露于视野内,仔细辨认,找出输精管后用电刀切开精索外筋膜和提睾肌,暴露并游离输精管阴囊段。于近睾端约1~2 cm处半切开输精管(图1A),观察有无精液流出,如未观察到精液,则可再次证实存在附睾梗阻。然后向输精管腹腔端注入亚甲蓝溶液1 mL后再注入足量生理盐水(图1B),如尿液颜色为蓝色或淡蓝色,则说明输精管腹腔端通畅。
2.2 附睾小管的准备用电刀小心切开睾丸鞘膜,将显微镜放大倍数调至8~12倍后仔细观察附睾体、尾部并寻找出扩张的、饱满的附睾小管,于附睾小管饱满处将附睾外膜圆形切开备用(图1C)。
2.3 输精管与附睾的吻合在原半切开处完全切断输精管,近睾端予以结扎,腹腔端则小心游离至足够长度。在鞘膜下方分离出一足够输精管通过的通道,注意避免损伤血管,然后将输精管腹腔段从此通道内拖入,并用9-0或8-0 Prolene线将输精管浆膜与附睾外膜缝合2针,起固定、减张之用,以便后续的吻合;将显微镜调整至12~18倍的放大倍数,在输精管切开面行“四点标记”(图1D),然后用2根10-0单针Prolene线行纵向套叠吻合术(即2根单针先分别由外到内从输精管浆肌层a1和b1处进针,在输精管腔内出针(图1E),再纵向平行贯穿附睾小管并留置(图1F),在两针之间纵向切开附睾小管至见附睾液流出,抽吸附睾液术中送检证实存在活精子后,从附睾小管上出针,然后由内到外分别从输精管腔内进针,于输精管浆肌层a2和b2处出针(图1G),最后拉紧2根缝线将附睾小管切口套入输精管腔内之后分别打结,完成吻合。套叠完成后用9-0 Prolene线将附睾外膜与输精管浆肌层缝合固定10~12针(图1H),缝合间距须均匀细密,以免附睾液漏出。吻合示意图如图2所示。吻合完毕后仔细止血,切口逐层关闭。
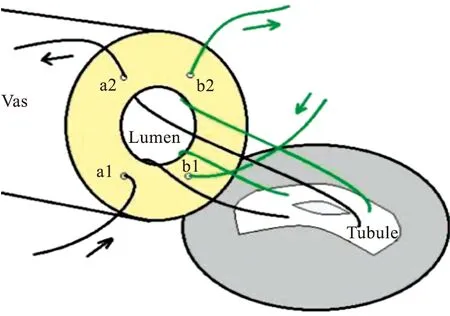
图2 改良单针法纵向套叠示意图[12]
3 术后处理
3.1术后需卧床休息并留置尿管3~5 d(视患者情况而定),避免进行剧烈活动,以免出现吻合口或伤口裂开、阴囊血肿等。
3.2术后伤口包扎时注意提吊阴囊,减少伤口张力。
3.3术后预防性使用抗生素,以免发生切口感染。
3.4术后1.5个月内禁止性生活,1.5个月后开始恢复排精;可在医生指导下口服促进生精药物;术后定期(一般为术后第1.5和第3个月各1次,之后每3个月1次直至术后1年)复查精液常规以证实复通。
4 手术的注意要点及自身经验
4.1 手术适应证的把握诊断附睾梗阻有以下要点:①2次以上(相隔6周以上)的精液常规检查提示无精子症;②精浆中性α-糖苷酶下降而精液量、pH、精浆果糖以及性激素水平正常;③阴囊触诊可能触及质硬附睾;④阴囊彩超及经直肠彩超提示睾丸、精囊和射精管无异常,而附睾部位淤积性改变(通常表现为附睾网格状改变);⑤必要时行睾丸活检证实生精功能存在。
4.2 术中远端输精管的探查远端输精管的通畅是进行MVE的必要条件。部分附睾梗阻患者可能会因感染、手术损伤等各种原因合并输精管梗阻,如果未经探查便盲目进行输精管与附睾的吻合,可能会导致手术失败。探查远端输精管是否通畅的方法一般是往远端输精管注射亚甲蓝,如若术中注射亚甲蓝溶液后尿液变为蓝色,则证实远端输精管通畅,可继续行输精管附睾吻合;反之则为梗阻,需要进一步处理。对于梗阻者,我们团队探索出用亲水性导丝对梗阻的远端输精管进行探查[14],根据插入导丝的长度以确定梗阻部位,进而决定后续处理。
4.3 单针法与纵向套叠缝合方式的改良目前,MVE常用的缝线可分为单针与双针;附睾小管切口的方向可分为纵向与横向。而根据这两方面,MVE主要包括单针法横向套叠、双针法横向套叠、双针法纵向套叠以及单针法纵向套叠。我们所用的单针纵向套叠法主要有以下优势:①对比昂贵且难以获得的双针缝线,单针缝线易于获取,特别是在双针缝线不可用的情况下,外科医师可采用单针法开展输精管附睾吻合术;②改良单针法改变了缝针顺序,操作更加简单,能够有效缩短手术时间,并且能避免交叉缝合,因此改良单针法更为高效、安全;③相较于横向套叠,纵向套叠的方式使吻合口管腔更大,术后复通率也十分可观;④我们将改良单针法与纵向套叠相结合,在保证术后复通率的同时,不仅拥有上述的优点,而且更易于手术医师进行学习与操作,对推广泌尿男科显微手术有相当积极的作用。
4.4 游离输精管是否保留输精管血管MVE作为治疗附睾梗阻的“金标准”术式,在游离输精管的过程中是需要结扎输精管血管的。国外的多篇文献报道了MVE的复通率超过80%[7,10],而国内的MVE复通率普遍不高于国外[8-9,11-13],我们考虑国内复通率较低的原因可能是输精管血管的结扎。国外附睾梗阻的主要原因为输精管结扎术,在输精管结扎时已经一起将输精管血管结扎,因此在行MVE前有足够时间代偿性地重新建立起输精管和附睾的局部血运;而在我国则以感染为主,既往并未结扎输精管血管,故在行MVE时结扎输精管血管可能导致术后局部血运不佳而影响术后复通率。所以我们设计的保留输精管血管MVE是1种更针对病因、病理及生理的改良吻合方式。但保留了吻合处血运,能否提高术后复通率?我们团队近些年来一直在努力实施和改进该术式,2018年由吕坤龙等[6]报道了保留输精管血管的MVE术后获得了83.1%的复通率,对比我们既往研究中结扎输精管血管的MVE术后61.5%的复通率,提升较大。但相比于常规离断输精管血管的MVE,保留输精管血管的MVE对术后复通率乃至怀孕率、生育率是否有更加积极的影响还缺乏足够的证据,因此,我们正在进行一个多中心﹑前瞻性及随机对照的临床研究来佐证保留输精管血管的有效性。
4.5 MVE的门槛通常MVE被认为是难度最高的泌尿男科显微外科手术,故完成该手术需要一定的门槛。首先,术者需要经过专门的显微外科培训。不同于开放手术与腔镜手术,也不同于血管吻合、神经吻合等手术,男性不育显微外科手术更加精细。在所有外科手术中,男科显微外科精道重建是唯一让手术医生在完成手术后,不能立刻知道手术效果、需要耐心等待数周、数月方知结果的手术。这类手术不仅是对显微外科培训成效的检验,也是对手术医生素质的极大挑战。因为人类的输精管内径仅有300~400 μm,附睾小管的内径约150~250 μm,而用于缝合输精管与附睾的10-0 Prolene线小于15 μm更为细微,所以对术者的要求也更高,因此显微培训至关重要。
自2001和2004年李石华教授等在《中华男科学杂志》首次报道了男性不育的显微外科概念之后,男性不育方面的显微外科技术逐渐在我国发展起来[15-17]。近6年来,在邓春华和涂响安教授等的领导和实施下,本团队目前为止已举办了10期显微男科手术学习班,其特色是:为每位学员分别提供1台显微镜,进行一对一的培训,同时每天都有专家、教授进行授课,为学员介绍显微男科的前沿进展。在学员逐步上手显微操作后,学习班的教师们会带领他们进行手术演示,每位学员均能获得至少一次的机会辅助教师完成显微手术。每位学员都能在大鼠身上进行显微镜下输精管吻合以及输精管附睾吻合的动物实验练习。在为期1周的练习后,学员能够基本掌握显微技术,为日后当地医院显微男科手术的独立开展打下了坚实的基础。该显微男科学习班内容充实、精彩纷呈,广受国内各地学员的好评,对我国泌尿男科显微事业的普及与发展起着重要的推动作用。
5 未来与展望
随着视频光学技术的发展,视频显微外科(包括4K3D、8K3D Video Microsurgery等)的概念逐渐兴起[18]。传统手术显微镜的使用,需要将医生的头目和躯体固定在同一位置,因此长时间的显微手术会对手术医生的身体造成慢性损害,而高风险的姿势、不良的人体工程学设计也会导致颈椎、躯干、肩部等部位的疾病,从而造成许多外科医生的慢性疼痛和职业损伤甚至残疾,缩短外科医生职业寿命,并可能间接严重影响手术安全[19-21]。而视频显微手术的优点是在不影响手术效果的前提下,不仅能提供更清晰的手术视野,而且能使手术医生以平视的方式进行手术,减轻医生的身体负担。近20年以来,众多学者在视频显微手术方面做出了诸多大胆的尝试,现已初步应用于泌尿男科。康奈尔大学李石华团队HAYDEN等[22-23]报道的4K3D OBYEYE视频显微手术具有如下优势:出众的人体工程学设计、轻便灵活、快速自动对焦、更为宽阔的工作距离(200~550 mm)、较佳的景深、高质量的4K3D视频输出、学习曲线短(针对有经验者)、零图像延迟、便于教学和分享等,从而提高了手术效率和教学质量。上述优势使得4K3D视频手术显微镜有机会引领未来显微外科手术的新方向。CHEN和HALPERN等[24-25]从男性不育显微外科的视角,详细论述了新近出现的视频手术显微镜的历史和现状,并指出男性生殖医学领域最新的技术创新即是视频显微外科。涂响安等[26]报道的裸眼3D辅助下输精管附睾吻合术,则证实了新的视频显微手术效果与传统的显微镜手术相比并无劣势(图3)。如果以上结论可经过进一步的研究证明,则视频显微手术可大力推广开来,这对手术医生的健康、显微手术效率及教学质量的提高将大有裨益。
6 总 结
MVE是国际公认治疗附睾梗阻的“金标准”。它不仅能提高附睾梗阻患者的自然怀孕率及生育率,还能够提高辅助生殖的成功率,使患者尝试辅助生殖的周期缩短,减轻了患者的经济负担。因此,MVE已成为附睾梗阻患者效果最好、效益最高的治疗方式。而改良单针法纵向套叠MVE在此基础上,使用了单针法纵向套叠的缝合方式,不仅减少了手术时间,有效避免了交叉缝合的情况,使该手术操作较其他术式更易上手,适用于大部分医师,而且能够保证具有同样高的术后复通率,手术并发症也极少。所以,该术式适合大范围推广,尤其是基础设施相对落后的基层医院。探索并解决男性不育的问题任重而道远,相信随着社会的发展和科技的进步,该手术以及其他泌尿男科显微手术能更广泛地惠及大众,更好地解决男性不育的难题。
7 致 谢
感谢美国康奈尔大学的李石华教授在百忙之中抽空为本文提出了宝贵的意见和点睛的修改,谨向李石华教授致以最真诚的谢意!
