锰氧化物催化剂催化燃烧挥发性有机物的研究进展
2021-06-29孙苓瑕
黎 靖 程 琰 孙苓瑕 杨 楠
(西南交通大学地球科学与环境工程学院,四川成都,611756)
随着石油、化工行业的日益发展,VOCs逐渐成为环境空气污染物中的主要成分,并引起诸多环境问题,如臭氧、光化学烟雾等。目前已有多种技术可用于VOCs的处理,如吸附、膜分离、冷凝、直接燃烧、催化燃烧和光催化等。在这些处理技术中,催化燃烧技术能够在较低温度下,对中、低浓度的挥发性有机物实现完全无害化处理,生成二氧化碳和水,不会造成二次污染,因此被认为是一种有效且绿色的处理技术[1]。催化剂是催化燃烧技术的核心,因此如何设计高效的催化剂是催化燃烧VOCs的关键问题。
常用的催化剂主要有贵金属和过渡金属催化剂。贵金属催化剂虽然性能优异,但是其成本较高,同时热稳定性较差且容易中毒,从而限制了其工业化的发展。因此,低成本、高稳定性的过渡金属氧化物催化剂得到了更多研究者的青睐。在众多过渡金属氧化物中,MnOX因为其具有多种可变化合价(+2、+3、+4、+7)以及良好的电子转移能力,能够进行快速的氧化还原反应,而表现出优异的催化活性。锰氧化物催化剂的催化活性与其结构、形态、表面化学状态以及多组分间协同作用等多种因素有着密切的关系。本文综述了近年来锰氧化物催化剂对VOCs催化燃烧的相关研究,讨论了单一型、掺杂型和负载型锰氧化物催化剂的结构形态以及对其催化活性的影响,为今后催化燃烧VOCs的研究提供一定参考。
1 单一型锰氧化物催化剂
由于锰元素具有多种可变价态,其可以形成如Mn2O3、Mn3O4、MnO2和MnO等多种氧化物。不同价态的锰氧化物催化剂在特定的条件下会表现出不同的催化活性。Kim等人[2]在研究中发现,得益于存在易于还原的Mn3+-O键,Mn3O4催化剂具有良好的氧迁移率,从而表现出优于MnO2和Mn3O4的催化活性;而Wang等人[3]在比较MnO2以及Mn2O3和Mn5O8的混合氧化物的催化性能中发现,MnO2催化剂由于具有更好的低温还原性和更高的表面吸附氧含量,而表现出更好的甲苯催化性能。单一型锰氧化物催化剂对VOCs催化活性可能受到催化剂的晶体结构和形貌、氧化还原能力以及活性氧种类等多种因素的影响。
1.1 晶型结构
MnO2的晶形结构是由[MnO6]八面体单元通过共用角或边的方式形成各种隧道及层状结构。在自然界中,MnO2晶体可被分为六种晶形结构:α-MnO2、β-MnO2、γ-MnO2、ε-MnO2、λ-MnO2和δ-MnO2,各类型MnO2的晶体结构模型示意图如图1所示。可以明显看到,α-MnO2、β-MnO2、γ-MnO2和ε-MnO2都为隧道结构;λ-MnO2是一种典型的尖晶石结构,具有(1×1)隧道;δ-MnO2具有由[MnO6]八面体形成的二维层状结构。其中,α-MnO2的(2×2)大尺寸隧道可容纳大多数金属阳离子(如K+、Ca2+、Na+、Mg2+、Ba2+或Pb2+)和水分子。二维层状δ-MnO2属于典型的单斜晶系,层间距较大,可容纳大量水分子、金属阳离子等物质。
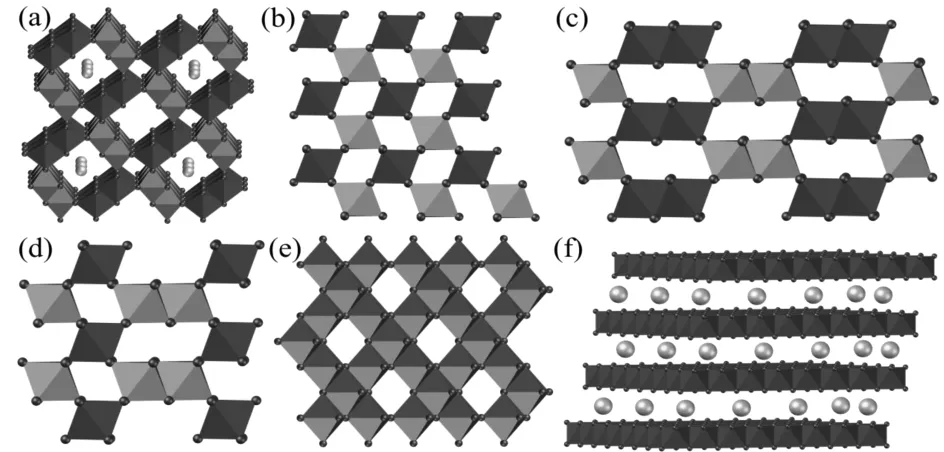
α-MnO2(a)、β-MnO2(b)、γ-MnO2(c)、ε-MnO2(d)、λ-MnO2(e)、δ-MnO2(f) 图1 各类型MnO2的晶体结构模型示意图
MnO2的不同晶型会影响其催化燃烧性质。Li等[4]通过水热法合成了纳米棒状的α-、β-、γ-MnO2和δ-MnO2催化剂,并比较了它们的甲苯催化燃烧活性。催化燃烧活性的顺序为β-<α-<γ-<δ-MnO2。δ-MnO2中的特殊层状结构使甲苯更容易被吸附在催化剂表面,因此其催化燃烧活性最好。Zhang等[5]采用水热法制备了α-,β-,γ-和δ-MnO2催化剂,并研究了各催化剂的催化燃烧性能。在四种催化剂中,δ-MnO2因为其特殊的层状结构,同时表面具有相对最多的活性氧物种,而表现出最高的甲醛催化性能。
1.2 形貌控制
形貌控制可以为纳米结构材料带来以下好处:(1)增加比表面积;(2)促进氧空位和表面缺陷的形成。到目前为止,已经获得了多种形态的MnO2晶体,并对其形貌依赖性的吸附和催化性能进行了研究。Wang等[6]通过控制水热合成温度(140、240和120 ℃)制备了一维纳米棒、线和管状的α-MnO2,比较了不同形貌的锰氧化物对甲苯催化活性的影响。他们发现,这些样品中氧的浓度和低温还原性均按α-MnO2纳米棒>α-MnO2纳米管>α-MnO2纳米线的顺序降低,这与它们对甲苯的催化脱除性能的顺序一致。在后续工作中,他们[7]再次通过水热法合成了纳米棒α-MnO2、纳米花ε-MnO2和纳米哑铃β-MnO2催化剂,催化活性顺序为纳米棒α-MnO2>纳米花ε-MnO2>纳米哑铃β-MnO2。
1.3 缺陷工程
表面缺陷会直接影响MnO2的活性,这些缺陷可以将分子氧或H2O转化为活性物质。根据Mars-Van Krevelen机理,晶格氧直接参与VOCs的氧化,因此其含量越高,催化活性越强。较高的氧空位有利于晶格氧中电子的转移,提高晶格氧活性。氧空位在金属氧化物中普遍存在,可作为多相催化反应的吸附位点和活性位点。
Dong等[8]在研究中说明了氧空位对MnO2的化学性质起着重要的调节作用。他们通过掺杂不同量的Cu2+取代二维层状MnO2中间层中的K+,从而产生不同浓度的氧空位。适量的氧空位能够增强催化剂中氧自由基的活性并提高其低温还原性。但是,氧空位浓度过高时,将不利于甲苯的催化燃烧。Wang等[9]使用四丁基氢氧化铵(TBAOH)合成了含有表面凹坑的Birnessite-MnO2,用于甲醛的催化燃烧。TBAOH产生的空间效应导致不规则的表面凹坑产生,表面凹坑的存在不仅提供了更大的比表面积,而且增加了不饱和锰和氧原子的数量,促进了氧化还原反应。
2 掺杂型锰氧化物催化剂
掺杂金属阳离子可以调控MnO2的物理化学性质。一方面,碱金属的引入会扰乱活性中心的电子态,增加电子基团的数量,促进O2-和-OH的循环再生;另一方面,金属阳离子取代配位的Mn3+和Mn4+,必然会改变配位环境,产生氧空位或影响邻近Mn-O键的键能,进而调节活性位点的活性。
2.1 K+掺杂
近年来,有研究报道称钾离子的掺杂对MnO2的形貌、晶体形态以及催化性能都会产生很大的影响。Wang等[10]通过氧化还原反应合成了4种具有不同层间阳离子(K+、Mg2+、Ca2+和Fe3+)的Birnessite型MnO2催化剂。其中,钾离子的引入增强了表面氧的活性,使表面氧与水反应以弥补催化过程中消耗的-OH,从而促进HCHO被连续完全氧化。Liu等[11]在高浓度KOH水溶液中合成了一种厚度为15 nm的MnO2纳米带,发现K+浓度会直接影响到纳米带的生长。Rong等[12]在系统研究了K+含量对Birnessite型MnO2的晶体形态、形貌及催化性能的重要影响后得出结论:较高的K+含量促进了催化剂中晶格氧的活性。然而,由于过量的K+与周围的氧原子相互作用,使得氧原子的迁移率降低,导致MnO2降解甲醛的催化活性降低。
2.2 其他金属掺杂
与其他金属氧化物的结合是提高催化性能的另一种常用方法。用于加入锰氧化物的金属元素通常包括Ce、Cu、Co、Fe、Ni、Zn和Cr等。在本文中主要阐述Ce、Cu和Co金属掺杂的相关研究。
Ce具有良好储氧/释氧能力和氧化还原性能,因此Ce能够明显增强锰氧化物的催化能力。Du等[13]采用水热合成法制备了Mn0.6Ce0.4O2催化剂。研究发现,在甲苯的催化燃烧过程中,Ce主要作用于甲苯的吸附,而Mn主要催化燃烧甲苯。后续研究者Quiroz等[14]研究了酸处理对MnOX-CeO2混合氧化物催化甲醛的影响。当MnOX-CeO2固溶体中的Mn含量稳定在50%以下时,酸处理对材料的结构和氧化还原性能力没有影响,然而当Mn在CeO2中的溶解度超过50%后,酸处理会极大地改变这些性质。
在Cu-MnOX催化剂中,通常认为CuXMn2O4尖晶石为主要活性相。Cu和Mn在催化过程中,以Mn3++Cu2+↔Mn4++Cu+的过程进行电子交换,因此Cu的加入使MnOX具有丰富的氧空位和良好的氧化还原能力。Li等[15]和Kim等[16]两个团队在研究金属阳离子掺杂时,得出了相同的结论,即在各种X-MnOX催化剂中,Cu-MnOX催化剂对甲苯的催化活性最高,说明Cu是修饰MnOX的优良元素。后续研究者Li等[17]采用一步水热氧化还原法制备了Cu-Mn双金属氧化物。结果表明,通过控制Cu/Mn的摩尔比可以调节所制备材料的晶格缺陷和氧空位浓度。其中,尖晶石结构的MnCu0.5中活性氧的含量和迁移率相对最高,可直接提高MnCu0.5的催化活性。
Co3O4具有许多电子缺陷,有利于活性氧的形成。因此Co也被认为是修饰MnOX的理想掺杂金属。Li等[18]采用氧化还原方法制备了具有缺陷的新型钴锰二元氧化物,该二元氧化物具有非晶态和高缺陷的特点,从而表现出优异的低温还原性和晶格氧迁移率。值得注意的是,作为一种有效的缺陷工程策略,非晶态二元氧化物表现出了优异的活性,可以为开发高效VOCs催化剂提供一些启示。
3 负载型锰氧化物催化剂
载体在催化剂中的促进作用主要有两点:(1)适当的载体可以分散活性成分,防止或延缓颗粒的聚集;(2)为催化反应的发生提供了空间。对于负载型锰氧化物催化剂,其活性主要取决于载体的性质、金属-载体的相互作用以及活性组分的负载量。例如Jung等[19]对比了在不同载体上,锰氧化物的甲苯催化性能,得到如下活性顺序:MnOX/γ-Al2O3>MnOX/SiO2>MnOX/TiO2,而这主要与氧化物中缺陷的数量有关。Guo等[20]研究了Cu-Mn活性相与Y型沸石、SiO2、γ-Al2O3、TiO2的协同作用,结果表明:由于在SiO2表面形成了大量的Cu-Mn固溶体,并存在较多的Cu2+和Mn3+离子,Cu-Mn/SiO2表现出最佳的活性和稳定性。
负载量对活性组分的分散性、催化剂的比表面积以及表面氧物种的浓度有显著影响,从而影响催化活性。Qin等[21]人研究了载体形态(棒状、六方和纤维状)对MnOX/SBA-15催化剂的影响。其中,MnOX/棒状SBA-15催化剂具有最为丰富的表面活性和良好的氧迁移率。对于沸石材料,可以通过改进离子交换方式和调整硅铝比来提高载体性能。Soylu等[22]通过不同的离子交换剂(NaCl、NH4NO3、NH4Cl)和离子交换次数(1.5、6、12、24、48、72 h)对斜发沸石(CLT)样品进行离子交换,制备出一系列MnO2/CLT催化剂。对比发现,在用NH4NO3处理CLT达到48 h后,CLT的催化活性达到最佳,这中间Lewis酸度为决定因素。
4 结论与展望
本文主要介绍了三种类型的锰氧化物催化剂对VOCs的催化燃烧。在单一型锰氧化物催化剂中,常通过调节催化剂的晶形结构、形貌和缺陷空位改性优化催化剂。在掺杂型锰氧化物催化剂中,钾离子以及Ce、Co、Cu的掺杂能够与Mn产生协同作用,从而提高了催化性能。最后,对于负载型锰氧化物催化剂,选择适当的载体,对载体进行改性处理,可以获得更大的比表面积、更好的分散性以及更强的金属-载体相互作用,从而提升催化性能。
在未来的研究中,还有一些问题值得我们去深入探讨。虽然VOCs在MnO2表面的氧化反应遵循MVK机制,但部分污染物在氧化过程中的主要中间体和反应路径尚不清楚。此外,对于亚表面晶格氧和表面吸附氧种、Mn3+和Mn4+在VOCs催化燃烧中的作用尚无一致意见。因此,对于VOCs在MnO2催化剂表面的催化燃烧机理尚需进一步研究。
