微生物燃料电池研究进展
2021-06-29李欣鹏
刘 禹, 李欣鹏
(中电建生态环境集团有限公司, 广东 深圳 518100)
微生物燃料电池(Microbial Fuel Cells,MFCs)是一种利用产电微生物将有机物中的化学能转化为电能的装置,该技术近十几年来发展迅速[1-3]。关于MFCs的产电研究发展方向主要集中在MFCs有机废弃物利用(生活及工业有机废水、有害物质降解),输出功率的提升(反应器构型优化、内阻降低,优势产电菌研究)与MFCs成本降低(电极材料及催化剂研究、无离子膜反应器研究)三大方向,且在各研究方向上均取得了一定突破,研究成果能够为MFCs的大规模应用提供理论与数据支撑[4]。随着研究的不断深入,出现了以微生物为催化剂降解有机物,且在连接负载或外加电压下可获得某些产物的微生物电化学系统(BES),在降解有机废弃物的同时,实现产能,H2与化学品合成,有机及无机污染物(氮、硝、酚类、重金属)去除等功能,展现了BES的广阔发展前景[5]。本文主要对微生物燃料电池反应器构型、利用底物及产电微生物的种类进行进展综述。
1 微生物燃料电池工作原理研究进展
微生物燃料电池技术的产电基础是氧化还原反应的发生,较为特别的是MFCs的氧化半反应是在微生物的催化作用下完成的[6-8]。图1是典型的双室型MFC的工作原理图[9]。MFC装置通常由阳极室、离子交换膜、阴极室组成。在阳极室内,有机污染物被微生物催化降解,微生物在代谢过程中产生电子和质子,产生的电子转移到阳极上再通过外电路传至阴极形成电流,发生氧化反应;在阴极室内,产生的质子通过离子交换膜到达阴极后与O2和电子发生还原反应生成H2O[8-11]。氧化还原过程的进行不断消耗电子与质子,进而促进微生物降解有机物的进程继续进行,电子与质子不断产生、传递、消耗形成闭合的电流回路[9-11]。在反应过程中需要严格保持MFCs阳极室的厌氧环境,其一是阳极室内的溶氧会改变阳极上的菌群结构,使好氧菌增多降低产电效率;其二是阳极室内的溶氧会取代电极成为电子受体与电子直接发生反应生成水而降低产电效率[9, 11]。

图1 双室型MFC工作原理图
2 反应器构型
MFCs的反应器构型从构造上分为单室型MFCs与双室型MFCs两大类[9-10, 12]。双室型MFCs由于阴、阳极距离较远,且中间隔有离子交换膜而具有较高内阻,常被用于特殊底物的产电研究、膜材料及阴、阳极等材料的性能测试等[13]。单室型MFCs没有阴极液,常以空气电极作为阴极,形成单室型空气阴极MFCs。相较于双室型MFCs,单室型MFCs没有阴极室而节省了一定了的材料成本,并且由于阴、阳极距离较小,内阻减小,输出功率密度增加[8-9, 14-15]。
单室型MFCs根据电极与膜的结构分布不同可分为3类:阴阳极与离子膜一体型MFCs[16]、阴极与离子膜一体型MFCs[17-19]、无离子交换膜型MFCs[20-22]。空气阴极MFCs常用含有Pt催化剂的碳基材料作为阴极,无需曝气,减少了MFCs的反应能耗。但其缺点是阴极含Pt催化剂成本较高,对于无膜型MFCs,氧气会透过阴极渗透进入阳极室抑制阳极厌氧产电菌生长,同时阴极上附着的好氧菌会与阳极厌氧产电菌形成竞争关系,降低反应器的库伦效率[13, 18]。
从形态上双室型MFCs又分为H型MFCs与方形MFCs,H型MFCs与方形MFCs构造如图2和图3所示[14]。通常H型MFCs的阴、阳极距离较远,且离子交换膜面积较小,导致H型MFCs的功率密度较小,但此型反应器操作简便且运行稳定常被用于基本参数测试、新底物利用、新型电极材料实验等基础研究中[14-15]。相较于H型MFCs,方形MFCs的阴阳极间距较小且其离子交换膜与电极的投影面积相似,因此方形MFCs能产生较高的输出功率[14-15]。

图2 双室型H型MFCs
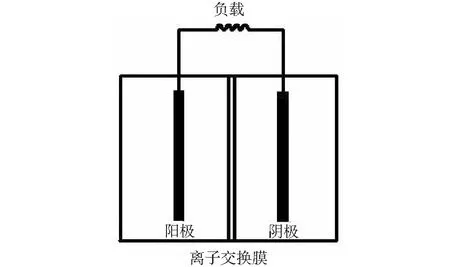
图3 双室型方型MFCs
除以上两种常用MFCs反应器构型外,研究者为减小溶液与阳极间的传质阻力,增大底物与阳极微生物间的有效接触面积,提高反应器产电效率,陆续出现了平板型MFC与升流式MFC等构型。平板型MFC在阴阳极间制作出“蛇形”或“S形”流道,开发出连续流MFC常用以处理高浓度有机底物[23 -24]。升流式MFC结合了UASB技术原理,液体上流有利于改善反应器水力条件,利用液体流动性质减小传质阻力,提高产电性能[25]。
3 用于MFCs的底物种类
MFCs的底物利用范围非常广泛[26-27]。目前,MFCs的可利用底物既包括醋酸盐、葡萄糖等低分子量有机物,又包括纤维素类、淀粉等高分子量有机物;MFCs的底物利用种类也从单一有机物体系转化为可利用的工业污水、生活废水、活性污泥等复合有机物体系[8-9, 22, 27-28]。值得一提的是MFCs技术较其他生物处理技术(厌氧消化)的优势在于MFCs技术可降解含酚类(对微生物有毒害作用)底物[28-29]。MFCs技术的利用底物转变既扩宽了其应用范围又为MFCs技术降解广泛有机污染物奠定了理论基础[30-31]。
低分子量有机物易被微生物利用,降解速率较快,因此产能相对较高[32- 33]。醋酸盐是部分高分子有机物代谢过程的终产物,且极易被微生物利用,因此常被研究者用作基础研究底物[34]。Logan BE研究了分别以乙酸盐与丁酸盐作为单室型MFC底物的产能效果[35],研究表明以乙酸盐为底物的MFC的功率密度(506 mW·m-2)比以丁酸盐为底物的MFC的功率密度高了66%,且其CV的氧化还原峰强度(最大电流1100 μA)也明显高于以丁酸盐为底物的MFC的氧化还原峰强度(最大电流343 μA)。
甲酸盐、丙酸盐、丁酸盐也是常用的MFC产电底物[36]。甲酸盐用作MFC底物时产电效果较其他挥发性有机酸盐的产电效果差[37],其最大功率密度与库伦效率也是其中最低的。丁酸盐用作MFC底物时产电效果较以乙酸盐为底物时的产电效果差,Rabaey K[38]等通过DGGE分析发现以丁酸盐为底物的MFC阳极菌群结构与以乙酸盐为底物的MFC阳极菌群结构差异较大,而其与以丙酸盐为底物的MFC阳极菌群结构却更为相似。
葡萄糖作为一种可发酵型底物,可被多种微生物降解利用,因此以其作为MFC底物时,MFC阳极菌群结构较为丰富[39]。研究者认为在以葡萄糖为底物时会产生互养过程,葡萄糖在发酵过程中会被降解为复杂的终产物包括乙酸、丙酸等,这些发酵副产物被产电微生物利用进而解除了葡萄糖转化的反馈抑制,促进发酵过程的进行[40-41]。李晶[42]等认为以葡萄糖为单一底物的MFC在产电过程中,葡萄糖首先被降解为乙酸、丙酸、乳酸三种初级发酵代谢产物,乙酸、丙酸可直接被利用产电,乳酸则需进一步被降解才可用于产电,且乙酸较易被产电菌利用。由于葡萄糖可被多种微生物降解利用,因此常将其作为辅助底物辅助降解难降解基质,李婕等以铁氰化钾溶液为阴极电子受体,构建了双室型MFC,以硝基苯(NB)与葡萄糖为混合底物研究NB的降解情况,结果表明NB与葡萄糖的混合底物可用于MFC产电,而MFC未见以纯NB为底物产电的情况[43]。
近年来,难降解及成分复杂的有机物在MFC中的降解产电研究成为热点[44-45],研究者期望将各种有机废弃物(纤维素类生物质、生活废水、工业污水)用于MFC中,实现有机废弃物的生物降解与MFC产能的双重目的[44- 45]。
纤维素类生物质原料来源广泛,产量巨大,其中也富含丰富的营养物质(糖类、蛋白质、小分子酸等),但纤维素类生物质原料较难生物降解,当将其作为MFC底物时,通常需通过物理或化学手段进行预处理,将其表面难降解结构破坏或将其降解为易被微生物利用的有机物[46]。Zhang Y[47]等研究了小麦秸秆水解液的产电特性及菌群结构,发现小麦秸秆水解液初始底物浓度为1000 mg·L-1时最大功率密度为123 mW·m-2,库伦效率在15.5%~37.1%之间;阳极悬浮液中的菌群结构与阳极表面菌群结构不同,功能也存在差异,悬浮液中的微生物将基质降解为可被产电菌利用的简单产物,继而阳极表面的微生物再利用降解后的产物进行产电。冯玉洁[48]等利用单室型空气阴极MFC反应器,以纤维素降解菌与产电菌的混合菌为生物催化剂,研究了气爆玉米秸秆固体的产电效果,结果表明以纤维素混合菌H-C与生物污水最为接种物时可获得较高输出电压,最大功率密度可达406 mW·m-2,仅比以葡萄糖为底物时低20%。
生活污水是居民日常生活中排出的废水,其中含有蛋白质、碳水化合物、脂肪、尿素、氨氮等[49]。目前,MFC能够利用的生活废水COD浓度低于其他可利用基质COD浓度,且生活废水的电导率较低(1.5~2 mS·cm-1),上述两点导致生活废水在MFC中的功率密度较乙酸、葡萄糖等易利用基质的低[50-53]。Logan B E[54]针对MFC利用的生活废水COD浓度低的缺陷,进行了生活废水为底物的多重电极连续流MFC的产电研究,在不改变空间域COD浓度的前提下改变时间域域的COD浓度,结果表明通过多个MFC装置串联的方式可使单个装置的COD浓度波动降至最低。
工业废水是工业生产过程中产生的废液,其种类繁多且成分复杂,通常都会对环境及人类产生一定的危害,因此工业废水均需经过处理后方可排放[55]。汪家权等进行了MFC处理苯酚废水的研究,研究表明MFC较传统的厌氧消化有强化废水生物处理的作用,且MFC能够耐负荷冲击,即使在苯酚浓度3.5 g·L-1的高负荷情况下,MFC的苯酚去除率仍可达60%[56]。高雄英等进行了MFC处理含铬废水的研究,并比较了化学阴极MFC及生物阴极MFC的产电及Cr6+的去除情况,结果表明生物阴极MFC在产电及Cr6+的去除两方面均较优,生物阴极MFC的最大输出电压为180.1 mV,(化学阴极MFC最大输出电压139.4 mV),生物阴极MFC的Cr6+去除率为66.4%[57](化学阴极MFC的Cr6+去除率42.8%)。表1对文献中不同底物产电研究进行概括。

表1 不同底物的产电研究
4 阳极产电微生物
产电微生物是能将其代谢过程中产生的电子通过某种方式传递至反应器阳极的微生物,产电微生物的发现对MFCs的发展有重要意义[61]。阳极产电微生物决定着MFCs中电子的产生与传递,是影响反应器底物降解效果与产电效果最重要的因素[2]。研究发现,混菌MFCs的产电效果与运行稳定性均优于纯菌MFCs,混菌中不同功能的微生物相互协同与竞争,可将复杂底物降解的更加完全,表明各类微生物间的协同作用有利于提升MFCs的产电性能[52]。混菌MFCs更利于探究未知的产电微生物种类及其电子传递机理,扩宽MFCs的底物利用范围,提高其产电产电性能[12]。
研究发现的产电微生物主要集中在变形菌门(Proteobacteria)与厚壁菌门(Firmicutes)两个主要门类,产电微生物多为兼性厌氧菌,以无氧呼吸和发酵为主要的代谢方式,通过氧化有机物生成CO2,并在电子传递过程中获得其生长所需能量[61- 62]。
地杆菌(Geobacter)属于变形菌门(Proteobacteria),β变形菌纲(Deltaproteobacteria)是一类非常重要的产电微生物,其中的G.metallireducens、G.sulfurreducens、G.psychrophilus、Geopsychrobacterelectrodiphilus与Desulfuromonasacetoxidans是目前已发现的产电微生物[63]。有研究发现,将石墨电极或Pt电极插入厌氧海水沉积物中,与其相连的阴极插入有溶氧的水中,其间便会产生电流,对阳极上附着的微生物群落进行分析,结果显示Geobacteracea菌科为其中的占优菌科,说明Geobacteracea可将其产生的电子传至电极。Gmetallireducens为严格厌氧菌,能够氧化芳香族化合物并以其为电子供体,电子转化率较强[64]。
Gsulfurreducens为专性厌氧菌,不能运动,能够完全氧化电子供体(乙酸、氨气)且以电极为电子受体,无需外加氧化还原介体即可与阳极进行电子传递[65-66]。
希瓦氏菌(Shewanella)属于Proteobacteria菌门,γ变形菌纲Gammaproteobacteria是另一类研究较多的产电微生物,其中的S.Putrefaciens与S.oneidensis是目前已发现的产电微生物[67- 68]。Shewanella为兼性厌氧菌,在有氧情况下能够彻底氧化丙酮酸和乳酸生成CO2;在无氧情况下,Shewanella能够氧化乳酸、丙酮酸等,其电子传递方式为膜传递[69-70]。微生物燃料电池中的主要产电微生物如表2所示。
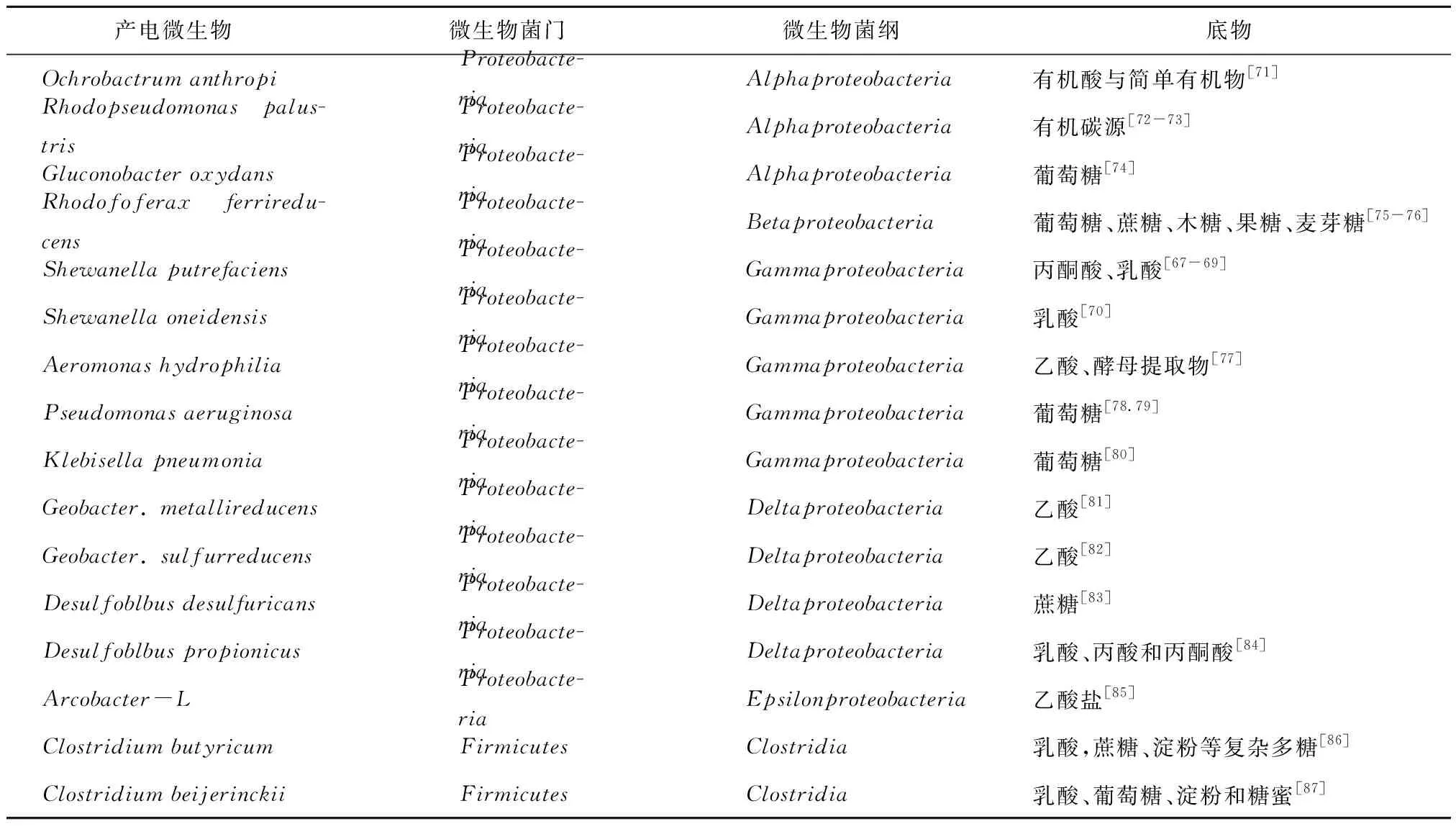
表2 不同底物的产电研究
5 结语
MFC作为一种新型有机废弃物处理及产能手段,已经成熟的应用于污染物底物处理领域,并具有良好的发展前景,但受制于电子低传输密度,使其工业应用化发展受到局限。
未来需继续针对微生物产电机理进入深入研究,提高微生物电子传输效率,同时进一步优化反应器结构,寻找更高效的电极材料。此外,还应持续研究该技术在有机废弃物处理(尤其是污染及毒害物质)方向、燃料及化学品合成方向、生物修复方向及生物医学方向的应用工艺条件及机理,使该技术具有产业化应用条件。
