基于营养风险筛查的个性化营养方案应用于失代偿期乙肝肝硬化患者的效果
2021-06-28罗美华
罗美华
营养代谢障碍是乙肝肝硬化患者进入失代偿期后最易出现的并发症,其不断加重可导致肝脏功能进一步恶化,造成恶性循环,早期给予良好营养支持可有效维护肝脏功能,延迟肝功能衰竭[1]。目前临床实际工作中对失代偿期乙肝肝硬化患者多采用常规基础治疗,疗效欠佳[2]。NRS2002营养风险筛查为在循证医学的指导下衍生出的重要营养筛查工具,是营养学及临床工作中最常用的工具,通过筛查能够根据患者机体需求制定出合理的饮食计划,但该方案在失代偿期乙肝肝硬化患者中鲜有报道[3]。本研究为探索失代偿期乙肝肝硬化患者的最佳营养支持,将营养风险筛查应用于失代偿期乙肝肝硬化患者中,现报道如下。
1 资料与方法
1.1 一般资料
选取笔者所在医院2019年12月-2020年6月收治的67例失代偿期乙肝肝硬化患者。纳入标准:确诊为乙肝肝硬化,且处于失代偿期;年龄18~60岁。排除标准:严重营养不良或具有吞咽功能障碍;具有重要器官严重衰竭。根据随机数字表法分为两组,对照组33例,男17例,女16例;年龄18~60岁,平均(46.51±0.82)岁;病程1~9年,平均(5.13±1.22)年。观察组34例,男16例,女18例;年龄18~60岁,平均(46.55±0.83)岁;病程1~9年,平均(5.15±1.23)年。两组基线资料比较差异无统计学意义(P>0.05),具有可比性。研究经医学伦理委员会审批,各患者或家属签署知情同意书。
1.2 方法
对照组常规饮食,每日热量达到30 kcal/kg以上,常规保肝、抗病毒等基础治疗。观察组在对照组基础上给予营养风险筛查联合个性化营养方案,患者入院后即用NRS2002营养风险筛查表评估营养状况,计算患者基础代谢率,确定每日所需热量,严格执行三餐能量分配。提醒患者注意钠盐摄入量控制在6 g/d以内,合并腹水患者适当补充维生素B;同时,患者禁止食用可引起血小板降低的食物如金枪鱼、沙丁鱼等。两组均连续干预3个月。
1.3 观察指标及评价标准
比较两组营养状态、肝功能水平及肠黏膜通透性水平。
1.3.1 营养状态 分别于治疗前后抽取患者静脉血,高速离心后测定总蛋白(TP)、血浆白蛋白(ALB)及血浆前白蛋白(PA)水平。
1.3.2 肝功能水平 测定患者治疗前后丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)及总胆红素(TBIL)水平。
1.3.3 肠黏膜通透性 以L(甘露醇)/M(乳果糖)值进行小肠黏膜通透性评价,L/M检测方法:患者禁食6 h后排空膀胱,口服乳果糖与甘露醇(2∶1)混合液1 000 ml,待2 h饮1 000 ml清水,将患者服药6 h内的尿液全部收集,并取样2 ml检测L、M含量。
1.4 统计学处理
使用SPSS 22.0软件对所得数据进行统计分析,计量资料以(±s)表示,采用t检验;计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后营养状态比较
治疗前两组TP、ALB及PA水平比较差异无统计学意义(P>0.05),治疗后两组各指标均高于治疗前,且观察组均高于对照组,差异均有统计学意义(P<0.05),见表1。
表1 两组治疗前后营养状态比较 [g/L,(±s)]
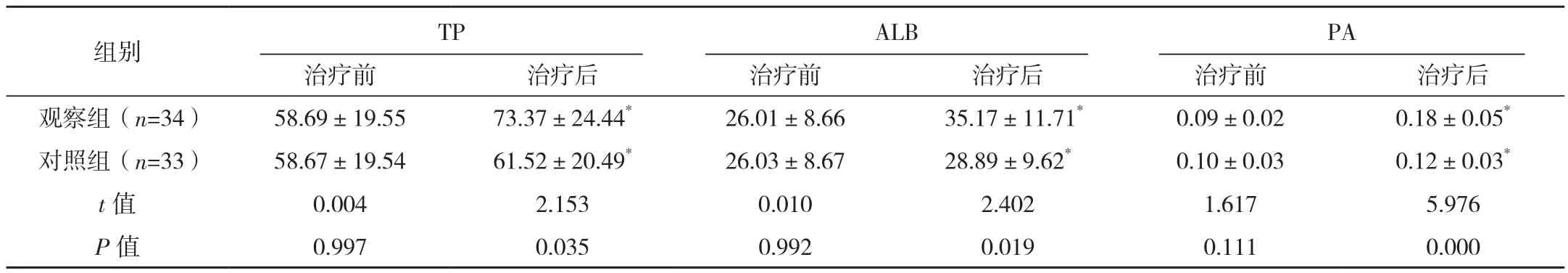
表1 两组治疗前后营养状态比较 [g/L,(±s)]
*与本组治疗前相比,P<0.05。
组别 TP ALB PA治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=34) 58.69±19.55 73.37±24.44* 26.01±8.66 35.17±11.71* 0.09±0.02 0.18±0.05*对照组(n=33) 58.67±19.54 61.52±20.49* 26.03±8.67 28.89±9.62* 0.10±0.03 0.12±0.03*t值 0.004 2.153 0.010 2.402 1.617 5.976 P值 0.997 0.035 0.992 0.019 0.111 0.000
2.2 两组治疗前后肝功能水平比较
治疗前两组ALT、AST及TBIL水平比较差异无统计学意义(P>0.05),治疗后两组各指标均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组治疗前后肝功能水平比较 (±s)
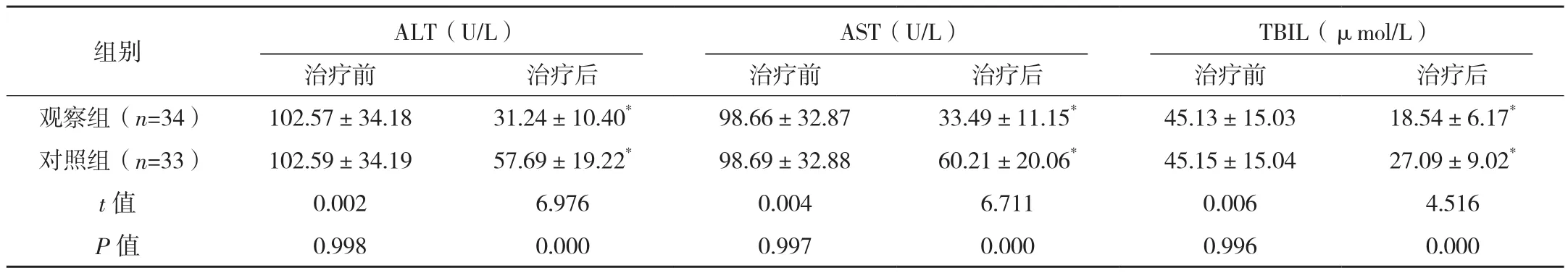
表2 两组治疗前后肝功能水平比较 (±s)
*与本组治疗前相比,P<0.05。
组别 ALT(U/L)AST(U/L)TBIL(μmol/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组(n=34) 102.57±34.18 31.24±10.40* 98.66±32.87 33.49±11.15* 45.13±15.03 18.54±6.17*对照组(n=33) 102.59±34.19 57.69±19.22* 98.69±32.88 60.21±20.06* 45.15±15.04 27.09±9.02*t值 0.002 6.976 0.004 6.711 0.006 4.516 P值 0.998 0.000 0.997 0.000 0.996 0.000
2.3 两组治疗前后肠黏膜通透性比较
治疗前两组肠黏膜通透性比较差异无统计学意义(P>0.05),治疗后两组肠黏膜通透性均低于治疗前,且观察组低于对照组,差异均有统计学意义(P<0.05),见表3。
表3 两组治疗前后肠黏膜通透性比较 (±s)
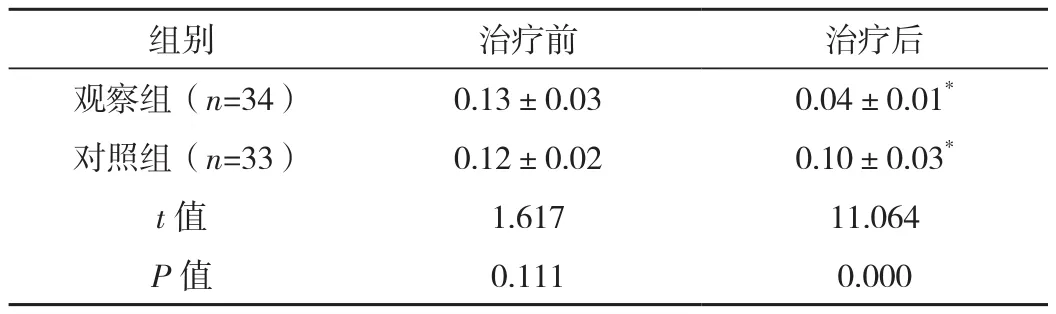
表3 两组治疗前后肠黏膜通透性比较 (±s)
*与本组治疗前相比,P<0.05。
组别 治疗前 治疗后观察组(n=34) 0.13±0.03 0.04±0.01*对照组(n=33) 0.12±0.02 0.10±0.03*t值 1.617 11.064 P值 0.111 0.000
3 讨论
乙肝肝硬化患者失代偿阶段是可逆性的,多数患者会出现营养不良的现象,且会随病情的发展逐渐加重。当前患者的传统饮食种类与热量比较单一[4],仅给予固定食谱,并未涉及个性化营养,对患者的病情进展和营养状态均不利。采用营养风险筛查可对患者营养状况受损程度进行有效评估[5],进而针对性地提出饮食建议,由于该种营养方案在失代偿期肝硬化阶段患者中鲜有报道,本研究对其进行分析。
基于营养风险筛查的个性化营养方案在患者入院时即进行营养状态评估,根据患者实际热量需求针对性设计食谱,有效融入对于蛋白质等营养素的需求[6],并根据患者的病情变化随时调整营养方案[7],达到机体高分解时对于热量的需要,提升机体的蛋白质水平,使免疫力增加[8],对于重要脏器功能的恢复有显著作用,进一步提升患者肝功能的恢复。
本研究对比了常规基础治疗和基于营养风险筛查的个性化营养方案对患者营养状态的改变,结果提示,治疗后两组TP、ALB及PA水平均高于治疗前,且观察组各指标均高于对照组,差异均有统计学意义(P<0.05)。说明基于营养风险筛查的个性化营养方案能够有效提高失代偿期乙肝肝硬化患者的机体内在营养。因根据患者实际的热量需求针对性设计食谱,有效融入对于蛋白质等营养素的需求,大大增加氮源合成[9],患者机体肌细胞内蛋白质可优先合成,对于营养状况的改善非常有利。
对于失代偿期乙肝肝硬化患者肝脏功能的监测尤为重要,可有效评估病情进展与预后。本研究中,结果显示,治疗后两组ALT、AST及TBIL水平均低于治疗前,且观察组各指标均低于对照组,差异均有统计学意义(P<0.05)。说明基于营养风险筛查的个性化营养方案可改善肝功能水平。患者入院时即进行营养状态评估,根据患者实际的热量需求针对性设计食谱,并根据患者的病情变化随时调整营养方案,可有效缓解患者的肝脏负担,从而显著提升肝功能的代偿能力。
研究表明,一旦患者的肠黏膜通透性增加,肠道内的菌群会有明显移位,导致患者出现自发性腹膜炎或内毒素血症,甚至会造成患者死亡,早期监测肠黏膜通透性水平对患者预后判断有着重要意义[10]。本研究结果显示,治疗后两组肠黏膜通透性均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05)。说明基于营养风险筛查的个性化营养方案可提升失代偿期乙肝肝硬化患者的肠黏膜通透性水平,这与基于营养风险筛查的个性化营养方案可提升患者的营养状况,对于胃肠功能受损进行缓解,可有效减少细菌及产物的移位,减轻肠黏膜的损伤有关,同时,也与营养流失减少,能够保证患者营养状态维持稳定有关[11-12]。
综上所述,基于营养风险筛查的个性化营养方案能够有效提高失代偿期乙肝肝硬化患者的机体内在营养,改善肝功能水平,并可提升肠黏膜通透性水平,值得临床推广。
