出血型胃肠间质瘤的临床及病理特性
2021-06-24张远航马晓龙员世超孟波刘忠昊温勇跃刘向
张远航,马晓龙,员世超,孟波,刘忠昊,温勇跃,刘向
(1.华北理工大学研究生学院,河北 唐山 063200;2.唐山市工人医院,河北 唐山 063000;3.河北医科大学研究生学院,河北 石家庄 050000)
0 引言
胃肠间质瘤 (gastrointestinal stromal tumors,GIST)是临床上最常见的来源于消化系统中的间叶组织来源的上皮下肿瘤,Cajal肠细胞(ICCs)是其前体细胞[1]。可发生在胃肠道的任何部位,最常见的生长部位是胃和空回肠,发病率为(8~20) /100万[2],其中肿瘤大部分来源于胃肠道的固有肌层,也有少数来源于黏膜肌层。临床中GIST极少发生淋巴结转移,肝转移或腹膜播散是其最常见远处转移途径和部位。临床中约七成的胃肠道间质瘤患者具有临床症状,主要表现为腹部胀痛、恶心、呕血、黑便等,这其中胃肠道出血是最常见的临床症状(占30%~40%)[3,4]。多数患者因胃肠道出血而就医。还有部分患者因出现了难以控制的胃肠道大出血,需要急诊手术。目前许多研究都围绕这一临床症状进行了探索[5,6]。
据相关研究显示影响胃肠质瘤患者预后、复发的高危因素主要包括瘤体的大小、有丝分裂数、肿瘤是否破裂等[7,8],且与肿瘤的位置有紧密联系。如胃和非胃间质瘤在瘤体大小相同,核分裂计数[9]相同的情况下,对肿瘤恶性程度的评价及病人的预后是不同的,即相同条件下胃来源肿瘤的相对胃以外来源的间质瘤恶性程度低。近几年伴随着甲磺酸伊马替尼等TKI类药物在临床上的使用,胃肠间质瘤患者的预后总生存时间得到了明显改善。
相关研究[10,11]显示,原癌基因c-KIT(60%-80%)或血小板衍生生长因子受体(PDGFRA)(10%-20%)突变是导致胃肠间质瘤的发生的主要原因,NCCN建议使用甲磺酸伊马替尼等酪氨酸激酶抑制剂(TKI)治疗GIST。该肿瘤细胞被认为是一种起源于平滑肌细胞中的名为Cajal的特殊细胞[12]。GIST最常见的生长模式是超出其来源的细胞表面向外性生长。值得注意的是肿瘤外生性生长易造成肿瘤破裂从而导致腹腔转移。美国国家综合癌症网络(机构)治疗指南和国家卫生研究院(NIH)危险分层分类肿瘤破裂列为间质瘤复发的危险因素,但临床工作中易忽略一种特殊形式的“破裂”即消化道出血。消化道出血主要是由局部黏膜受侵导致缺血性坏死或肿瘤受挤压破裂所致。然而,关于导致胃肠道间质瘤出血相关影响因素的研究相对较少。为了进一步探寻这一问题,本研究旨在探讨导致胃肠道出血相关影响因素及其可能的机制。
1 数据与方法
1.1 数据
回顾性收集并分析2010年9月至2020年6月174例在唐山市工人医院经手术治疗的胃肠间质瘤患者的临床及病理资料。纳入标准:(1)原发性胃肠道间质瘤患者;(2)瘤体直径大于2厘米;(3)无其他恶性肿瘤病史(4)临床病理资料完整。174例患者中只有150例符合这些纳入标准。对符合入组标准的150例进行了统计分析。
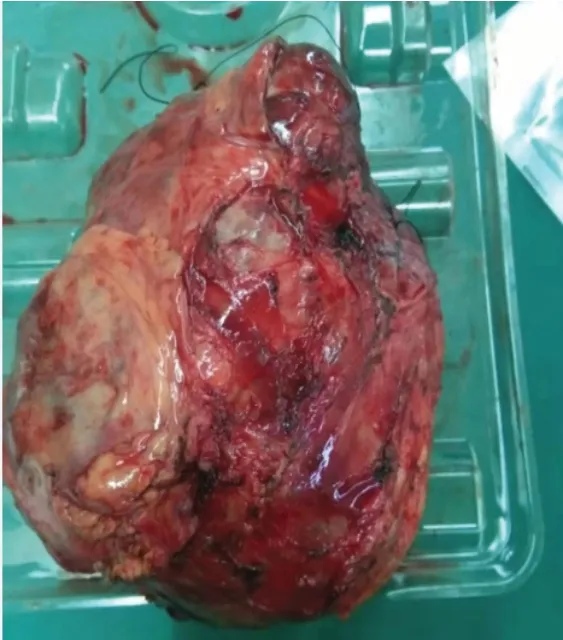
图1 巨大间质瘤伴黏膜表面破溃出血(约260mm)
1.2 方法
所有胃肠道间质瘤均有完整临床资料及病理诊断。统计的临床病理资料包括性别、年龄、肿瘤部位、细胞形态、瘤体大小、TNM分期、是否出血、是否行R0切除术、细胞核分裂计数及免疫组化相关指标。根据以下标准判断患者是否消化道出血:(1)吐血、便血或OB检测阳性确认;(2)胃肠镜下确认;(3)数字减影血管造影技术确认、CT或ECT;(4)手术记录或术后病理证实。
1.3 统计学分析
采用SPSS 22.0统计学软件进行数据分析。计数资料和排序资料的处理采用皮尔逊卡方检验。对独立样本的测量数据进行了非参数秩和检验。之后筛选出具有统计学意义的参数类别,应用logistic回归进行多因素数据分析。同时定义了P<0.05差异具有统计学意义。
2 结果
2.1 患者信息
正如在表1中给出的研究结果。数据集包含150例胃肠间质瘤患者,其中男性78例,女性72例。患者年龄小于60岁的72例,60岁及以上的患者78例。整体年龄结构分布在27~85岁,平均63.19岁。其中66例因黏膜破裂而发生胃肠道出血。其余94例患者无消化道出血迹象。原发肿瘤位于胃部位93例,非胃部位57例。肿瘤直径3cm~30cm,平均直径8.25cm。有65例患者有丝分裂计数大于5/50HPF。

表1
2.2 消化道出血相关因素
消化道出血相关因素见表2。经单因素卡方检验得出,以下因素与消化道出血有关:间质瘤的大小;瘤体的位置;肿瘤T阶段;肿瘤M阶段以及是否行R0切除术。利用logistic回归多因素分析对这些具有统计学意义的因素进行分析,结果如表3。分析提示胃肠间质瘤的发生部位是影响胃肠道出血的独立危险因素(P<0.001),原发于胃以外部位的胃肠道间质瘤更容易引起消化道出血。

表2 入组胃肠间质瘤患者是否伴有消化道出血的临床特征分析

表3
3 讨论
相关研究证实胃肠道间质瘤最常见的原因是KIT和PDGFRA突变[13],可发生在胃肠道的任何部位。肿瘤大小、有丝分裂数和肿瘤部位是GIST危险分层最主要的危险因素,并作为判断患者预后主要参考指标[15]。然而,目前的GIST预后方法准确率较低,需要额外的指标。该研究结果显示,瘤体的位置特别是有胃肠道出血表现的GIST是判断患者预后的重要参数,与先前已知的危险因素基本一致。此外,本研究还发现消化道出血患者行R0切除是非常有必要的,因为一旦GIST在腹腔内破裂后会明显增加腹腔内播散概率,导致患者预后差。即便如此较无出血患者发生转移的几率也大大增加了,这可能解释了消化道出血影响预后的原因。
出血是GIST较为常见的临床表现,发生率约为36%-45%[3,4]。出血主要是由于消化道黏膜被肿瘤侵袭所导致,可以认为是肿瘤破裂的一种特殊形式,出血可导致肿瘤细胞扩散,影响患者预后。在此项研究中,消化道出血患者约占入组患者集38%,与以往研究报道的比例基本一致。通过表2可以得出,GIST的TNM分期与消化道出血相关,T分期阶段较晚的间质瘤更诱发胃肠道出血。如果瘤细胞有远处转移,胃肠道出血的概率将明显增加,提示消化道出血可能是导致瘤细胞远处转移的非常重要危险因素。
GIST引起的胃肠道出血影响患者的预后,可能是因为肿瘤的生长会限制消化道黏膜的生长,导致局部黏膜血供减少并与消化液腐蚀性一起造成黏膜细胞坏死,最终导致溃疡性出血。另一种可能是当肿瘤侵犯并侵蚀黏膜或黏膜下血管[16]时,因血管破裂导致消化道出血。在我们的研究中,56例胃肠道出血包括25例胃出血和31例非胃出血。通过比较这些差异,我们得出结论:非胃间质瘤更容易引起消化道出血。另一项研究同样报道非胃肿瘤更倾向于向坏死[17]进化。
虽然GIST具有一定的恶性倾向,但与其他消化系统恶性肿瘤[18]不同,手术切除时无需进行周围淋巴结清扫仅需要行楔形切除或部分切除即可完全切除肿瘤。然而,即使瘤体完全切除,术后复发或转移的可能性约为50%[19]。在TKI药物应用临床之前,手术是治疗GIST的唯一方法,5年生存率约为47%[20]。近年来,伊马替尼等药物的使用改善了患者的预后,术前的辅助治疗增加了R0切除的可能性[21]。即便如此,GIST仍有可能在术后5年内复发,尤其是高危人群[22,23]。因此,视术后随访显得尤为重要[4,6,19]。虽然已有[24]的相关研究显示具有胃肠道出血表现的间质瘤患者的无复发生存期和总生存期均较短。但胃肠道出血是GIST复发和死亡的独立危险因素,正逐渐引起学术界的认识,因此同时应该增加这一方面的研究,增加GIST作为判断预后情况的重要指标。
