药物相关性间质性肺疾病四例误诊分析
2021-06-24李秀业赵惠敏
李秀业,杨 霁,赵惠敏
药物相关性间质性肺疾病(drug-induced interstitial lung diseases, DILD)是由不同种类药物引起的肺部弥漫性疾病,以肺部小血管、肺间质及肺泡纤维化和炎症为主要变化,可以引起多种多样的临床表现[1]。DILD并不少见,在美国占所有肺间质疾病的1.9%~3.5%[2],在中国的发病率常被低估。目前,已知有几百种药物可以引起DILD,如抗肿瘤、抗微生物、心血管药物,以及表皮生长因子受体酪氨酸激酶抑制剂和生物免疫制剂等。DILD临床表现多样无特异性,缺乏特异性的血清标志物,并且肺部组织病理类型与其他间质性肺疾病相似,使其诊断比较困难,导致误诊误治较多。本研究回顾性分析2014年1月—2020年1月在我院治疗DILD病例的临床资料,共诊治DILD 10例,其中4例曾被误诊误治,误诊率40%,现分析其误诊原因并总结防范措施,以提高临床医师对本病的认识,降低误诊率。
1 病例资料
【例1】男,68岁。因咳嗽伴活动后气短20 d,加重10余天入院。患者20 d前受凉后出现咳嗽,无明显咳痰,伴活动后呼吸困难,无发热、乏力、食欲缺乏、体质量减轻,未处理。患者10余天前上述症状加重,于社区医院就诊,胸部X线检查示:双肺炎症,给予头孢类药物及茶碱片,症状无改善并呈进行性加重。既往高血压病、2型糖尿病10余年;自身免疫性脑炎、癫痫3个月余,现口服奥卡西平0.3 g,2/d。查体:体温35.9℃,心率78/min,呼吸22/min,血压123/62 mmHg,意识清楚,口唇无发绀,全身皮肤黏膜正常,浅表淋巴结未触及增大;胸廓对称,双肺呼吸音粗,可闻及少许湿啰音,未闻及胸膜摩擦音;心、腹查体无异常,双下肢无水肿。医技检查:①血气分析示:pH值7.46、氧分压52 mmHg、二氧化碳分压48 mmHg、血氧饱和度0.88;②胸部X线检查示:双肺渗出性病变。入院诊断考虑肺炎。给予莫西沙星抗感染治疗,患者咳嗽、咳痰及喘息症状无改善,然后完善胸部CT检查,与3个月前胸部CT检查结果对比发现:①双肺弥漫性间质性肺炎,间质纤维化,较前新出现;②肺气肿及双肺多发实性微结节,大致同前。分析病情:患者3个月前胸部CT正常,本次出现双肺弥漫性网格影、斑片状影等间质改变,结合患者3个月前因自身免疫性脑炎、癫痫发作口服奥卡西平治疗,发病时间与应用奥卡西平相同,高度怀疑与应用该药物相关,考虑奥卡西平致DILD,嘱患者停用奥卡西平,并口服泼尼松40 mg,1/d,症状缓解出院。患者院外泼尼松逐渐减量,总疗程半年,随访至今未复发。奥卡西平致DILD患者治疗前后胸部CT检查见图1。

图1 奥卡西平致药物相关性间质性肺疾病患者治疗前后胸部CT检查(男,68岁)
【例2】男,78岁。因间断胸闷1年,加重伴发热6 d入院。患者1年前活动过程中出现胸闷、气短,未予诊治。6个月前无明显诱因出现胸痛,行冠状动脉造影显示:冠心病,左主干+双支病变,术后予二级预防药物治疗好转出院。6 d前受凉后出现发热,最高体温39℃,伴寒战、咳嗽、咳少量黄痰,伴胸闷、憋气,无胸痛、咯血等;于当地社区医院查血常规显示白细胞明显升高(12.8×109/L);胸部X线检查可见双肺渗出影,以左下肺为主;考虑肺部感染,给予头孢类药物及左氧氟沙星治疗3 d,自觉症状未好转,遂就诊我院急诊科考虑“心功能不全合并肺部感染”收入心内科。患者有脑梗死病史6年,无后遗症;肥厚型心肌病1年;阵发性心房颤动病史2~3年,半年前行射频消融术治疗,术后坚持口服胺碘酮0.2 g/d。查体:体温36.3℃,心率53/min,呼吸18/min,血压118/53 mmHg。意识清楚,口唇无发绀,全身皮肤黏膜正常,浅表淋巴结未触及增大;胸廓对称,双肺呼吸音粗,可闻及少许湿啰音,未闻及胸膜摩擦音;心、腹查体无异常,双下肢轻度水肿。实验室检查:①血气分析示:pH值7.4、氧分压71 mmHg、二氧化碳分压31 mmHg、血氧饱和度0.94;②血常规检查示:白细胞11.6×109/L、中性粒细胞8.6×109/L。患者入院后给予改善心功能及抗感染治疗,咳嗽、气短症状无改善,后完善胸部CT检查示:双肺多发斑片状阴影伴小叶间隔增厚,双肺胸膜下多发细网格样改变伴散在磨玻璃样阴影,伴胸膜下线。请呼吸科会诊考虑患者本次主要为胺碘酮致DILD,转入呼吸科给予甲泼尼龙40 mg静脉滴注治疗,1/d,3 d后改为泼尼松30 mg口服,1/d。半个月后复查胸部CT示:间质性肺炎明显吸收,遂出院,院外泼尼松逐渐减量,总疗程半年,随访至今未复发。
【例3】男,66岁。因咳痰伴憋气3周入院。患者3周前出现咳痰、憋气症状,咳黄黏痰,量多,咳嗽时前胸疼痛,活动受限,日常活动即出现憋气,休息可有改善,伴食欲减退,全身乏力。否认发热、寒战,否认心悸、夜间阵发性呼吸困难、双下肢水肿。遂来我院门诊就诊,血常规示:白细胞8×109/L、中性粒细胞百分比0.756。给予阿奇霉素0.5 g口服,1/d,共治疗4 d,效果不佳。遂再次来我院,完善胸部X线检查示:双肺渗出影,以“肺炎”收入院。既往史:40年前因幽门梗阻行胃大部切除术;1年半前因心室颤动行起搏器植入术,术后规律服用硫酸氢氯吡格雷25 mg/d,胺碘酮0.2 g/d,美托洛尔25 mg/d。查体:体温36.5℃,心率68/min,呼吸18/min,血压88/55 mmHg。意识清楚,口唇无发绀,全身皮肤黏膜正常,浅表淋巴结未触及增大;胸廓对称,双肺呼吸音粗,左肺闻及中量湿啰音,双肺未闻及胸膜摩擦音;心律齐,未闻及杂音;腹部查体无异常,双下肢无水肿。医技检查:①血常规示:白细胞8×109/L、血红蛋白127 g/L、血小板351×109/L、中性粒细胞百分比0.756;②胸部X线检查示:双肺多发渗出影,起搏器植入术后;③血气分析示:pH值7.45、氧分压68 mmHg、二氧化碳分压39 mmHg、血氧饱和度0.94;④胸部高分辨CT示:双肺多发斑片状、索条状高密度影,考虑炎症。患者入院后给予美洛西林钠舒巴坦钠及痰热清注射液治疗,症状无改善。详细询问病史,患者半年前体检胸部X线片可见肺间质改变,给予抗感染治疗后复查胸部CT示双肺胸膜下斑片及索条影增多,可见网格样改变;结合患者1年半前行起搏器植入术后规律服用胺碘酮,服药1年后逐渐出现活动后憋气、咳嗽,查体左下肺可闻及爆裂音,未见杵状指;考虑患者为胺碘酮致DILD,机化性肺炎可能,加用甲泼尼龙40 mg静脉滴注,1/d,1周后改为口服泼尼松30 mg,1/d,并逐渐减量,随访至今未复发。胺碘酮致DILD患者治疗前后胸部CT检查见图2。
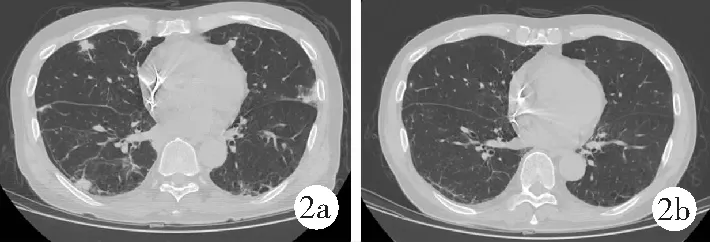
图2 胺碘酮致药物相关性间质性肺疾病患者治疗前后胸部CT检查(男,66岁)
【例4】女,56岁。因活动后喘憋2个月余,进行性加重2周入院。既往因左侧乳腺癌在我院乳腺外科行左侧乳腺改良根治术,术后给予紫杉醇300 mg+吡柔比星70 mg辅助化疗,化疗前患者胸部X线片正常,查体:体温36.0℃,心率94/min,呼吸18/min,血压150/90 mmHg,意识清、精神好,口唇无发绀,左侧乳腺癌术后,胸廓对称,双肺呼吸音清,未闻及干湿啰音和胸膜摩擦音;心律齐,未闻及杂音;腹部查体无异常,双下肢无水肿。患者辅助化疗45 d后出现咳嗽症状,同时伴喘息活动后加重,于社区医院就诊考虑支气管哮喘,给予茶碱片后症状略有改善。患者于我院继续辅助化疗后再次出现活动后喘憋,并呈进行性加重,查体:体温36.5℃,心率68/min,呼吸18/min,血压128/63 mmHg;意识清楚,口唇无发绀,全身皮肤黏膜正常,浅表淋巴结未触及增大;胸廓对称,双肺底可闻及少许爆裂音,未闻及胸膜摩擦音;心、腹查体无异常,双下肢无水肿。医技检查:①血气分析示:pH值7.37、氧分压82 mmHg、二氧化碳分压31 mmHg、血氧饱和度0.97;②胸部CT示:双肺下叶外带间质增厚,呈细网格状改变;患者出现间质性肺炎,查阅文献并结合病史、用药史考虑诊断为紫杉醇致DILD,嘱患者停用紫杉醇,并予祛痰、吸氧等对症处理,患者咳嗽、气短症状逐渐缓解,半个月后复查胸部CT示双下肺间质性肺炎明显吸收,随访至今未复发。
2 讨论
2.1疾病概述 DILD是指由药物引起的以肺泡壁为主要病变部位,同时波及细支气管、肺泡腔、肺小血管的炎症和间质纤维化,从而引起一系列病理和生理变化,近年来其发病率越来越高。目前认为DILD主要有两种发病机制,且二者可能是相互作用、相互依赖的。①直接肺细胞损伤:这是一种直接的、剂量依赖的毒性损伤,导致肺细胞或肺功能膜内皮直接的损伤,可能是一种或多种细胞毒性机制起作用。②免疫调节的肺损伤:部分患者在服用特定药物时会出现由免疫介导的肺损伤,药物可以引起不同类型的变态反应,其中多数变态反应是由T淋巴细胞介导的[3]。在临床上,DILD可由多种药物引起,其发病可能在用药后1 d内,也可能在用药几年后才出现。DILD可表现为无症状或仅有轻度的咳嗽,或是咳嗽、喘息症状逐渐加重,严重者可导致呼吸衰竭、急性呼吸窘迫综合征甚至死亡。有研究报道,DILD发病时的严重程度是患者病死率最可靠的预测因子,而引起DILD的危险因素还包括性别、年龄、吸烟、药物剂量及肺部基础疾病等[4]。
2.2临床表现 DILD的临床表现是非特异性的,可出现间质性肺疾病共同的临床表现如发热、干咳、进行性或活动性呼吸困难、低氧血症等[5],查体可闻及肺部爆裂音和杵状指,少部分患者可没有肺部阳性体征。晚期患者可出现发绀、乏力、体质量下降,未经治疗者常因呼吸衰竭死亡。本组4例均出现咳嗽、气短及喘息症状,2例查体可闻及爆裂音,1例出现发热,均未出现杵状指。
2.3辅助检查 ①高分辨率计算机断层扫描(HRCT):HRCT是目前评估DILD的最佳非侵入性诊断方法。DILD的HRCT影像表现与其他原因引起的间质性肺疾病或特发性间质性肺炎相似,常见影像类型包括:非特异性间质性肺炎、普通型肺炎、过敏性肺炎、弥漫性肺泡损伤、机化性肺炎和弥漫性肺泡出血等。Cleverley等[6]报道,HRCT预测DILD组织病理学表现的准确率仅45%,但在疾病诊断和治疗反应监测方面具有较高价值。②血清标志物:涎液化糖链抗原(KL-6)是一种黏液类糖蛋白,由Ⅱ型肺泡细胞和支气管上皮细胞分泌,能够反映肺泡上皮细胞及肺间质的损伤程度,是间质性肺疾病的标志物[7]。然而,在DILD中KL-6的特异性尚未确定,有文献报道,只在弥漫性肺泡损伤和慢性间质性肺炎患者中发现KL-6水平增加,而嗜酸粒细胞性肺炎、过敏性肺炎和机化性肺炎未见升高[8]。此外,有文献报道表面活性蛋白A和D也是肺纤维化的特定标志物[9]。③支气管镜和支气管灌洗:支气管镜检查有助于确定DILD的存在,支气管灌洗的关键作用是帮助排除其他原因,特别是感染;也可用于淋巴瘤、血管炎、肺出血或传染性病原体肺炎的鉴别诊断。④肺活检:肺活检的作用仅限于小型研究,由于DILD没有特定的组织病理学表现[10],在诊断DILD时,活检的常规使用证据有限,但在诊断不确定或排除其他原因时能起到一定作用。
2.4诊断 根据美国胸腔学会/欧洲呼吸学会的分类[11],DILD是公认的弥漫性肺病亚型,但其临床、病理和影像学特征是无特异性的,很难与其他间质性肺炎相鉴别。另外,DILD的临床表型、影像学和组织病理学表现在不同药物之间及同种药物的不同患者之间差异很大。因此,DILD是一种排除诊断,这给临床医师带来了严重的挑战。DILD的诊断通常需要有以下要点:①用药与呼吸道体征和症状之间有明确的时间关联,并且此种药物是曾经出现并报道过的DILD。②最重要的是排除其他原发或继发肺疾病,如感染、肺水肿、辐射引起的肺部损伤、基础疾病进展等,而肺癌并发DILD患者,则难以鉴别是药物性肺损伤还是肺癌进展。③停用药物后症状是否随着停药而消退。④大部分患者同时应用多种药物,需要证实其中某种药物可导致患者肺部病变,同时应排除其他药物没有引起DILD。⑤特定的血清学标志物、胸部影像学、组织病理学和临床特征通常不能明确诊断DILD。因此,临床诊断DILD需综合临床特点、用药史、组织病理学及胸部影像学表现。最后根据上述结果总体评价药物与肺部损伤的关系,划分为3个等级:明确因果关系、可能性很大及可能[12]。本文4例起病均与用药有明显的时间关系,其中例2和例3的肺部影像学改变与既往文献报道相似,故服用该药引起肺损伤的可能性很大。
2.5治疗 对于DILD的治疗,没有明显缺氧的患者初始治疗是立即停用可疑或致病药物,严重缺氧的患者初始治疗是在停用致病药物的同时给予糖皮质激素,推荐口服泼尼松0.5~1.0 mg/(kg·d),出现呼吸衰竭时可酌情应用甲泼尼龙500~1000 mg/d,治疗3 d后逐渐减量[13-14]。对于糖皮质激素治疗效果不佳或不能耐受者,可考虑加用免疫抑制剂治疗,常用的药物有硫唑嘌呤、环孢素等[13]。大多数患者在停药及糖皮质激素或免疫抑制剂治疗后呼吸道症状逐渐缓解,肺功能逐渐恢复,本文4例经治疗后均恢复良好,少数肺损伤严重或发现较晚呈肺纤维化改变的患者预后较差。
2.6误诊原因分析
2.6.1对本病认识不足,发病率被低估:DILD是引起弥漫性肺病的常见原因,部分临床医师对药物相关性肺疾病不甚了解,而且对DILD的临床特点和影像学表现不熟悉,诊断思维狭隘,是导致DILD误诊的主要原因。本文2例胺碘酮引起的DILD中,1例因既往冠心病冠状动脉造影术后入住心内科,本次出现胸闷、憋气伴咳痰、发热误诊为心功能不全合并肺部感染,心内科未明确诊断仅给予对症支持治疗效果不佳,经呼吸科会诊才明确诊断。另1例也是初诊考虑为肺炎,治疗效果不佳,完善胸部CT检查并详细询问病史明确诊断。上述2例说明DILD在临床中并不少见,要时刻警惕,并且初诊患者因所患疾病不同可能就诊不同科室,如抗心律失常药物导致者在心内科,而抗甲状腺功能亢进药物导致者在内分泌科,所以不但要提高呼吸科医师的相关知识,还需要加强相关科室医师对DILD的认识。
2.6.2临床表现多种多样,且无特异性:①起病时间长短不一:可以从用药后当天至数年发生。②临床表现严重程度不一:可以无症状,也可以出现呼吸衰竭,甚至引起急性呼吸窘迫综合征导致死亡。③肺损伤病理表现多样:同一种药物可以引起不同的病理改变,如胺碘酮致DILD病理可表现为非特异性间质性肺炎、弥漫性肺泡损伤、机化性肺炎和过敏性肺炎等[15];不同的药物又可出现相似的病理改变。本文例1和例3均有咳嗽、咳痰症状误诊为肺炎;例2因既往冠心病冠状动脉造影术后,出现咳嗽、胸闷伴发热症状,误诊为心功能不全合并肺部感染;例4因喘憋症状较明显误诊为支气管哮喘。
2.6.3临床诊断较为困难:DILD缺乏特异性的血清标志物,无特异诊断手段,因此要求医师应结合患者临床特点、实验室检查、影像学检查并排除其他病因进行综合诊断。病理学检查并不能确诊DILD,由于其无法区分原发还是药物继发间质性病变,故需综合考虑并明确肺部病理学改变与药物暴露之间可能存在的因果关系,并除外其他的肺部疾病。
2.6.4缺乏特异性影像学和病理表现:药物引起的肺损伤胸部影像学及病理表现无特异性,不同药物引起的间质性肺疾病呈多样性,同一种药物可以引起不同的胸部影像学及病理改变,不同药物也可以引起相似的影像学及病理改变。如胺碘酮可以引起过敏性肺炎表现,也可以引起机化性肺炎表现。本文例2和例3均为胺碘酮致DILD患者,其中例2肺部影像为非特异性间质性肺炎表现,例3肺部影像为机化性肺炎样表现,给临床诊断带来一定的困难。
2.6.5由于胸部影像学的不同误诊为其他疾病:DILD影像学表现多种多样,当胸部CT主要表现为外周及胸膜下分布的斑片实变影时,易误诊为普通肺炎(如例2),而有时机化性肺炎可表现为肺内结节,需与肺恶性肿瘤、肺结核等相鉴别。胸部影像学表现为蜂窝肺时如未详细询问病史,特别是用药史就很容易误诊为特发性肺间质纤维化。
2.7防范误诊措施 ①临床医师应加强学习,了解DILD相关知识及最新进展,同时还要了解其他相关学科知识,拓展诊断思维,仔细查体,全面分析病情。②临床诊断中应尽可能详细的询问病史,尤其是用药史,特别是存在肺部间质病变的患者一定询问长期用药史并警惕出现DILD的可能性。③在临床工作中出现无法解释的肺部新发病灶或呼吸系统症状患者,均需排除DILD可能。④对于突然出现的肺部病变尤其是间质性病变,不能用感染、肿瘤或其他常见病因解释者,应除外药物因素。⑤对长期应用胺碘酮、甲氨蝶呤等较易引起肺损伤药物的患者,应注意有无引起肺毒性的危险因素,尽量减少剂量和缩短用药时间,并定期复查胸部影像学检查和肺功能,以便早期发现。建议长期口服胺碘酮者每半年复查肺功能和胸部X线片,弥散功能较前减少>20%者应进一步完善胸部CT检查明确诊断[16]。
综上所述,DILD在临床上较常见,常因临床表现及胸部影像学表现不典型而漏诊、误诊。DILD临床表现多种多样,诊断需结合临床、实验室及影像学资料,并明确用药与DILD的发病有相关性,给医师的诊治工作带来了较大挑战。因此,临床医师应加强对DILD的认识,掌握其影像学特点,对药物性肺损伤保持高度警惕性,仔细鉴别诊断,以减少误诊。
