花旗泽仁主要活性成分在大鼠胰岛素抵抗脂肪组织的分布
2021-06-23李佳欣陈思琦葛鹏玲
李佳欣 朱 蕾 陈思琦 葛鹏玲
胰岛素抵抗(IR)是一种病理生理状态,在这种状态下,细胞对胰岛素降血糖活性的反应性降低。IR常与高胰岛素血症、腰围增加或内脏肥胖、高甘油三酯和低高密度脂蛋白的代谢性血脂异常以及脂肪变性有关,这些特征统称为代谢综合征,称之为“普通胰岛素抵抗”[1]。
在过去的20年里,一致性观点认为脂肪组织是肝脏和骨骼肌代谢和细胞信号的主要调节者[2,3]。因此,高脂饮食(HFD)或肥胖条件下的脂肪组织功能障碍被认为通过循环、中枢神经系统或外显体的潜在释放,向其他代谢组织传递破坏性信号[3~6]。可能存在3种机制来调节这种脂肪组织对其他组织的控制和全身葡萄糖稳态:①通过促进合成或限制脂解,在白色脂肪细胞库中进行脂质隔离,从而防止有毒脂质在肝脏和骨骼肌中积聚并受到损害在脂肪营养不良[7,8];②特殊的米色和棕色脂肪细胞内葡萄糖和脂肪酸氧化率高,增加了能量消耗并减少了脂质负荷[9,10];③生物活性因子的分泌,这些生物活性因子可以靶向大脑、肝脏、骨骼肌、胰岛或其他组织[11,12]。
从IR肺胃热盛、津气两伤、肾气亏虚等病理特点出发,故用西洋参补阴清热之功,补肺胃之阴,清肺胃之热;泽泻清热利湿,化浊降脂之利;薏苡仁渗湿止泻,除痹散结之功,组成花旗泽仁中药复方。但花旗泽仁治疗2型糖尿病胰岛素抵抗的主要活性成分被机体吸收后,能否被在靶组织或靶器官达到一定的分布浓度,是其发挥改善胰岛素抵抗的关键所在。实验对大鼠灌胃花旗泽仁水煎液后,测定人参皂苷Rb1、泽泻醇A-24-醋酸酯和9-HODE相于胰岛素抵抗相关组织——脂肪组织中的浓度,观察这些成分在脂肪组织中的分布特点及浓度随时间变化的规律。
材料与方法
1.实验材料及动物:人参皂苷Rb1标准品,泽泻醇A-24-醋酸酯标准品由成都MUST生物技术有限公司提供。9-HODE标准品由美国Sigma公司提供。地西泮标准品由中国药品生物鉴定所提供。西洋参、泽泻和薏苡仁由黑龙江省世一堂中药饮片厂提供。氮气由哈尔滨春霖气体有限公司提供。安捷伦6460三重四级杆串联质谱由美国Agilent公司提供。涡旋混合仪由美国Scientific公司提供。5810R离心机由德国Eppendorf AG公司提供。由黑龙江中医药大学实验动物中心购买清洁级Sprague-Dawley(SD)3月龄雄性大鼠42只,且体质量约为200g,实验动物合格证号:SCXK(黑)2013-004。适应性喂养1周,房间温度在20℃左右,相对湿度50%左右。
2.花旗泽仁水煎液,储备液及工作液的制备:花旗泽仁水煎液按本课题组前期工作方法制备[13]。于25ml容量瓶中放置地西泮5mg,并甲醇进行溶解,所配得内标储备液的浓度为200μg/ml。分别精密称取泽泻醇A-24-醋酸酯、人参皂苷Rb1与9-HODE 0.4mg、4mg、2mg,继续用甲醇溶解,分别制得浓度为40μg/ml、400μg/ml、200μg/ml的储备液。用甲醇配制工作液:人参皂苷Rb1:1、2、4、10、20、40、100、200μg/ml;泽泻醇A-24-醋酸酯:0.02、0.04、0.1、0.2、0.4、1、2、4μg/ml;9-HODE:0.2、0.4、1、2、4、10、20、40μg/ml。
3.标准曲线组织样品及质量控制样品的配制:工作溶液浓度为:人参皂苷Rb1为0.05~10.00μg/ml;泽泻醇A-24-醋酸酯为0.001~0.200μg/ml;9-HODE为0.01~2.00μg/ml。质量控制样品浓度为:人参皂苷Rb1为 0.1、1、8μg/ml;泽泻醇A-24-醋酸酯为 0.002、0.02、0.16μg/ml;9-HODE为0.02、0.2、1.6μg/ml。
4.液相色谱及质谱检测条件:液相色谱柱为C18柱(1.8μm,100.0mm×3.0mm),其流速为0.3ml/min,柱温为40℃,进样体积为10μl,自动进样器温度4℃。流动相:A相为水(含0.1%甲酸),B相为乙腈。各个样品的分析周期为12min,人参皂苷Rb1与泽泻醇A-24-醋酸酯洗脱方式为梯度洗脱详见表1,各待测成分的质谱参数详见表2。

表1 流动相洗脱程序

表2 待测成分的质谱检测参数
5.人参皂苷Rb1,泽泻醇A-24-醋酸酯及9-HODE组织样品处理方法:精密称取脂肪组织样品0.5g,加入0.9%氯化钠注射液超声10min进行组织匀浆制备。将100μl组织匀浆准确加入500μl含内标(地西泮为0.1μg/ml)的甲醇溶液,12000r/min高速离心10min,在30℃氮气流下将上清液吹干,剩余残渣加入甲醇100μl,高速离心10min复溶。
6.组织样品方法学考察:(1)选择性:选取脂肪组织样品,加入混合标准样品制成浓度为人参皂苷Rb1:1μg/ml;泽泻醇A-24-醋酸酯:0.2μg/ml的标准添加组织样品。另取空白脂肪组织配制成9-HODE浓度为0.02μg/ml的标准添加组织样品,并与空白组织一同处理进样分析。(2)线性范围和定量下限:将人参皂苷Rb1与泽泻醇A-24-醋酸酯混合标准曲线组织样品及9-HODE标准曲线组织样品分别进样分析,获得待测组分与内标峰面积值。纵坐标(y):人参皂苷Rb1、泽泻醇A-24-醋酸酯峰面积与内标物地西泮峰面积做比,横坐标(x):标准组织样品浓度。另外,以纵坐标为9-HODE峰面积,以横坐标为9-HODE标准组织样品浓度。(3)基质效应和提取回收率:将配制好的质量控制脂肪组织样品进行进样分析,待测成分与内标峰面积A3。组织样品处理后,分别加入与质量控制样品同等浓度的人参皂苷Rb1、泽泻醇A-24-醋酸酯与内标混合标准溶液及9-HODE标准溶液,峰面积A2。将上述混合标准溶液与9-HODE标准溶液直接进样分析,得到峰面积A1。(4)精密度和准确度:将配制好的质量控制脂肪组织样品分别按照组织样品处理方法进行进样分析,得到3种待测组分及内标峰面积值,求算组织样品日内精密度与准确度。连续3天进样分析,求算组织样品日间精密度和准确度。(5)样品稳定性:反复冻融3次后进样分析;于25℃室温下放置4h后进样分析;2周后进行进样分析;于自动进样器12h后进样分析。
结 果
1.方法学考察:选择性如图1~图2为待测组分与内标色谱图结果,结果显示在待测组分和内标的出峰位置,空白各组织匀浆中的其他内源性成分对测定不造成干扰。待测组分和内标的保留时间如下:人参皂苷Rb1保留时间为 6.2min,泽泻醇A-24-醋酸酯保留时间为9.4min,地西泮保留时间为1.7min,9-HODE的保留时间为2.7min。

图1 组织样品色谱图

图2 9-HODE的组织样品色谱图
2.线性范围与定量下限:标准曲线在各浓度范围内均显示线性良好,人参皂苷浓度为Rb1:0.05~10.00μg/ml;泽泻醇A-24-醋酸酯浓度为0.001~0.200μg/ml;9-HODE浓度为0.01~2.00μg/ml。待测组分的平均回归方程详见表3。

表3 待测组分在脂肪组织中的平均回归方程、相关系数与定量下限(n=6)
3.基质效应和提取回收率:低、中、高3个浓度下,3种活性成分均存在一定的基质效应,均为85%~115%,且精密度相对标准偏差均<20%,符合生物样品分析要求。提取回收率结果显示,3种待测组分结果均在80%左右。组织处理方法对待测组分提取回收率良好,重现性均较好,均符合分析要求(表4)。

表4 待测组分在大鼠脂肪组织中的基质效应和提取回收率
4.精密度和准确度:3种待测组分在脂肪组织中的日内与日间精密度均<20%,日内与日间准确度为±20%,数据表明待测组分在大鼠各组织中的精密度与准确度符合生物样品的分析要求(表5)。

表5 待测组分在大鼠脂肪组织中的精密度和准确度(n=6)
5.样品稳定性:低、中、高3个浓度下,相对偏差均为±20%,且相对标准偏差均<20%,待测组分在大鼠脂肪组织中的稳定性符合生物样品的分析要求(表6)。

表6 待测组分在大鼠脂肪组织中的稳定性(n=6)
6.花旗泽仁主要活性成分在大鼠胰岛素抵抗脂肪组织中的分布结果与特点:大鼠灌胃给予花旗泽仁水煎液0、0.25、0.5、1、2、6和8h后,花旗泽仁3种主要活性成分在脂肪组织中的浓度详见表7。人参皂苷Rb1在给药后在脂肪组织中分布较慢,给药后1h内脂肪中未发现分布或分布较少。人参皂苷Rb1在给药6h后,于脂肪组织中浓度最高。泽泻醇A-24-醋酸酯进入脂肪组织的速度较快,给药8h后于在脂肪组织中检测浓度相对较高。9-HODE脂肪组织中分布较多,大鼠口服花旗泽仁水煎液后脂肪组织中9-HODE的含量均出现了不同程度的增加,便于其在胰岛素抵抗相关组织中发挥作用,同时随着体内代谢与排泄过程,9-HODE含量逐渐降低并趋于基础值(图3~图5)。

表7 大鼠口服花旗泽仁水煎液后待测组分在脂肪组织中的浓度(μg/g)

图3 大鼠口服花旗泽仁水煎液后人参皂苷Rb1在脂肪组织的分布

图4 大鼠口服花旗泽仁水煎液后泽泻醇A-24-醋酸酯在脂肪组织的分布
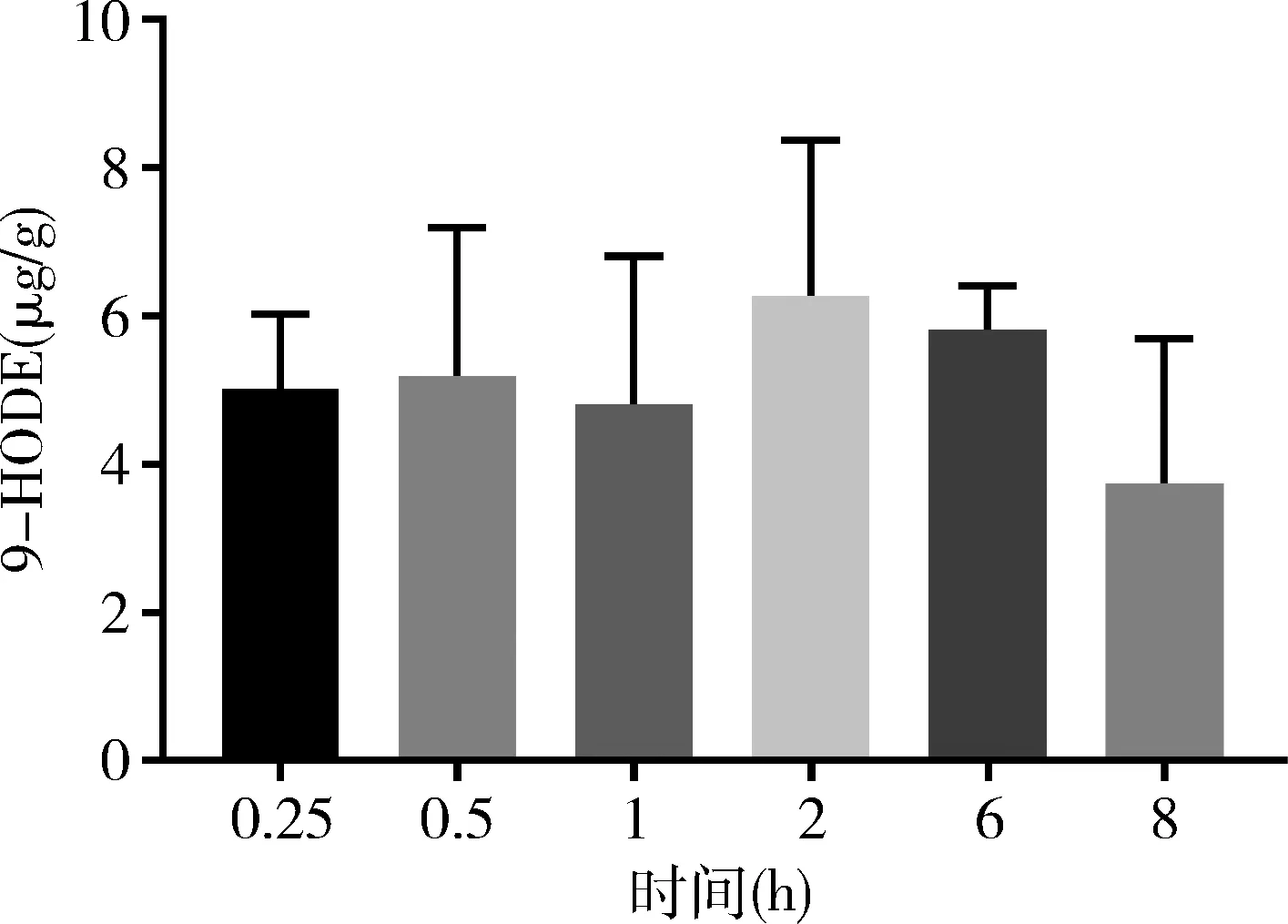
图5 大鼠口服花旗泽仁水煎液后9-HODE在脂肪组织的分布
讨 论
Xiong等[14]研究发现,小鼠腹腔注射人参皂苷Rb1后,能显著降低高脂饮食大鼠的空腹血糖,提高糖耐量,表明人参皂苷Rb1能有效维持血糖稳态。Yu等[15]报道人参皂苷Rb1通过上调肝脂蛋白的表达,降低了db/db小鼠肝脏脂质外区的堆积。此外,人参皂苷Rb1还可以有效降低血液中的游离脂肪酸,提高胰岛素敏感度。本实验将花旗泽仁水煎液给与大鼠后,发现人参皂苷Rb1分布速度略慢,2h后在脂肪组织上的分布增加,且6h后分布最多。
泽泻在我国医学中已被用于糖尿病的治疗。体外实验显示其降血糖活性。测定3T3-L1脂肪细胞培养液中葡萄糖和脂质水平,分析α-葡萄糖苷酶的抑制作用。与抗糖尿病药物噻唑烷二酮类比较,0.5g/kg剂量的泽泻乙醇提取物在3T3-L1脂肪细胞模型中增加了葡萄糖摄取而不是脂肪生成,同时在25μg/ml剂量下抑制了α-葡萄糖苷酶活性。实验给予花旗泽仁后,泽泻醇A-24-醋酸酯进入脂肪组织速度较快,且1h后随着时间增加分布增多,给药8h后于在脂肪组织中检测浓度相对较高。
Liu等[16]使用高脂肪饮食(HFD)诱导小鼠肥胖,并检测薏苡仁(CS)治疗对微生物组成和功能的调节。研究表明,CS引起的肠道菌群结构改变与抗肥胖和抗糖尿病作用有关。实验表明大鼠口服花旗泽仁水煎液后脂肪组织中9-HODE的含量均出现了不同程度的增加,同时随着体内代谢与排泄过程,9-HODE含量逐渐降低并趋于基础值。
综上所述,3种活性成分在胰岛素抵抗相关组织——脂肪中均有分布,有利于其在治疗2型糖尿病胰岛素抵抗的过程中发挥药理作用。
