3M PetrifilmTM快速菌落总数测试片的评价
2021-06-21张温玲曾维杨
林 杰,郑 晶,柯 璐,徐 珊,陈 彬,张温玲,曾维杨
(福州海关技术中心//福建省检验检疫技术研究重点实验室,福建 福州 350003)
菌落总数是用来判定食品被细菌污染的程度及卫生质量,它反映食品在生产过程中是否符合卫生要求,以便对被检样品作出适当的卫生学评价。菌落总数的多少在一定程度上标志着食品卫生质量的优劣,因此菌落总数在食品原料、加工过程以及成品的微生物检验中作为卫生指标菌需要进行监测[1-3]。由于商品化测试片方法具有简便、易于识别菌落、可以节约大量培养基配制和操作时间,因此近年来得到广泛应用,相关产品也有不少[4-7]。3M PetrifilmTM快速菌落总数测试片与国家标准GB 4789.2—2016比较,培养时间从48 h缩短到24 h,能更快出具结果,以便于更快地判定食品的安全性。为了更加科学规范的使用测试片,根据SN/T 3256—2012《食品微生物检验方法确认技术规范》和SN/T 2775—2011《商品化食品检测试剂盒评价方法》的要求,对3M PetrifilmTM快速菌落总数测试片进行评价试验,评估其在食品中菌落总数检测的准确性和适用性。
1 材料与方法
1.1 材料与试剂
菌株:弗氏柠檬酸杆菌 ATCC8090、大肠杆菌ATCC8739、金黄色葡萄球菌ATCC6538、蜡样芽孢杆菌ATCC11778、奇异变形杆菌 ATCC43071,均购自上海汉尼生物技术有限公司。
试剂:平板计数琼脂培养基, 3M PetrifilmTM快速菌落总数测试片,营养肉汤,生理盐水。
1.2 仪器与设备
KD-TBC-300M电子天平,福建科迪技术有限公司;Stomacher3500拍击式均质器,英国SEWARD;恒温培养箱,德国BINDER。
1.3 方法
1.3.1标准菌株及菌悬液的制备
将标准菌株弗氏柠檬酸杆菌ATCC8090、大肠埃希氏菌ATCC8739、金黄色葡萄球菌ATCC6538、蜡样芽孢杆菌ATCC11778、奇异变形杆菌 ATCC43071分别复活后,混合接种于营养肉汤中, 37℃混合培养 18~24 h备用。
1.3.22种方法对比线性和准确度
根据SN/T 3256—2012《食品微生物检验方法确认技术规范》和SN/T 2775—2011《商品化食品检测试剂盒评价方法》的要求,选择5类15种样品进行试验。其中选择8种自然污染样品进行试验,另外选择7种样品进行人工污染,将1.3.1混合培养液以适当的比例稀释后,按高、中、低3个接种水平添加到样品中混匀制备成测试样品,2个水平之间差一个数量级。每种样品同时按照3M PetrifilmTM快速菌落总数测试片方法和GB 4789.2—2016《食品安全国家标准 食品微生物学检验 菌落总数测定》进行检测,自然污染样品结果见表1,人工污染样品结果见表2。
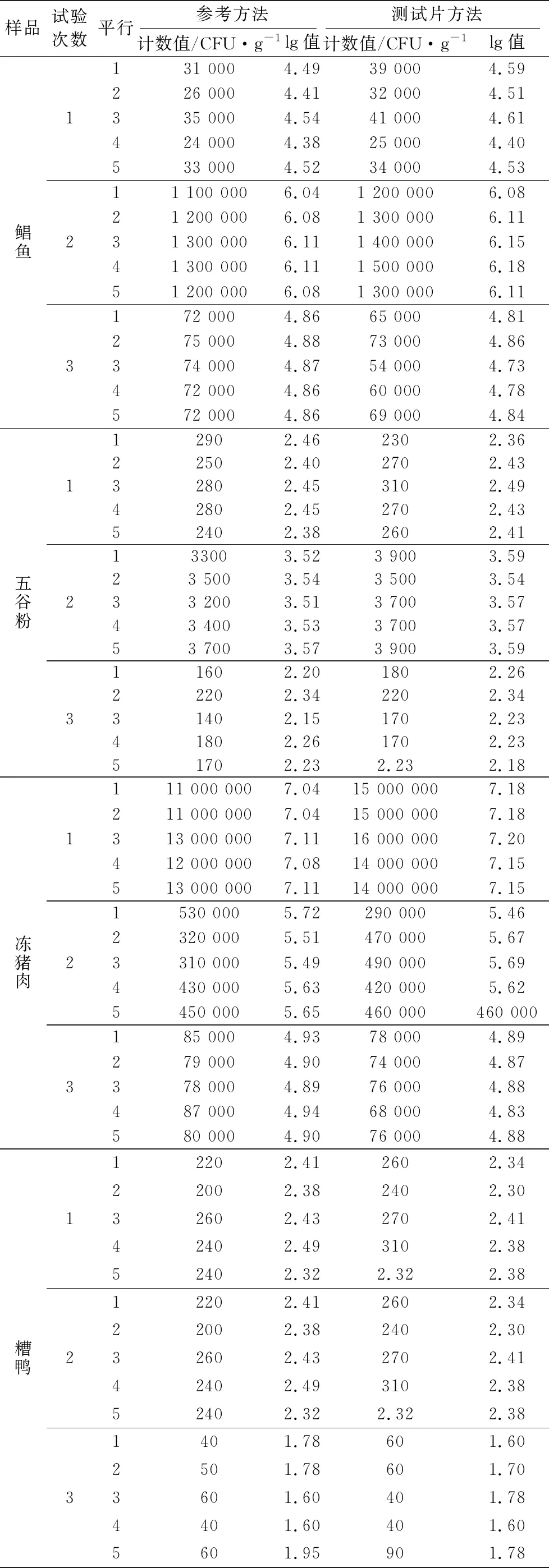
续表1

续表1
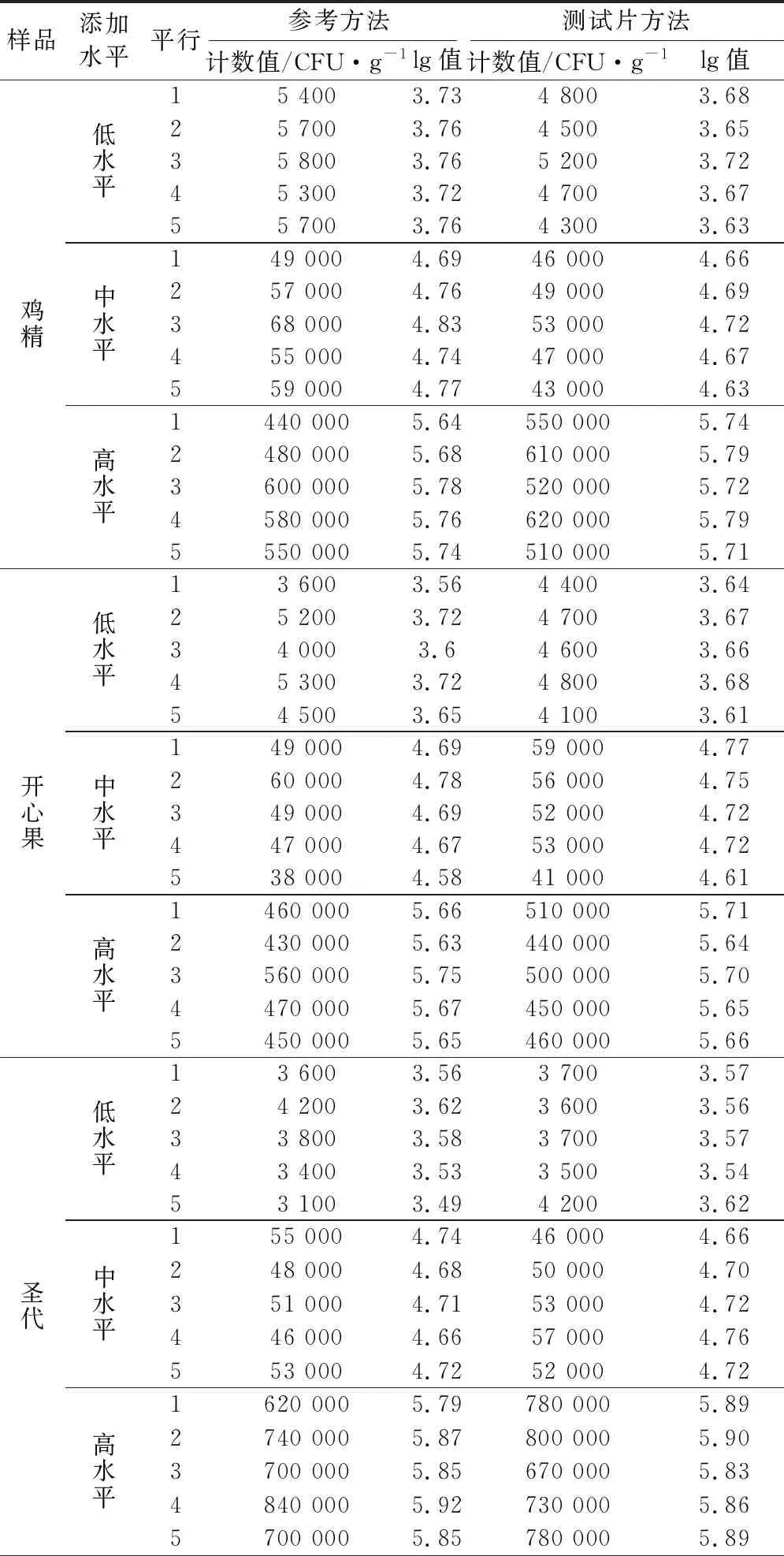
表2 7种人工污染样品两种方法测试结果
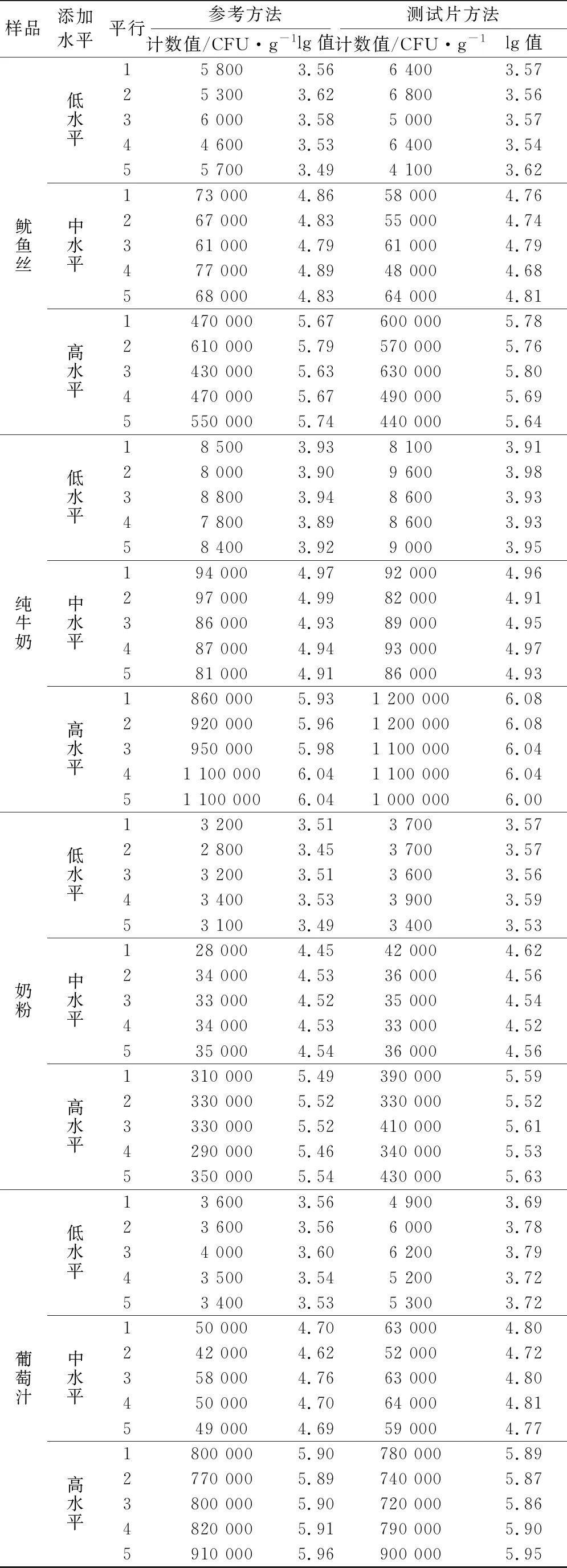
续表2
1.3.3测试片耐变性
耐变性是指对同一样品用一个分析方法,在各种正常检测条件下进行分析,保证该分析方法的可行性。耐变性评价由以下步骤组成:确定可能影响检测结果的因素,对每一种因素稍作改变,采用合适的方法进行耐变性检验。对于菌落总数检测而言,培养温度和培养时间是2个主要影响因素,因此选用2个污染水平纯牛奶样品对培养温度和培养时间两个变量进行耐变性试验,结果见表5。
1.3.4测试片批间变异
为了验证测试片的稳定性,取3个不同批号测试片对2个污染水平奶粉样品进行批间变异试验,结果见表6。
1.3.5实验室间协同试验
选用牛奶样品,添加弗氏柠檬酸杆菌、大肠埃希氏菌、金黄色葡萄球菌、蜡样芽孢杆菌、奇异变形杆菌等 5种菌混合培养物,制备成高、中、低3个接种水平的冻干样品,发送8家实验室进行协同试验。每一接种水平样品同时用测试片方法和参考方法进行测试,每一接种水平样品做5个平行,检测结果见表7和表8。
2 结果和分析
2.1 线性和准确度
微生物学检测数据通常不是正态分布的,为了获得更加对称的分布,所以将计数结果转化成对数形式,比较测试片方法与参考方法的一致性。
对每种食品2种方法的测试结果作回归曲线图,得出线性方程和相关系数,以考察测试片方法与参考方法的相关性。用t检验比较2种方法的差异性,结果见表3。用标准偏差和相对标准偏差考察方法的重复性,结果见表4 。
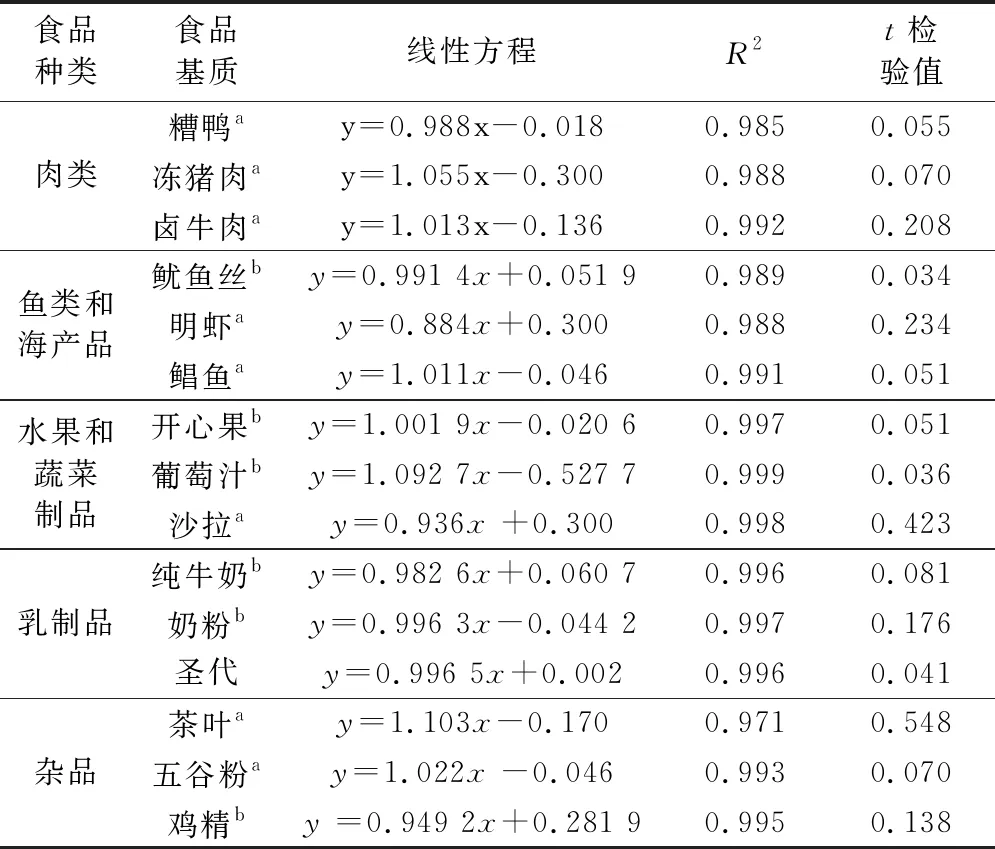
表3 线性方程、相关系数和t值
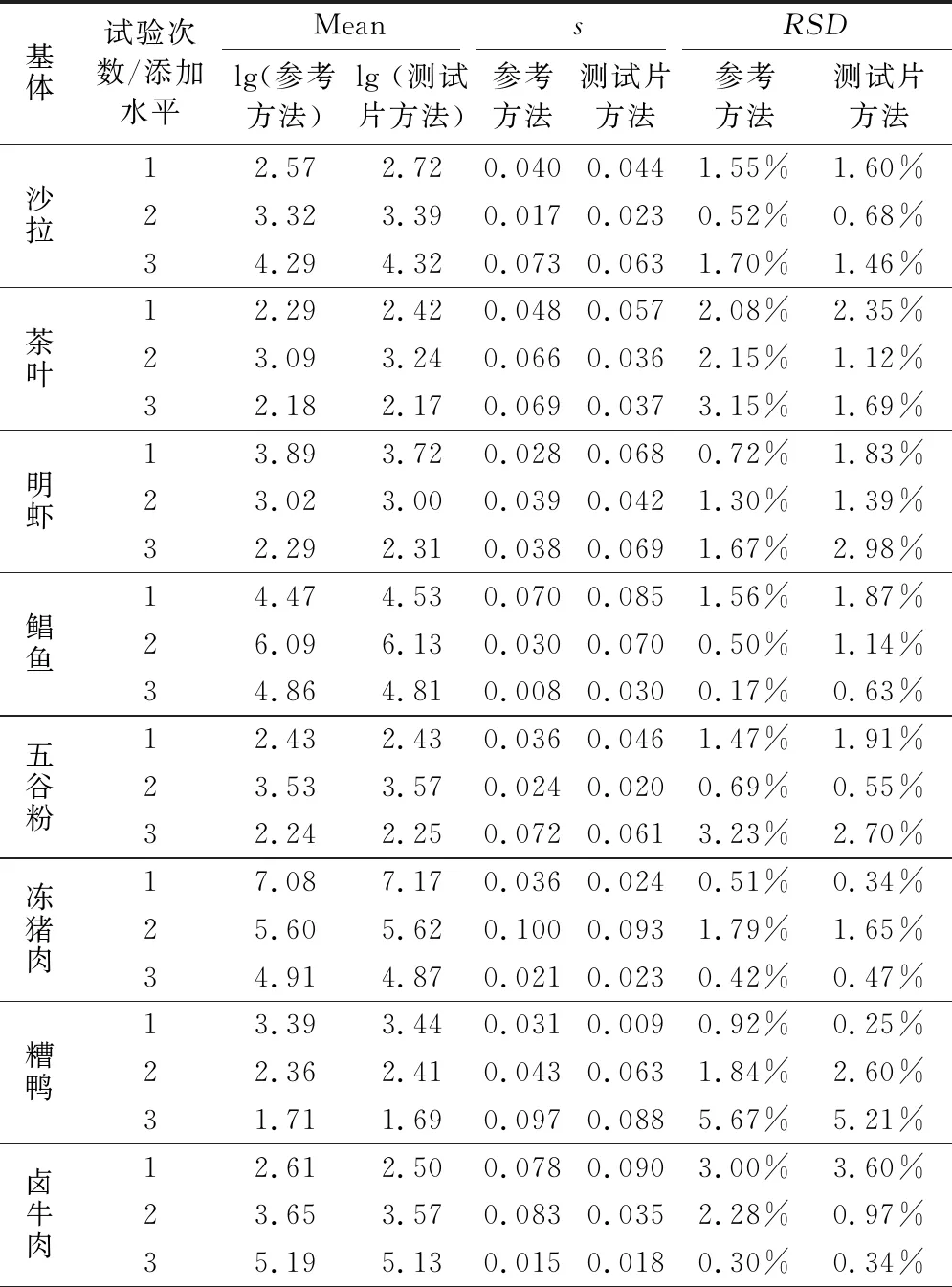
表4 重复性分析结果

续表4
从表3可见,5类15种食品相关系数均大于0.97,t值均小于t0.05(15)=2.131,说明3M PetrifilmTM快速菌落总数测试片方法和参考方法GB 4789.2—2016无显著性差异。从表4可见5类15种食品测试片法的标准偏差在0.009~0.093,相对标准偏差在0.25%~5.21%;参考方法的标准偏差在0.008~0.100,相对标准偏差在0.30%~5.67%。两种方法的标准偏差和相对标准偏差无显著差异,可以说明3M PetrifilmTM快速菌落总数测试片方法准确度较高。
2.2 测试片耐变性
耐变性试验及分析结果见表5。
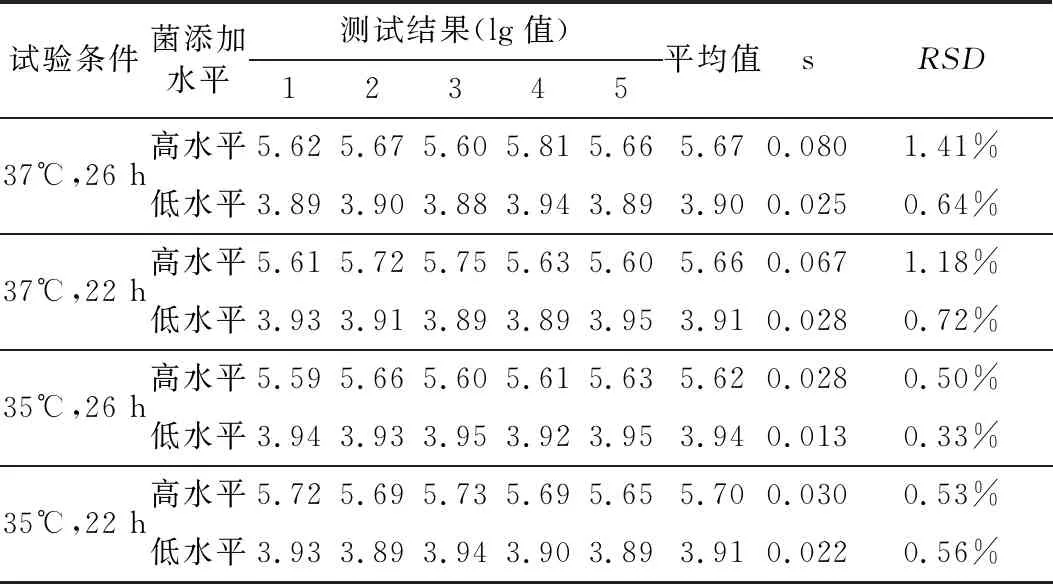
表5 耐变性试验及分析结果
经验证,培养温度选择35℃和37℃,培养时间选择22 h和26 h对检测结果的标准偏差s与在重复性条件下得到的标准偏差s无显著差异,表明测试片对培养温度36±1℃和培养时间24±2 h的耐变性范围不影响检测结果。
2.3 测试片批间变异
批间变异试验及分析结果见表6。
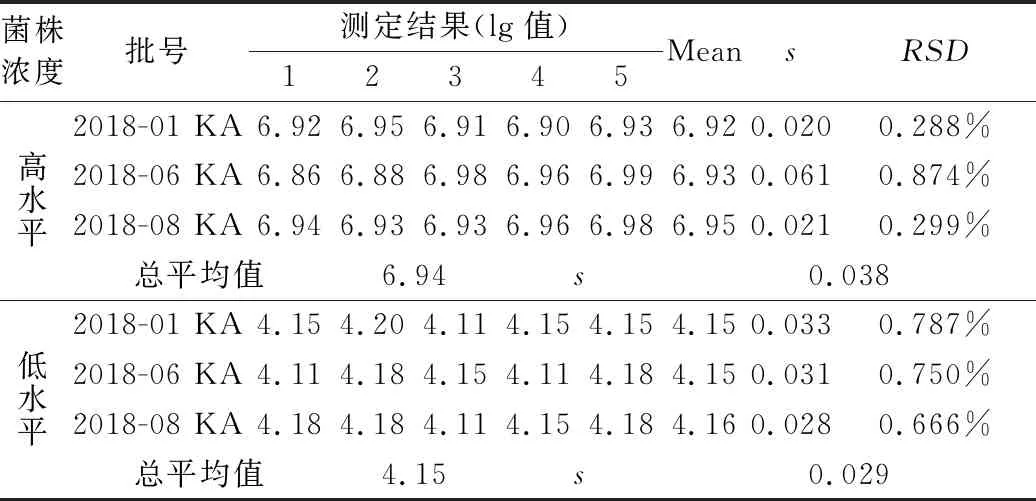
表6 批间变异试验及分析结果
三个不同批号测试片测试结果的标准偏差s与在重复性条件下得到的标准偏差s没有明显差别,说明不同批号产品无显著差异。
2.4 实验室间协同试验
协同实验室内重复性分析结果见表7和表8。
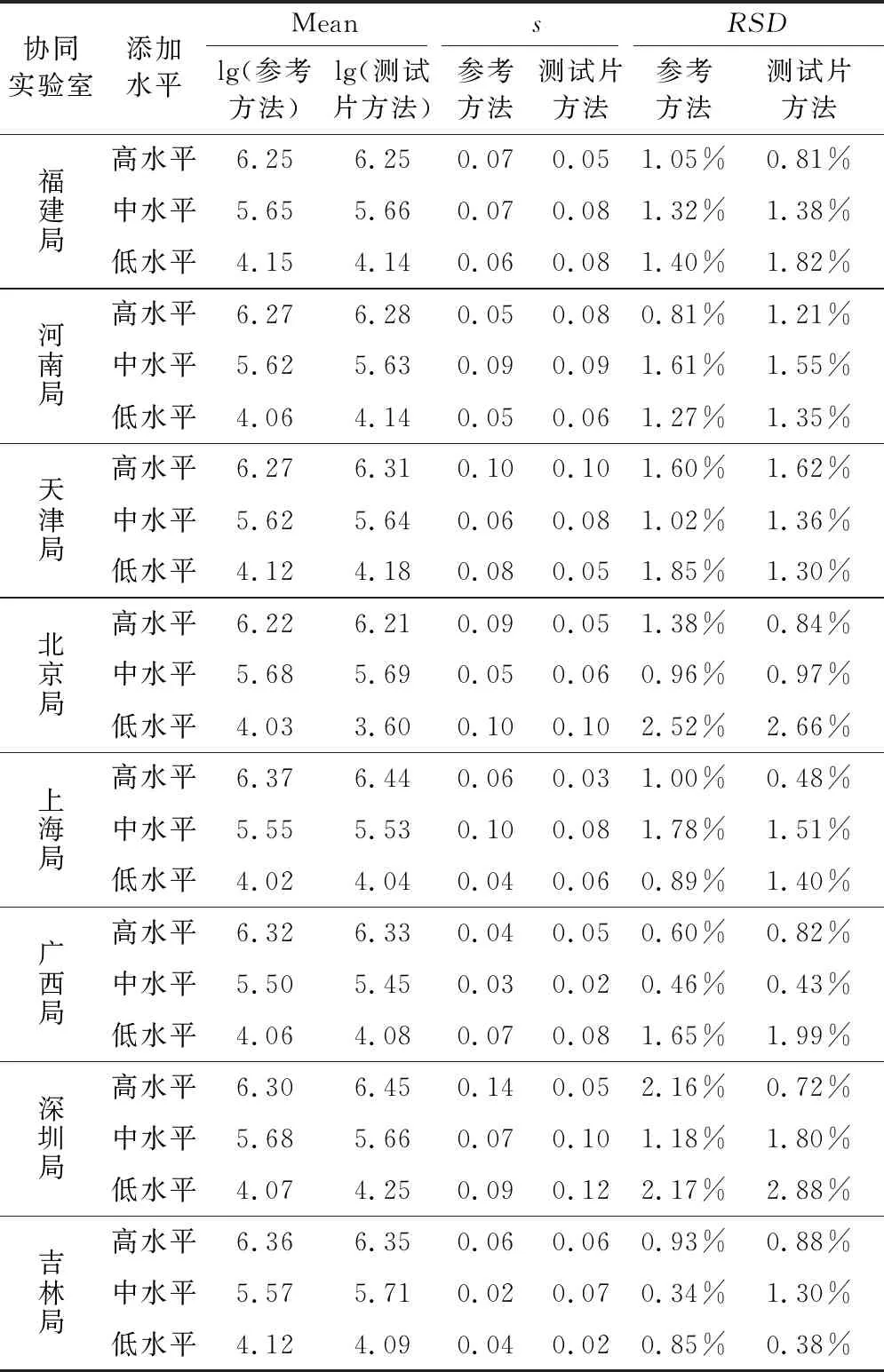
表7 协同实验室内重复性分析结果
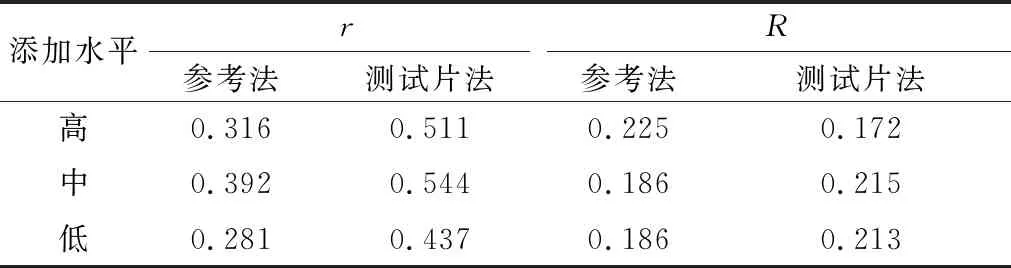
表8 协同实验室间重复性和再现性结果
经柯克伦检验剔除离群值后统计协同实验室间重复性和再现性[8],8家实验室对高、中、低3个接种水平样品的5个平行测试,结果2个方法的重复性值r和再现性值R比较接近,说明2种测试方法无显著差异。
3 结论
通过5大类15种食品2种检测方法的比对试验,重复性结果和统计t检验结果,以及8家实验室协同试验结果重复性和再现性分析,均说明3M PetrifilmTM快速菌落总数测试片和国家标准GB 4789.2—2016在食品检测上无显著性差异。耐变性结果表明,测试片在检测的培养温度和培养时间范围内对检测结果没有影响;批间变异结果表明不同批号测试片的检测结果无显著差异,说明测试片稳定性良好。综上所述, 3M PetrifilmTM快速菌落总数测试片检测结果准确,产品性能稳定,能满足食品菌落总数的检测要求。
