西格列汀对应用大剂量胰岛素效果欠佳的2型糖尿病的疗效分析
2021-06-18梁焯辉刘倩雯梁红玉赵凡区苑清黎惠贞
梁焯辉,刘倩雯,梁红玉,赵凡,区苑清,黎惠贞
(江门市人民医院内分泌科,广东 江门 529000)
目前,2型糖尿病(type 2 diabetes mellitus,T2DM)的发病率不断增高,而血糖控制达标率却不容乐观。T2DM主要是由环境和遗传等多种因素共同导致的代谢紊乱性疾病,临床表现以血糖升高为主[1]。胰岛素抵抗和胰岛B细胞功能受损是诱发2型糖尿病发生发展的重要原因[2]。有效的血糖控制是目前公认的改善T2DM近远期预后的关键措施,但部分T2DM患者口服血糖药物后仍控制不佳[3]。目前,胰岛素治疗是糖尿病患者常用手段,但部分糖尿病患者存在胰岛素抵抗,导致胰岛素治疗效果欠佳,而加大胰岛素剂量血糖仍然无法得到有效的控制,对于此类患者需要联合具有增加胰岛素敏感性的药物进行治疗,以期有效控制血糖水平。治疗2型糖尿病一线主要药物为二甲双胍、吡格列酮等,而在我国一线药物治疗的糖尿病患者中,仍存在血糖控制不佳者。二肽基肽酶-4(dipeptidyl peptidase-4,DDP-4)抑制剂西格列汀是一种新型口服降糖药,可为治疗血糖控制不佳患者提供新的选择[4]。本研究旨在探讨应用大剂量胰岛素后血糖控制仍欠佳的2型糖尿病患者,联合DDP4抑制剂治疗的临床疗效及安全性,望为临床治疗T2DM提供新的方法。
1 资料与方法
1.1 一般资料
选取江门市人民医院于2018年10月至2019年10月收治的180例2型糖尿病患者为研究对象,所有患者均符合1998年世界卫生组织(World Health Organization,WHO)关于2型糖尿病诊断标准,糖化血红蛋白(glycosylated hemoglobin,HbAlC)高于7.0%,或空腹血糖(fasting blood-glucos,FPG)不低于7.0 mmol/L和餐后2 h血糖(blood glucose at 2 h postprandial,2 h-PG)不低于10.0 mmol/L。纳入标准:(1)符合WHO中有关T2DM 诊断标准;(2)单用胰岛素治疗12周以上,每日剂量>50 U,血糖仍控制不佳者。排除标准:(1)1型糖尿病、妊娠糖尿病及其他类型糖尿病者;(2)合并心、肝、肾等严重系统性疾病者;(3)合并分泌系统疾病、恶性肿瘤者;(4)合并精神病、感染性、自身免疫性疾病者;(5)近期内口服降糖类药物治疗者;(6)合并与糖尿病相关的急性并发症者。将180例患者分为3组,每组各60例。A组加用西格列汀治疗24周,B组加用二甲双胍治疗24周,C组加用吡格列酮治疗24周。各组一般资料比较,差异无统计学意义(P>0.05)。见表1。本研究经医院伦理委员会批准,符合医学伦理学标准。
1.2 方法
所有患者均给予胰岛素治疗,每日剂量>50 U。A组加用西格列汀治疗24周,B组加用二甲双胍治疗24周,C组加用吡格列酮治疗24周,治疗分为导入期、治疗中段阶段(前12周)和治疗后段阶段。(1)导入期(第1~2周)A组应用西格列汀片(默沙东制药有限公司,0.1 g/粒)0.1 g/d;B组应用二甲双胍片(中美上海施贵宝制药有限公司,0.5 g/粒)0.5 g/次,2次/d;C组应用吡格列酮胶囊(四川绿叶制药股份有限公司,30 mg/粒)30 mg/d,期间记录起始胰岛素剂量、收集观察指标和记录不良反应发生频率。(2)治疗中段阶段(前12周)按导入期治疗方案应用12周,根据血糖情况调整胰岛素剂量,记录胰岛素剂量、收集观察指标、记录不良反应发生频率。(3)治疗后段阶段(后12周)B组二甲双胍剂量增加至1 g/次,2次/d,其他两组剂量不变。根据血糖情况调整胰岛素剂量,所有患者治疗过程中均需密切监测血糖情况并及时调整胰岛素剂量,治疗过程中均未出现严重不良反应。
表1 各组一般资料比较
1.3 观察指标
1.3.1 临床疗效 显效:FPG及2h-PG持续显示为正常水平;有效:FBG及2h-PG水平较治疗前降低≥20%;无效:FBG及2h-PG水平较治疗前降低<20%或升高。总有效率=(显效+有效)/总例数×100%。
1.3.2 胰岛功能水平检测 于清晨采集患者治疗前后空腹静脉血5 mL,3 000 rpm离心10 min,留血清待测。采用AU680型全自动生化分析仪及配套试剂盒(美国贝克曼库尔特公司)检测空腹胰岛素(fasting insulin,FINS)、餐后2 h 胰岛素(insulin 2 h after meal,2 h INS)、空腹C肽(fasting C-peptide,FCP)、餐后2 h C肽(C peptide 2 h postprandial,2 hCP)、胰岛B细胞功能水平(levels of islet B cell function,HOMA-B)及胰岛素抵抗指数(insulin resistance index,HOMA-IR)。
1.3.3 糖脂代谢水平检测 采用高压液相色谱法测定血清糖化血红蛋白 (glycated hemoglobin,HbAlc);采用AU680型全自动生化分析仪及配套试剂盒(美国贝克曼库尔特公司)检测空腹血糖(fasting plasma glucose,FPG)、总胆固醇(total cholesterol,TC)、三酰甘油(triacylglycerol,TG)、低密度脂蛋白-胆固醇(low density lipoprotein cholesterol,LDL-C)和高密度脂蛋白-胆固醇(high density lipoprotein cholesterol,HDL-C)。
1.3.4 肝功能水平检测 采用日立7060型全自动生化分析仪及配套试剂盒(日本日立公司)检测尿素氮 (urea nitrogen,BUN)、丙氨酸氨基转移酶 (alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶 (aspartate amino transferase,AST) 及血肌酐 (serum creatinine,Scr)。
1.3.5 炎症因子水平检测 采用Model550全自动多功能酶标仪(美国BIO-RAD公司),通过酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)检测炎性因子血清白细胞介素6(interleukin-6,IL-6)、C反应蛋白(C-Reactive Protein,CRP)及肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平,所用试剂盒购置美国BIOTANG公司。记录治疗过程中出现的不良反应事件。其中低血糖事件,以血糖≤3.9 mmol/L为低血糖事件,血糖≤2.8 mmol/L并出现意识障碍或需他人协助为严重低血糖事件。
1.4 统计学分析
2 结果
2.1 三组临床疗效比较
治疗后,A组总有效率为95.0%,高于B组的91.7%和C 组的88.3%,但差异无统计学意义(P>0.05)。见表2。
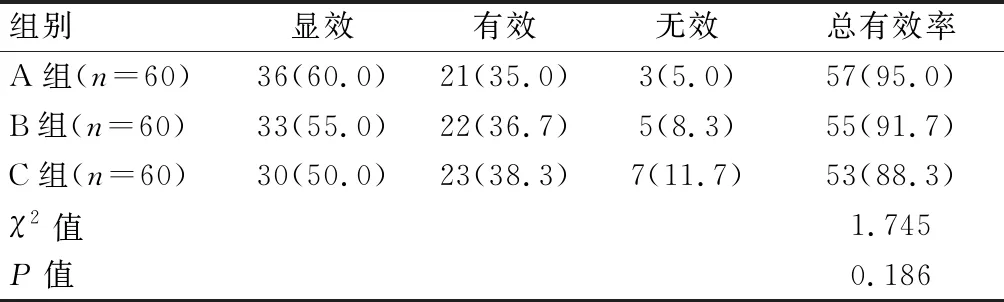
表2 各组治疗后临床疗效比较[n(%)]
2.2 各组治疗前后胰岛功能水平比较
治疗前,各组FINS、2 h INS、FCP、2 h CP、HOMA-B及HOMA-IR水平比较,差异无统计学意义(P>0.05);治疗后,各组FINS、2 h INS、FCP、2 h CP、HOMA-B水平明显升高,HOMA-IR显著降低(P<0.05),A组HOMA-B水平高于B和C组(P<0.05)。见表3。
表3 各组治疗前后胰岛功能水平比较
2.3 各组治疗前后糖脂代谢水平比较
治疗前,各组HbAlc、FPG、TC、TG、LDL-C及HDL-C水平比较,差异无统计学意义(P>0.05);治疗后,各组HbAlc、FPG、TG、LDL-C水平均明显下降(P<0.05),各组间比较差异无统计学意义(P>0.05)。见表4。
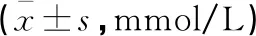
表4 各组治疗前后糖脂代谢水平比较
2.4 各组治疗前后炎性因子水平
治疗前,各组CRP、IL-6和TNF-α水平比较,差异无统计学意义(P>0.05);治疗后,各组CRP、IL-6和TNF-α水平较治疗前显著降低(P<0.05),各组间比较差异无统计学意义(P>0.05)。见表5。
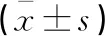
表5 各组治疗前后炎性因子水平比较
2.5 各组治疗前后肝肾功能指标比较
治疗前后,各组肝肾功能指标ALT、AST、BUN和Scr水平比较,差异均无统计学意义(P>0.05)。见表6。
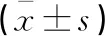
表6 各组治疗前后肝肾功能指标比较
2.6 各组治疗过程中不良事件发生情况
各组治疗过程中均未发生严重低血糖事件,A组低血糖等不良反应发生率为6.7%,低于B组的23.3%和C组的25.0%(P<0.05)。见表7。
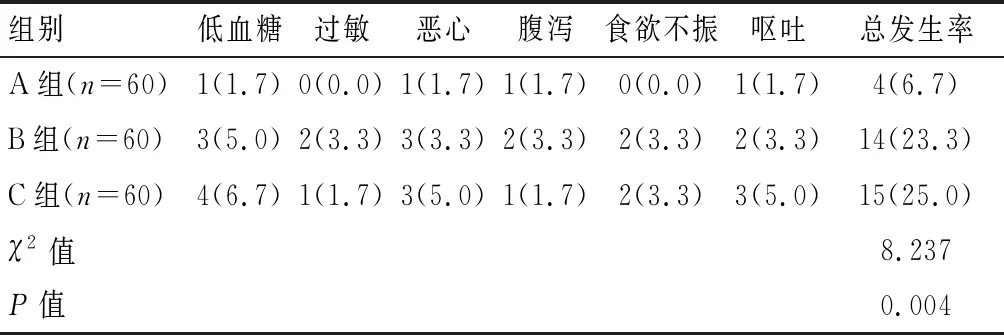
表7 各组治疗过程中不良事件发生情况[n(%)]
3 讨论
目前,随着生活方式的改变、工作节奏的变化,高糖、高脂、高盐的饮食摄入,2型糖尿病的发生率呈不断上升的趋势,对人类的健康已造成了严重的影响[5]。研究[6]表明,对患者进行良好的血糖控制,可以延缓其并发症的发生,进而提高患者的生活质量,降低医疗费用。选择合理有效方便安全的降糖方案,有利于慢病管理的上下联动,使患者的血糖控制得更好,从而降低并发症的发生。但部分糖尿病患者存在胰岛素抵抗,采用大剂量胰岛素治疗后血糖仍然控制不佳,因此需要对此类患者增加有胰岛素增敏作用的药物进行联合治疗[7]。近些年,2型糖尿病的治疗方案不断完善,患者的血糖控制总体逐渐趋于良好,但仍然有大部分患者对血糖波动控制较差,且部分传统的降血糖药物对降低患者餐后血糖波动贡献率小,不良反应较大等,导致患者的依从性较差,进而降低了治疗效果。目前,临床使用较多的糖尿病药物为噻唑烷二酮类和双胍类。噻唑烷二酮类药物容易造成患者体重增加,增加心衰发生的风险[8];双胍类药物长期服用会导致多种不良反应,如胃肠道不适、增加乳酸含量,加大代谢综合征患者乳酸中毒的风险[9]。因此,部分患者无法长期使用噻唑烷二酮类和双胍类药物,只能加大胰岛素的使用剂量,导致胰岛素抵抗加剧,体重明显增加。选择安全有效的降糖药对治疗胰岛素抵抗的2型糖尿病患者具有重要的意义。
DPP-4抑制剂是一类新型的口服降糖药,可稳定肠促胰岛素、胰高血糖素样肽1 (glucagon-like peptide 1,GLP-1)和葡萄糖依赖的促胰岛素多肽(glucose-dependent insulinotropic ploypeptide,GIP)的循环水平,从而增加葡萄糖介导的胰岛素分泌,GLP-1也能减少胰高血糖素的分泌。DPP-4抑制剂通过抑制DPP-4酶的活性,促进GLP-1和GIP的表达,进而提高血清胰岛素水平和降低血清胰高血糖素,以葡萄糖依赖的方式改善高血糖[10-11]。在2型糖尿病的治疗中,不仅要对患者的血糖进行严格的控制,还应尽量减少其血糖波动幅度和不良反应的发生。另外,血脂的控制也十分的重要,安全有效、长久地改善患者的血糖血脂已成为2型糖尿病治疗及降低大血管和微血管并发症发生的重要研究方向[12-13]。二甲双胍、吡格列酮在治疗2型糖尿病中已取得显著的疗效,其作用机制为增加机体组织对胰岛素的敏感度,提高胰岛素介导的葡萄糖利用率,并抑制肝糖原异生,改善胰岛素抵抗的状态[14-15]。本研究发现,DDP-4抑制剂西格列汀治疗2型糖尿病可取得和传统降糖药二甲双胍、吡格列酮相当的疗效。另外,西格列汀治疗后可显著提高患者胰岛功能,改善糖脂代谢水平,降低机体慢性炎症反应,且不损伤肝脏功能。此外,西格列汀治疗后HOMA-B水平高于B和C组,可见西格列汀能够进一步提高对胰岛B细胞的保护作用,增加其对葡萄糖的反应,在高糖条件下促进胰岛素分泌,从而增加组织细胞对葡萄糖的利用率[16]。对各组治疗过程中不良反应发生情况的统计发现,各组治疗过程中均未发生严重低血糖事件,但A组治疗过程中低血糖等不良反应发生率为6.7%,低于B组的23.3%和C组的25.0%,即西格列汀可降低低血糖发生率,但未增加胃肠道不良反应,安全性较高。
综上所述,DDP-4抑制剂西格列汀相比传统口服降糖药,在显著改善患者血糖状况的同时,不增加低血糖等不良反应的发生,并对胰岛B细胞起着潜在的保护作用,可作为与胰岛素联合用药治疗的理想选择。
