骨瘤康颗粒质量标准研究
2021-06-16刘秋艳段佩利金燕飞张海波
刘秋艳 段佩利 金燕飞 张海波
河南中医药大学第三附属医院,河南 郑州 450008
骨瘤康颗粒为国家级名中医王祥麒教授临床用于治疗肾精亏虚型骨转移癌的经验方,处方由白芍、熟地黄、山慈菇、白芥子、川芎、皂角刺等十二味中药组成,具有补肾填精、柔肝止痛、化痰散结的功效[1-2]。 骨瘤康颗粒临床以汤剂入药,味苦量大,服用不便,故将其研制成颗粒剂[3-5]。为控制制剂质量,本研究参照文献[6-14 ]采用薄层色谱法对方中熟地黄、川芎、白芍三味中药进行鉴别,采用高效液相色谱法对骨瘤康颗粒中芍药苷含量进行测定,从而保证制剂的安全性及有效性。
1 仪器与试药
1.1 仪器 Thermo U3000 高效液相色谱仪-紫外检测器(美国赛默飞世尔科技公司);Good Look-1000型全自动薄层色谱成像系统(上海科哲生化科技有限公司); EYELA N-3000 旋转蒸发仪 (日本 Rikakikai 公司); HK250型超声波清洗器(上海科导台式超声波清洗器);硅胶G薄层板(青岛海洋化工厂)。
1.2 试药 骨瘤康颗粒三批中试样品(批号20190407、20190413、20190422 ),芍药苷对照品(上海源叶生物科技有限公司,批号为:X27F8C30162,含量≥98%) ;熟地黄对照药材 (中国药品生物制品检定所)、川芎对照药材(中国药品生物制品检定所)、乙腈、磷酸( 色谱纯,天津四友);水为超纯水(自制);其他试剂均为分析纯。
2 方法与结果
2.1 定性鉴别
2.1.1 熟地黄薄层色谱鉴别 取骨瘤康颗粒10 g, 加水50 mL, 加热至沸,放冷,离心,上清液用乙酸乙酯振摇提取2次,每次30 mL,合并乙酸乙酯液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。取熟地黄对照药材4 g,加水60 mL,煎煮1 h,滤过,滤液同法制成对照药材溶液。另取缺熟地黄的阴性对照,同法制成阴性对照溶液。照薄层色谱法[2015年版《中国药典》四部通则0502]试验,吸取上述三种溶液各10 μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯(1∶1)为展开剂,展开,取出,晾干,喷以2,4-二硝基苯肼乙醇试液。置日光与紫外灯(365 nm)下检视,供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点。阴性样品无干扰。如图1、图2所示。


2.1.2 白芍薄层色谱鉴别 取骨瘤康颗粒 2.0 g,加乙醇10 mL,振摇5 min,滤过,滤液蒸干,残渣加乙醇1 mL使溶解,作为供试品溶液;取芍药苷对照品,加乙醇制成每1 mL含1 mg的溶液,作为对照品溶液。另取缺白芍的阴性对照品2.0 g,同法制成阴性对照溶液。照薄层色谱法[2015年版《中国药典》四部通则0502]试验,吸取上述三种溶液各10 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,在l05℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。阴性无干扰。如图3所示。
2.1.3 川芎薄层色谱鉴别 取骨瘤康颗粒 2.0 g,加乙醚20 mL,加热回流1 h,滤过,滤液挥干,残渣加乙酸乙酯2 mL使溶解,作为供试品溶液。另取川芎对照药材1 g,同法制成对照药材溶液。照薄层色谱法[2015年版《中国药典》四部通则0502]试验,吸取上述三种溶液各10 μL,分别点于同一硅胶GF254薄层板上,以正己烷-乙酸乙酯(3∶1)为展开剂,展开,取出,晾干,置紫外灯(254 nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点 。阴性无干扰。如图4所示。


2.2 含量测定
2.2.1 色谱条件及系统适用性实验 以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1%磷酸溶液(14∶86)为流动相;检测波长为230 nm。
2.2.2 溶液制备 对照品溶液的制备:取芍药苷对照品适量,精密称定,加甲醇制成每1 mL含60 μg的溶液,即得。
供试品溶液的制备:取骨瘤康样品2 g,精密称定,置50 mL量瓶中,加稀乙醇35 mL,超声处理(功率240 W,频率45 kHz)30 min,放冷,加稀乙醇至刻度,摇匀,滤过,取续滤液,即得。
阴性对照溶液:按样品处方比例及工艺制备不含白芍的阴性样品,照上述供试品溶液的制备方法制成阴性对照溶液
2.2.3 专属性试验 分别吸取对照品溶液,供试品溶液以及阴性对照品溶液各10 μL,分别进样。供试品与对照品在相应位置处出现相同色谱峰,阴性对照在对照品峰相应的位置上无干扰,说明专属性良好。如图5所示。

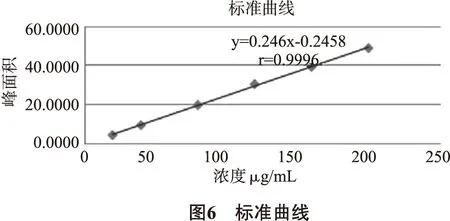
2.2.4 线性关系的考察 精密吸取浓度为200 μg/mL的对照品储备液0.5 mL、1 mL、2 mL、4 mL、6 mL、8 mL、10 mL于10 mL量瓶中,用甲醇溶液配成浓度为10、20、40、80、120、160、200 μg/mL的对照品溶液,摇匀,分别吸取上述对照品溶液10μL进样,按设定色谱条件测定,浓度μg/mL为横坐标,峰面积为纵坐标,进行线性回归,得回归方程:y=0.246x-0.2458,r=0.9996,实验结果见表1及图6。试验结果表明,芍药苷在 20~200μg/mL的浓度范围内,与峰面积呈良好的线性关系。

表1 线性关系实验结果 (n=6)
2.2.5 精密度试验 取上述对照品溶液(浓度:60 μg/mL),连续进样6次,结果见表2。试验结果表明:RSD为1.41%,表明使用该测定方法仪器精密度良好。

表2 精密度试验结果 (n=6)
2.2.6 稳定性试验 取同一批供试品溶液,于0、2、4、6、12、24 h各测定峰面积(A)1次,结果见表3。试验结果表明:RSD为0.64% ,结果表明供试品溶液在24 h内稳定性较好。

表3 稳定性试验结果
2.2.7 重现性试验 取同一批样品6份,按供试品溶液制备并测定,结果见表4。试验结果表明,RSD为0.45%,样品重复性较好。

表4 重现性试验结果
2.2.8 回收率试验 精密量取已知含量同一批号的样品1 mL,置50 mL量瓶中,平行取样6份,精密加入浓度为60 μg/mL的对照品溶液0.45 mL、0.75 mL、1.05 mL各两份,加稀乙醇35 mL,超声处理(功率240 W,频率45 kHz)30 min,放冷,加稀乙醇至刻度,摇匀,滤过,取续滤液,用0.45 μm微孔滤膜滤过,取续滤液 ,依法测定,计算回收率,RSD值,结果见表5。

表5 回收率试验结果
由以上结果得出平均加样回收率96.74%, RSD为 1.48%。说明此方法准确可行。
2.2.9 样品含量测定 取骨瘤康颗粒3批中试产品样品每批2份。按2.2.2制备方法制得供试品溶液及对照品溶液,按照2.2.1项下色谱条件对不同批次样品进行测定,用外标法计算芍药苷含量,结果见表6。
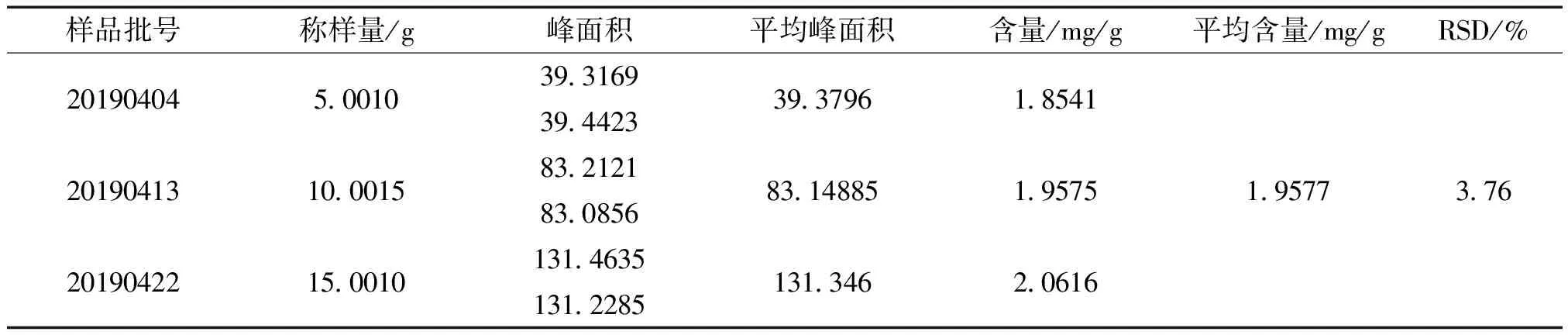
表6 三批样品含量测定结果
由以上得出:三批骨瘤康颗粒样品芍药苷的含量在1.8541~2.0616 mg/g, 考虑到药材的差异性,以及不同批次转移率的不同,再加上样品批次较少, 按最低含量下浮30%制订骨瘤康颗粒质量标准中芍药苷含量[11], 暂定骨瘤康颗粒中芍药苷含量不少于1.30 mg/g。
3 讨论
骨瘤康颗粒组方从“肾主骨生髓”的理论出发,以补肾为根本。方中熟地黄补肾填精,白芍柔肝止痛,二药共为君药。但熟地黄2015年版《中国药典》规定其指标性成分为毛蕊花糖苷, 在含量检测指标筛选时,预实验过程中首先对熟地黄中所含指标性成分毛蕊花糖苷进行HPLC含量检测方法研究。采用多种方法对其进行检测,供试品色谱中无相应峰。经查阅相关文献,毛蕊花糖苷不稳定[15],在长时间加热过程中易发生美拉登反应,因此无法作为含量控制指标[16-18]。 2015年版《中国药典》规定白芍的指标性成分为芍药苷。实验首先对制剂中熟地黄、白芍、川芎、山慈菇、白芥子等中药进行薄层色谱定性鉴别研究。查阅文献山慈菇暂未收载其薄层鉴别标准。白芥子薄层色谱鉴别阴性干扰严重,无法作为定性鉴别项。熟地黄、川芎、白芍薄层色谱鉴别斑点清晰,重现性好,阴性无干扰,故将熟地黄、川芎、白芍作为该制剂的定性控制指标。
实验对白芍的指标性成分芍药苷进行HPLC含量检测,在20~200 μg/mL 的浓度范围内,与峰面积呈良好的线性关系,r=0.9996(n=6),平均加样回收率96.74%,RSD为1.48%(n=6)。其方法专属性好、精密度高、重复性好、稳定性强,能较好控制主药指标成分含量。可作为骨瘤康颗粒的含量测定。
因此,利用薄层色谱法对骨瘤康颗粒中熟地黄、川芎、白芍三味中药进行定性鉴别,其斑点清晰,专属性强;使用HPLC法对骨瘤康颗粒中的芍药苷进行含量测定,十八烷基硅烷键合硅胶为填充剂,乙腈-0.1%磷酸溶液(14∶86)为流动相;检测波长为230 nm,其线性方程为y=0.246x-0.2458,r=0.9996,平均加样回收率96.74%,RSD为1.48%(n=6)。 3批制剂中芍药苷平均含量分别为1.9577,RSD值为3.76%。因此本实验所建立的熟地黄、川芎、白芍TCL鉴别方法及芍药苷含量测定方法准确易行,精密度、稳定、重复性均较好,能有效控制骨瘤康颗粒制剂质量。
