椰浆中椰子蛋白的提取、分离和鉴定
2021-06-15林塬吴毓炜王焱吉哲蓉乐学义
林塬 吴毓炜 王焱 吉哲蓉 乐学义

摘 要:为了更好地了解市售椰浆中椰子蛋白质量状况,本研究以市售的10种椰浆为样品,采用反向高效液相色谱(reversed-phase high performance liquid chromatography,RP-HPLC)及十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(sodium laurylsulfonate-polyacrylamide gel electrophoresis,SDS-PAGE)对提取蛋白进行分析,采用基质辅助激光解吸电离飞行时间串联质谱(matrix-assisted laser desorption/ionization tandem time-of-flight mass spectrometry,MALDI-TOF/TOF-MS)对蛋白进行鉴定。结果表明:椰浆RP-HPLC约在10.4 min和11.9 min分别出现1个色谱峰,大多数样品峰面积大小都与蛋白标签含量一致,SDS-PAGE条带数量和颜色的深浅与RP-HPLC得到的峰面积结果一致,个别样品标签含量高,SDS-PAGE能分离出的蛋白条带数量也较多,但RP-HPLC的椰子蛋白峰面积小,经MALDI-TOF/TOF-MS鉴定,部分条带没有鉴定出椰子有关的肽段或蛋白。研究结果为椰浆蛋白的食品安全与质量控制提供了方法参考和示范。
关键词:椰浆;蛋白分析;鉴定;RP-HPLC;SDS-PAGE;MALDI-TOF/TOF-MS
中图分类号:S667.4 文献标识码:A
Extraction, Isolation and Identification of Coconut Protein from Coconut Milk
LIN Yuan1, 2, WU Yuwei2, WANG Yan2, JI Zherong2, LE Xueyi1*
1. Department of Applied Chemistry, South China Agricultural University, Guangzhou, Guangdong 510642, China; 2. Products Quality Supervision and Testing Institute of Hainan Province / National Quality Supervision and Inspection Center for Tropical Agriculture Products, Haikou, Hainan 570203, China
Abstract: In order to better understand the quality of coconut protein in commercially available coconut milk, 10 types of coconut milk were used as the samples bought from the market. Reversed-phase high performance liquid chromatography (RP-HPLC) and sodium laurylsulfonate-polyacrylamide gel electrophoresis (SDS-PAGE) were used to analyze the extracted proteins, identified through matrix-assisted laser desorption/ionization tandem time-of-flight mass spectrometry (MALDI-TOF/TOF-MS). There were two peaks in RP-HPLC of coconut milk at 10.4 min and 11.9 min, the peak area of most samples were consistent with the protein label content. The number of SDS-PAGE bands and intensity were consistent with the peak area results obtained by RP-HPLC. Some samples had high label content, and SDS-PAGE could separate more protein bands, but the peak area of coconut protein from RP-HPLC was small. The protein bands were identified with MALDI-TOF/TOF-MS and no coconut-related peptides or proteins were identified. This method could be used for the isolation and identification of coconut protein in coconut milk.
Keywords: coconut milk; protein analysis; identification; RP-HPLC; SDS-PAGE; MALDI-TOF/TOF-MS
DOI: 10.3969/j.issn.1000-2561.2021.04.029
椰子(Cocos nucifera L.)是棕櫚科(Palmae)椰子属(Cocos)植物[1],是世界上重要的果树之一[2]。椰肉富含蛋白,易于被人体吸收,有较好的保健效果,如具有抗糖尿病活性[3]、抗氧化活性[4]和降低血脂[5]等作用,近年来引起了人们的兴趣[6]。椰子肉中蛋白质的种类包括球蛋白、谷蛋白、白蛋白和醇溶蛋白等[7]。椰子全身是宝,但其可食部分比例较小、加工麻烦,不宜直接将其作为生产原料。椰子果肉被加工成纯椰浆,在保持其营养物质和天然风味的同时解决了运输麻烦的问题,降低贮存费用,便于广泛使用。
椰浆目前的研究主要集中在挥发性风味成分及脂肪酸的类型和含量[8]、浓缩方法(常压、真空)对椰浆各指标的影响[9]、真空浓缩椰浆的护色工艺[10]和真空浓缩椰浆形成稳定乳状液的乳化剂配比[11]等。椰子中蛋白质的分离和鉴定研究很少,1930年美国科学家从椰子蛋白质中分离出一种分子量约208 kDa的球蛋白,并命名为Cocosin[12]。Hagenmaier等[13]采用Sephadex G-200层析方法对椰子蛋白进行了分析,发现3个蛋白质峰。Huang等[14]采用双向电泳(2-DE)技术对椰子蛋白进行了分析,通过MS/MS鉴定出7S球蛋白、一种类似于谷蛋白和受体样蛋白激酶的蛋白质。椰子蛋白含有人体所需的氨基酸,通过椰子蛋白的分析方法还可分离出椰子蛋白并测定其氨基酸含量[15-16]。
椰子蛋白的含量与其品种、生长环境等有关,在生产椰浆的过程中为保证椰浆中蛋白质的含量,可能会加入其他蛋白质。椰浆的内控要求中,蛋白质含量是一项重要的指标,目前用于测定蛋白质的方法是GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》中的凯氏定氮法,该方法是一种测定蛋白质的经典方法,具有广泛性、操作相对简单、实验成本低和准确性高等优点,缺点是测定结果为总有机氮,只要是含氮的物质,都被当成蛋白质计入结果,不能准确评定椰浆质量。本研究以反应后的椰子蛋白的RP-HPLC、SDS-PAGE以及MALDI-TOF MS的鉴定结果为评价指标,研究椰浆蛋白的定性分析方法,旨在为椰浆蛋白的食品安全与质量控制提供方法参考和示范。
1 材料与方法
1.1 材料
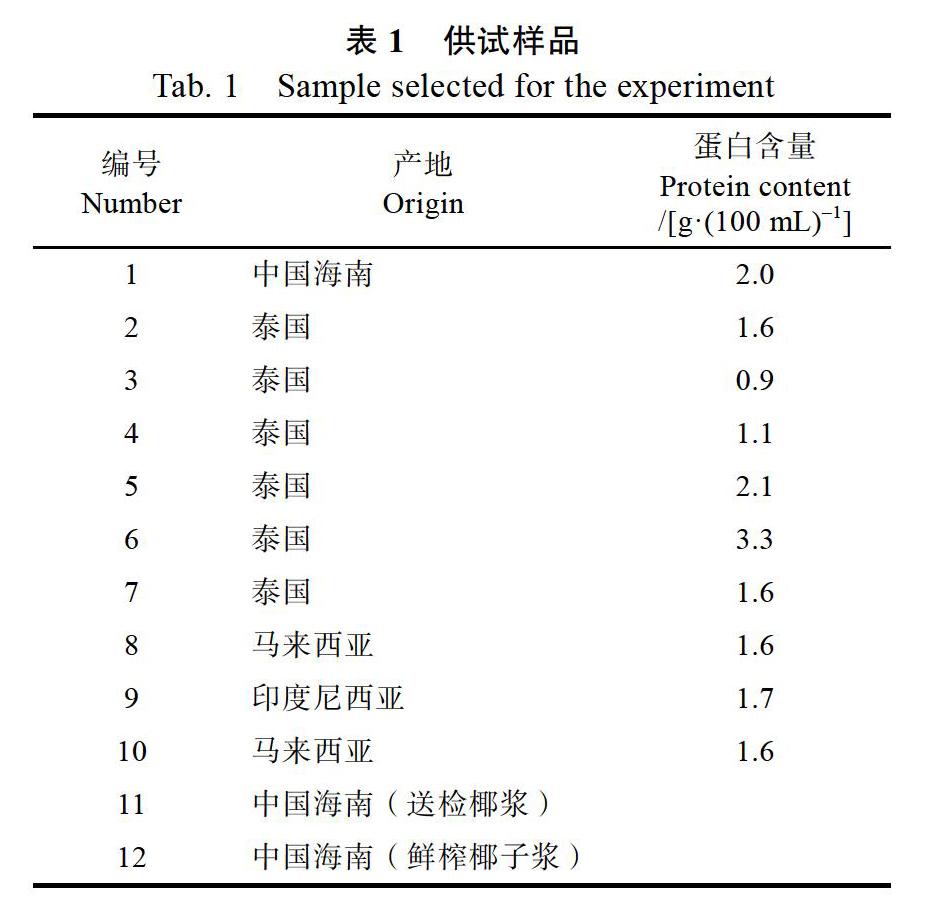
1.1.1 材料与试剂 供试椰子为海南绿色高种(Cocos nucifera L., Hainan Tall, green fruit),老椰子,市售10种椰浆样品信息见表1。
乙腈和三氟乙酸,色谱纯,美国Tedia公司;磷酸二氢钾、磷酸氢二钾、三羟甲基氨基甲烷、氨基乙酸、十二烷基硫酸钠、丙烯酰胺、过硫酸铵及溴酚蓝,均为分析纯,广州化学试剂厂;考马斯蓝(分析纯),国药集团化学试剂有限公司;水为超纯水。
蛋白提取液:取磷酸氢二钾5.5 g与磷酸二氢钾0.41 g,加超纯水溶解并将pH调到8.0,最后定容至1000 mL为碱提取液。
1.1.2 仪器与设备 Agilent 1200高效液相色谱仪(美国Agilent公司)、Sigma 3-18K冷冻高速离心机(德国Sigma公司)、Mini-protea Tetra system蛋白电泳仪(美国Bio-rad公司)、超纯水系统(美国Millipore公司)、S20K型pH计(瑞士梅特勒-托利公司)、5800MALDI基质辅助激光解吸电离飞行时间串联质谱(美国AB SCIEX公司)、ZM200高速粉碎机(德国Retsch公司)。
1.2 方法
1.2.1 样品制备及提取 鲜榨椰子浆:椰子去掉椰衣后取出椰子肉,去褐色种皮,用粉碎机粉碎成椰子肉泥(粉碎机上安装1 mm的筛),将残渣过滤后取滤液为椰浆。总蛋白的提取参照文献[17]中的方法,略有改动。称取椰浆4 g,加入蛋白提取液40 mL,4 ℃水浴中磁力搅拌提取0.5 h后,4 ℃、6000 r/min离心15 min,去掉上层油脂及底层沉淀,取中间层澄清液,将澄清液pH调至蛋白质等电点即pH 3.5,4 ℃、6000 r/min离心15 min,弃掉上清液,用超纯水清洗沉淀3次,加入5 mL提取液溶解蛋白,4 ℃冷藏備用。
1.2.2 液相色谱分离条件 流动相A为含有体积分数0.1%三氟乙酸的乙腈溶液,流动相B为含有体积分数0.07%三氟乙酸的超纯水,色谱柱为Agilent PLRP-S(300A,8 μm,250 mm×4.6 mm),检测波长214 nm,流速为1 mL/min,进样体积10 μL,柱温24 ℃。经过反复多次的试验,最终采用线性梯度洗脱程序为:开始1~2 min,34% A;2~4 min,34%~37% A;4~8 min,37%~42% A;8~10 min,42%~45% A;10~11 min,45%~42% A;11~13 min,42%~38% A;13~15 min,38%~34% A。此条件下,色谱峰峰形好且得到有效的分离。
1.2.3 SDS-PAGE蛋白电泳条件 椰子蛋白的SDS-PAGE分析参照文献[18]的方法,SDS-PAGE分离胶的浓度为12.5%,浓缩胶的浓度为4%。在进行电泳试验时先恒定功率在5 W/胶,约1 h后蛋白条带从浓缩胶进入到分离胶,再将功率恒定在10 W/胶直至电泳结束。用考马斯亮蓝G-250染色,先用10%乙酸脱色,再用5%乙酸脱色,最后用水去除凝胶上的染色背景,然后扫描凝胶。
1.2.4 MALDI-TOF/TOF-MS条件 MALDI- TOF/TOF-MS分析参照文献[19]中的方法,从凝胶上挖取对应的蛋白条带,然后加100 μL超纯水洗15 min,去除水,用移液枪头将蛋白条带捣碎,利于后期酶与蛋白充分接触,提高酶切效率。加入100 μL脱色液—[50% 100 mmol/L碳酸铵(NH4)2CO3,50% 乙腈ACN],置于摇床振荡30 min。加入100 μL 100% ACN,摇床振荡脱水10 min,重复该步骤2次至胶粒变为纯白色。开盖,除去ACN,置超净台中干燥,直至ACN完全挥发,小心将离心管盖扣好,防止干胶粒蹦出。根据胶粒大小加入3~5 μL胰酶(20 ng/μL酶液),以完全覆盖胶粒为佳,盖好置于冰浴约1 h,使胶粒充分吸收酶液。根据胶粒大小,加入5~8 μL胰酶缓冲液,以覆盖胶粒为佳,在PCR仪(热盖设置为100 ℃左右,防止样品蒸发)37 ℃酶解16 h。酶解结束后先加入0.8 μL酶解液到质谱靶上,近干后加入0.8 μL酶解液,待其近干再加入0.8 μL基质(浓度5 mg/mL),待其完全干后即可进行质谱鉴定。
将所得到的质谱信息通过MASCOT 2.2软件以植物界的分类法(绿色植物,包括6 686 534个序列)为基础,在美国国立生物技术信息中心(NCBI)数据库(发布版本NCBI prot 20180429,包括152 462 470个序列和55 858 910 152个残基)进行检索。MASCOT软件搜索参数如下,搜索类型:MS/MS离子搜索;酶:胰蛋白酶/ P;固定修饰:脲基(C);可变修饰:氧化(M);质量值:同位素;蛋白质量:不受限制;肽质量公差:±300×10?6;碎片质量公差:±0.3 Da;最大错位:1;查询数量:158。
2 结果与分析
2.1 椰浆的液相色谱分析
椰浆提取蛋白经液相色谱分析,在10.3 min和11.9 min分别有1个峰。此次分析的椰浆样品分别来自中国海南、泰国、马来西亚、印度尼西亚,椰浆中蛋白含量范围为0.9~3.3 g/100 mL(表1)。从图1可知,除5号和6号样品外,其余椰浆蛋白的2个色谱峰面积之和与产品标识的蛋白含量基本呈正相关;1号样品的蛋白质含量最大(2.0 g/100 mL),色谱峰面积之和也是最大。
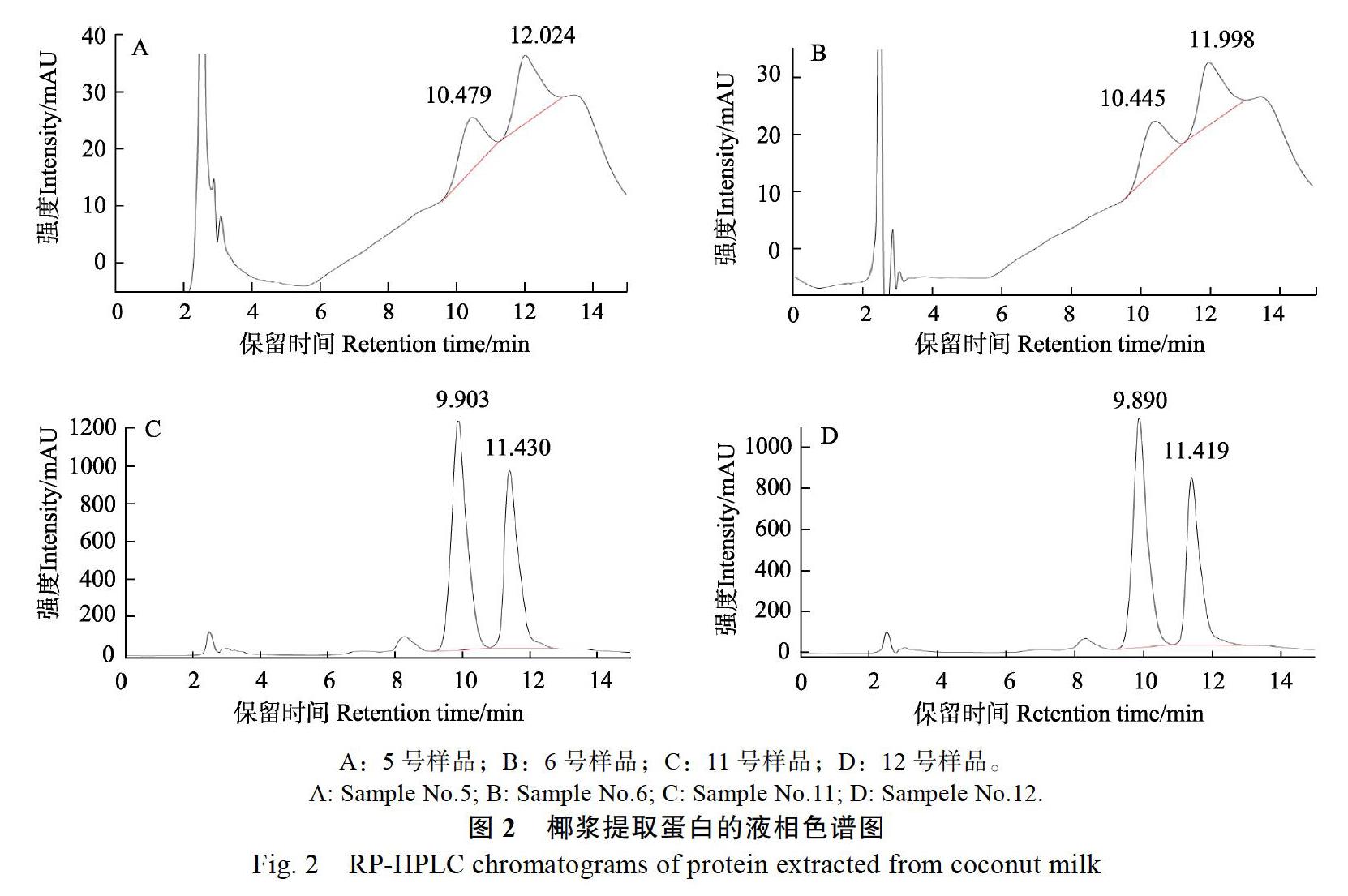
5号和6号样品的液相色谱图见图2,椰浆蛋白液相色谱峰面积之和表现出与产品标识的蛋白含量结果不一致。其中,6号样品的蛋白质含量为3.3 g/100 mL,2个色谱峰的峰面积都与3号样(蛋白含量为0.9 g/100 mL)的峰面积相差不大。结果表明,除去实验带来的误差,5号和6号样品中的蛋白质含量与标签中蛋白含量不符,标签的蛋白含量可能由凯氏定氮法测得,但这种氮并非椰浆蛋白质中的氮。
11号样品为海南本地企业送检样,与鲜榨椰子浆(12号样品)液相色谱图结果最为相近(图2C、图2D)。3次平行样的平均峰面积详见表2。图2A中5号椰浆液相色谱峰的保留时间分别为10.479 min和12.024 min,与图2D中鲜榨椰子浆提取的蛋白溶液色谱图峰型相似,但低浓度椰浆的2个色谱峰的出峰时间都推后了约0.5 min,如果以第1个峰为分子、第2个峰为分母,计算相对保留时间,获得椰浆的相对保留时间为1.14 min,鲜榨椰子汁的相对保留时间为1.15 min,相对保留时间差为0.01 min,这可能是由于蛋白质的浓度不同、椰浆的处理工艺不同或是在椰浆生产过程中加入了不同添加剂而导致的结果。
2.2 椰浆电泳图
椰浆的电泳图条带少且颜色浅。在中国海南和泰国产的椰浆样品1~7号中,除6号样品外,其他样品的电泳图都较为相似,6号样品因蛋白浓度高,电泳图条带比其他样品的条带清楚,且6号电泳图在19~26 kDa之间比其他椰浆多了1条条带(图3)。电泳结果表明,6号样品中含有
一定量的蛋白质,与标签含量一致,但这与液相色谱峰面积较小的结果不一致,可能是椰浆生产工艺中产生或是加入的蛋白。5号样品的电泳条带少且颜色浅,这与液相色谱峰面积小的结果一致,与标签含量不一致。8~10号椰浆为马来西亚的椰浆,这3个样品的电泳条带个数基本一致,但各个条带深浅有区别,说明含有的蛋白种类基本相同但是含量有所差异。
2.3 MALDI-TOF/TOF-MS鉴定结果
从凝胶上挖取具有代表性的蛋白条带(挖点见图3),用MALDI-TOF/TOF-MS进行鉴定,根据Mascot (http://www.matrixscience.com)搜索,椰浆的9个挖点中有6条蛋白条带均鉴定出vicilin-like antimicrobial peptides 2-1, partial [Elaeis guineensis](豌豆球蛋白样抗菌肽2-1,部分[油棕])。MALDI-TOF/TOF-MS图见图4,图中标出特征肽段QQPFYDEGMR(分子量1270.59)的二级图谱,条带2、3、6、7、8都鉴定出豌豆球蛋白样抗菌肽2-1,部分[油棕],这些条带的MALDI-TOF/TOF-MS图谱与条带1的相似。根据质谱鉴定出的氨基酸序列,通过Swiss-modle(https://swissmodel.expasy.org/inte ractive)数据比对,得到许多同源序列,选定相关性最高的作为待测蛋白质列模板,与63 kDa 类球蛋白的条带具有最高相关性的模板为豌豆球蛋白模板(4lej.1.A),相似性为37.50%~38.81%,63 kDa 类球蛋白也是椰子中的高丰度蛋白,含量较高[20]。
由图3的条带9鉴定出3种蛋白,除了63 kDa类球蛋白[油棕]外,还鉴定出7S球蛋白[油
棕]和11S球蛋白同种型1[椰子],MALDI-TOF/ TOF-MS图谱见图5。图中标出了7S球蛋白[油棕]:EEVFMAGPEER(分子量 1293.622)、11S球蛋白同种型1[椰子]:GDEVAIFTPR(分子量1104.604)和63 kDa类球蛋白[油棕]:VAIIETNP NT FVLPSHFD AEA LL FVAR(分子量2984.696)代表性的特征肽段,鉴定结果见表3。椰浆中鉴定出的7S和11S球蛋白,与文献报道结果一致[21]。
椰浆的电泳图基本都有的3个条带,分别为26 kDa、35~49 kDa和49 kDa。6、8、9、10号椰浆电泳图上26 kDa的条带比鲜榨椰子浆中的蛋白条带深,6号样品的条带3和8号样品的条带8均鉴定为豌豆球蛋白样抗菌肽2-1,可能是由于椰浆的生产工艺使得蛋白质分解成多肽而产生了此条带的蛋白。所有椰浆35~49 kDa之间的条带和49 kDa的條带都比鲜榨椰子浆的条带浅,可能是由于椰浆生产加工过程中,部分蛋白因理化因素发生了变性而析出,导致蛋白质浓度下降。6号样品的第4和第5条条带,没有鉴定出椰子相关的肽段或蛋白,这与高效液相色谱峰面积小的结果一致,可推测出6号椰浆样品加入非椰子蛋白的概率大。
3 讨论
椰浆用途广泛,可作为食品添加剂,椰子果肉被加工成椰浆,可保持其营养物质和天然风味。椰浆的9个挖点中有6条蛋白条带鉴定出vicilin-like antimicrobial peptides 2-1,partial [Elaeis guineensis](豌豆球蛋白样抗菌肽2-1,部分[油棕]):QQPFYDEGMR(分子量1270.59)。Zheng等分别于2016、2019年从椰饼分离蛋白水解物中分离出2条抗氧化肽Pro-Gln-Phe-Tyr-Trp(865.02 Da)、ArgPro-Glu-Ile-Val(612.36 Da)[22]和具有ACE抑制和抗氧化作用的3条活性肽KAQYPYV、KIIIYN和KILIYG[23]。这些结果表明,椰子蛋白是一种具有生物活性肽的潜在来源。
通常用于植物蛋白的分析方法有十二烷基凝胶电泳(SDS-PAGE)、高效液相色谱(HPLC)和基质辅助激光解吸电离飞行时间质谱(MALDI- TOF/TOF-MS)等。MALDI-TOF/TOF-MS因具有高通量、高分辨率、低检测线和准确性,更适用于植物蛋白的定性分析。本研究以RP-HPLC得到的色谱峰面积和SDS-PAGE条带数量和颜色的深浅相互验证,并与MALDI-TOF/TOF-MS鉴定出的肽段根据Mascot搜索匹配的蛋白质的信息为评价指标,研究了椰浆中椰子蛋白的定性分析方法,可初步判定椰浆蛋白与产品标识是否相符,判断椰浆蛋白是否来源于椰子蛋白,可作为椰浆中掺入非椰子蛋白的有效鉴定方法,具有广阔的应用空间,为椰浆蛋白的食品安全和质量控制提供了方法参考和示范。
在椰浆和鲜榨椰子浆的HPLC图中,都有2个明显的色谱峰,特别是在鲜榨椰子浆中,这2个色谱峰的峰面积更大。在今后的研究中,可研究批量分离纯化这2个蛋白色谱峰的方法,明确这2种椰子蛋白物理化学性质;椰子蛋白有促进健康和预防疾病的潜力,可采用已有的现代生物学技术开发出这2种椰子蛋白更多的附加值,在生产椰子蛋白质产品时,通过加酸、碱、酶等,得到更容易消化且功能性更好的椰子蛋白质产品;也可将这2种纯化后的椰子蛋白作为标准品,用HPLC外标法检测和评价椰子产品蛋白含量,而不是只检测氮含量,使得椰子蛋白的检测更合理和简化,对于椰子产品的应用与推广都具有重要的意义。
参考文献
[1]Paix?o L B, Brand?o G C, Araujo R G O, et al. Assessment of cadmium and lead in commercial coconut water and industrialized coconut milk employing HR-CS GF AAS[J]. Food Chemistry, 2019, 284(30): 259-263.
[2]Debmandal M,Mandal S. Coconut (Cocos nucifera L: Arecaceae): In health promotion and disease prevention[J]. Asian Pacific Journal of Tropical Medicine, 2011, 4(3): 241-247.
[3]Salil G, Nevina K G, Rajamohan T. Arginine rich coconut kernel protein modulates diabetes in alloxan treated rats[J]. Chemico-Biological Interactions, 2011, 189(1-2): 107-111.
[4]Thaiphanit S, Anprung P. Physicochemical and emulsion properties of edible protein concentrate from coconut (Cocos nucifera L.) processing by-products and the influence of heat treatment[J]. Food Hydrocolloids, 2016, 52: 756-765.
[5]Mini S, Rajamohan T. Influence of coconut kernel protein on lipid metabolism in alcohol fed rats[J]. Indian Journal of Experimental Biology, 2004, 42(1): 53-57.
[6]Espino-Sevilla M T, Jaramillo-Flores M E, Hernandez- Gutierrez R, et al. Functional properties of ditaxis heterantha proteins[J]. Food Sciences and Nutrition, 2013, 1(3): 254- 265.
[7]Jin T C, Wang C, Zhang C, et al. Crystal structure of cocosin, a potential food allergen from coconut (Cocos nucifera)[J]. Journal of Agricultural and Food Chemistry, 2017, 65(34): 7560-7568.
[8]桂 青, 禤小鳳. 基于GC-MS法的离心浓缩椰浆风味成分及脂肪酸组成分析[J]. 热带农业科学, 2016, 36(4): 77-81.
[9]郑亚军, 李 艳, 胡 荣, 等. 常压浓缩和真空浓缩对浓缩椰浆的品质影响[J]. 食品工业科技, 2015, 36(22): 241-245.
[10]沈晓君, 李晓煜. 真空浓缩椰浆的护色工艺研究[J]. 广东农业科学, 2015, 42(20): 91-96.
[11]李晓煜, 沈晓君, 赵松林, 等. 真空浓缩椰浆乳化稳定性探究[J]. 食品与发酵工业, 2015, 41(4): 141-146.
[12]张建国, 赵松林. 椰子蛋白质的功能特性研究进展[J]. 中国科技纵横, 2016, 8: 241-242,245.
[13]Hagenmaier R, Cater C M, Mattil K F J. A characterization of two chromatographically separated fractions of coconut protein[J]. Italian Journal of Food Science, 1972, 37: 4-6.
[14]Huang J M, Liu X Q, Lan Q, et al. Proteomic profile of coconuts[J]. European Food Research and Technology, 2016, 242(3): 449-455.
[15]Robert W, Julius W. Isolation of coconut storage proteins by polyacrylamide-gel electrophoresis[J]. Analytical Biochemistry, 1976, 75: 498-508.
[16]Rasyid F, Manullang M, Hansen P M T. Isolation and characterization of coconut protein[J]. Food Hydrocolloids, 1992, 6(3): 301-314.
[17]郑亚军, 赵松林, 陈 华, 等. 椰子果肉中蛋白质亚基的组成与含量分析[J]. 热带作物学报, 2008, 29(6): 704-709.
[18]Wang X, Shi M, Wang D, et al. Comparative proteomics of primary and secondary lutoids reveals that chitinase and glucanase play a crucial combined role in rubber particle aggregation in Hevea brasiliensis[J]. Journal of Proteome Research, 2013, 12(11): 5146-5159.
[19]Wang X, Wang D, Sun Y, et al. Comprehensive proteomics analysis of laticifer latex reveals new insights into ethylene stimulation of natural rubber production[J]. Scientific Reports, 2015, 5(13778): 1-19.
[20]Lin Y, Wang Y, Ji Z R, et al. Isolation, purification, and identification of coconut protein through SDS-PAGE, HPLC and MALDI-TOF/TOF-MS[J]. Food Analytical Methods, 2020, 13(6): 1246-1254.
[21]Saha B, Sircar G, Pandey N, et al. Mining novel allergens from coconut pollen employing manual de novo sequencing and homology-driven proteomics[J]. Journal of Proteome Research, 2015, 14(11): 4823-4833.
[22]Zheng Y J, Li Y, Zhang Y L, et al. Purification, characterization and synthesis of antioxidant peptides from enzymatic hydrolysates of coconut (Cocos nucifera L.) cake protein isolates[J]. RSC Advances, 2016, 6(59): 54346- 54356.
[23]Zheng Y J, Li Y, Li G F. ACE-inhibitory and antioxidant peptides from coconut cake albumin hydrolysates: Purification, identification and synthesis[J]. RSC Advances, 2019, 9(11): 5925-5936.
責任编辑:崔丽虹
